La estenosis luminal es más frecuente en la enfermedad de Crohn (EC) dado su compromiso transmural. Antes de proceder a cualquier tratamiento endoscópico se debe descartar la presencia de una estenosis neoplásica. La dilatación endoscópica con balón se ha utilizado en varias series como tratamiento de las estenosis benignas, principalmente en EC con afectación del de íleon distal, colon o anastomosis quirúrgicas, con un éxito de entre el 51 y el 85%, aunque la recurrencia es alta. El uso concomitante de esteroides inyectados (triamcinolona) tras la dilatación endoscópica muestra unos resultados más duraderos, aunque la experiencia publicada es escasa. Ante pacientes con estenosis luminal resistente a la técnica convencional, disponemos de 3 técnicas endoscópicas emergentes que pueden ser de utilidad: stents metálicos autoexpandibles, endoprótesis biodegradables e inyección intralesional de infliximab.
Luminal stenosis is frequent in Crohn's disease (CD) due to transmural involvement. Before any endoscopic treatment, the presssence of neoplastic stenosis should always be excluded. Endoscopic balloon dilatation has been used in several series to treat benign stenosis, mainly in CD with involvement of the distal ileon, colon or surgical anastomosis, with success rates of 51% to 85%, although recurrence is high. The concomitant use of injected steroids (triamcinolone) after endoscopic dilatation produces longer-lasting results, but there are few published reports. In patients with luminal stenosis refractory to conventional endoscopy, three emerging techniques may be useful: self-expanding metallic stents, biodegradable endoprostheses and intralesional infliximab injection.
De acuerdo con la clasificación de Viena1,2, las estenosis se definen como un estrechamiento constante de la luz (radiológica, endoscópica o quirúrgica) con dilatación preestenótica o signos obstructivos, sin enfermedad penetrante, en cualquier momento de la evolución de la enfermedad.
Las estenosis en la enfermedad inflamatoria intestinal (EII) se cree que son el resultado de la respuesta cicatricial a la inflamación crónica de la pared intestinal, con fibrosis e hipertrofia del músculo liso, que conduce a un estrechamiento de la luz3. La estenosis luminal, bien por actividad inflamatoria u obstrucción intestinal, es más frecuente en la enfermedad de Crohn (EC) que en la colitis ulcerosa (CU) dada su afectación transmural, aunque disponemos de pocos datos epidemiológicos de cara a conocer su prevalencia4. Pueden aparecer en cualquier parte del tracto digestivo, pero son más habituales en íleon terminal, anastomosis ileocolónica y colónicas. En la EC las estenosis más frecuentes son las posquirúrgicas, fundamentalmente a nivel de la anastomosis ileocolónica. Las estenosis en la CU nos deben hacer sospechar la presencia de un cáncer colorrectal (CCR), por lo que estos pacientes deben ser referidos a colectomía o una nueva colonoscopia en 3 meses con biopsias dirigidas5.
Todas las estenosis pueden ser subsidiarias de tratamiento endoscópico, pero en todas ellas la evaluación histológica es fundamental dado que pueden estar malignizadas, por lo que antes de decidir cualquier tratamiento endoscópico de las mismas deben tomarse biopsias de la zona; de hecho, una lesión estenosante en un paciente con CU es neoplásica en hasta un 25% frente a un 11% de los pacientes con EC6.
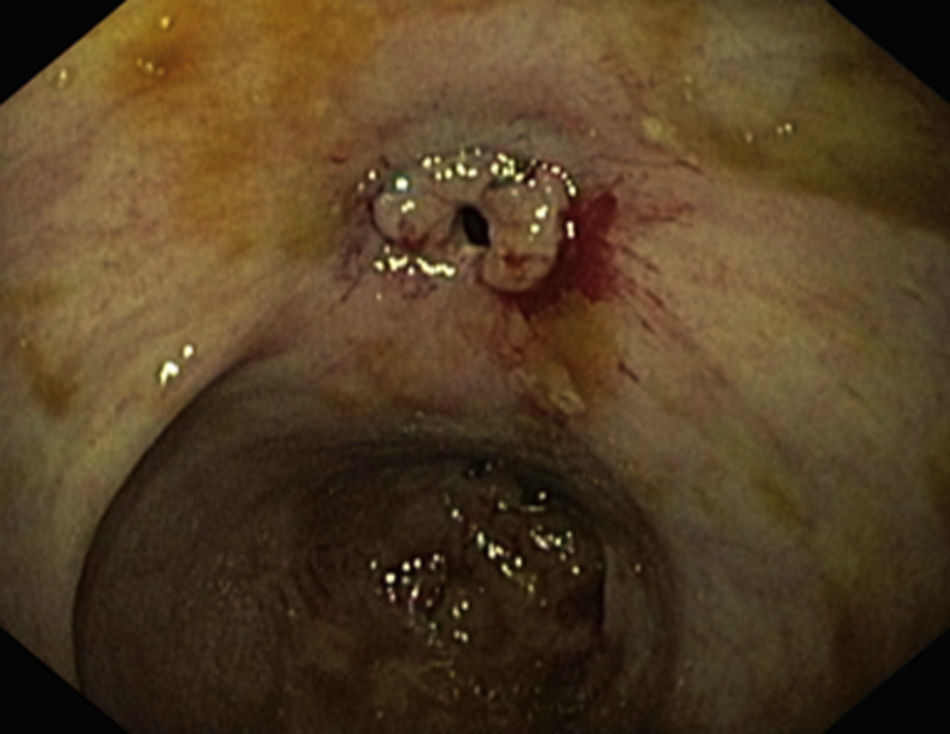
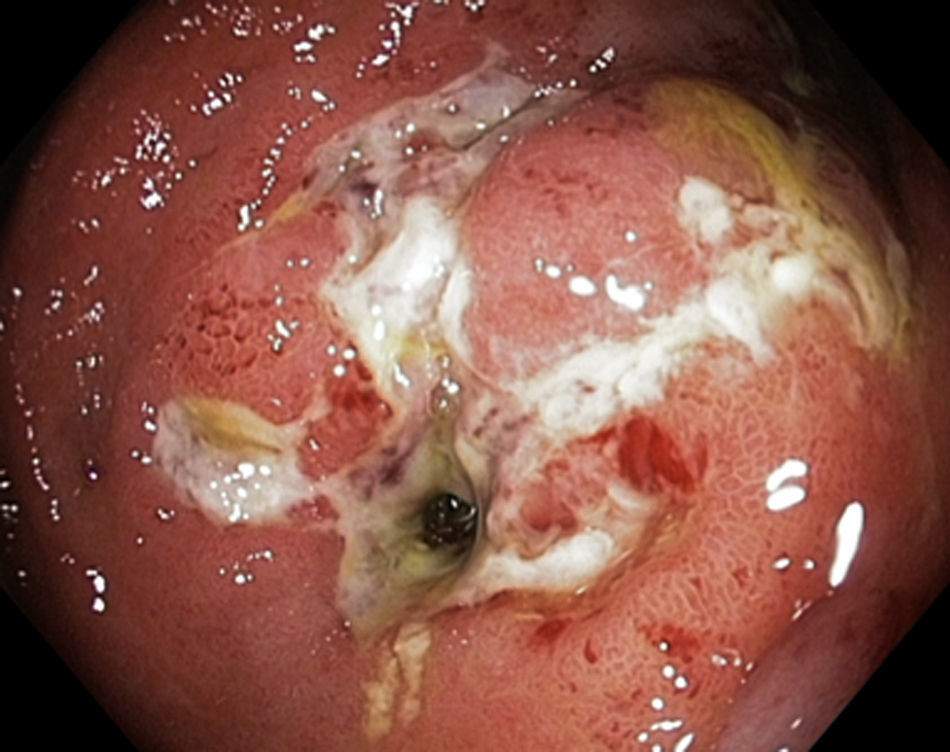
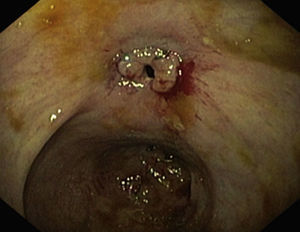
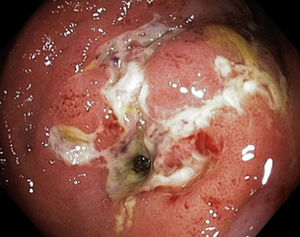
Las estenosis luminales benignas pueden ser fibróticas (fig. 1), que son cortas y tienen una mucosa lisa que no sangra al contacto, o inflamatorias (fig. 2), que son más largas y presentan una mucosa inflamada y friable, en ocasiones ulcerada o precedida de úlceras.
Las estenosis son habitualmente silentes, pero pueden presentarse con clínica, aguda o más habitualmente recurrente, de dolor abdominal posprandial, distensión u obstrucción franca. En pacientes con estenosis sintomáticas resistentes al tratamiento médico, o bien cuando éstas son fibróticas, la cirugía7,8, aunque es eficaz, no es un tratamiento definitivo. El abordaje quirúrgico puede ser mediante estricturoplastia o resección intestinal. La recurrencia posquirúrgica es alta independientemente de la técnica empleada, requiriendo una segunda cirugía el 50% de los pacientes a los 10 años9, por lo que el tratamiento endoscópico es una buena alternativa y tiene su papel.
Las tratamientos endoscópicos disponibles hoy en día para tratar las estenosis luminales incluyen la dilatación endoscópica con balón, con o sin inyección intralesional de corticoides. La duración del beneficio de la dilatación endoscópica es limitada, con necesidad de repetición de endoscopias y dilataciones periódicas, con el consiguiente riesgo de perforación. A la vista de situación se han propuesto nuevos tratamientos endoscópicos emergentes, con una experiencia muy escasa en todos ellos, como es la implantación de prótesis expandibles, metálicas o biodegradables, y la inyección local de infliximab.
Dilatación con balónLas estenosis sintomáticas pueden tratarse endoscópicamente mediante dilatación con balones neumáticos de diferentes calibres, que se pasan a través del canal de trabajo, y permiten la práctica de la dilatación bajo control visual endoscópico, pudiendo prescindir del control radiológico. La toma de biopsias obtiene mayores resultados cuando se realiza tras la dilatación de la estenosis.
La introducción de los balones de Gruentzig han permitido solucionar las estenosis del tubo digestivo. La técnica de dilatación con balón es muy variable, y depende en gran medida de las preferencias y experiencia del endoscopista que la practica10. Se emplean 2 diámetros de balón, hasta 25mm, o bien de 18-20mm, presentando este último menos complicaciones.
Las tasas de complicaciones se sitúan en un 20% con balones de 25mm, y del 10% con balones de 18-20mm11. La hemorragia posdilatación se maneja de forma conservadora. Se realiza con insuflación mantenida de 1 a 4 min, teniéndose que repetir en varias ocasiones. Existen discrepancias en la definición de dilatación satisfactoria, clásicamente entendida como aquella que permite pasar un endoscopio de 13mm, ya que un diámetro de 13mm no siempre se asocia a alivio sintomático.
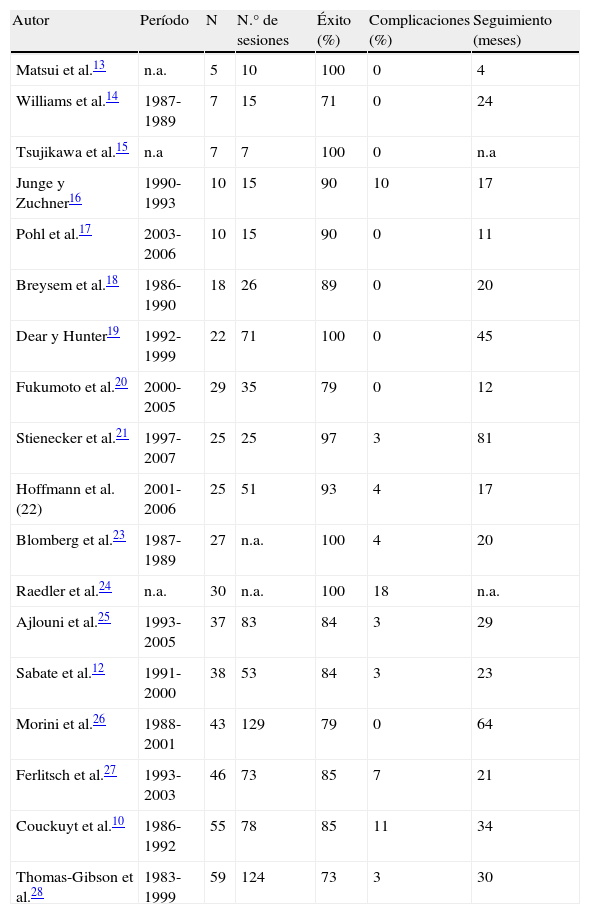
La dilatación por balón presenta una tasa éxito de entre el 51 y el 85%, aunque la recurrencia es alta; de hecho, un 43% de los pacientes que reciben dilatación endoscópica requieren cirugía a los 5 años12. El problema es que la mayoría de los estudios son retrospectivos y con series pequeñas10,12–28 (tabla 1). El grupo que obtiene mejores resultados son las estenosis fibróticas y posquirúrgicas, con un 80-100% de respuesta. En el caso de estenosis inflamatorias, los pacientes deben recibir previamente tratamiento médico y solo tratar endoscópicamente una vez mejorada la inflamación29. En ocasiones, la presencia de una estenosis angulada o larga impide el paso del balón, por lo que una opción es realizar la dilatación con hilo-guía.
Resultados publicados en la literatura médica de la dilatación endoscópica con balón en pacientes con estenosis luminal por enfermedad inflamatoria intestinal
| Autor | Período | N | N.° de sesiones | Éxito (%) | Complicaciones (%) | Seguimiento (meses) |
| Matsui et al.13 | n.a. | 5 | 10 | 100 | 0 | 4 |
| Williams et al.14 | 1987-1989 | 7 | 15 | 71 | 0 | 24 |
| Tsujikawa et al.15 | n.a | 7 | 7 | 100 | 0 | n.a |
| Junge y Zuchner16 | 1990-1993 | 10 | 15 | 90 | 10 | 17 |
| Pohl et al.17 | 2003-2006 | 10 | 15 | 90 | 0 | 11 |
| Breysem et al.18 | 1986-1990 | 18 | 26 | 89 | 0 | 20 |
| Dear y Hunter19 | 1992-1999 | 22 | 71 | 100 | 0 | 45 |
| Fukumoto et al.20 | 2000-2005 | 29 | 35 | 79 | 0 | 12 |
| Stienecker et al.21 | 1997-2007 | 25 | 25 | 97 | 3 | 81 |
| Hoffmann et al.(22) | 2001-2006 | 25 | 51 | 93 | 4 | 17 |
| Blomberg et al.23 | 1987-1989 | 27 | n.a. | 100 | 4 | 20 |
| Raedler et al.24 | n.a. | 30 | n.a. | 100 | 18 | n.a. |
| Ajlouni et al.25 | 1993-2005 | 37 | 83 | 84 | 3 | 29 |
| Sabate et al.12 | 1991-2000 | 38 | 53 | 84 | 3 | 23 |
| Morini et al.26 | 1988-2001 | 43 | 129 | 79 | 0 | 64 |
| Ferlitsch et al.27 | 1993-2003 | 46 | 73 | 85 | 7 | 21 |
| Couckuyt et al.10 | 1986-1992 | 55 | 78 | 85 | 11 | 34 |
| Thomas-Gibson et al.28 | 1983-1999 | 59 | 124 | 73 | 3 | 30 |
n.a.: no aparece.
Los mejores resultados se obtienen con estenosis de 2 a 4cm de longitud, ya que longitudes superiores a 4cm se asocian a fallo técnico. El fallo técnico ocurre en un 21% de las dilataciones26. Los pacientes suelen requerir varias sesiones de dilatación; de hecho, la dilatación se puede repetir hasta obtener una mejoría clínica con desaparición de la sintomatología obstructiva.
Los criterios para la dilatación endoscópica son:
- 1.
Estenosis corta.
- 2.
Inflamación mínima.
- 3.
No hay evidencia de fístula o angulación de la estenosis.
- 4.
No hay evidencia de cáncer.
- 5.
Acceso fácil con el endoscopio.
- 6.
Preferiblemente única.
La disponibilidad de enteroscopia de doble balón amplía en forma importante el alcance de la dilatación endoscópica existiendo en la literatura médica solo descripción de casos que recogen su uso con éxito en pacientes con estenosis de intestino delgado.
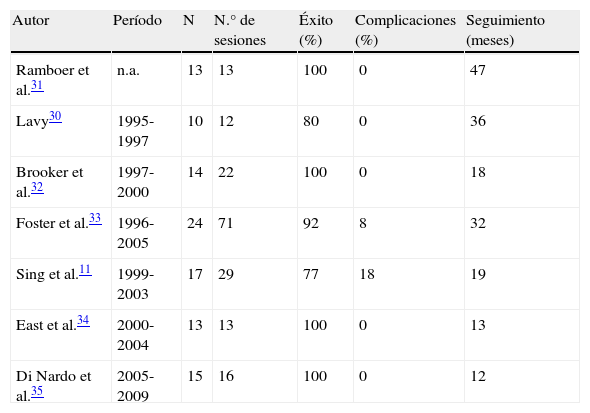
Dilatación endoscópica con balón e inyección de corticoides intralesionalesDebido a los resultados subóptimos a largo plazo de la dilatación endoscópica con balón, se han propuesto técnicas adyuvantes que mejoren los resultados. En casos de estenosis con un importante componente inflamatorio y fibrótico se ha descrito que la inyección local de corticoides en la zona estenótica tras la dilatación permite reducir el número de dilataciones, ya que evita las reestenosis debida a la cicatrización del desgarro producido por la dilatación. La dilatación con balón neumático asociada a inyección de corticoides intralesionales (triamcinolona) ha demostrado su utilidad desde 199530, pero no existen estudios controlados que avalen su uso. En la tabla 2 se muestran los resultados de los 7 estudios publicados hasta la fecha, con una tasa de éxito de entre el 77 y el 100%, después de un seguimiento de 12-47 meses11,30–35.
Resultados publicados en la literatura médica de la dilatación endoscópica con balón e inyección local de esteroides en pacientes con estenosis luminal por enfermedad inflamatoria intestinal
| Autor | Período | N | N.° de sesiones | Éxito (%) | Complicaciones (%) | Seguimiento (meses) |
| Ramboer et al.31 | n.a. | 13 | 13 | 100 | 0 | 47 |
| Lavy30 | 1995-1997 | 10 | 12 | 80 | 0 | 36 |
| Brooker et al.32 | 1997-2000 | 14 | 22 | 100 | 0 | 18 |
| Foster et al.33 | 1996-2005 | 24 | 71 | 92 | 8 | 32 |
| Sing et al.11 | 1999-2003 | 17 | 29 | 77 | 18 | 19 |
| East et al.34 | 2000-2004 | 13 | 13 | 100 | 0 | 13 |
| Di Nardo et al.35 | 2005-2009 | 15 | 16 | 100 | 0 | 12 |
n.a.: no aparece.
Desde su introducción en la década de los noventa, las prótesis metálicas autoexpandibles se han empleado con éxito para descomprimir una oclusión maligna de colon, evitando una cirugía de emergencia. La experiencia con estas prótesis en oclusiones benignas de colon es muy escasa, con un éxito terapéutico del 76%, una tasa de migración de la prótesis del 11%, y un riesgo de perforación del colon en el 4% de los casos, principalmente en contexto de diverticulosis36–39.
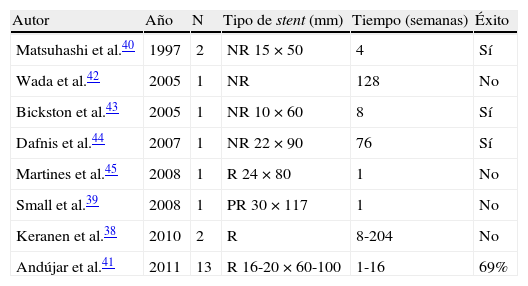
En la tabla 3 se muestran los resultados publicados en la literatura médica de la implantación de prótesis metálicas expandibles en pacientes con estenosis luminal por enfermedad inflamatoria intestinal38–45. Las evidencias disponibles son muy escasas, en forma de casos clínicos o series cortas de casos. La serie más amplia (n=13) corresponde a un estudio multicéntrico español con pacientes con EC y estenosis luminal resistente, de la que solo se dispone de datos en formato abstract41. Estos autores aconsejan la implantación de prótesis métalicas recubiertas durante un período de 4 a 6 semanas, obteniendo una eficacia del 69%, aunque con una tasa alta de migración distal.
Resultados publicados en la literatura médica de la implantación de prótesis metálicas expandibles en pacientes con estenosis luminal por enfermedad inflamatoria intestinal
| Autor | Año | N | Tipo de stent (mm) | Tiempo (semanas) | Éxito |
| Matsuhashi et al.40 | 1997 | 2 | NR 15×50 | 4 | Sí |
| Wada et al.42 | 2005 | 1 | NR | 128 | No |
| Bickston et al.43 | 2005 | 1 | NR 10×60 | 8 | Sí |
| Dafnis et al.44 | 2007 | 1 | NR 22×90 | 76 | Sí |
| Martines et al.45 | 2008 | 1 | R 24×80 | 1 | No |
| Small et al.39 | 2008 | 1 | PR 30×117 | 1 | No |
| Keranen et al.38 | 2010 | 2 | R | 8-204 | No |
| Andújar et al.41 | 2011 | 13 | R 16-20×60-100 | 1-16 | 69% |
NR: prótesis no recubierta; PR: prótesis parcialmente recubierta; R: prótesis totalmente recubierta.
La administración sistémica de infliximab ha demostrado su utilidad en inducir la curación mucosa46,47; no obstante, existen muy pocas evidencias de que sea útil en mejorar las estenosis fibróticas. En estos 2 trabajos se ha constatado que los niveles tisulares de infliximab predicen la respuesta mucosa; por ello, la inyección local intralesional podría ser más eficaz que la administración sistémica. En función de esta hipótesis se ha propuesto que esta inyección directa en una estenosis luminal puede mejorar el grado de inflamación, con la consiguiente mejoría del edema de la submucosa, permitiendo una dilatación de la luz intestinal. La inyección intraarticular de infliximab ha mostrado su eficacia en la artritis reumatoide48 y en la artritis inflamatoria aguda49. La inyección local de infliximab (15-21mg) en la enfermedad perianal induce una resolución de las fístulas complejas en 10 de 15 pacientes50. Biancone et al.51 publicaron los resultados de un estudio con 8 pacientes con EC y recurrencia posquirúrgica no estenosante a los que se les inyectó infliximab en las lesiones mucosa perianastomosis. En todos los pacientes la dosis media administrada por sesión fue 30mg (dosis máxima 60mg), inferior a la dosis requerida en la infusión intravenosa (5mg/kg). En 7 de los 8 pacientes se constató una mejoría en el número y extensión de las lesiones, manteniéndose en remisión durante el período de seguimiento (rango 14-21 meses desde la inyección).
La única experiencia publicada que evaluó la eficacia de la inyección local de infliximab en pacientes con EC y estenosis luminal fue reportada en el año 20084. Se evaluaron 3 pacientes con estenosis luminal distal resistente al tratamiento con infliximab sistémico, a los que se les inyectó infliximab de forma radial intralesional, en dosis de 100mg por sesión (rango 90-120mg). Los 3 pacientes presentaron una buena respuesta a corto plazo (2 semanas), que se mantuvo después de un seguimiento medio de 10 meses.
Pese a estos resultados aún es pronto para establecer conclusiones. Por otra parte, en estudios recientes52,53 se ha sugerido que la inhibición de factor de necrosis tumoral alfa (TNF-α) aumenta el riesgo de linfoma, aunque no está claro que exista el mismo riesgo de tipo local.
Prótesis biodegradablesLas prótesis biodegradables se pueden considerar como una alternativa válida eficaz, ya que presentan una mayor flexibilidad que las prótesis metálicas y plásticas, y no precisan su retirada54. Estas prótesis pueden estar hechas de varios polímeros sintéticos como el ácido poliláctico o el ácido poliglicólico, o sus polímeros como la polidioxanona. La degradación de estos materiales se produce por hidrólisis. La velocidad de su degradación depende de su tamaño y estructura (cristalinidad y porosidad), pero también de la temperatura, el pH y el tipo de tejido sobre el que asientan55. Las endoprótesis biodegradables están hechas de polidioxanona, que es el material empleado en las suturas reabsorbibles, y con las que hay gran experiencia en estenosis esofágicas. Los resultados disponibles nos muestran que estos dispositivos son eficaces, aunque en algunos casos hay que repetir el procedimiento a largo plazo. La fuerza radial de estas endoprótesis se mantiene durante 6-8 semanas, la desintegración de la prótesis ocurre a las 11-12 semanas, sabiendo que el pH bajo (ácido) acelera la degradación.
La implantación intestinal de las prótesis biodegradables es técnicamente posible y relativamente simple; sin embargo existen algunos aspectos mejorables, como la reacción mucosa hiperplásica y la tasa de migración. En 2 trabajos se ha descrito una reacción mucosa hiperplásica después de la inserción de estas prótesis en esófago en el 3% de los pacientes56,57.
En la actualidad, para aplicar este tipo de dispositivos necesitamos poder pasar el sistema de implantación a través de la estenosis, por lo que el diámetro mínimo es de 28 F (9,4mm). Por todo ello es preciso dilatar previamente la estenosis y marcar el extremo distal de la estenosis con clips o lipiodol. La inserción de la prótesis se facilita con un sobretubo, guiada por hilo-guía y bajo control radiológico.
La experiencia con estas prótesis en las estenosis de íleon y colon es escasa pero muy prometedora58. Recientemente, el mismo grupo de autores ha publicado en Endoscopy59 su experiencia con 11 pacientes con estenosis luminal en EC, principalmente localizada en la anastomois ileocolónica. Se emplearon 3 modelos de stent (18-25mm de cuerpo y 40-80mm de longitud), lo que permite una prótesis a medida que disminuya el riesgo de migración. Después de un período de seguimiento medio de 17 meses en un 73% de los pacientes (n=8) se resolvió la estenosis. La migración del stent aconteció de forma precoz en 2 pacientes, sin que se describiera ninguna reacción hiperplásica. Estos autores proponen una mejor selección del diseño y calibre de la prótesis para evitar esta tasa de migración.
ConclusiónLa estenosis luminal es más frecuente en la EC dada la afectación transmural. Antes de proceder a cualquier tratamiento endoscópico se debe descartar la presencia de una estenosis neoplásica. La dilatación endoscópica con balón se ha utilizado en varias series como tratamiento de las estenosis benignas, principalmente en EC con afectación del íleon distal, colon o anastomosis quirúrgicas, con un éxito de entre 51 a 85% aunque la recurrencia es elevada. El uso simultáneo de esteroides inyectados (triamcinolona) tras la dilatación endoscópica muestra unos resultados más duraderos, aunque la experiencia publicada es escasa. Ante pacientes con estenosis luminal resistente a la técnica convencional, disponemos de 3 técnicas endoscópicas emergentes que pueden ser de utilidad: stents metálicos autoexpandibles, endoprótesis biodegradables e inyección intralesional de infliximab.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.