El delirium es un gran síndrome geriátrico que afecta a un importante porcentaje de los pacientes mayores hospitalizados. Implica relevantes consecuencias negativas para los usuarios y profesionales, y puede prevenirse. El objetivo del presente artículo es identificar y describir los instrumentos predictivos del riesgo de padecer delirium en pacientes hospitalizados. Para finalizar, se analizan las fuentes de heterogeneidad y escasez de herramientas de este tipo, así como las razones de que su uso no se haya extendido en la práctica clínica.
Delirium is a major geriatric syndrome that affects a significant percentage of elderly hospitalized patients. It involves major negative consequences for users and professionals and can be prevented. The aim of this paper is to identify and describe the tools for predicting delirium in hospitalized patients. Lastly, the work analyzes the sources of heterogeneity and the scarcity of such instruments, as well as the reasons why their use is not widespread in clinical practice.
El delirium es un «gran síndrome geriátrico» cuya frecuencia de aparición oscila entre el 10–56% de los pacientes mayores hospitalizados1–3 y aumenta con la edad, siendo muy frecuente a partir de los 75–80 años4,5, e inusual por debajo de los 606. La identificación de los pacientes mayores en riesgo de padecer delirium durante su hospitalización es un objetivo clínico que permitiría focalizar los esfuerzos preventivos en este grupo de usuarios, reduciendo los efectos negativos que este cuadro clínico implica. Es evidente que, a no ser que el protocolo de prevención del delirium se aplique de forma sistemática a cualquier paciente ingresado mayor de 65 años, es indispensable contar con un instrumento que mida el riesgo que un usuario concreto presenta de padecer delirium, en base a factores de riesgo. Por ello, el objetivo de este trabajo es identificar y describir los instrumentos predictivos de delirium en pacientes mayores hospitalizados.
El delirium: definición, clínica y factores de riesgoEl Manual Diagnóstico y Estadístico de Trastornos Mentales (DSM-IV)7 caracteriza el delirium como una alteración de la conciencia y un cambio de las funciones cognoscitivas que se desarrollan a lo largo de un breve periodo de tiempo (horas/días) y tiende a fluctuar a lo largo del día. Es la consecuencia fisiológica directa de una enfermedad médica, de una intoxicación/abstinencia de sustancias, o de varias de estas causas.
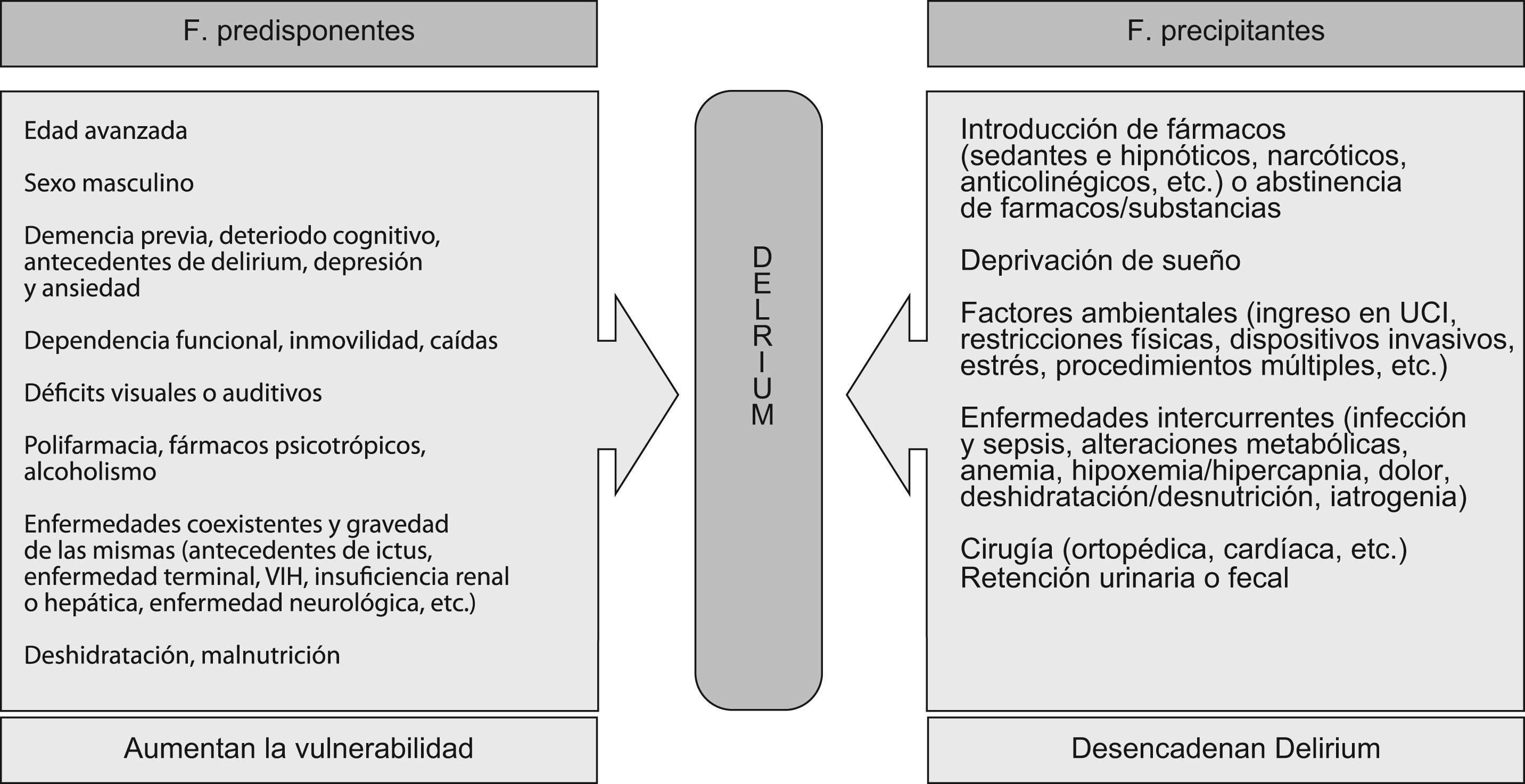
Se considera el delirium como un cuadro «de etiología multifactorial»5,8,9, resultado de la interacción compleja entre personas mayores vulnerables y causas precipitantes múltiples (fig. 1). El efecto de estos 2 tipos de factores (de vulnerabilidad y precipitantes) es acumulativo9,10: el riesgo de delirium aumenta a medida que aumenta la vulnerabilidad del paciente y/o el número/intensidad de los factores precipitantes.
Modelo multifactorial del Delirium9–11.
A pesar de la existencia de criterios diagnósticos para el delirium y de instrumentos diagnósticos, como el Confusion Assessment Method (CAM)11,12, en la práctica muchos casos no se diagnostican. Según Cole et al13, una de las razones que provocan esta situación es que no se identifican ni vigilan los pacientes con riesgo alto de delirium.
El delirium se asocia a una elevada morbilidad7,12,14 y a una mayor mortalidad (entre un 9–34%)14,15 en los pacientes que lo presentan. Es además un predictor de institucionalización y rehospitalización5,7,14 e implica un incremento de los días de estancia hospitalaria y un aumento de los costes sanitarios asociados14,16,17.
Los efectos sobre los profesionales que atienden a este tipo de usuarios no deben despreciarse. Según Rogers y Gibson, las enfermeras describían el cuidado de pacientes delirantes como frustrante, extenuante, desafiante y que consume mucho tiempo (time-consuming) ya que implica siempre una mayor carga de trabajo, mayor inseguridad (agresiones físicas y/o verbales), dilemas y conflictos en el cuidado y baja autoestima del profesional18.
En relación con la prevención del delirium, esta es un objetivo deseable para disminuir los efectos adversos en el paciente y en los profesionales, y para reducir los costes económicos asociados19. Aunque escasos, existen algunos trabajos que miden el efecto que intervenciones preventivas de delirium tienen, no solamente en la reducción de la incidencia, duración y severidad del cuadro, sino también en los resultados en salud de los pacientes20. Se han demostrado reducciones de los tiempos de estancia21,22 y de los ratios de mortalidad durante la hospitalización21, También se han objetivado reducciones en los costes económicos asociados al ingreso en instituciones sanitarias de larga estancia tras el alta23. Por otro lado, es importante señalar que dada la naturaleza multifactorial del delirium, los programas de prevención diseñados incluyen habitualmente varias áreas de intervención20,21. Un ejemplo de ello en nuestro ámbito nacional es un reciente estudio que demuestra la eficacia de una intervención multicomponente en la reducción de la incidencia de delirium24.
Instrumentos predictivos del riesgo de deliriumEl primer intento de construir una regla predictiva del delirium parte de Inouye et al en 199325. En un estudio prospectivo de cohortes, se incluyen pacientes de medicina general de más de 70 años sin demencia o delirium en el momento de admisión. El instrumento se construye a partir de la cohorte de desarrollo (107 pacientes), e incluye 4 factores de vulnerabilidad. Los investigadores asignan un punto a cada ítem para definir los grupos de riesgo (tabla 1). Tras la aplicación del nuevo instrumento a la cohorte de validación (174 pacientes), se obtienen unos ratios de delirium del 3%, 16% y 32% para los grupos de riesgo leve, moderado y alto respectivamente. Los autores concluyen que el instrumento predictivo muestra su validez en la identificación y estratificación de pacientes de riesgo, en cohortes independientes. No obstante, se señalan algunas limitaciones, como una muestra escasa o la exclusión de pacientes con demencia severa previa (que pudo haber reducido la fuerza predictiva del «deterioro cognitivo preexistente»). Además, la exclusión en el modelo de algunos factores de riesgo por su baja prevalencia puede haber subestimado la habilidad predictiva de los mismos.
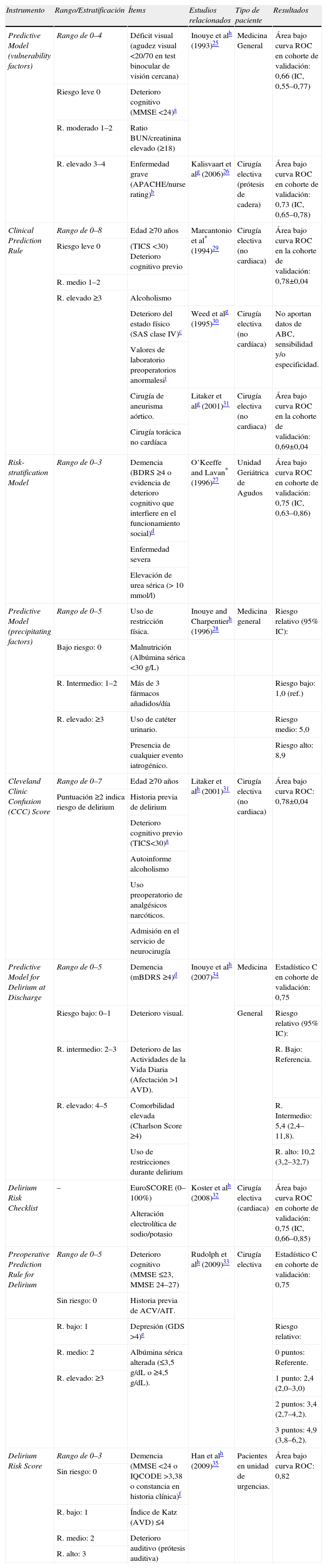
Instrumentos para la valoración del riesgo de presentar delirium
| Instrumento | Rango/Estratificación | Ítems | Estudios relacionados | Tipo de paciente | Resultados |
| Predictive Model (vulnerability factors) | Rango de 0–4 | Déficit visual (agudez visual <20/70 en test binocular de visión cercana) | Inouye et alh (1993)25 | Medicina General | Área bajo curva ROC en cohorte de validación: 0,66 (IC, 0,55–0,77) |
| Riesgo leve 0 | Deterioro cognitivo (MMSE <24)a | ||||
| R. moderado 1–2 | Ratio BUN/creatinina elevado (≥18) | ||||
| R. elevado 3–4 | Enfermedad grave (APACHE/nurse rating)b | Kalisvaart et alg (2006)26 | Cirugía electiva (prótesis de cadera) | Área bajo curva ROC en cohorte de validación: 0,73 (IC, 0,65–0,78) | |
| Clinical Prediction Rule | Rango de 0–8 | Edad ≥70 años | Marcantonio et al* (1994)29 | Cirugía electiva (no cardiaca) | Área bajo curva ROC en la cohorte de validación: 0,78±0,04 |
| Riesgo leve 0 | (TICS <30) Deterioro cognitivo previo | ||||
| R. medio 1–2 | |||||
| R. elevado ≥3 | Alcoholismo | ||||
| Deterioro del estado físico (SAS clase IV)c | Weed et alg (1995)30 | Cirugía electiva (no cardíaca) | No aportan datos de ABC, sensibilidad y/o especificidad. | ||
| Valores de laboratorio preoperatorios anormalesii | |||||
| Cirugía de aneurisma aórtico. | Litaker et alg (2001)31 | Cirugía electiva (no cardiaca) | Área bajo curva ROC en la cohorte de validación: 0,69±0,04 | ||
| Cirugía torácica no cardíaca | |||||
| Risk-stratification Model | Rango de 0–3 | Demencia (BDRS ≥4 o evidencia de deterioro cognitivo que interfiere en el funcionamiento social)d | O’Keeffe and Lavan* (1996)27 | Unidad Geriátrica de Agudos | Área bajo curva ROC en cohorte de validación: 0,75 (IC, 0,63–0,86) |
| Enfermedad severa | |||||
| Elevación de urea sérica (> 10mmol/l) | |||||
| Predictive Model (precipitating factors) | Rango de 0–5 | Uso de restricción física. | Inouye and Charpentierh (1996)28 | Medicina general | Riesgo relativo (95% IC): |
| Bajo riesgo: 0 | Malnutrición (Albúmina sérica <30g/L) | ||||
| R. Intermedio: 1–2 | Más de 3 fármacos añadidos/día | Riesgo bajo: 1,0 (ref.) | |||
| R. elevado: ≥3 | Uso de catéter urinario. | Riesgo medio: 5,0 | |||
| Presencia de cualquier evento iatrogénico. | Riesgo alto: 8,9 | ||||
| Cleveland Clinic Confusion (CCC) Score | Rango de 0–7 | Edad ≥70 años | Litaker et alh (2001)31 | Cirugía electiva (no cardiaca) | Área bajo curva ROC: 0,78±0,04 |
| Puntuación ≥2 indica riesgo de delirium | Historia previa de delirium | ||||
| Deterioro cognitivo previo (TICS<30)a | |||||
| Autoinforme alcoholismo | |||||
| Uso preoperatorio de analgésicos narcóticos. | |||||
| Admisión en el servicio de neurocirugía | |||||
| Predictive Model for Delirium at Discharge | Rango de 0–5 | Demencia (mBDRS ≥4)d | Inouye et alh (2007)34 | Medicina | Estadístico C en cohorte de validación: 0,75 |
| Riesgo bajo: 0–1 | Deterioro visual. | General | Riesgo relativo (95% IC): | ||
| R. intermedio: 2–3 | Deterioro de las Actividades de la Vida Diaria (Afectación >1 AVD). | R. Bajo: Referencia. | |||
| R. elevado: 4–5 | Comorbilidad elevada (Charlson Score ≥4) | R. Intermedio: 5,4 (2,4–11,8). | |||
| Uso de restricciones durante delirium | R. alto: 10,2 (3,2–32,7) | ||||
| Delirium Risk Checklist | – | EuroSCORE (0–100%) | Koster et alh (2008)32 | Cirugía electiva (cardiaca) | Área bajo curva ROC en cohorte de validación: 0,75 (IC, 0,66–0,85) |
| Alteración electrolítica de sodio/potasio | |||||
| Preoperative Prediction Rule for Delirium | Rango de 0–5 | Deterioro cognitivo (MMSE ≤23, MMSE 24–27) | Rudolph et alh (2009)33 | Cirugía electiva | Estadístico C en cohorte de validación: 0,75 |
| Sin riesgo: 0 | Historia previa de ACV/AIT. | ||||
| R. bajo: 1 | Depresión (GDS >4)e | Riesgo relativo: | |||
| R. medio: 2 | Albúmina sérica alterada (≤3,5g/dL o ≥4,5g/dL). | 0 puntos: Referente. | |||
| R. elevado: ≥3 | 1 punto: 2,4 (2,0–3,0) | ||||
| 2 puntos: 3,4 (2,7–4,2). | |||||
| 3 puntos: 4,9 (3,8–6,2). | |||||
| Delirium Risk Score | Rango de 0–3 | Demencia (MMSE <24 o IQCODE >3,38 o constancia en historia clínica)f | Han et alh (2009)35 | Pacientes en unidad de urgencias. | Área bajo curva ROC: 0,82 |
| Sin riesgo: 0 | |||||
| R. bajo: 1 | Índice de Katz (AVD) ≤4 | ||||
| R. medio: 2 | Deterioro auditivo (prótesis auditiva) | ||||
| R. alto: 3 |
MMSE: Mini-Mental Status Examination (mide el deterioro cognitivo). TICS: Telephone Interview for Cognitive Status (modificación validada del MMSE, de administración verbal).
APACHE: Acute Physiology And Chronic Health Evaluation. Mide la severidad del estado físico del paciente independientemente de su diagnóstico.
BDRS: Blessed Dementia Rating Scale. mBDRS: Modified Blessed Dementia Rating Scale (entrevista a un familiar/allegado del paciente para detectar si existe demencia).
GDS: Geriatric Depresion Scale. Un GDS >4ha mostrado buena sensibilidad (83–100%) y especificidad (65–84%) para la sintomatología depresiva33.
IQCODE: Informant Questionnaire on Cognitive Decline in the Elderly. Mide el deterioro cognitivo percibido por un familiar o allegado sobre los cambios en el sujeto mayor en los últimos 10 años35.
Este primer instrumento predictivo fue validado por Kalisvaart et al26 en 2006, en una amplia muestra de 603 pacientes quirúrgicos de edad igual o superior a los 70 años. En este estudio, la incidencia de delirium en el grupo de riesgo bajo fue de 3,8%, y de 11,1% y 37,1% en los grupos de riesgo moderado y alto respectivamente. La regla predictiva de Inouye et al para pacientes de medicina general puede extrapolarse a pacientes de cirugía ortopédica, a pesar de que el ratio BUN/creatinina no predijo el delirium en esta cohorte, al contrario que en el estudio original. Por otra parte, Kalisvaart et al identificaron otros factores de riesgo significativos (edad y admisión urgente) que incrementarían la fuerza predictiva del instrumento si se añadían. No obstante, este estudio de validación también muestra limitaciones, como la posibilidad de omisión de algún caso de delirio o el hecho de que los pacientes incluidos formaran parte de otro estudio sobre la eficacia de ciertas medidas preventivas de delirium, que podrían haber actuado como variables de confusión, a pesar de las precauciones de los investigadores.
O’Keeffe y Lavan presentan en 1996 un sistema de estratificación del riesgo de delirium en pacientes ancianos ingresados en una unidad geriátrica de agudos27. Tras la construcción del instrumento a partir de una cohorte de derivación de 100 pacientes, se incluye la presencia de demencia, de enfermedad severa y de valores anormales de sodio, como predictores de delirium en el momento de admisión, asignando un punto a cada ítem. Al aplicarse en el grupo de validación (84 individuos) se observa una adecuada estratificación en grupos de riesgo (13% de delirium en el grupo con 0 puntos, 32% en el grupo con 1 punto, 50% en el grupo con 2 puntos y 100% en el grupo con 3 puntos). Aún así, las limitaciones en cuanto al tamaño muestral, la exclusión de pacientes con sordera o la medición de algunas variables (alcoholismo, déficit visual) sin instrumentos diagnósticos adecuados deben ser tenidas en cuenta a la hora de valorar el rigor en la construcción del instrumento.
El mismo año, Inouye y Charpantier elaboran otra regla predictiva, esta vez basada en factores precipitantes28. Repiten el tipo de diseño y paciente, construyendo 2 cohortes (desarrollo y validación), de 196 y 312 participantes respectivamente. Al aplicar el instrumento desarrollado a la cohorte de validación, presentan delirium un 4%, 20% y 35% de los grupos de bajo, medio y alto riesgo respectivamente. Hay 9 veces más riesgo de delirium en el grupo de alto riesgo que en el de bajo riesgo, de manera que la herramienta muestra un buen comportamiento predictivo. Pero la contribución más importante de este estudio es que demuestra la interrelación existente entre factores de riesgo predisponentes y los factores de riesgo precipitantes, ya que el riesgo «basal» de estos mismos pacientes también fue medido, mostrando un fenómeno de «doble gradiente», que indica que ambos tipos de factores contribuyen a la aparición de delirium de manera independiente28.
Marcantonio et al29 proponen en 1994 la primera regla predictiva de delirium en pacientes de cirugía mayor no cardiaca (descartando los casos de deterioro cognitivo severo que impida obtener el consentimiento informado y los de delirium prevalente), y construyen una cohorte de desarrollo (876 pacientes) y otra de validación (465 pacientes). Se identifican los factores de riesgo independientes de delirium postoperatorio en la cohorte de desarrollo para construir la herramienta (tabla 1). Se asigna un valor de 1 punto a cada factor, excepto a la cirugía de aneurisma aórtico (2 puntos), que presenta un mayor valor de riesgo asociado. Se estratifica el riesgo (tabla 1) y se comprueba el buen comportamiento del instrumento en la cohorte de validación: 2% de delirium postoperatorio en pacientes de riesgo leve, 11% en los de riesgo medio, 50% en los de riesgo alto. Pero a pesar de contar con una muestra importante y de construir y validar la regla predictiva en cohortes independientes, el estudio de Marcantonio et al muestra una serie de debilidades, como la no distinción entre factores de vulnerabilidad (edad, alcoholismo, deterioro cognitivo, deterioro físico severo) y factores precipitantes (alteraciones bioquímicas en sangre o el tipo de cirugía) o el hecho de no contemplar factores intraoperatorios que pueden influir en la aparición del delirium.
Weed et al30 aplican en 1995 la Clinical Prediction Rule (CPR) de Marcantonio et al en una muestra de 138 pacientes sometidos a cirugía (de cáncer de cabeza y cuello), estratificándolos en grupos de riesgo leve, medio o elevado, en los que la incidencia de delirium fue del 9%, 19% y 25% respectivamente. No obstante, los resultados de esta investigación pierden robustez cuando los autores no usan un método validado para el diagnóstico de delirium (DSM, CAM) sino únicamente incluyen en el estudio aquellos casos «lo suficientemente severos como para ser identificados por los cirujanos o enfermeras», lo que implica un probable sesgo de omisión de casos de delirium.
Litaker et al31 intentan validar la CPR aplicándola a una muestra de 500 pacientes mayores de 50 años, y obteniendo una sensibilidad en la correcta identificación del delirium significativamente más baja que en el estudio original (47,4% vs 61,8%, para una puntuación de la CPR ≥2 puntos). A partir de la misma muestra, construyen una nueva herramienta predictiva, la Cleveland Clinic Confusion (CCC) Score cuyos ítems difieren parcialmente de los incluidos en la CPR (tabla 1). Se asigna un punto a cada factor excepto al autoinforme de alcoholismo (2 puntos), que en este estudio muestra mayor valor predictivo de delirium. La herramienta estratifica los pacientes en 2 grupos: sin riesgo de delirium (CCC Score ≤1 punto) y con riesgo de delirium (CCC Score ≥2 puntos). Los autores recalcan el elevado valor predictivo negativo que poseen ambas herramientas (CPR y CCC Score), lo que les da un valor añadido para la detección de pacientes con bajo riesgo de padecer delirium. Sin embargo, la mayor debilidad de la investigación de Litaker et al es que el nuevo instrumento desarrollado no se valida en una cohorte independiente de pacientes.
Continuando la línea de investigación en pacientes quirúrgicos, Koster et al32 llevan a cabo un estudio prospectivo en el que se incluyen pacientes de cirugía cardiaca electiva, de edad de 45 años o mayor y que no presenten delirium preoperatorio. Los investigadores construyen una lista de control que incluye factores de riesgo preoperatorios de delirium. Tras el análisis estadístico, 2 factores de riesgo (EuroSCOREa elevado y alteraciones electrolíticas de sodio/potasio) muestran ser predictores independientes de delirium y se construye una fórmula predictiva en base a ambos. Si se considera una probabilidad de desarrollar delirium del 50%, la sensibilidad de esta regla es del 25% y la especificidad del 95,5%. No obstante, las limitaciones de este estudio son múltiples: una muestra reducida de pacientes, la no existencia de una cohorte de validación distinta a aquella en la que se desarrolla el instrumento y la incapacidad de la fórmula para estratificar en grupos de riesgo.
Otra regla predictiva para pacientes sometidos a cirugía cardíaca es la desarrollada por Rudolph et al33 en 2 cohortes de 122 (desarrollo) y 109 pacientes (validación) mayores de 60 años, excluyendo aquellos que presentaban delirium previo. Se determinaron los factores preoperatorios independientemente asociados a delirium que constituirían la regla predictiva, y se establecieron puntos de corte significativos para operativizar el instrumento (tabla 1). Se asignó un punto a cada ítem excepto al deterioro cognitivo con un MMSE ≤23 (2 puntos). A mayor puntuación, mayor riesgo de delirium y mayor severidad del mismo. Son varias las fortalezas que refuerzan los resultados obtenidos por Rudolph et al: el estudio se realizó en varios centros asistenciales; se ajustaron factores precipitantes intraoperatorios y finalmente, al establecer 2 categorías de deterioro cognitivo (tabla 1) se incluyeron como pacientes de riesgo aquellos que sin traspasar el umbral tradicional de demencia (MMSE <24) muestran grados más leves de deterioro cognitivo. Por otra parte, una de las limitaciones más importantes del instrumento es que no permite identificar correctamente a los pacientes con bajo riesgo, pues el valor de riesgo más bajo medido es de 18–19%.
Inouye et al34 desarrollan en 2007 una nueva herramienta para detectar usuarios en riesgo de delirium persistente al alta. El diseño de la investigación no varía respecto las anteriores, con 2 cohortes de pacientes de medicina general de 70 años o más (491 individuos en la cohorte de desarrollo y 461 en la de validación). Se recogen las características basales y los factores precipitantes que pueden favorecer la aparición del delirium en la cohorte de desarrollo, destacando 5 predictores independientes de delirium persistente. Se asigna 1 punto a cada ítem para construir la regla predictiva y se establecen grupos de riesgo (tabla 1). Una vez aplicado el instrumento en la cohorte de validación, los ratios de delirium al alta resultaron del 3%, 14% y 27% en los grupos de riesgo bajo, intermedio y elevado respectivamente, con 10 veces más riesgo de padecer delirium persistente en el grupo de riesgo elevado que en el de bajo riesgo.
Finalmente, uno de los más recientes instrumentos predictivos es el de Han et al35, cuya escala de medición del riesgo de delirium se basa en factores predisponentes (tabla 1) y es aplicable a pacientes que ingresan en la unidad de urgencias. A pesar del buen comportamiento predictivo en su muestra de 303 pacientes, esta regla predictiva no es validada en una cohorte independiente, y la robustez de los resultados se ven coartada por el tamaño de la muestra y porque los investigadores limitaron el número de covariables incluidas en el modelo multifactorial para evitar sobreajuste del mismo, lo que podría tener como consecuencia que algunos factores de riesgo de delirium no se hayan tenido en cuenta.
Discusión: dificultades y futuras líneas de investigaciónA pesar de la trascendencia del delirium y sus consecuencias en pacientes, familias y profesionales, el interés por desarrollar un instrumento de medida del riesgo de desarrollar este cuadro clínico durante el ingreso hospitalario es reciente. Los primeros estudios25,27–29 datan de la década de los 90, y exceptuando la validación de Litaker et al en 200131 sobre la Clinical Prediction Rule (Marcantonio, 1994), no se retoma esta línea de investigación hasta hace escasamente 3 años26,32–35. Por otra parte, son pocos los estudios que intentan validar un instrumento anterior26,30,31. En España no se ha publicado ninguna investigación de este tipo.
Las razones en la escasez y en la heterogeneidad de los estudios pueden deberse tanto a diferencias metodológicas (tipo de población estudiada, diferencias en la medición de un mismo ítem) como a la misma naturaleza del delirium (de etiología multifactorial y aparición en cualquier tipo de paciente mayor ingresado).
Las diferencias entre las poblaciones estudiadas junto con el hecho de que cualquier paciente mayor hospitalizado presenta un riesgo potencial de delirium, ha generado una gran variedad de instrumentos predictivos: para pacientes de medicina general25,27,28,34, pacientes quirúrgicos29,31–33, y de unidades de urgencias35. Incluso considerando solo a pacientes quirúrgicos, el tipo de cirugía puede introducir heterogeneidad: por ejemplo, la intervención urgente de fractura de cadera está asociada con un mayor riesgo inherente de desarrollar delirium que la cirugía ortopédica electiva36. Se puede observar, al comparar los instrumentos descritos para pacientes quirúrgicos, como varía el «perfil» de riesgo según las características de las poblaciones de estudio: Litaker et al31, incorporan como predictor en la CCC Score la «admisión en neurocirugía» (que constituye un 23% de la cohorte de desarrollo), mientras que Marcantonio et al29, no incluyen este tipo de intervención en su muestra, e identifican otros predictores quirúrgicos en su Clinical Prediction Rule.
La edad avanzada es otro factor de riesgo que se incluye solo en algunos instrumentos, también probablemente debido a los criterios de selección de la muestra. Aquellas reglas predictivas en las que no se incluye la edad como ítem, proceden de estudios en los que la edad de corte mínima para participar era de 6033, 6535 o 70 años25,26,28,34, lo que puede debilitar la fuerza predictiva de esta variable en relación al delirium.
Otros ítems, en cambio, aparecen únicamente en uno de los instrumentos revisados, apuntando otra vez a la influencia del tipo de población estudiado: el uso preoperatorio de narcóticos, la historia previa de delirium31, la comorbilidad34, el deterioro auditivo35, o la depresión y la historia previa de ACV/AIT33.
No obstante, hay que señalar que también existen puntos comunes. El deterioro cognitivo previo ha mostrado ser un predictor independiente del delirium y forma parte de instrumentos predictivos dirigidos a pacientes quirúrgicos29,31,33, pacientes de medicina general25,27 y pacientes de unidades de urgencias35, hecho que sugiere que esta variable posee un peso importante a la hora de cuantificar el riesgo de delirium en cualquier tipo de paciente.
Otro motivo que explica la diversidad y escasez de los resultados es la etiología multifactorial del cuadro. Los factores de riesgo predisponentes y precipitantes del delirium descritos en la literatura son numerosos y además, se interrelacionan en un fenómeno de doble gradiente9,28. A pesar de la importancia de esta diferenciación, un número considerable de escalas predictivas29,31–33 no la tienen en cuenta. Solamente los trabajos de Inouye et al consideran de forma explícita esta distinción, generando instrumentos basados en factores de vulnerabilidad25, en factores precipitantes28 o en ambos34.
Finalmente, otra fuente de heterogeneidad en los resultados puede estar relacionada con el uso de diferentes métodos para medir un mismo factor de riesgo36. Por ejemplo, el deterioro cognitivo se mide habitualmente mediante el Mini-Mental Status Exam25,29,31, aunque también se usan otras escalas como el short Informant Questionnaire of Cognitive Decline (IQCODE) o la información de la historia clínica35. El consumo de alcohol es medido por Litaker et al31 mediante el cuestionario CAGE, mientras que Marcantonio et al preguntan directamente al paciente si «tiene actualmente algún problema por beber demasiado alcohol»29.
Llegados a este punto, es necesaria una reflexión sobre el motivo que subyace al hecho de que ninguno de estos instrumentos haya calado en la práctica clínica. Una de las razones puede ser la ya comentada heterogeneidad de herramientas, específicas para uno u otro tipo de pacientes: no existe una herramienta «general», que mida la vulnerabilidad de una persona a padecer delirium independientemente del motivo de ingreso. Por otra parte, son herramientas complejas, compuestas por ítems que a su vez, se miden con otras escalas, lo que requiere tiempo y esfuerzo y aumenta la carga de trabajo de los profesionales que atienden a este tipo de pacientes. Finalmente, la falta de interés de los propios autores para validar sus instrumentos en otras muestras de pacientes, junto con la escasez de estudios de validación de otros investigadores, ha resultado en una falta de suficiente evidencia clínica que respalde su aplicación a la práctica.
Sin embargo, es indispensable considerar la complejidad que envuelve al delirium como cuadro clínico y cuestionarse la viabilidad de construir y aplicar una herramienta predictiva de este tipo. La gran diversidad de factores predisponentes y precipitantes (algunos de ellos específicos de un tipo concreto de usuario), las interrelaciones estrechas que existen entre estos factores de riesgo, y el aumento de la carga de trabajo asociada al uso de instrumentos predictivos complejos, son algunas de las razones que deben considerarse para sopesar los costes y beneficios de una herramienta predictiva de delirium en la práctica clínica. Especialmente si se tiene cuenta que su uso no es imprescindible para la aplicación de medidas preventivas a la población de riesgo.
Así pues, es necesario plantear qué estrategia preventiva presenta mejor relación coste beneficio: la aplicación de medidas preventivas de delirium a la población general de ancianos hospitalizados, o por el contrario, la intervención únicamente en aquellos grupos de riesgo elevado o moderado de presentar el cuadro, identificados en base a una herramienta predictiva de delirium.
Las futuras líneas de investigación emergen de esta situación y reclaman la atención de los investigadores interesados en el delirium y en sus consecuencias: la validación en español de alguno de los instrumentos ya construidos, o el impacto que el uso de estas herramientas tiene sobre los resultados en pacientes o profesionales, son algunas de ellas.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Al Dr. Josep Pérez-Castelló y a Joan de Pedro Gómez, por su colaboración en la revisión del documento.
EurosSCORE: European System for Cardiac Operative Risk Evaluation. Es una escala con un rango de 0–100%, y está constituida por la combinación de varios factores de riesgo para la cirugía cardiaca (emergencia, fracción de eyección reducida, disfunción neurológica, enfermedad pulmonar crónica, etc.)32