As novas diretrizes da Organização Mundial de Saúde (OMS) para o uso de drogas antirretrovirais na prevenção e no tratamento de infecção pelo vírus HIV foram publicadas agora, em março de 2016. No entanto, desde o final de 2015 algumas dessas proposições já estão disponíveis no site da OMS. A principal mudança em relação às diretrizes de 2013 é a recomendação de tratar a todos os pacientes, independente da contagem de células TDC4 – recomendação esta válida para adultos, adolescentes e crianças. O tratamento de pacientes com doença clínica mais avançada (estágios clínicos 3 ou 4 da OMS) ou com níveis de linfócitos TCD4 inferiores a 350 células/mL ainda é definido como prioritário. No entanto, diversas evidências sólidas, publicadas desde a última versão das diretrizes, em 2013, reforçaram o tratamento imediato. Os ensaios clínicos randomizados detalhados nos estudos START, TEMPRANO e HPTN52 comprovando que o tratamento precoce leva a menores taxas de morbidade e mortalidade para os pacientes e menor transmissão do vírus, com potencial impacto no controle mundial da epidemia, constituem o arcabouço teórico racional que deu sustentação às novas diretrizes da OMS. 1
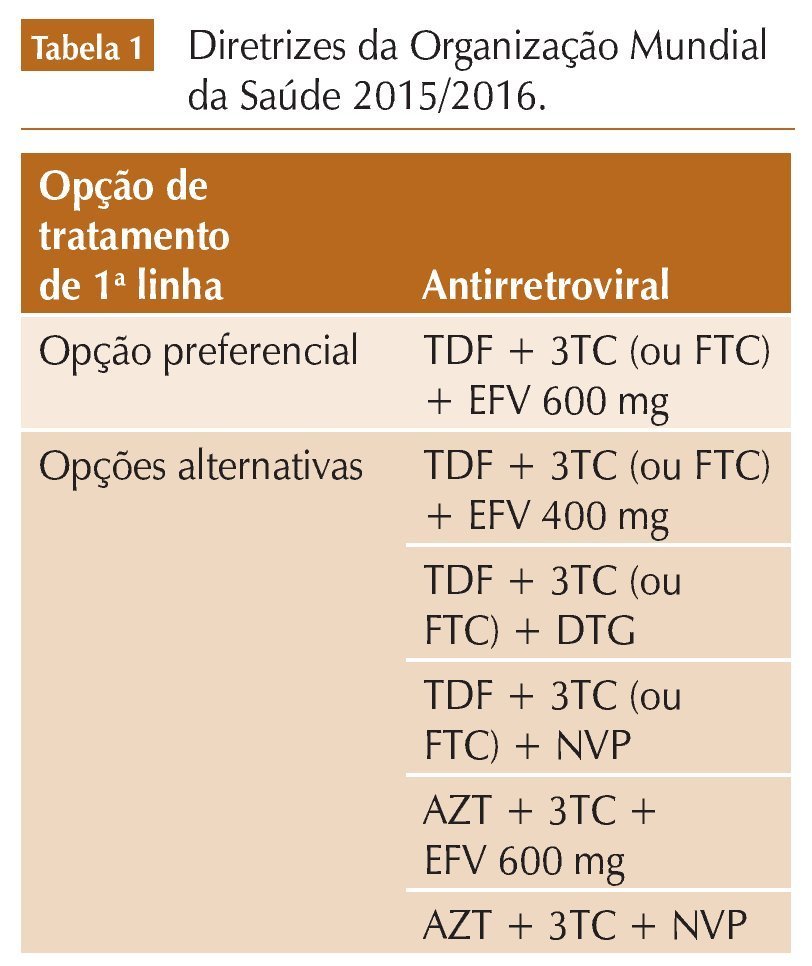
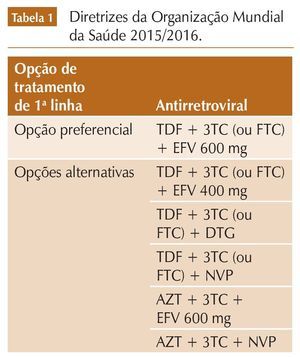
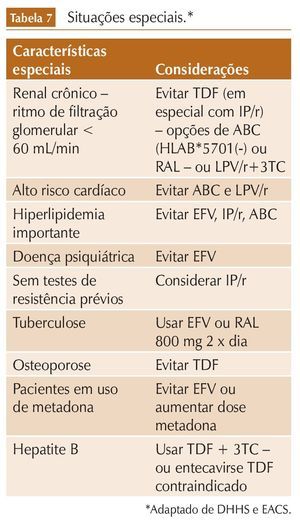
Em relação a que drogas utilizar, a OMS mantém como opção preferencial a combinação de tenofovir (TDF) + lamivudina (3TC) ou emtricitabina (FTC) + efavirenz (EFV) em dose padrão de 600 mg, com início em adultos e adolescentes virgens de tratamento. Essa opção é justificada com base em eficácia, tolerabilidade, conveniência, disponibilidade em combinações fixas, compatibilidade com tratamento de comorbidades (como tuberculose) e potencial de uso em várias e diferentes populações2 (tabela 1). A OMS justifica a limitação de apenas uma opção preferencial com o objetivo de simplificar o tratamento.
Significativa novidade na diretriz da OMS é a inclusão do dolutegravir e do EFV como opções alternativas para início de tratamento.
Uma significativa novidade na dire-triz da OMS é a inclusão do dolutegravir (DTG) e do EFV em dose de 400 mg, mais baixa que a usual (600 mg), como opções alternativas para início de tratamento. O DTG é justificado por sua eficácia virológica, com grande barreira genética, poucas interações e baixas taxas de interrupção de tratamento. O EFV de 400 mg tem eficácia comparada à dose maior (600 mg) desta droga, com menor toxicidade e potencial de reduzir custos e mesmo o tamanho da pílula. A OMS argumenta em seu site que essas duas drogas não são classificadas, no momento, como opções preferenciais em razão do uso ainda limitado fora de ensaios clínicos, e ainda por dúvidas em eficácia e segurança em pacientes gestantes e naqueles com coinfecção HIV-tuberculose. A zidovudina (AZT) e a nevirapina (NVP) são mantidas como opções alternativas (tabela 1), com a justificativa de que as novas alternativas já descritas ainda demandam algum tempo para sua disponibilidade mais ampla.
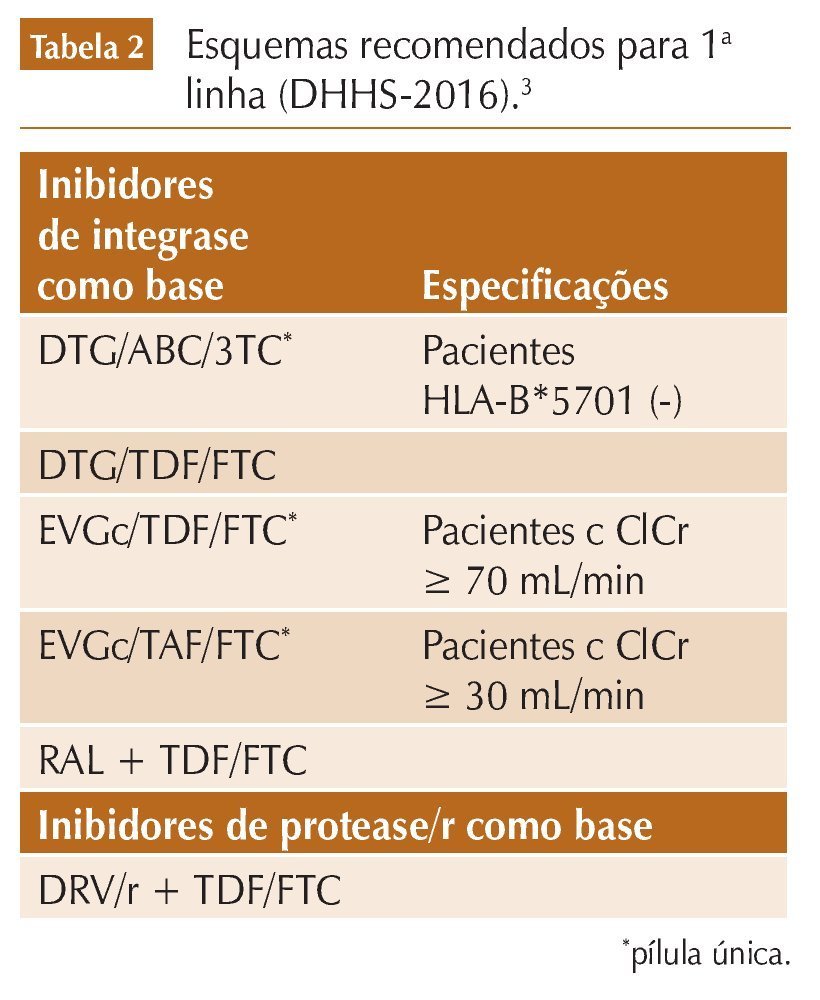
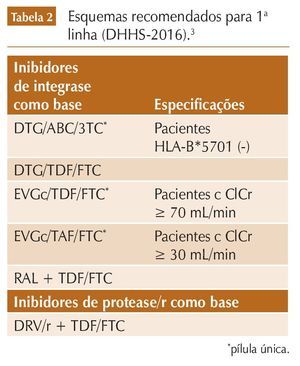
O Department for Health and Human Services (DHHS, Departamento de Saúde e Serviços Humanos) dos EUA atualizou suas diretrizes para uso de antirretrovirais em adultos e adolescentes, em janeiro de 2016.3 Desde 2012, o DHHS recomendava iniciar tratamento em todos os indivíduos infectados pelo HIV, independente da contagem de células CD4. A novidade é a expressão de grau de evidência mais sólida – A1 – para início em todos os extratos de CD4. A marca mais significativa de como começar a terapia na nova diretriz americana é o predomínio dos inibidores de integrase (INI) entre os esquemas escolhidos para início de tratamento em pacientes virgens de terapia. Entre os seis esquemas recomendados para primeira linha, cinco são com INI; apenas um com inibidor de protease reforçado com ritonavir (IP/r), e nenhum com inibidor da transcriptase reversa do HIV-1 análago de não nucleosídio (ITRNN) (tabela 2). A preferência pelos INI, que parece ser uma tendência que vem se firmando nos países desenvolvidos, deve-se, segundo o painel, à sua elevada eficácia, aos poucos efeitos colaterais e à redução das interações com drogas associadas ao citocromo CYP 3A4. O DHHS sugere que esquemas com DTG, raltegravir (RAL) ou elvitegravir (EVG) sejam usados na maioria dos pacientes, com exceção daqueles com aderência incerta ou quando o tratamento precisa começar antes da disponibilidade de resultados de testes de resistência – situações em que a maior barreira genética dos IP com booster, representado no consenso pelo darunavir/r (DRV/r), os tornam a melhor opção de escolha.
O DTG está em duas opções de início, com TDF + FTC ou com abacavir (ABC) + 3TC. O painel sustenta essas opções com base em três ensaios clínicos principais, nos quais o DTG foi superior ao EFV (SPRING), superior ao DRV/r (FLAMINGO), e não inferior ao RAL (SPRING 2). Entre as poucas interações, devem ser lembrados o aumento do nível sérico de metformina (2 × em média), a necessidade de ajuste de dose com rifampicina (DTG 50 mg 2 × dia) e o cuidado de não o usar próximo de antiácidos contendo cálcio/magnésio ou laxantes (recomendado 2 horas antes ou 6 horas depois).
O EVG também está disponível em duas opções. A primeira é a associação com TDF + FTC e cobicistat (COBI), em pílula única. O COBI é um potente inibidor do citocromo CYP3A, sem atividade anti-HIV, que funciona como potenciador do INI, permitindo seu uso em dose única. Essa associação não é recomendada em pacientes com clearance de creatinina < 70 mL/min. A segunda opção, muito recentemente aprovada pela Food and Drug Administration, é a nova combinação em pílula única de tenofovir alafenamida (TAF) com FTC e EVG/COBI. O TAF é uma pró-droga do TDF, disponível em dosagem de 10 mg, nessa combinação (com INI). Enquanto o TDF disoproxil clássico é convertido a TDF no plasma e depois a TDF difosfato nas células linfoides, o TAF permanece na forma de pró-droga até entrar nas células linfoides. O TAF teria, assim, eficácia semelhante ao TDF, com menor toxicidade renal e óssea. Essa nova associação pode ser usada em pacientes com clearance de creatinina ≥ 30 mL/min. Existem planos de combinações em dose fixa de TAF na dose de 25 mg em associação com IP e ITRNN.
O RAL segue disponível com TDF e FTC. Essa é a única opção do painel para primeira linha com esse INI.
Com relação às duplas de nucleosídios, TDF/FTC ainda é o mais indicado. ABC deve ser usado apenas em pacientes com HLAB*5701(-) e pode, quando associado ao DTG, ser usado com segurança até em pacientes com carga viral pré-tratamento > 100.000 cópias/mL.
Nas diretrizes americanas, o EFV passou a ser considerado uma opção alternativa, e não mais preferencial.
Nas diretrizes americanas, o EFV passou a ser considerado uma opção alternativa, e não mais preferencial, pela primeira vez em muitos anos, em razão de preocupações com tolerância a longo prazo, com maior descontinuação de tratamentos por causa de toxicidade do sistema nervoso central e possível associação com suicídios.4 O atazanavir/r (ATV/r) também foi movido de opção preferencial para alternativa, em razão de maior interrupção por toxicidade em grande ensaio clínico, quando comparado com DRV/r ou RAL.5
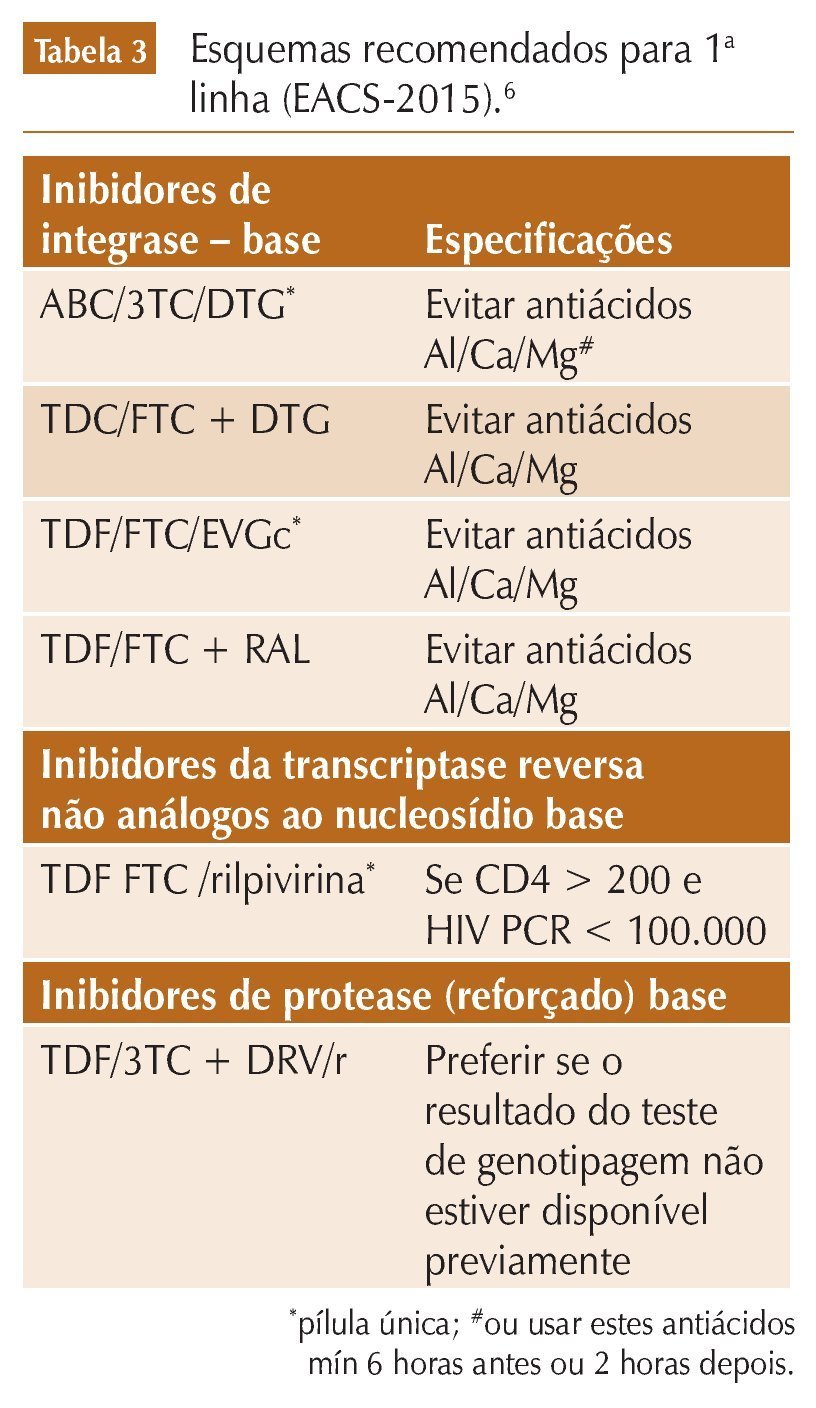
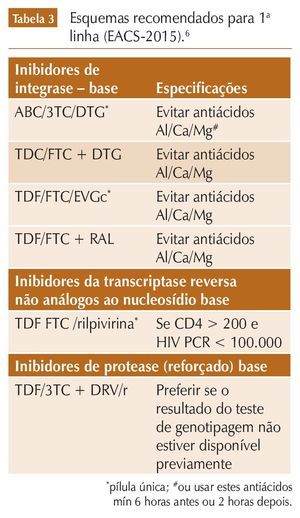
Em outubro de 2015, a European AIDS Clinical Society (EACS) atualizou suas diretrizes de tratamento, já na oitava versão.6 O tratamento também é indicado para todos os pacientes, com a ressalva de possível exceção para os controladores de elite com níveis altos e estáveis de células TD4. O teste de resistência genotípica é sempre recomendado antes do início do tratamento, da mesma maneira que nas diretrizes do DHHS. Caso os testes de resistência não estejam disponíveis antes do tratamento, também é recomendado incluir um IP reforçado no esquema a ser usado. Há quatro esquemas de primeira linha recomendados tendo como base o uso de INI (DTG, EVG e RAL), um tendo ITRNN (rilpivirina – RPV) e um com IP reforçado (DRV/r). Todos usam TDF/FTC como esqueleto base, exceto por uma associação ABC-3TC com DTG (tabela 3).
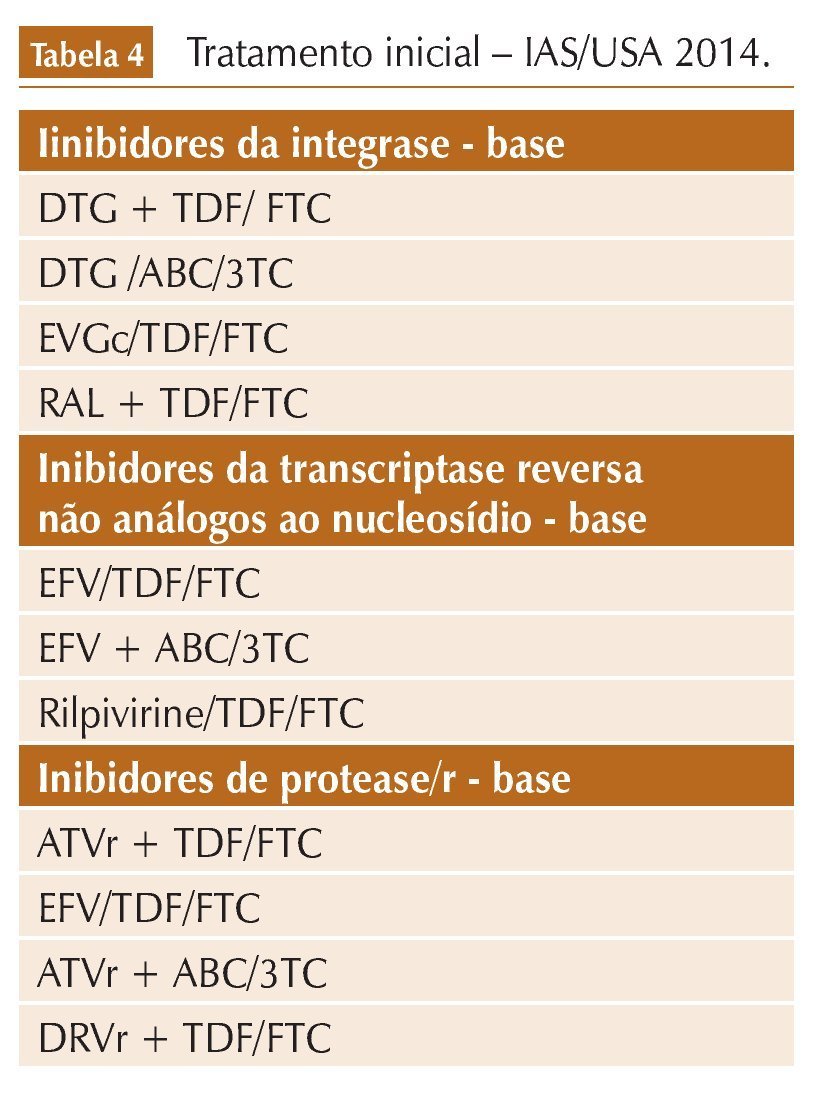
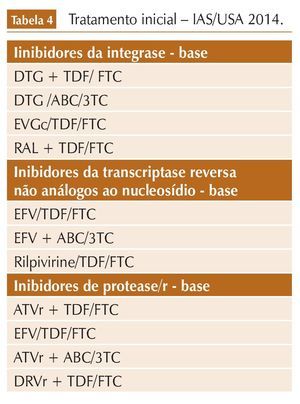
A diretriz do IAS-USA7 (painel americano da Sociedade Antiviral Internacional) é de meados de 2014, ainda não atualizada recentemente. Esse painel elenca 10 regimes para tratamento inicial – quatro com INI, três com IP reforçado e três com ITRNN (tabela 4). O tratamento já era indicado para todos os pacientes infectados, independente dos níveis de CD4.
A associação britânica de HIV atualizou suas diretrizes de tratamento de adultos em 2015. O esqueleto de tratamento com ITRN ainda é TDF-FTC, com ABC-3TC como alternativa. Como terceiro agente na associação, são sugeridos dois IP (ATV/r e DRV/r), três INI (DTG, EVG e RAL) e um ITRNN (RPV). O EFV também deixou de ser uma droga preferencial para os britânicos, e foi movido para a categoria de drogas alternativas no tratamento. A diretriz inglesa sustenta como base dessa decisão, também, a maior frequência de interrupção de tratamento com EFV e o maior risco de suicídios com meta-análise de estudos Aids Clinical Trials Group (ACTG).4
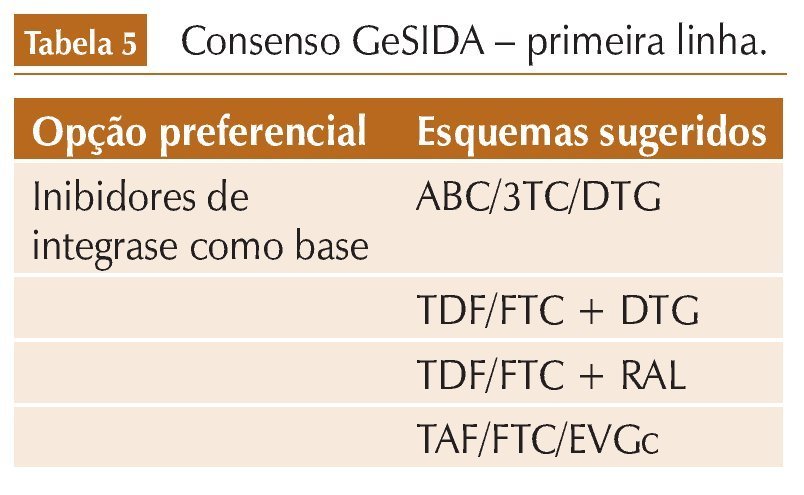
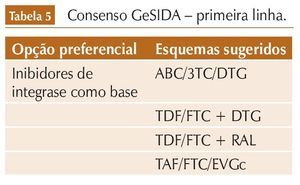
O documento de consenso do GeSIDA (Espanha) foi atualizado em janeiro de 2016 e contém somente INI como opções preferenciais de tratamento de HIV em primeira linha.
O documento de consenso do GeSIDA (Espanha) foi atualizado em janeiro de 2016 e contém somente INI como opções preferenciais de tratamento de HIV em primeira linha (virgens de terapia).9 A diretriz espanhola já contempla o TAF em uma das opções de primeira linha em coformulação com FTC, EVG e COBI (tabela 5).
O Protocolo Clínico e as Diretrizes Terapêuticas para manejo da infecção pelo HIV em adultos do Ministério da Saúde do Brasil é de 2013, e não foi atualizado recentemente. Desde então, a diretriz brasileira já recomendava tratamento para todas as pessoas vivendo com HIV e AIDS, independente de contagem de células CD4, antes mesmo dos resultados dos estudos SMART e TEMPRANO, mas já com as notícias de impacto na transmissão e no controle da epidemia (HPTN52). O protocolo recomenda enfaticamente a opção por um único esquema preferencial, o TDF-3TC-EFV em pílula única, com dose fixa combinada. Em casos de contraindicação ao TDF, devem ser usados, em ordem de preferência, AZT ou ABC ou didanosina. Em caso de contraindicação ou intolerância ao EFV, a primeira opção indicada é a NVP.10 O consenso comenta o risco maior de toxicidade hepática com a NVP em estudos na Tailândia, em especial em mulheres com linfócitos TCD4 ≥ 200 células/mL e em homens com CD4 ≥ 400 células/mL. Considerando o tratamento precoce corretamente defendido pelo próprio protocolo, esse risco potencial é um enorme obstáculo ao uso da NVP nessa escala sugerida. Em situações em que esteja impossibilitado o uso de EFV ou NVP, o consenso determina como segunda linha de tratamento de pacientes virgens de terapia o uso de IP, com preferência pelo lopinavir/r (LPV/r), “em razão da coformulação, experiência de uso, maior número de estudos clínicos, potência e durabilidade, menor custo e facilidades logísticas”. As alternativas ao uso de LPV/r são, também pela ordem, ATV/r e fosamprenavir/r (FPV/r) (tabela 6).
O Brasil é pioneiro na distribuição de drogas antivirais à população vivendo com HIV-AIDS.
O Brasil é pioneiro na distribuição de drogas antivirais à população vivendo com HIV-AIDS. O programa atendia, em janeiro de 2016, a cerca de 455.000 pessoas. É evidente que a sustentabilidade do programa é essencial ao controle da epidemia no país, e quaisquer decisões que afetem esquemas preferenciais têm que ser analisadas à luz de custos e fármaco-economia. No entanto, é imperioso refletir se os atuais esquemas preferenciais permitem ao país cumprir a meta de 90/90/90 (90% dos pacientes diagnosticados; 90% tratados; e 90%, sob controle virológico), definida pela UNAIDS, em termos de adesão, interrupção de tratamento por efeitos colaterais etc. Também a opção única por esquemas de ITRNN com menor barreira genética, sem disponibilidade de testes de resistência antes de iniciar o tratamento, é outro ponto que desperta polêmica, em razão de taxas de resistência primária aos INNTR já registradas em algumas cidades brasileiras.
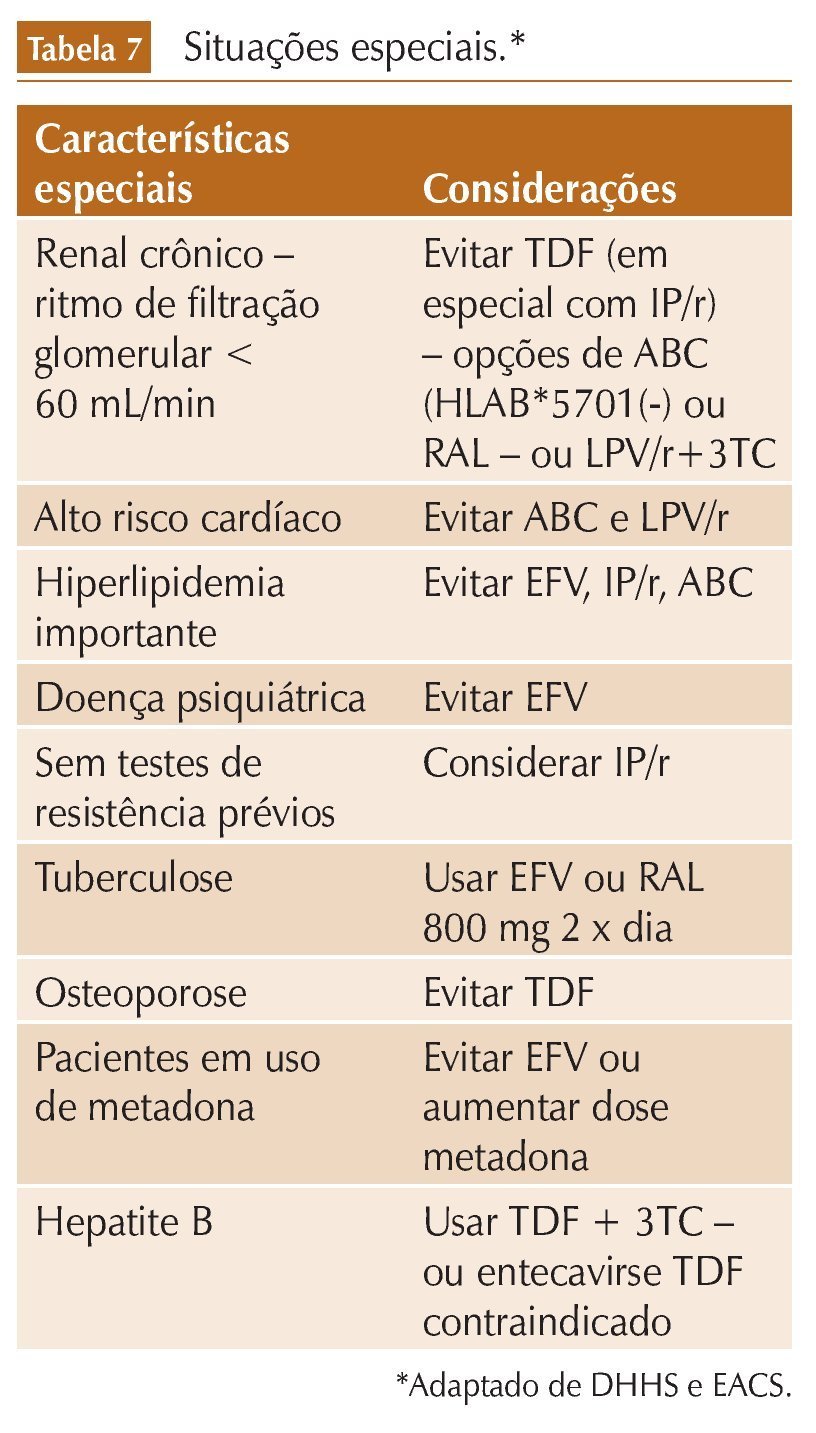
Em uma situação ideal, na qual fosse possível individualizar a terapia de acordo com as características especiais do paciente a ser tratado, o DHHS e EACS sugerem adaptar o esquema de acordo com a tabela 7. Considerando que nas circunstâncias atuais ainda não se dispõe de cura, até porque não há como eliminar os reservatórios do vírus HIV no organismo, é necessário estruturar uma terapia antirretroviral por décadas de vida, que seja efetiva e possa interferir menos possível na qualidade de vida das pessoas vivendo com HIV/AIDS.
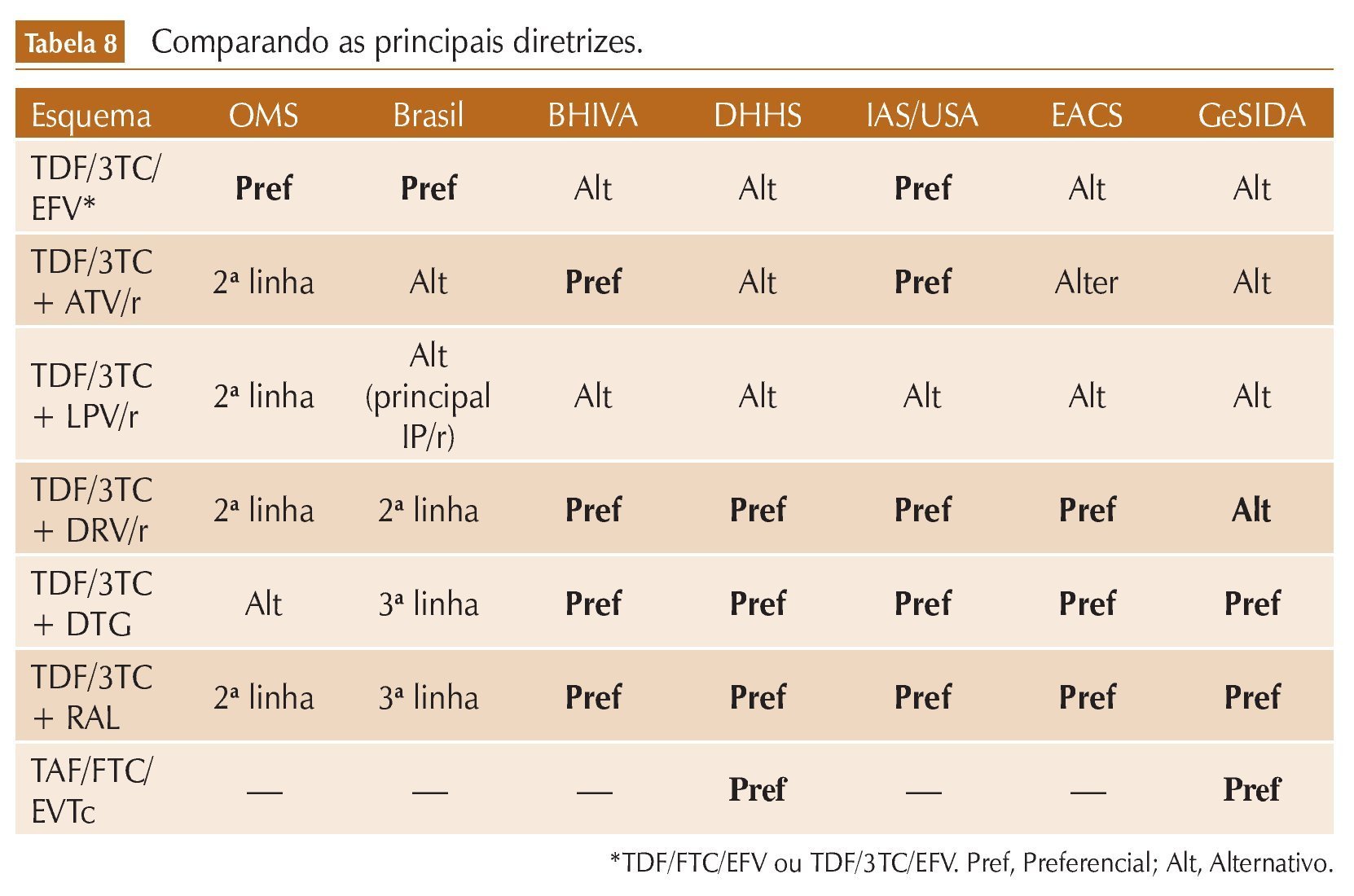
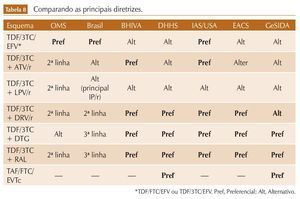
Concluindo, a tabela 8 compara a posição de alguns dos principais esquemas como preferencial ou alternativos nas diferentes diretrizes.