Las prótesis aorticas de rápido despliegue aparecieron hace 10 años para tratar la estenosis aórtica. El sistema de válvula Edwards Intuity es una prótesis biológica basada en la válvula Edwards Magna con un marco infraanular. Presentamos los resultados clínicos y hemodinámicos a corto y largo plazo obtenidos con esta prótesis biológica.
MétodosCiento diecisiete pacientes (65% varones, 75±4,5 años) con estenosis aórtica (gradiente medio preoperatorio de 49,6±12mmHg) recibieron una prótesis Edwards Intuity entre septiembre de 2012 y diciembre de 2019. Se incluyeron en una base de datos prospectiva que recogía diferentes variables. La media de seguimiento fue de 36±21meses.
ResultadosMortalidad hospitalaria del 3,4%, supervivencia al año, a los 3 y 6 años del 95%, 90% y 81%, respectivamente. Se utilizó hemiesternotomía media superior en 78 pacientes (67%). La mediana de tiempos de isquemia miocárdica y de circulación extracorpórea de toda la serie fueron 40 (33-50) minutos y 59 (48-73) minutos. Gradientes medios al alta, al año y a los 2 años fueron 10±4mm, 9±3,5mm y 8,4±3,4mmHg. Ocho pacientes (7%) necesitaron marcapasos en el postoperatorio. Dos pacientes (0,6%) se reintervinieron en seguimiento por endocarditis y otro (0,3%) se reintervino por fuga periprotésica.
ConclusiónEl sistema de válvula Edwards Intuity presenta buenos resultados clínicos y hemodinámicos a corto y largo plazo. Estas prótesis aórticas se pueden considerar una alternativa a las prótesis convencionales, sobre todo en cirugía de mínimo acceso y en intervenciones complejas.
Rapid deployment aortic valves appeared ten years ago to treat aortic stenosis. The Edwards Intuity Valve System is a biological prosthesis based on the Edwards Magna valve with an infra-annular framework. We present the short and long-term clinical and hemodynamic results obtained with this biological prosthesis.
MethodsOne hundred seventeen patients (65% male, 75±4.5 years) with aortic stenosis (mean preoperative gradient of 49.6±12mm Hg) received an Edwards Intutiy prosthesis between September 2012 and December 2019. They were included in a prospective data base that collected different variables. The mean follow-up was 36±21 months.
ResultsHospital mortality of 3.4%. Survival at one, three and six years of 95%, 90% and 81%, respectively. Upper hemisternotomy was used in 78 patients (67%). The median times of myocardial ischemia and extracorporeal circulation for the entire series were 40 (33-50) minutes and 59 (48-73) minutes. Average gradients at discharge, one year and two years were 10±4mm, 9±3.5mm and 8.4±3.4mmHg. Eight patients (7%) required pacemakers in the postoperative period. Two patients (0.6%) underwent surgery for endocarditis and another (0.3%) underwent surgery for periprosthetic leak.
ConclusionThe Edwards Intutiy valve system presents good short and long term clinical and hemodynamic results. These aortic prostheses can be considered an alternative to conventional prostheses, especially in minimal access surgery and in complex interventions.
La estenosis aórtica sintomática es actualmente la forma más común de enfermedad valvular cardiaca en los países desarrollados1. Habitualmente se trata mediante el reemplazo de la válvula aórtica nativa enferma, bien con cirugía convencional, bien con técnica transcatéter2. La cirugía convencional ha sido el tratamiento de elección en los últimos 50 años para todos los casos, aunque ahora se utiliza sobre todo en los casos de riesgo preoperatorio bajo o intermedio, o en aquellos pacientes que necesitan de procedimientos combinados.
En la cirugía convencional de la estenosis aórtica se ha producido un cambio significativo hacia un mayor uso de prótesis biológicas en posición aórtica debido, por un lado, al envejecimiento progresivo de la población, y por otro a una mayor duración y excelente comportamiento hemodinámico de dichas prótesis3,4.
En la última década han aparecido las prótesis aórticas de rápido despliegue (PARD) para el tratamiento quirúrgico convencional de la estenosis aórtica sintomática. Las PARD acortan los tiempos quirúrgicos y facilitan los abordajes quirúrgicos menos agresivos, simplificando así todo el proceso quirúrgico5–10.
En 2016 publicamos nuestra experiencia inicial con la PARD Edwards Intuity11. El objetivo principal del presente trabajo es presentar los resultados clínicos y hemodinámicos a corto y largo plazo con el sistema de válvula Edwards Intuity en nuestro centro en los últimos 7 años.
Los objetivos del estudio fueron los análisis de la mortalidad a corto y largo plazo, la detección de deterioro protésico estructural o no estructural a corto y largo plazo y el estudio de la función hemodinámica de la prótesis con ecocardiografía transtorácica. Se recogió también la aparición de cualquier evento adverso relacionado con la prótesis en estudio, de acuerdo con las guías publicadas para informar de mortalidad y morbilidad después de cirugía valvular cardiaca, tanto a corto como a largo plazo12. Se recogieron las reintervenciones, tanto precoces como en el seguimiento.
Material y métodosEste es un estudio observacional y prospectivo en el que se registraron todos los pacientes a los que se les implantó una PARD Edwards Intuity (tanto el modelo 8300A como el modelo 8300AB o Elite) en nuestro hospital, entre septiembre de 2012 y diciembre de 2019.
Los criterios de inclusión y exclusión fueron descritos anteriormente11. De forma resumida, se incluyeron pacientes con estenosis aórtica severa o con doble lesión aórtica con predominio de la estenosis. Los pacientes con insuficiencia aórtica severa, dilatación de la aorta ascendente o de la raíz aórtica o con endocarditis aguda fueron excluidos.
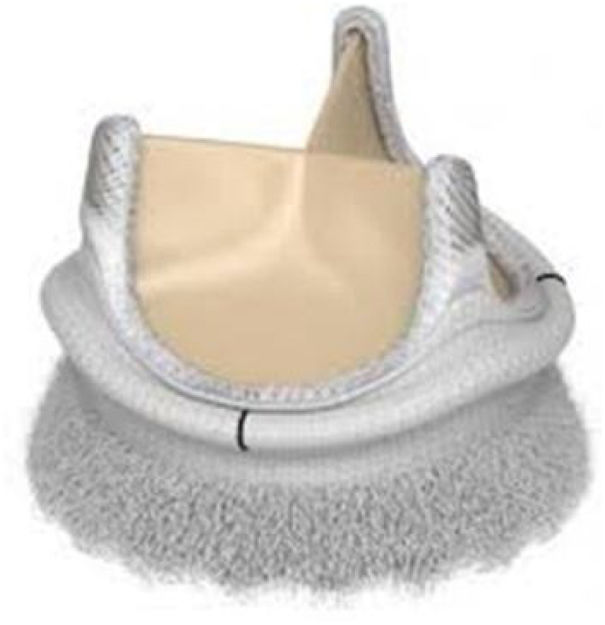
El abordaje del corazón se realizó bien mediante una esternotomía media completa (EMC), bien mediante una hemiesternotomía media superior (HEMS) según criterio del cirujano. La prótesis Edwards Intuity se basa en la prótesis aórtica biológica de pericardio Carpentier-Edwards Perimount Magna Ease, a la que se ha añadido un marco expandible de acero inoxidable infraanular (fig. 1). El procedimiento de implante de esta prótesis es sencillo11. Tras una aortotomía en palo de hockey hacia seno no coronario se realiza la resección de la válvula aórtica nativa y la decalcificación habitual del anillo aórtico; se utilizan 3 suturas guía en el nadir de los senos aórticos, se coloca la prótesis en posición supraanular, se despliega el marco infraanular con balón a una presión entre 3 y 5 atmosferas, según el tamaño de la prótesis, durante 10s y se anudan las 3 suturas guía.
Se registraron las variables clínicas y demográficas de cada paciente, el tratamiento previo, la situación funcional preoperatoria y la analítica basal preoperatoria. Se analizaron también el ECG y la ecografía transtorácica preoperatorias. El riesgo preoperatorio se calculó con la escala EuroScore13,14. Se recogieron variables operatorias de interés como la vía de abordaje, el tipo de prótesis implantada, la presencia de cirugía asociada, el tiempo de isquemia miocárdica, el tiempo de circulación extracorpórea (CEC) y la necesidad de reintervención por sangrado o por problemas esternales.
Se realizó un seguimiento clínico a los 3 meses y anualmente tras el alta hospitalaria. Se registraron diversas variables, incluyendo el éxito en el implante, la mortalidad periprocedimiento (≤30 días) y tardía (>30 días), la necesidad de marcapasos permanente (MPP) en el postoperatorio inmediato y en el seguimiento, la necesidad de reoperación precoz o tardía y su causa, la necesidad de transfusión durante el ingreso y los días de estancia en la unidad de cuidados intensivos y en el hospital. También se registraron los reingresos hospitalarios tras el alta y su causa, los episodios tromboembólicos, los episodios de sangrado, las fugas periprotésicas (FPP) y las endocarditis precoces y tardías.
Consideraciones éticasLos pacientes fueron informados y dieron su consentimiento para la recogida y análisis de sus datos clínicos. El trabajo cuenta con la valoración y aprobación del Comité Ético de Investigación Clínica del Hospital Clínico Universitario Virgen de la Arrixaca de Murcia (Área I del Servicio Murciano de Salud).
Análisis estadísticoLas variables cualitativas fueron expresadas como frecuencias y sus porcentajes y comparadas mediante el test de la Chi cuadrado de Pearson. Las variables cuantitativas fueron sometidas a una prueba de homogeneidad de Kolmogorov-Smirnov. Aquellas variables cuantitativas con distribución normal se expresaron como media±desviación estándar y fueron comparadas mediante el test de la «t» de Student. Aquellas variables cuantitativas con distribución no normal fueron expresadas como mediana y rango intercuartílico (25-75%) y fueron comparadas con el test de la U de Mann-Whitney. Las variables continuas se compararon mediante las correlaciones de Pearson, de Spearman o de Tau-b de Kendall, según tuvieran distribución normal o no. Se utilizó el método de estimación de Kaplan-Meier para conocer las diferencias en la supervivencia. La tasa anual de eventos durante el seguimiento se estimó como el cociente del número de eventos totales y el tamaño muestral entre el tiempo de seguimiento en años multiplicado por 100.
El programa estadístico utilizado fue el SPSS versión 24.0 (SPSS. IBM. Chicago, IL®). Se consideró significación estadística una p<0,05.
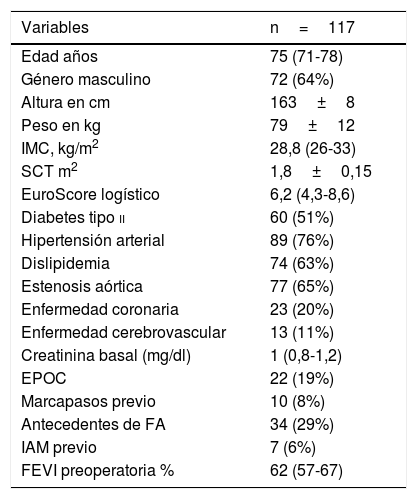
ResultadosSe implantó la PARD Edwards Intuity en un total de 117 pacientes. La mediana de edad fue de 75 (71-78) años y 76 (64%) eran varones. A 25 (22%) pacientes se les implantó el modelo 8300A entre septiembre de 2012 y febrero de 2014 y al resto de la serie (92, 78%) se les implantó el modelo 8300AB o Elite entre abril de 2014 y diciembre de 2019. En el 56% de serie los pacientes estaban en una clase funcional de la NYHA 3 o 4, y la mediana de la clase funcional preoperatoria fue de 3 (2-3). El riesgo de mortalidad preoperatoria según el Euroscore logístico fue 6,2 (4,3-8,6). El diagnóstico del 65% de los pacientes fue estenosis aórtica aislada y la mediana de la fracción de eyección preoperatoria fue de 62 (57-67). La tabla 1 recoge las variables basales de la población en estudio.
Características basales de los pacientes intervenidos
| Variables | n=117 |
|---|---|
| Edad años | 75 (71-78) |
| Género masculino | 72 (64%) |
| Altura en cm | 163±8 |
| Peso en kg | 79±12 |
| IMC, kg/m2 | 28,8 (26-33) |
| SCT m2 | 1,8±0,15 |
| EuroScore logístico | 6,2 (4,3-8,6) |
| Diabetes tipo ii | 60 (51%) |
| Hipertensión arterial | 89 (76%) |
| Dislipidemia | 74 (63%) |
| Estenosis aórtica | 77 (65%) |
| Enfermedad coronaria | 23 (20%) |
| Enfermedad cerebrovascular | 13 (11%) |
| Creatinina basal (mg/dl) | 1 (0,8-1,2) |
| EPOC | 22 (19%) |
| Marcapasos previo | 10 (8%) |
| Antecedentes de FA | 34 (29%) |
| IAM previo | 7 (6%) |
| FEVI preoperatoria % | 62 (57-67) |
EPOC: enfermedad pulmonar obstructiva crónica; FA: fibrilación auricular; FEVI: fracción de eyección del ventrículo izquierdo; IAM: infarto agudo de miocardio; IMC: índice de masa corporal; Kg: kilogramos; SCT: superficie corporal total..
En lo referente a la cirugía 20 (17%) fueron cirugías urgentes y 15 (13%) fueron cirugías combinadas (8 revascularizaciones miocárdicas [53%], 3 resecciones de miocardiopatías hipertróficas y 4 ligaduras de orejuela izquierda). Como vía de abordaje quirúrgica se utilizó la EMC en 39 pacientes (33%) y la HEMS en 78 pacientes (67%). Hubo 3 reconversiones a EMC (3,8%), las 3 por sangrado. Solo en un caso (0,9%) se utilizó la canulación periférica, en los pacientes restantes se utilizó canulación central con acceso directo en la aorta ascendente y en la orejuela derecha o la vena cava superior. En 2 pacientes sobre un total de 119 (1,7%) se cambió a una prótesis convencional, ambos casos al principio de la curva de aprendizaje por dudar sobre si la prótesis había bajado bien en pacientes con tractos de salida pequeños. Los 2 pacientes se dieron de alta sin incidencias y se excluyeron de análisis posteriores.
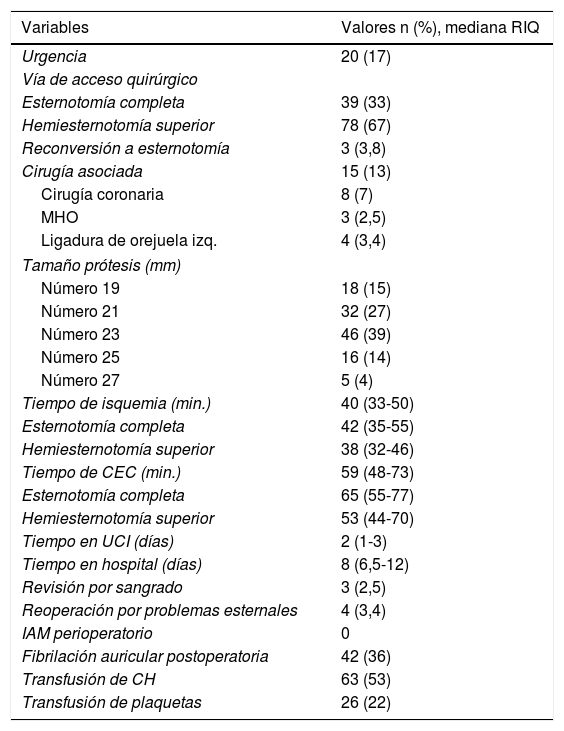
Cuarenta y seis pacientes de la serie recibieron una prótesis Edwards Intuity n.° 23 (39%), seguido por número 21 (27%), número 19 (15%), número 25 (14%) y número 27 (4%) (tabla 2). La mediana de los tiempos de isquemia miocárdica y de circulación extracorpórea de toda la serie, incluyendo los casos combinados, fueron de 40 (33-50) minutos y de 59 (48-73) minutos respectivamente. Encontramos diferencias significativas en los tiempos de CEC entre los pacientes con acceso por HEMS y los de EMC (53 [44-70] min. vs. 65 [55-77] min., p=0,02), pero no en los tiempos de isquemia miocárdica (38 [32-46] min. vs. 42 (35-55) min.; p=0,074).
Factores operatorios y eventos postoperatorios precoces de los pacientes intervenidos
| Variables | Valores n (%), mediana RIQ |
|---|---|
| Urgencia | 20 (17) |
| Vía de acceso quirúrgico | |
| Esternotomía completa | 39 (33) |
| Hemiesternotomía superior | 78 (67) |
| Reconversión a esternotomía | 3 (3,8) |
| Cirugía asociada | 15 (13) |
| Cirugía coronaria | 8 (7) |
| MHO | 3 (2,5) |
| Ligadura de orejuela izq. | 4 (3,4) |
| Tamaño prótesis (mm) | |
| Número 19 | 18 (15) |
| Número 21 | 32 (27) |
| Número 23 | 46 (39) |
| Número 25 | 16 (14) |
| Número 27 | 5 (4) |
| Tiempo de isquemia (min.) | 40 (33-50) |
| Esternotomía completa | 42 (35-55) |
| Hemiesternotomía superior | 38 (32-46) |
| Tiempo de CEC (min.) | 59 (48-73) |
| Esternotomía completa | 65 (55-77) |
| Hemiesternotomía superior | 53 (44-70) |
| Tiempo en UCI (días) | 2 (1-3) |
| Tiempo en hospital (días) | 8 (6,5-12) |
| Revisión por sangrado | 3 (2,5) |
| Reoperación por problemas esternales | 4 (3,4) |
| IAM perioperatorio | 0 |
| Fibrilación auricular postoperatoria | 42 (36) |
| Transfusión de CH | 63 (53) |
| Transfusión de plaquetas | 26 (22) |
CEC: circulación extracorpórea; CH: concentrado de hematíes; IAM: infarto agudo de miocardio; izq.: izquierda; min: minutos; MHO: miocardiopatía hipertrófica obstructiva; UCI: unidad de cuidados intensivos.
La mediana de la estancia en la UCI y en el hospital de toda la serie fueron 2 (1-3) días y 8 (6,5-12) días, respectivamente. La mortalidad hospitalaria de la serie fue de 4 pacientes (3,4%) (2 por fallo cardiaco, otro por fibrilación ventricular postoperatoria y otro por ictus postoperatorio). Hubo 2 fallecimientos entre los pacientes a los que se les realizó el recambio valvular aislado (1,9%) y otros 2 pacientes fallecieron entre los pacientes con procedimientos asociados (13% [p=0,024]). Cuatro pacientes sufrieron un accidente cerebrovascular agudo en el postoperatorio inmediato (3,4%).
Los pacientes operados mediante HEMS presentaban menor riesgo operatorio (mediana de Euroscore logístico 6 [4-8]) que aquellos operados con EMC (incluyendo los pacientes con procedimientos asociados) (mediana de Euroscore logístico de 7 [4,5-13]) (p=0,030).
Tres pacientes necesitaron revisión por excesivo sangrado postoperatorio (2,5%) y 4 (3,4%) tuvieron reoperaciones antes de los 30 días por problemas esternales. En ambos eventos no hubo significación estadística al analizar la vía de acceso (5% en EMC de reoperaciones por sangrado frente a 1,3% en HEMS; p=0,215, y 8% en EMC de reoperaciones por problemas de esternón frente a 1,3% en HEMS; p=0,072).
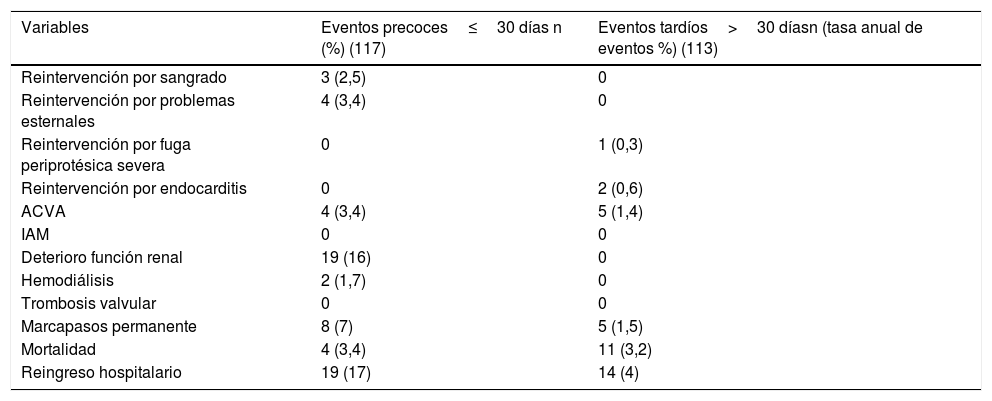
No encontramos degeneración estructural de las prótesis implantadas a corto plazo, pues solo 4 pacientes (3,5%) presentaron FPP mayor de 1 al alta hospitalaria. En relación con el estudio de valores hemodinámicos, encontramos que el gradiente transprotésico medio de toda la serie al alta fue de 10±4mmHg. La media del área de todas las prótesis al alta fue de 1,9±0,5cm2 y el área media de todas las prótesis ajustadas por la superficie corporal al alta fue de 1±0,25cm2/m2. Solo en un caso (1%) se produjo una desproporción prótesis-paciente severa y en 25 (23%) la desproporción fue moderada. Al alta hospitalaria 14 pacientes (12%) presentaban algún grado de FPP; en 10 (8,5%) era trivial y en 4 (3,5%) fue mayor de 1. Ocho pacientes necesitaron de un MPP en el ingreso (7%). Finalmente, 19 (16%) pacientes reingresaron de forma precoz en el hospital por diferentes causas. La tabla 3 recoge los eventos postoperatorios precoces y tardíos.
Eventos postoperatorios precoces y tardíos
| Variables | Eventos precoces≤30 días n (%) (117) | Eventos tardíos>30 díasn (tasa anual de eventos %) (113) |
|---|---|---|
| Reintervención por sangrado | 3 (2,5) | 0 |
| Reintervención por problemas esternales | 4 (3,4) | 0 |
| Reintervención por fuga periprotésica severa | 0 | 1 (0,3) |
| Reintervención por endocarditis | 0 | 2 (0,6) |
| ACVA | 4 (3,4) | 5 (1,4) |
| IAM | 0 | 0 |
| Deterioro función renal | 19 (16) | 0 |
| Hemodiálisis | 2 (1,7) | 0 |
| Trombosis valvular | 0 | 0 |
| Marcapasos permanente | 8 (7) | 5 (1,5) |
| Mortalidad | 4 (3,4) | 11 (3,2) |
| Reingreso hospitalario | 19 (17) | 14 (4) |
ACVA: accidente cerebrovascular agudo; IAM: infarto agudo de miocardio.
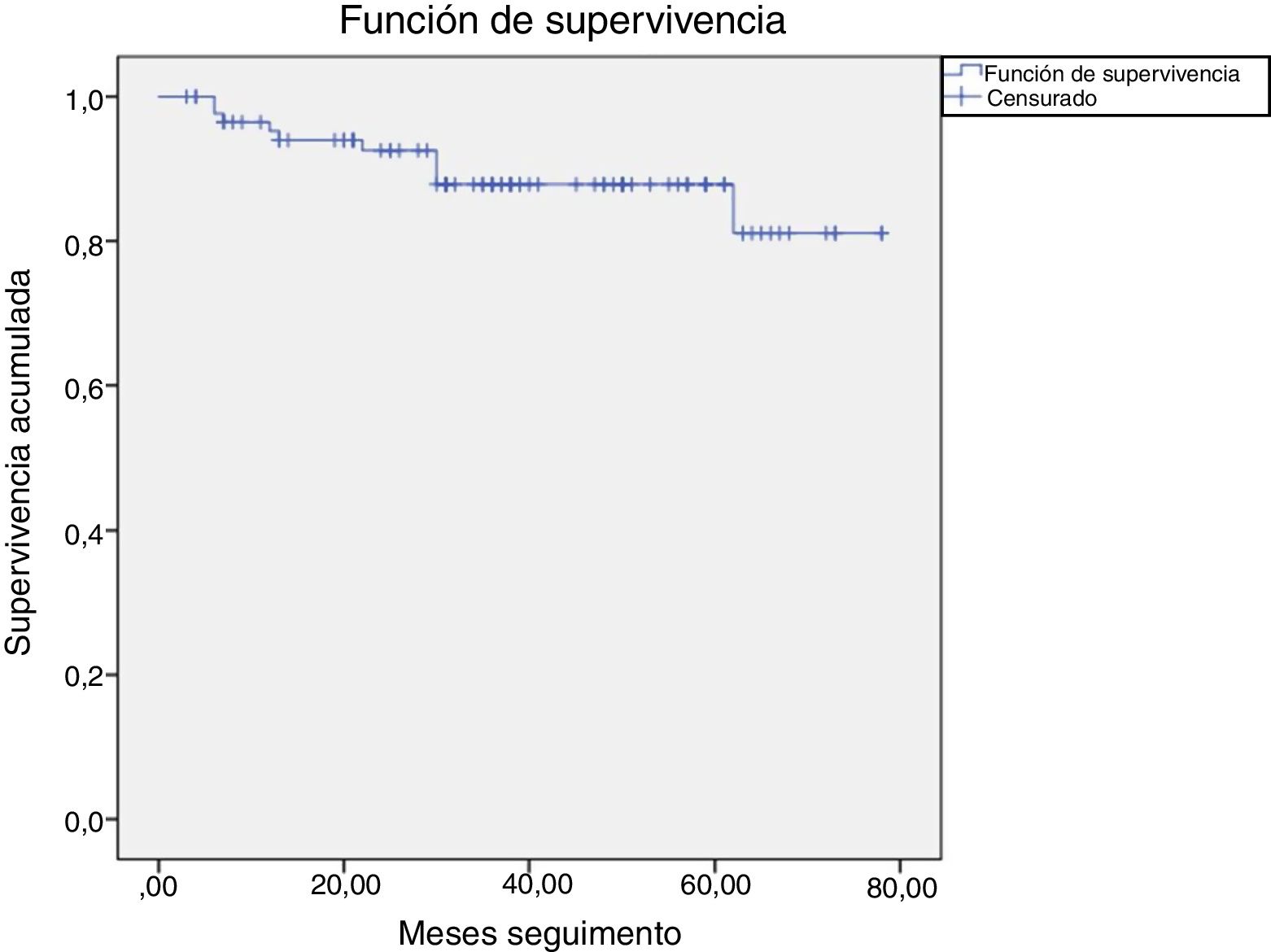
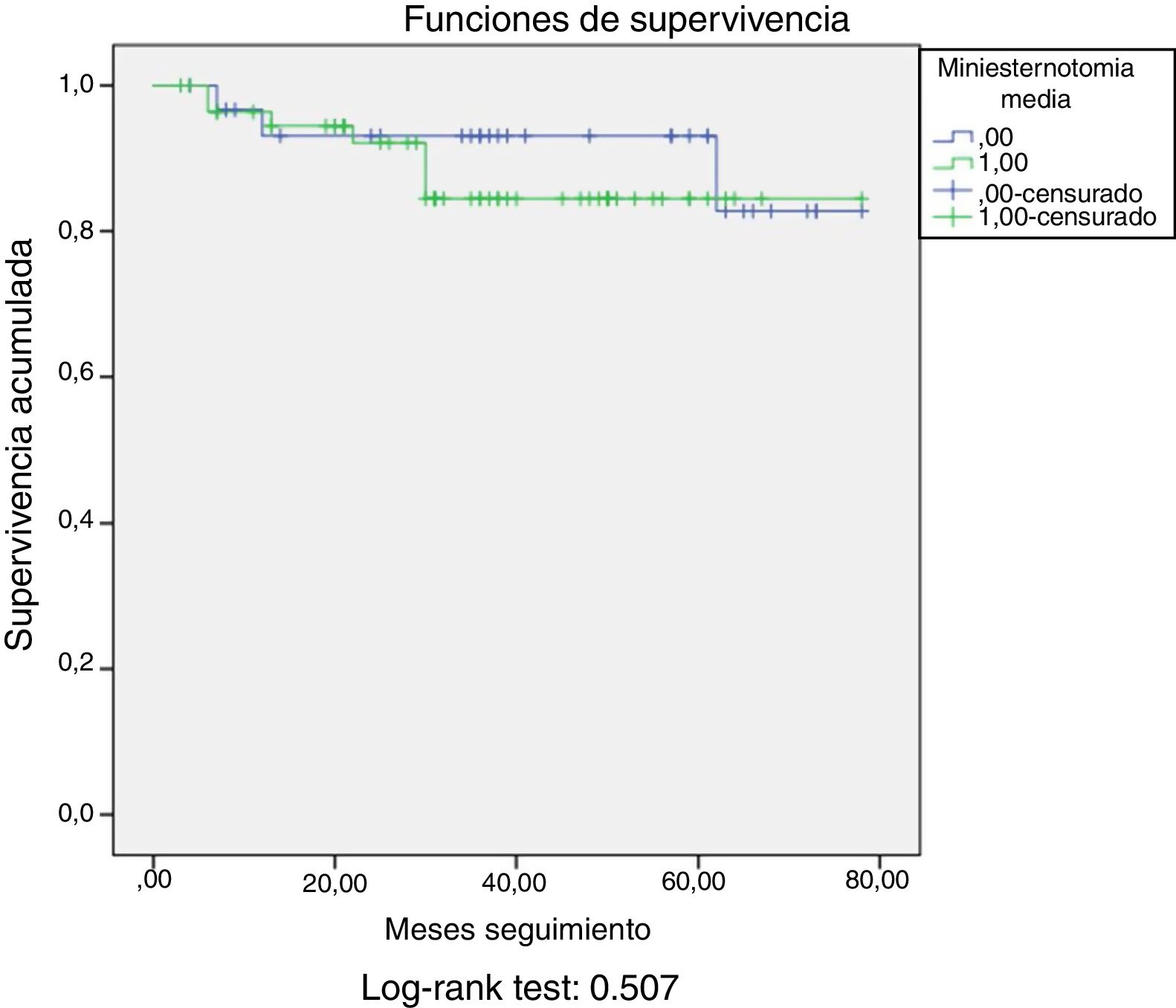
La media de seguimiento fue de 36±21 meses. Durante este periodo 11 pacientes fallecieron (tasa anual del 3,2%), 3 por ictus, 3 por infecciones a diferentes niveles, 2 por endocarditis, 2 por neoplasias y uno por insuficiencia cardiaca. La supervivencia a largo plazo de toda la serie fue 95%, 88% y 81% a uno, 3 y 6 años respectivamente (fig. 2). No hubo diferencias en la supervivencia a largo plazo entre las poblaciones con EMC y con HEMS (log rank test=0,507) (fig. 3).
Por otro lado, 5 pacientes (4,27%; tasa anual de 1,4% al año) sufrieron un ictus durante el seguimiento.
Ocho pacientes (6,8%; tasa anual del 2,3%) en el seguimiento presentaron FPP mayor de 1.
A 3 pacientes se les explantó la prótesis en el seguimiento (tasa anual del 0,9% al año). Esto fue debido a un caso de FPP de grado 3 con repercusión clínica a los 23 meses de la intervención, con implante de una prótesis convencional, y a 2 casos de endocarditis que requirieron ser reintervenidos a los 22 y a los 73 meses de la primera intervención.
Cinco pacientes necesitaron de un MPP durante el seguimiento (tasa anual del 1,5%) (tabla 3).
La mediana del grado funcional postoperatorio en el seguimiento fue de 1 (1-1).
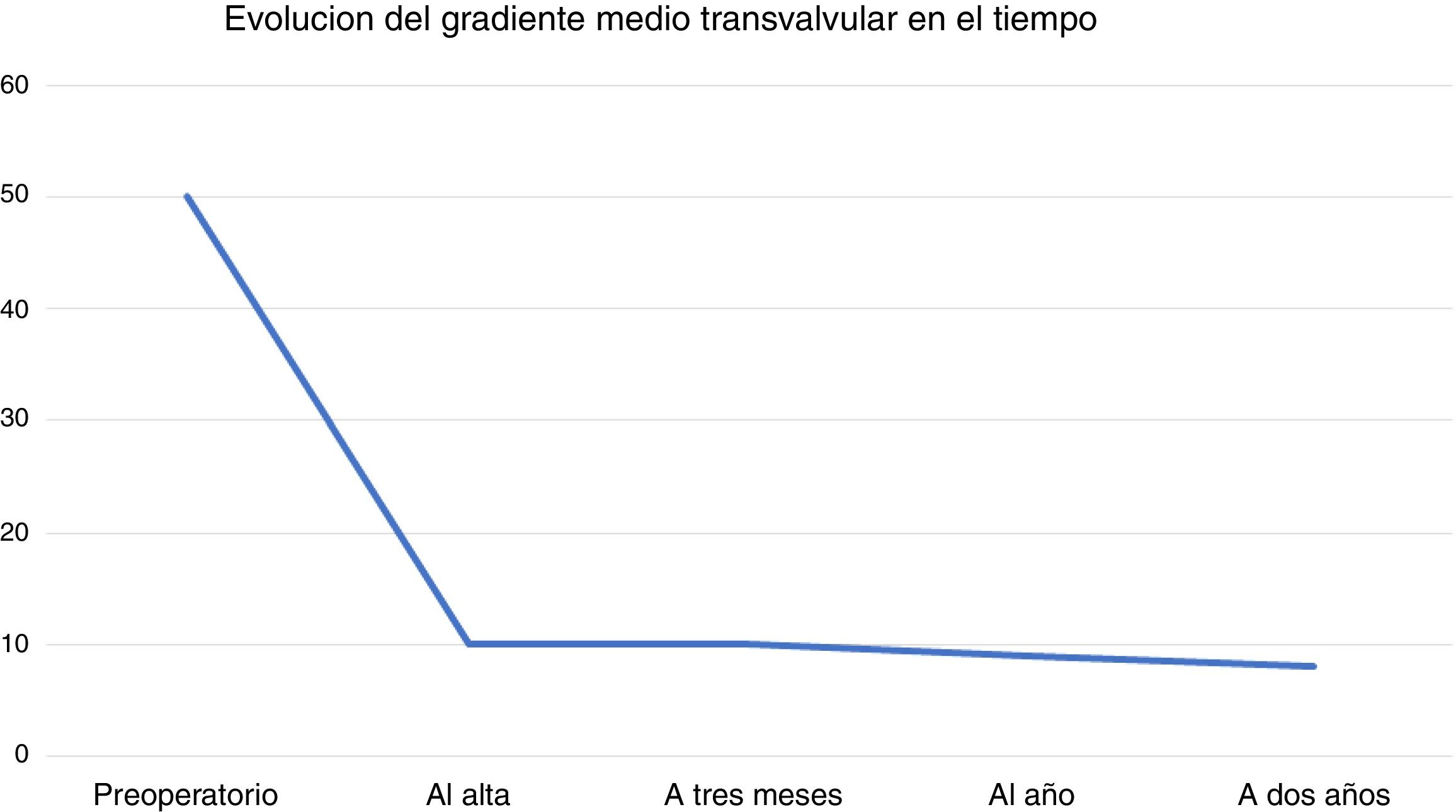
El gradiente transprotésico medio de toda la serie a los 3 meses, al año y a los 2 años fue de 9,9±3,7mm, 9,1±3,5mm y 8,4±3,4mmHg, respectivamente (fig. 4). Por último 14 pacientes (tasa anual de 2,3%) ingresaron en el hospital en el seguimiento por diferentes causas (tabla 3).
DiscusiónEn este estudio presentamos nuestra experiencia con el sistema de válvula Edwards Intuity durante los últimos 7 años.
Las prótesis aórticas de rápido despliegue y las prótesis sin suturas5–7 surgieron hace 10 años en la práctica clínica, combinando la experiencia clínica y la técnica de las prótesis aórticas biológicas convencionales con los avances tecnológicos aportados por las prótesis transcatéter. En concreto, el sistema de válvula Edwards Intuity se basa en la prótesis biológica Perimount Magna Ease, a la que se añade un marco expandible infraanular que permite la fijación de la prótesis con solo 3 suturas.
El éxito técnico en el implante en nuestra serie fue cercano al 98%, un dato destacable teniendo en cuenta que se incluye la curva de aprendizaje de los cirujanos y que se compara muy bien con la de otras series recientes7,10,15–17, que oscilan entre el 94% y el 97%.
La mortalidad hospitalaria de nuestra serie fue del 3,4%, cifra en el rango de la mortalidad recogida en el registro de la SECCE del año 2017 para cirugía valvular aórtica aislada o combinada18, estimadas entre 3-5%. La supervivencia al año, a los 3 y 6 años en nuestra población es superior al 80%, lo que consideramos adecuado, en consonancia con series más numerosas de la misma prótesis16,17,19, e incluso algo mejor que los resultados publicados con otra prótesis sin sutura20.
Además, nuestros datos refuerzan el concepto de que las PARD favorecen los abordajes quirúrgicos menos agresivos. Así, entre nuestros pacientes más de 2/3 fueron intervenidos vía HEMS, porcentaje mayor que los referidos en series ya publicadas tanto en América15 como en Europa16,17, que varían entre el 40% y el 47%. Un dato a resaltar es que en las 3 reconversiones a EMC registradas la causa fue siempre sangrado de difícil control y no problemas de acceso ni de implante de la prótesis.
Por otro lado, los tiempos quirúrgicos de nuestros pacientes fueron cortos. Estos tiempos reducidos son similares a los referidos en otros estudios europeos con la misma PARD7,10, pero mucho menores que los tiempos recogidos en las grandes series de centros americanos de cirugía valvular aórtica convencional21 o en la base de la STS para cirugía convencional de sustitución valvular aórtica, que son de 78 y 106minutos respectivamente22. Tiempos quirúrgicos similares recogieron Borger et al. en 2015, en un estudio aleatorizado entre prótesis convencionales vía esternotomía media y PARD con mínimo acceso9,23. Además, ya en nuestra experiencia inicial con la prótesis Edwards Intuity, objetivamos una disminución del 30% en los tiempos de isquemia y de CEC, al compararlos con los tiempos recogidos con prótesis aórticas convencionales11. En la actualidad hay estudios que muestran la asociación independiente entre tiempos de isquemia miocárdica y de CEC prolongados y mayor morbimortalidad24,25.
En nuestra serie no encontramos ningún caso de degeneración estructural de la prótesis, ni a corto ni a largo plazo. Tampoco registramos ninguna trombosis en las prótesis implantadas, aunque la ausencia de clínica no descarte la trombosis subclínica26. La trombosis protésica clínica o subclínica sobre prótesis biológicas es un problema muy estudiado en la actualidad, y aunque su prevalencia parece más alta entre las prótesis transcatéter, también está presente en las prótesis quirúrgicas convencionales27,28. En nuestra serie sí observamos una tasa anual de ictus del 1,4%, la mayoría de probable origen tromboembólico.
Debido a su sistema de anclaje infraanular, la posibilidad de aparición de fugas paravalvulares en las prótesis Edwards Intuity es un tema de preocupación. En nuestra población, al alta hospitalaria, el 12% de los pacientes presentaban algún tipo de FPP, la mayoría eran fugas triviales y solo una pequeña proporción eran mayores de 1. Durante el seguimiento la proporción de pacientes que se identificaron con fugas mayores que trivial fue algo superior. No obstante, es importante destacar que en el seguimiento solo se reintervino a una paciente por FPP severa, lo que supone una muy baja tasa anual de reoperación por fuga. Estos datos son compatibles con los informados por otras series con la misma PARD16,17,19, con prótesis quirúrgicas convencionales29 y con prótesis transcatéter30, que varían entre 2,7% y 6%.
Desde un punto de vista hemodinámico el comportamiento de la prótesis Edwards Intuity ha sido muy bueno. Los gradientes medios transprotésicos presentaron estabilidad y una leve tendencia a la disminución al año y a los 2 años. Estos datos confirman los hallazgos de otras series europeas con la misma PARD16,17,19. Este comportamiento hemodinámico tan favorable de la prótesis Edwards Intuity se podría explicar por la ausencia de parches de teflón infraanulares presentes en las prótesis convencionales, que podrían obstruir en parte el tracto de salida del ventrículo izquierdo, y también por la expansión de dicho tracto de salida del ventrículo izquierdo al dilatarse con el balón a presión utilizado para fijar esta PARD.
Respecto a la endocarditis protésica esta es una complicación grave y de tratamiento complejo. En nuestra serie no hubo ningún caso hospitalario, pero sí encontramos 3 durante el seguimiento. Por este motivo, 2 pacientes fueron reintervenidos, datos que son comparables con los informados por las grandes series de prótesis transcatéter31.
La tasa de necesidad de MPP en el postoperatorio precoz de nuestra serie fue similar a otras series más numerosas con la misma prótesis7,16, pero menor que en otros estudios15,17 que informan tasas entre el 8,6% y el 11,9%. Sin embargo, nuestra tasa de MPP precoz se encuentra dentro de la esperada para las prótesis convencionales32, que oscila entre el 3% y el 12%, pero es mucho menor que la que se ha informado en las series de prótesis transcatéter33, que llega al 16,4%. Recientemente hemos estudiado este tema más en profundidad34 y encontramos que el antecedente de infarto de miocardio y la toma de amiodarona preoperatoria se asociaban con mayor incidencia de MPP en el postoperatorio en esta población. Pero es posible que al desplegar el marco expandible infraanular para fijar la prótesis mediante presión en el tracto de salida del ventrículo izquierdo, se generen fuerzas radiales que puedan dañar el sistema de conducción en el septo interventricular.
LimitacionesExisten algunas limitaciones en relación con nuestro estudio. Se trata de un trabajo que presenta los resultados de un único centro, con un diseño observacional, retrospectivo y que carece de grupo control. Además se incluye en la experiencia la curva de aprendizaje del grupo quirúrgico. Sin embargo, creemos que la cohorte estudiada muestra una imagen real de la situación clínica del tratamiento de la estenosis aórtica en la actualidad. Del mismo modo, cabe destacar que las variables clínicas y el seguimiento han tenido una cumplimentación elevadas.
ConclusionesNuestros resultados con la PARD Edwards Intuity a corto y largo plazo son adecuados en términos de supervivencia, gradientes transprotésicos, duración y seguridad. El sistema valvular Edwards Intuity favorece los abordajes menos agresivos y reduce los tiempos quirúrgicos. Las tasas de fugas periprotésicas, marcapasos permanentes postoperatorios, endocarditis y deterioro estructural están dentro de valores clínicamente aceptables.
Se debe mantener el seguimiento de estos pacientes para continuar recogiendo información sobre su evolución y esperar que los resultados de estudios multicéntricos16,35 aporten más datos sobre estas poblaciones. Estos buenos resultados nos deben animar a utilizar el sistema de válvula Edwards Intuity en procesos quirúrgicos cada vez más complejos.
Conflicto de interesesJosé María Arribas declara haber recibido honorarios como orador de Edwards Lifesciences LLC. El resto de autores declara no tener conflicto de intereses.