Presentamos el inusual caso de un paciente adulto con diagnóstico de canal auriculoventricular intermediario y válvula auriculoventricular izquierda con músculo papilar único potencialmente en paracaídas, denominada así porque previamente a la reparación la entrada al ventrículo izquierdo está preservada a través de la hendidura o zona de aposición. La incidencia de esta combinación varía entre el 3,8 y el 14% en diferentes series de pacientes reparados en la infancia. La tendencia en la mayoría de los grupos es el cierre parcial o completo de la hendidura. Dependiendo de las anomalías asociadas, en la válvula auriculoventricular izquierda están descritas diferentes técnicas como el split del músculo papilar, la ampliación del velo lateral izquierdo con parche, anuloplastia posterior, resección de cuerdas tendinosas, etc. En nuestro paciente, debido a la potencial estenosis tras la reparación, se decidió realizar un split horizontal del músculo papilar único, seguido de uno vertical para dividir en dos cabezas el músculo que daba cuerdas tendinosas al borde libre de los velos puente superior e inferior. Tras esto se consideró que la entrada al ventrículo izquierdo era suficiente para realizar el cierre completo de la hendidura. Además, el velo posterior era de escaso desarrollo y presentaba cuerdas cortas, por lo que se decidió realizar anuloplastia posterior para subir el velo posterior y disminuir la distancia con el velo anterior.
La evolución postoperatoria fue buena. En el momento del alta, la válvula auriculoventricular izquierda presentaba un gradiente medio de 3mmHg e insuficiencia leve.
We present the unusual case of an adult patient with a diagnosis of intermediate atrioventricular canal and left atrioventricular valve with potentially parachute single papillary muscle, so named because, prior to repair, the inlet to the left ventricle is preserved through the cleft or zone of apposition. The incidence of this combination varies between 3.8% and 14% in different series of patients repaired in childhood. The tendency in most groups is partial or complete closure of the cleft. Depending on the associated anomalies in the left atrioventricular valve, different techniques are described, such as split of the papillary muscle, enlargement of the left lateral leaflet with a patch, posterior annuloplasty, resection of chordae tendineae, etc. In our patient, due to potential stenosis after the repair, we decided to perform a horizontal split of the single papillary muscle, followed by a vertical one to divide the muscle that gave tendinous chords to the free edge of the upper and lower bridge leaflets into two heads. After this, we considered that the entrance to the left ventricle was enough to perform complete closure of the cleft. In addition, the posterior leaflet was poorly developed and presented short cords, so we decided to perform a posterior annuloplasty to raise the posterior leaflet and decrease the distance with the anterior leaflet. The postoperative evolution was good. At discharge, the left atrioventricular valve had a mean gradient of 3mmHg and mild insufficiency.
Presentamos el caso de un paciente de 35 años de edad que acude a la consulta preoperatoria con el diagnóstico de canal auriculoventricular (AV) intermediario y con el siguiente estudio preoperatorio:
ECG: ritmo sinusal (RS). Frecuencia cardiaca (FC) 70lpm. Eje horizontal a −80°. Intervalo PR 244ms. Bloqueo completo de rama derecha del Haz de His (BCRDHH) y hemibloqueo anterior izquierdo del Haz de His (HBAIHH).
Rx tórax: índice cardiotorácico aumentado a expensas de cavidades derechas.
Ecocardiograma: levocardia, levoapex; situs solitus.
Concordancia AV y ventriculoarterial (VA). Dilatación significativa de ambas aurículas. Septo interauricular con defecto tipo ostium primum de unos 2,1-2,2cm con membrana de la fosa oval aneurismática.
Ventrículo izquierdo de morfología y función normal sin anomalías segmentarias, aunque con movimiento anómalo septal y rectificación del mismo por sobrecarga de ventrículo derecho.
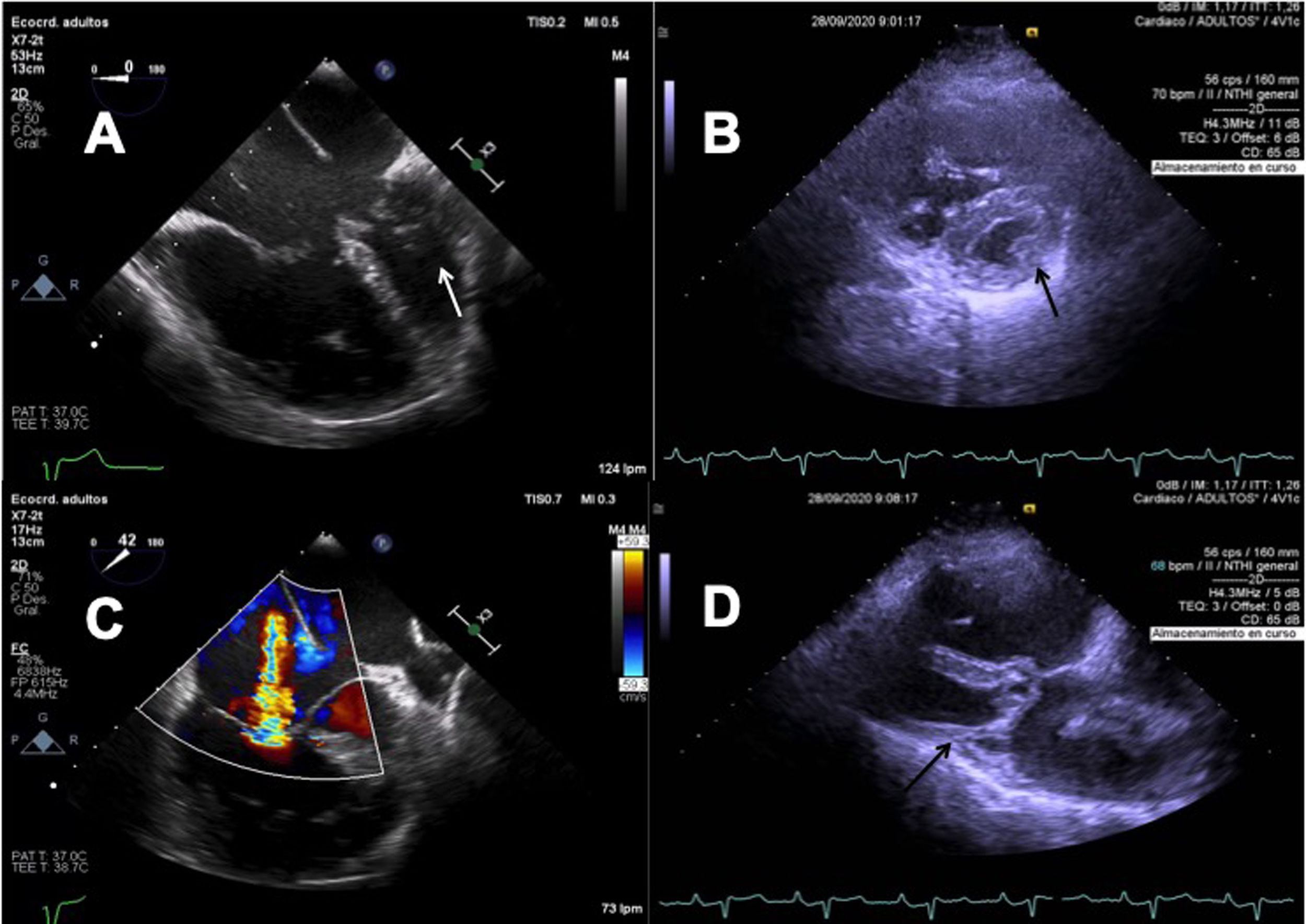
Ventrículo derecho dilatado (55mm en plano apical 4 cámaras) con función sistólica conservada. Se observan válvulas AV independientes ancladas sobre un aneurisma del septo membranoso sin paso de color a través del mismo. Ambas válvulas AV (izquierda y derecha) están situadas en el mismo plano con un anillo fibroso común. No se visualiza «cleft» mitral ni insuficiencia por doppler color, aunque el plano paraesternal eje corto no permite el estudio completo de la válvula mitral. Válvula tricúspide con insuficiencia moderada (grado II/IV). Válvula pulmonar con velos engrosados y tronco pulmonar dilatado (28mm). No ductus. Válvula aórtica trivalva, sin gradiente a nivel del tracto de salida del ventrículo izquierdo. Raíz aórtica normal. Pericardio normal. Vena cava inferior normal. No se consigue visualizar seno coronario (fig. 1). En resumen:
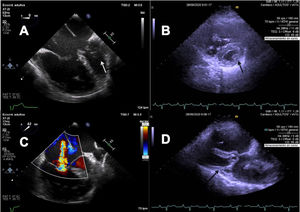
A) Imagen de ecocardiograma transesofágico intraoperatorio. Se observa gran dilatación de cavidades derechas. La flecha blanca señala el músculo papilar único. B) Imagen de ecocardiograma transtorácico preoperatorio subcostal corto. La flecha negra señala el músculo papilar único. C) Imagen de ecocardiograma transesofágico intraoperatorio. Se identifica insuficiencia tricúspide severa. D) Imagen de ecocardiograma transtorácico preoperatorio paraesternal eje largo. La flecha negra indica el músculo papilar único.
Cardiopatía congénita tipo canal auriculoventricular intermediario con shunt a nivel de comunicación interauricular ostium primum que origina sobrecarga de ventrículo derecho y signos indirectos de presión pulmonar elevada.
Cateterismo cardiaco. Coronariografía: coronarias epicárdicas sin lesiones. Codominancia.
Cateterismo derecho: hipertensión pulmonar leve (presión arterial pulmonar media de 25mmHg, resistencias pulmonares totales 3,6UW, arteriolares 1,6UW) precapilar.
Se objetiva bloqueo AV 2:1 intermitente (asintomático) y frecuentes pausas sinusales.
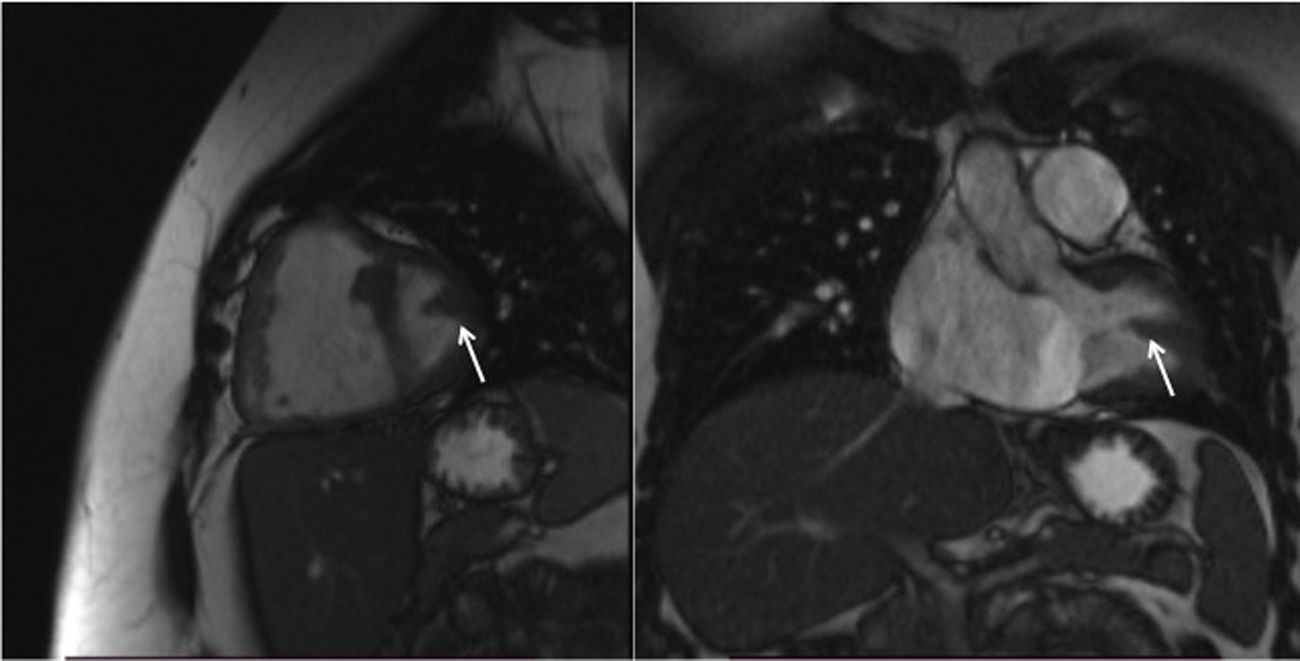
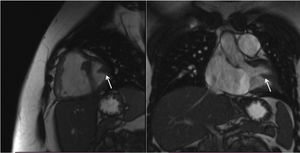
RMN cardiaca: se identifica comunicación interauricular ostium primum amplia que en el plano de 4C llega a medir 2cm, con severa sobrecarga de volúmenes de cavidades derechas (VTD de 217ml/m2) con fracción de eyección de ventrículo derecho conservada. Aneurisma en septo interventricular sin evidente comunicación interventricular (CIV). Aplanamiento septal interventricular por sobrecarga de cavidades derechas. Qp/Qs de entre 3,9 y 4,4 dependiendo del método de valoración. Dilatación del tronco de la arteria pulmonar hasta 4,2cm (fig. 2).
Holter: RS con FC media de 64lpm (mínimo 41 - máximo 104lpm). Durante gran parte del registro se evidencian frecuentes episodios (al menos 340 cuantificados) de bloqueo sinoauricular de 2.o grado tipo II, algunos con escape auricular diferente al sinusal, que no condicionan pausas sinusales significativas (máxima 2 segundos). Sin evidencia de bloqueo AV. Sin evidencia de fibrilación auricular o arritmias ventriculares registradas.
Debido a la sobrecarga de cavidades derechas en ausencia de hipertensión pulmonar significativa se decide la intervención quirúrgica para la reparación de la cardiopatía.
En el examen intraoperatorio se identifica un anillo valvular único con dos orificios valvulares independientes, con componente de CIV ocluido por tejido de cierre. Aparentemente se trata de un canal AV intermediario con componente de CIV cerrado en la evolución. Se identifica así mismo cleft o hendidura de la válvula AV izquierda, con un músculo papilar único que deja como único orificio de entrada al ventrículo izquierdo dicha hendidura mitral.
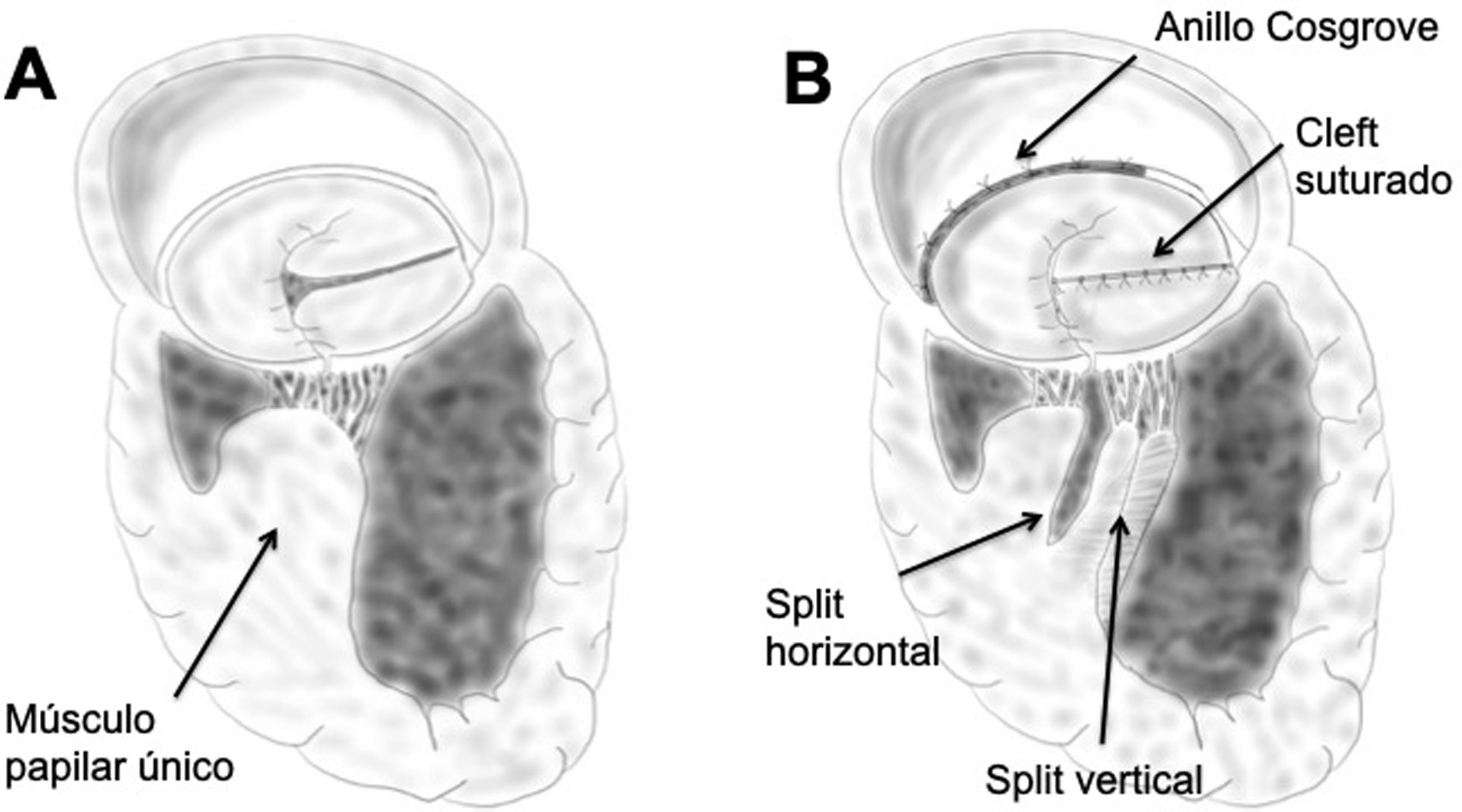
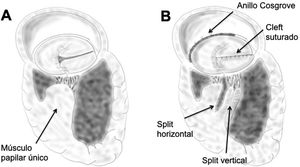
Considerando que dicho orificio de entrada quedaría estenótico tras el cierre de la comunicación interauricular se realiza split amplio del aparato subvalvular tanto en sentido horizontal como en sentido vertical, ampliando la superficie de entrada a través de la válvula AV izquierda. Tras esto, se vuelve a examinar la válvula y se decide el cierre completo del cleft con puntos en 8 de goretex 4/0. Se implanta además anillo incompleto de Cosgrove-Edwards® número 34.
A pesar de lo documentado en el estudio preoperatorio, la aurícula izquierda impresiona de pequeño tamaño, por lo que se decide resecar la membrana de la fosa oval ampliando la comunicación interauricular para posteriormente cerrar todo el defecto con parche de pericardio heterólogo y ampliar así el tamaño de la aurícula izquierda.
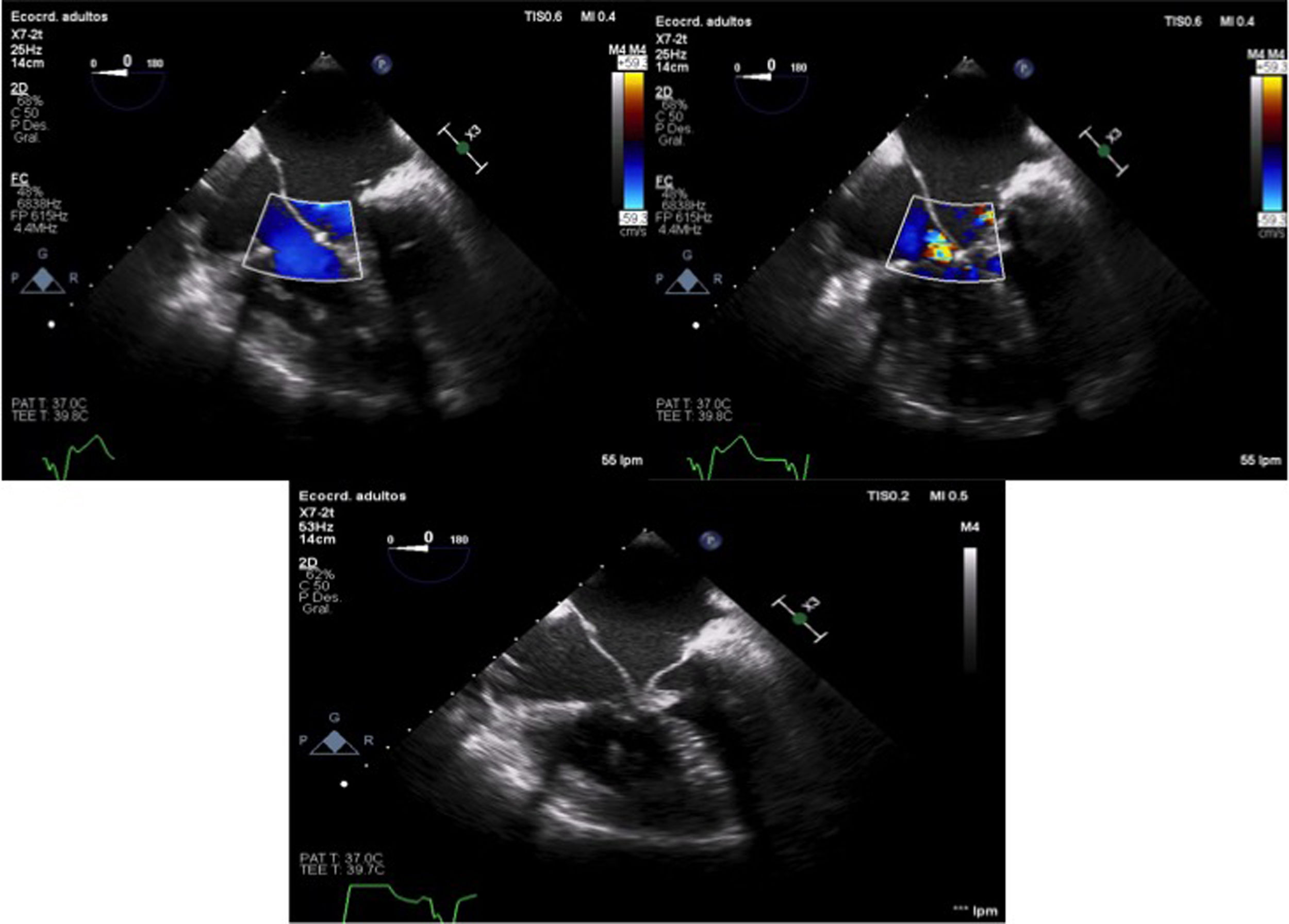
En cuanto a la válvula AV derecha, presenta una falta evidente de tejido a nivel septal (gap tricuspídeo), por lo que se decide cerrar el gap aproximando el tejido de los velos puente superior e inferior. Finalmente se implanta anillo tricúspide Carpentier-Edwards® Physio número 28 (figs. 3 y 4).
El destete de la circulación extracorpórea se produce sin incidencias. Tras la reparación el paciente alterna periodos de ritmo sinusal con episodios de bloqueo AV completo. El postoperatorio no presenta incidencias salvo la necesidad de implante de marcapasos definitivo, por episodios de bloqueo AV intermitente.
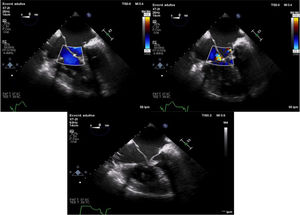
El alta hospitalaria se produce a los 10 días del postoperatorio, con el siguiente ecocardiograma:
Cavidades izquierdas de tamaño normal, con fracción de eyección de ventrículo izquierdo normal y movimiento septal anómalo, secundario a alteraciones de la conducción. Se detecta insuficiencia mitral ligera residual. Ligero gradiente subaórtico. Cavidades derechas dilatadas, con parámetros de funcionalidad del ventrículo derecho ligeramente disminuidos.
No se registra insuficiencia tricúspide para el cálculo de presión pulmonar, con tiempo de aceleración ligeramente acortado (90ms). No se documentan cortocircuitos.
Conclusión: Dilatación de cavidades derechas. Insuficiencia mitral residual ligera. Hipertensión pulmonar ligera. Mínimo derrame pericárdico poscirugía.
DiscusiónSchiebler et al.1 describen por primera vez una válvula mitral en paracaídas como aquella en la que las cuerdas tendinosas de los velos se insertan en un músculo papilar único. Posteriormente, Shone et al.2, en 1963, popularizan el término incluyéndolo en un complejo que asocia anillo supramitral, válvula mitral en paracaídas, estenosis subaórtica y coartación aórtica. Distinguen dos entidades similares, la forma completa en la que realmente existe un músculo papilar único y la forma parcial en la que existen dos músculos papilares muy próximos entre sí y donde uno de ellos (habitualmente el anterolateral) es hipoplásico.
Oosthoek et al.3 distinguen entre válvula mitral en paracaídas y paracaídas-like en aquellos casos en los que uno de los músculos papilares es predominante y se encuentra anclado a la base y a la cara lateral de la pared libre del ventrículo izquierdo.
Habitualmente las cuerdas tendinosas se encuentran engrosadas y acortadas, las comisuras pueden encontrarse escasamente desarrolladas, y es frecuente la presencia de anillo supramitral. Todo ello suele provocar restricción en la movilidad de los velos.
En el caso del canal AV, previamente a la reparación, se habla de potencial válvula en paracaídas, debido a que la zona de la hendidura normalmente evita la estenosis de la válvula AV izquierda.
En ocasiones la válvula AV izquierda en paracaídas puede asociarse con ventrículos disbalanceados (ventrículo derecho dominante), lo que obliga, en ocasiones, a una paliación univentricular en niños4.
La incidencia en el seno del canal AV oscila entre el 3,8 y el 14%.
Sharma et al.5 describen el manejo de la zona de aposición en 28 pacientes, niños; 16 pacientes con diagnóstico de canal AV completo y 12 con diagnóstico de formas parciales. Un total de 21 pacientes tenían formas parciales de válvula en paracaídas y 7 pacientes formas completas. Su preferencia es el cierre completo de la hendidura, aceptando gradientes medios de hasta 8mmHg, debido a que la mayor parte de las reintervenciones sobre la válvula AV izquierda se produce por insuficiencia en vez de por estenosis valvular.
Wetter et al.6 demostraron que el cierre del cleft en el canal AV completo reducía la proporción de pacientes con regurgitación significativa del 28 al 9%.
Se han descrito diferentes técnicas adicionales al cierre de la hendidura de la válvula AV izquierda, tales como split de los músculos papilares, fenestración de las cuerdas tendinosas engrosadas, plastias de aumento del velo lateral con parche, etc.
El grupo de Myers7 realiza split del músculo papilar dividiéndolo en dos y separándolo de la pared libre del ventrículo izquierdo.
También intentan, siempre que es posible, el cierre completo de la hendidura. Su serie es de 24 pacientes, todos ellos canal AV completo y en 16 se trataba de canales AV disbalanceados.
Ambos grupos (Myers y Sharma) hacen hincapié en el estudio preoperatorio mediante ecocardiografía para identificar este grupo de pacientes y evaluar el manejo intraoperatorio de los mismos.
Lacour-Gayet et al.8 postulan la mayor incidencia de lesiones obstructivas del lado izquierdo en pacientes con diagnóstico de canal AV y cariotipo normal. Encuentran 39 pacientes (56% de la serie) con lesiones obstructivas del lado izquierdo; de ellos, 14 pacientes con válvula mitral en paracaídas. Al contrario que en las dos series anteriores, su preferencia es no cerrar la zona de la hendidura o hacerlo parcialmente.
El diagnóstico en adultos es inusual, tanto de forma aislada como en asociación con otra cardiopatía. No hemos encontrado en la revisión ningún caso de canal AV con válvula mitral en paracaídas.
En nuestro caso, planteamos la posibilidad de no tocar la válvula AV izquierda, pero la entrada de la misma a través de la hendidura parecía insuficiente, ya que aunque previamente a la cirugía la válvula no presentaba gradiente a su través, presumiblemente al cerrar el cortocircuito izquierda-derecha, la válvula presentaría estenosis significativa. Por ello, se decidió realizar split amplio del aparato subvalvular tanto en sentido horizontal como vertical. Tras realizar el split, la entrada de la válvula AV izquierda se consideró lo suficientemente amplia, por lo que se decidió el cierre completo del cleft. Además, el velo lateral o mural se encontraba escasamente desarrollado, por lo que se decidió implantar un anillo incompleto para disminuir la distancia entre el velo anterior y el mural.
En el ecocardiograma poscirugía el paciente presenta insuficiencia de la válvula AV izquierda residual leve con ligera aceleración del flujo a nivel subaórtico en probable relación con el split del músculo papilar único.
En el último seguimiento, 6 meses después de la cirugía, el paciente se encuentra asintomático, presenta insuficiencia ligera y ausencia de estenosis de ambas válvulas AV, presión pulmonar estimada normal y ausencia de cortocircuito residual a nivel del septo interauricular.
ConclusionesAunque se trata de una combinación extremadamente rara, consideramos que el manejo intraoperatorio debe ser similar al empleado en la edad infantil. La posibilidad de dejar abierta la zona de la hendidura de la válvula AV izquierda, probablemente, conlleva mayor riesgo de estenosis (e insuficiencia) tras la septación de la comunicación interauricular.
Por otro lado, aunque la reparación es preferible, el fallo de esta y la necesidad de implante de una prótesis valvular no implica los mismos problemas que en los neonatos o lactantes de bajo peso.
Consideraciones éticasEstudio sobre caso clínico anonimizado, realizado sobre practica clínica habitual, no implicando manejo de cohorte de pacientes ni la utilización de técnicas, dispositivos o tratamientos en fase de ensayo clínico. Los autores cuentan con el consentimiento informado del paciente para la publicación de este trabajo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.