La implantación de la válvula aórtica transcatéter (TAVI) se ha establecido como el tratamiento primario para la estenosis aórtica severa sintomática, particularmente en los pacientes mayores de 75 años y aquellos con alto riesgo quirúrgico. En las últimas 2 décadas, el número de procedimientos para la TAVI han aumentado significativamente, y se espera que esta tendencia continúe. A pesar de que el acceso transfemoral es el preferido para la TAVI, no es adecuado en hasta el 20% de los pacientes debido a contraindicaciones anatómicas como el tamaño inadecuado del vaso, los ejes iliofemorales muy calcificados o la tortuosidad extrema del vaso. Esto ha impulsado la exploración y el desarrollo de enfoques de la TAVI no transfemoral, incluyendo los abordajes intratorácicos y extratorácicos.
La aparición de las distintas vías de acceso para la TAVI no ha sido simultánea, y la elección entre los accesos intratorácicos y extratorácicos es compleja, influenciada por la anatomía del paciente, las comorbilidades y la experiencia del centro tratante. El enfoque transapical, clasificado bajo intratorácicos, ha sido la principal alternativa no transfemoral durante casi una década. Sin embargo, la aparición de accesos extratorácicos, como el transcarotídeo y el transubclavio, ha expandido los horizontes de la TAVI, ofreciendo potencialmente mejores resultados para ciertas poblaciones de pacientes.
Transcatheter aortic valve implantation (TAVI) has become the primary treatment for symptomatic severe aortic stenosis, particularly in patients over 75 years of age and those at high surgical risk. In the last two decades, the number of TAVI procedures has significantly increased, and this trend is expected to continue. Despite the preference for transfemoral access in TAVI, it is unsuitable for up to 20% of patients due to anatomical contraindications such as inadequate vessel size, heavily calcified iliofemoral vasculature, or extreme vessel tortuosity. This has led to the exploration and development of non-TF TAVI approaches, including intrathoracic and extrathoracic approaches.
The emergence of different access routes for TAVI has not been simultaneous, and the choice between intrathoracic and extrathoracic accesses is multifaceted, influenced by the patient's anatomy, comorbidities, and the expertise of the treating center. The transapical approach, classified as intrathoracic, has been the main non transfemoral alternative for nearly a decade. However, the emergence of extrathoracic accesses, such as the transcarotid and transsubclavian approaches, has broadened the horizons of TAVI, potentially offering better outcomes for specific patient populations.
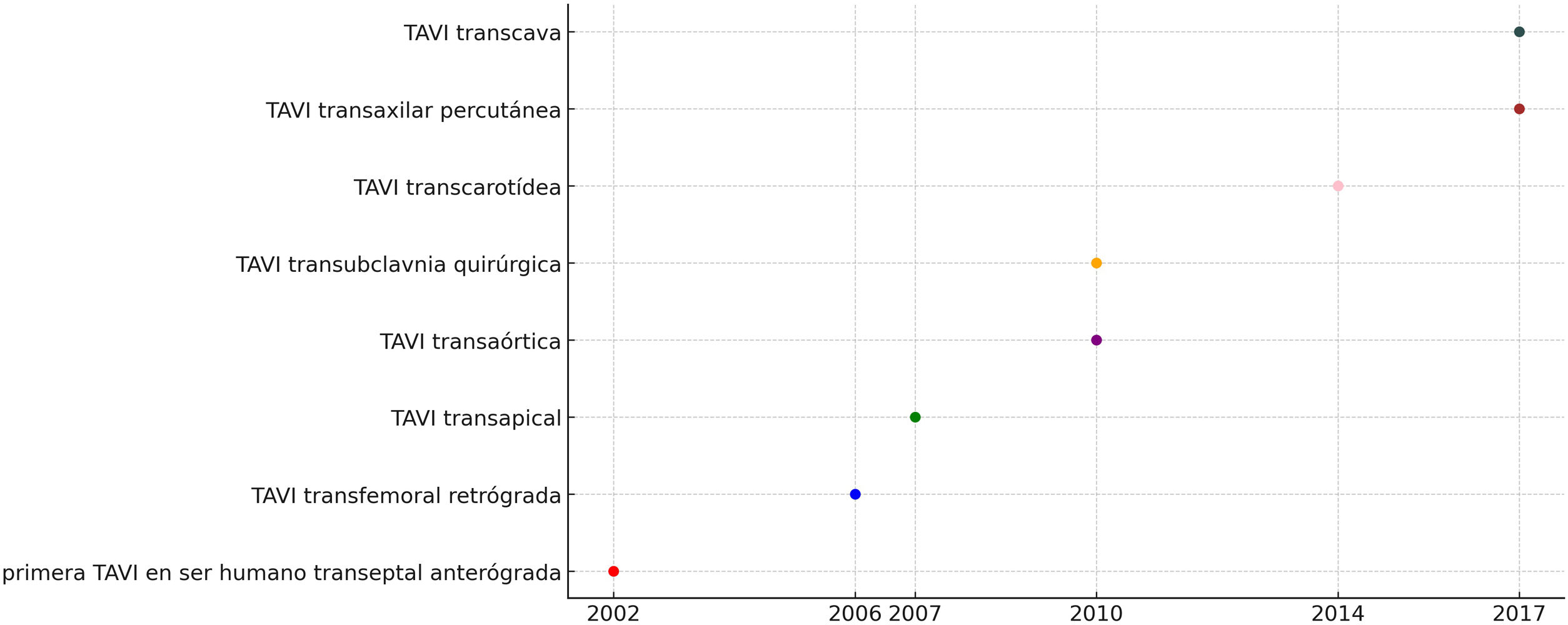
La implantación de la válvula aórtica transcatéter (TAVI, por sus siglas en inglés) se ha consolidado como el tratamiento primario para la estenosis aórtica severa sintomática, especialmente en pacientes de 75 años o más, y aquellos con alto riesgo quirúrgico1. En las últimas 2 décadas, el número de procedimientos de la TAVI ha aumentado significativamente, y se espera que esta tendencia continúe. Aunque el acceso transfemoral (TF) es el acceso preferido para la TAVI, no es adecuado en hasta el 20% de los pacientes, debido a contraindicaciones anatómicas como tamaño del vaso inadecuado, ejes iliofemorales muy calcificados o tortuosidad extrema del vaso2. Esto ha llevado a la exploración y al desarrollo de enfoques de la TAVI no-TF, incluyendo abordajes intratorácicos (IT) y extratorácicos (ET). La aparición de las distintas vías de acceso para la TAVI no ha sido simultánea como podemos ver en la cronología representada en la figura 1.
La elección entre los accesos IT y ET es multifacética, influenciada por la anatomía del paciente, las comorbilidades y la experiencia del centro tratante. Mientras que el enfoque transapical (TA), clasificado bajo IT, ha sido la principal alternativa no-TF durante casi una década, la aparición de accesos ET, como el transcarotídeo (TC) y el transubclavio (TS), ha ampliado los horizontes de la TAVI, ofreciendo potencialmente mejores resultados para ciertas poblaciones de pacientes. La elección del acceso vascular a menudo está influenciada por la experiencia del operador y las comorbilidades del paciente. Datos recientes del registro STS/ACC TVT han mostrado un cambio en la preferencia de enfoques de la TAVI no-TF, con los accesos ET ganando prominencia en los últimos años3–5.
En nuestro servicio de cirugía cardíaca, entre enero del año 2009 y marzo del año 2023, realizamos 402 TAVI no-TF, de las que 279 fueron TA y 123 TC y TS. El análisis de nuestros resultados mostró que los abordajes ET presentan una mortalidad hospitalaria y mortalidad global a un año significativamente inferior, menos complicaciones respiratorias, menos fibrilación auricular postoperatoria, menor incidencia de síndrome de bajo gasto cardíaco postoperatorio, y una notablemente inferior estancia postoperatoria.
En esta revisión vamos a explorar las principales alternativas no-TF de las que disponemos actualmente los cirujanos cardíacos, incluyendo su evolución, su ejecución técnica, sus ventajas e inconvenientes.
TAVI transapical (TA-TAVI): consideraciones técnicas y riesgos asociadosHistoriaEl acceso TA ha sido un pilar en el desarrollo de la TAVI. Descrito inicialmente por Lichtenstein et al.6, este enfoque alcanzó su máxima utilización durante el ensayo PARTNER I y el lanzamiento comercial de la primera generación de la válvula Edwards SAPIEN.
Procedimiento- 1.
Identificación del ápex cardíaco: se realiza con el paciente ya colocado en decúbito supino con una leve elevación del hemitórax izquierdo. Se localiza el ápex cardíaco mediante ecocardiografía transtorácica (ETT) en plano axial. Se escoge el espacio intercostal más bajo en que se visualiza el ventrículo izquierdo (VI). La identificación del ápex del VI presenta mayor dificultad en pacientes obesos, con enfermedad pulmonar obstructiva crónica (EPOC) tipo enfisematoso y en pacientes reoperados.
- 2.
Realización de minitoracotomía: el acceso TA comienza con una toracotomía limitada, de longitud máxima 4-6cm. Se emplea como referencia la localización previa de espacio intercostal de ápex mediante ETT.
- 3.
Exposición apical: se expone el ápex del corazón y se colocan tracciones de seda en el pericardio. Idealmente se recomienda emplear un separador blando tamaño pequeño para incisiones de diámetro de 2,5 a 6cm. El separador blando maximiza la exposición con una mínima incisión en piel; no produce retracción intercostal y, por tanto, se minimiza el dolor postoperatorio y el trauma quirúrgico, y favorece la hemostasia de la pared torácica.
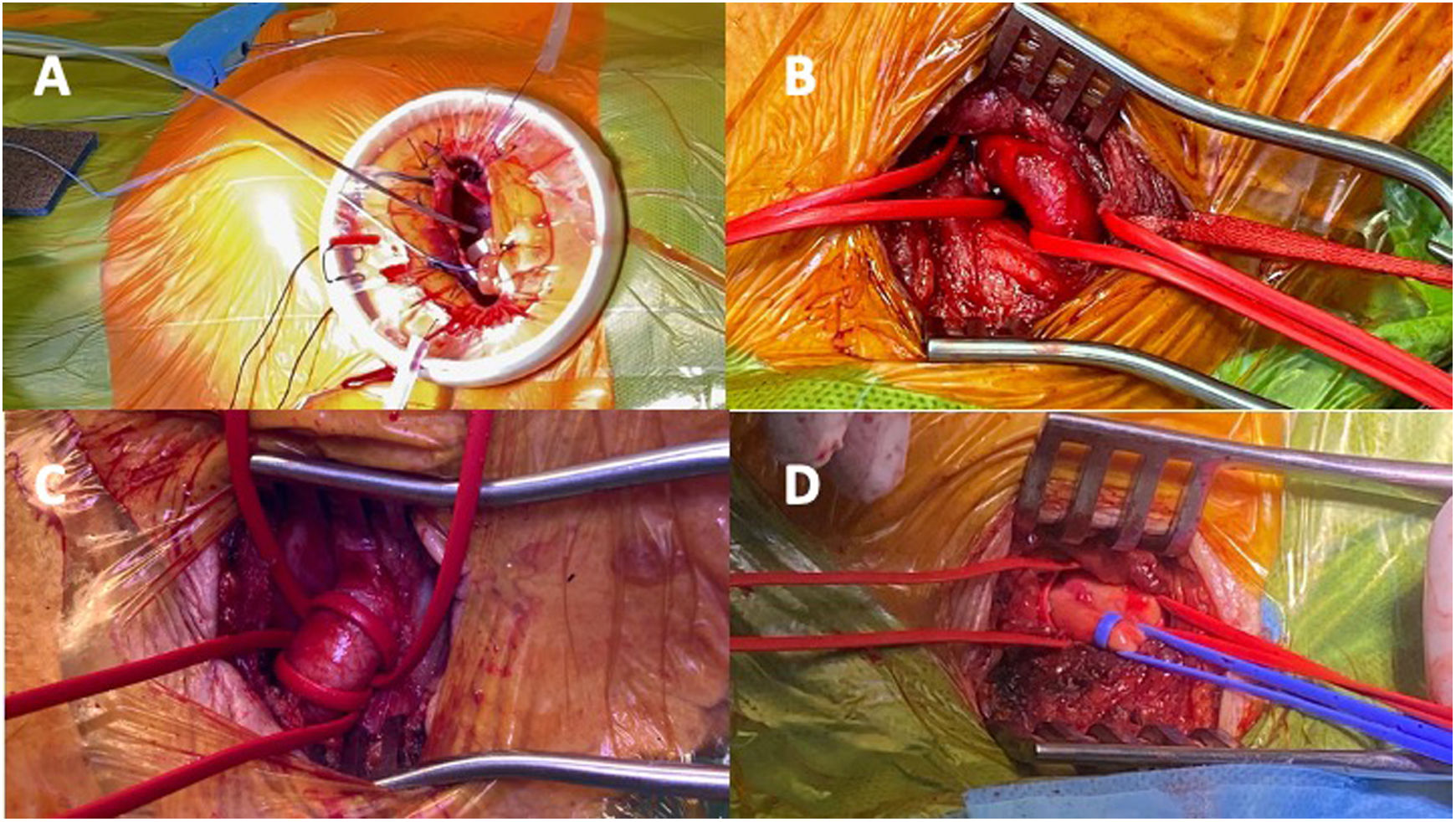
A continuación, se colocan suturas reforzadas con teflón 1,5-2cm anchura en el área de acceso previsto del VI, generalmente lateral al ápex real. Se debe seleccionar la sutura según el tipo de bolsa de tabaco que vayamos a realizar (suturas de monofilamento 2-0 aguja 3/8 circular 26mm o monofilamento 3-0 aguja 1/2 circular 36mm). Es de vital importancia colocar los puntos perpendiculares a la superficie del VI cogiendo todo el espesor del miocardio, pero sin entrar en la cavidad del VI (fig. 2A).
El siguiente paso es colocar el cable de marcapasos bipolar epicárdico temporal ventricular y comprobar la captura del marcapasos en modo VVI con 20mV de salida ventricular a una frecuencia de 180-200lpm y observar la respuesta de la tensión arterial.
- 4.
Punción apical: se realiza una punción en el ápex expuesto con una aguja de calibre 18G. Control con ecocardiografía transesofágica (ETE) y fluoroscopia de la posición de las guías.
- 5.
Introducción de la guía: se introduce una guía estandar punta en J 0.035” en el ápex, la cual es posteriormente reemplazada por una guía rígida en la aorta descendente realizándose el intercambio sobre un catéter tipo pigtail. Sobre la guía de alto soporte se avanza un introductor específico de mayor tamaño (24-33F Ascendra o Ascendra II, Edwards Lifescience Way. Irvine CA, US), seguido por el despliegue de la válvula.
- 6.
Hemostasia: se recomienda reducir la presión arterial mediante el uso de estimulación rápida, retirando el introductor de alto calibre y anudando las suturas reforzadas. Es fundamental no tensar en exceso las suturas.
- 7.
Cierre: se deja un drenaje torácico curvo y se cierra la minitoracotomía.
- •
La integridad del tejido apical puede ser impredecible. La degeneración del tejido apical o una adiposidad apical excesiva, frecuentes hallazgos con la edad se asocian a complicaciones hemorrágicas y a la aparición tardía de pseudoaneurismas del ápex del VI.
- •
Durante el ensayo PARTNER I, el 42% de los pacientes se sometieron al acceso TA, experimentando mayores tasas de mortalidad hospitalaria, insuficiencia renal, sangrado y estancias hospitalarias más largas en comparación con los procedimientos TF7. Además, los datos indican que el acceso TA estuvo asociado con una mayor lesión miocárdica en comparación con otras vías de acceso8.
- •
Los pacientes con enfermedades pulmonares crónicas, y en particular aquellos con EPOC, presentan riesgos con el enfoque TA. Estos pacientes a menudo experimentan tiempos de ventilación posprocedimientos más prolongados, sugiriendo que se debería evitar el TA en este grupo9.
- •
La insuficiencia mitral (IM) representa una complicación potencial durante la ejecución de una TAVI, la cual puede demandar variadas estrategias terapéuticas en función del mecanismo subyacente (1). Se ha evidenciado una incidencia que fluctúa entre el 8,5 y el 10,5%, variabilidad que probablemente se atribuye a los diferentes criterios de evaluación adoptados en distintos estudios (2). La IM puede ser primaria, originada por una lesión o disfunción del velo o del aparato subvalvular; o secundaria, derivada de una dilatación o disfunción del VI (3). Diversos mecanismos han sido delineados (1-4), incluyendo: daño estructural del aparato valvular o subvalvular mitral, colisión de la prótesis aórtica contra el velo anterior mitral, rotura de las cuerdas tendinosas, movimiento sistólico anterior del velo anterior mitral o una contracción biventricular asincrónica inducida por la estimulación del ventrículo derecho mediante un marcapasos unicameral, entre otros. Ciertos mecanismos son transitorios y reversibles10, mientras que otros pueden desencadenar una IM severa y definitiva, deteriorando consecuentemente el pronóstico del paciente.
Los grandes registros de pacientes de alto riesgo mostraron tasas de mortalidad a 30 días y a un año que varían del 9 al 14% y del 25 al 32% después de la TAVI TA3,11–13. Si bien el acceso TA jugó un papel crucial en las etapas iniciales de la TAVI, su uso ha disminuido debido a las complicaciones asociadas y los avances en otros métodos de acceso. Sin embargo, es esencial entender las particularidades de esta técnica para aquellos casos donde pueda considerarse apropiada.
TAVI transaórtico (TAo-TAVI): consideraciones técnicas y riesgos asociadosHistoriaEl acceso transaórtico (TAo) para la TAVI surgió como una alternativa a los enfoques tradicionales, buscando minimizar las complicaciones observadas con el acceso apical en poblaciones específicas.
La vía TAo para la TAVI fue introducida por primera vez en 2010 por Latsios et al.14. Diseñada principalmente para pacientes ancianos y frágiles, esta técnica busca evitar las complicaciones relacionadas con el acceso apical del VI. Aunque se realiza una esternotomía parcial superior, existen variantes que preservan el esternón, como aquellas que utilizan una incisión a través de la muesca supraesternal.
ProcedimientoLa anestesia general es obligatoria para el procedimiento. Se debe tener precaución con pacientes que han tenido esternotomías previas, especialmente si cuentan con injertos de bypass coronario aún permeables. Además, una aorta ascendente fuertemente calcificada suele ser una contraindicación.
Es crucial una evaluación meticulosa con TAC para determinar la viabilidad del acceso TAo. Las características deseadas en el sitio de acceso vascular incluyen:
- •
Ausencia de calcificación.
- •
Trayectoria que permita al operador dirigir el introductor de forma recta para el despliegue del dispositivo.
- •
Espacio adecuado entre la punta del introductor y el anillo valvular aórtico para una expansión completa del balón durante el despliegue. Habitualmente, este punto se sitúa al menos a 50mm del anillo aórtico en el cuadrante externo superior de la aorta, conocido como la «zona Tao»15.
La elección entre una esternotomía mini J o una toracotomía derecha mini depende de la relación entre el esternón y la aorta ascendente. La esternotomía mini J se favorece si la aorta ascendente se sitúa cerca de la línea media o a la izquierda y se encuentra a una profundidad mayor de 6cm del esternón. Por otro lado, la toracotomía derecha mini se prefiere cuando la mayoría de la aorta está hacia la derecha del borde esternal.
Consideraciones y complicacionesComo con cualquier procedimiento, el TAo-TAVI no está exento de riesgos:
- •
Perforación ventricular: ya sea por un alambre guía extremadamente rígido o por un cable de marcapasos intravenoso.
- •
Disección aórtica: aunque rara, esta complicación puede surgir debido a un trauma intimal aórtico con dispositivos TAVI.
Es imperativo que los profesionales estén alerta a estos posibles problemas y tomen las precauciones necesarias durante el procedimiento.
ResultadosEl acceso TAo para la TAVI ofrece una alternativa viable en casos seleccionados, permitiendo la implantación de válvulas en los pacientes que de otro modo podrían no ser candidatos adecuados para enfoques más convencionales. Datos de grandes registros en pacientes de alto riesgo muestran tasas de mortalidad a 30 días y un año después de la TAo TAVI que varían del 6 al 10% y del 19 al 30%13,16. Las complicaciones vasculares mayores, eventos de hemorragia mayor y accidentes cerebrovasculares mostraron tasas similares entre los enfoques TA y TAo13,17. Thourani et al.13 reportaron una tasa más alta de mortalidad no ajustada a 30 días y un año en el grupo de acceso TAo; sin embargo, estas diferencias dejaron de ser estadísticamente significativas tras un análisis ajustado por riesgo.
TAVI transubclavia: características técnicas del acceso TSHistoriaLa técnica del acceso transubclavio o transaxilar (TS) ha ido adquiriendo importancia con la evolución de las válvulas cardíacas transcatéter (THV). La tendencia a la reducción de los diámetros de las fundas de entrega de estas válvulas ha incentivado el uso de vasos periféricos como una alternativa más ventajosa en comparación con el tradicional acceso TF. Ruge et al. destacaron al realizar con éxito el primer caso de TAVI mediante el acceso TS en 200718.
A diferencia de la arteria iliofemoral, que tiende a calcificarse con la edad, la arteria axilar/subclavia muestra una sorprendente resistencia a la calcificación. Esto podría explicar por qué los pacientes con enfermedad vascular periférica avanzada, incluso con enfermedad oclusiva aortoilíaca, pueden ser susceptibles la TAVI TS.
Según el registro STS/ACC TVT, hasta 2019, más del 50% de los casos no-TF se realizaron a través de un enfoque IT12. Sin embargo, el uso de accesos IT ha ido disminuyendo gradualmente en los últimos 5 años debido a la irrupción de los enfoques ET12. Alrededor del año 2017, los accesos transaxilares/TS comenzaron a superar a los enfoques IT12,13. Posteriormente, los datos de 2019 del registro STS/ACC TVT indicaron que el acceso transcárpico emergió como una alternativa no-TF especialmente atractiva12,13.
ProcedimientoEl acceso puede efectuar bien a través de la arteria subclavia o bien de la arteria axilar, cuya profundidad y tortuosidad varía según la constitución corporal del paciente. Esta arteria, cercana al plexo braquial, requiere un manejo meticuloso. Es común encontrar características como elongaciones, tortuosidades y falsos acodamientos, más prevalentes en pacientes mayores o aquellos con hipertensión arterial con vasos elongados. Estas tortuosidades suelen ser corregibles, sobre todo en ausencia de calcificaciones significativas. Por ello, se recomienda el uso de introductores largos, de 45cm19, para trabajar desde el propio arco aórtico.
En el análisis radiológico de las arterias subclavias puede haber artefactos como una infraestimación de las medidas de la luz de la arteria subclavia en el segmento arterial posterior a la clavícula, o como el hallazgo de falsos acodamientos de las arterias subclavias debido a la posición de los miembros superiores al realizar una TAC torácica.
Aunque ambas arterias subclavias son potencialmente accesibles, casi todos los procedimientos se realizan por el lado izquierdo, ya que el acceso derecho implica una mayor tortuosidad y una alineación posterior con el anillo aórtico notablemente más compleja.
El abordaje de la arteria subclavia puede realizarse a través de una incisión infraclavicular en su tercio medio, con una longitud de 4-5cm, para acceder a su parte más distal. Es importante considerar que, en esta zona, la arteria subclavia presenta numerosas ramificaciones pequeñas, lo que puede complicar la hemostasia. Una alternativa es acceder a la arteria axilar mediante una incisión más distal, paralela al surco deltopectoral. Utilizando un separador autoestático de Adson, se diseca el tejido subcutáneo hasta llegar a la fascia del pectoral mayor. A continuación, se diseca este músculo para acceder al pectoral menor. El músculo pectoral menor se tracciona lateralmente o se secciona parcialmente, exponiendo así el paquete axilar. Después de disecar la vaina del paquete vascular axilar, se visualizan la vena axilar y, en un plano superior y más profundo, la arteria axilar (fig. 2B). Una vez controlada la arteria con dos vessel loop, se procede a realizar una sutura en «bolsa de tabaco» con Prolene® 5/0 o una sutura simple con teflón en forma de «U». Sin embargo, basados en nuestra experiencia, hemos optado por no realizar ninguna sutura previa al implante, reconstruyendo simplemente la arteria con una sutura longitudinal simple al finalizar el procedimiento, lo que reduce significativamente la probabilidad de estenosis residual.
Consideraciones y complicacionesUna de las principales desventajas de la vía TS es su mayor tasa de ACV comparado con otras vías20. El mecanismo del accidente cerebrovascular es probablemente multifactorial, incluyendo una mayor carga aterosclerótica de estos pacientes sin TF, mayor prevalencia de enfermedad cerebrovascular, acceso axilar/subclavia izquierdo versus derecho, diámetro del vaso y riesgo de oclusión de la arteria vertebral durante la colocación del introductor, severidad de la calcificación del arco aórtico, y uso de dilatación pre y posprocedimiento19.
Ciertos factores anatómicos pueden limitar la vía TS como la ruta de acceso alternativo preferido para la TAVI, tales como tortuosidad significativa del vaso, tamaño inadecuado del vaso, presencia de un bypass coronario con arteria mamaria interna izquierda permeable, angulación pronunciada de la subclavia al arco (por ejemplo, >80°), y angulación significativa de la raíz aórtica (≤70° para la subclavia izquierda, ≤30° para la derecha en Evolut R, Medtronic Minneapolis, MN US). Sin embargo, en casos de tortuosidad o limitación de tamaño del vaso, podría ser factible un abordaje supraclavicular a la arteria subclavia 5.
La vía TS puede lograrse tanto percutánea como quirúrgicamente, ofreciendo ambos accesos resultados comparables a corto plazo. Sin embargo, el acceso TS percutáneo representa un desafío técnico, sobre todo en pacientes con obesidad, y que el control de la arteria de urgencia podría ser técnicamente difícil en casos de complicación vascular. De hecho, Dahle et al.5, demostraron que al utilizar una válvula cardíaca transcatéter expandible con balón, el acceso percutáneo frente al acceso quirúrgico a la arteria axilar/subclavia tuvo resultados similares. Esto plantea la pregunta de si los costes adicionales del equipo y la complejidad asociada con el acceso percutáneo a expensas de una incisión de 4-5cm son necesarios. Dada la proximidad del plexo braquial a la arteria axilar, los riesgos asociados con un acceso percutáneo fallido que lleve a complicaciones neurológicas pueden ser devastadores. Además, uno de los beneficios no intencionados de un abordaje quirúrgico es que si el paciente desarrolla un bloqueo cardíaco completo que requiere la implantación de un marcapasos permanente, este puede ser realizado a través del mismo sitio de acceso inmediatamente después.
ResultadosEn una población de riesgo intermedio/alto, los resultados de la TAVI a través del acceso TS arrojan tasas de mortalidad del 3 al 10% a 30 días y del 20 al 30% al año. En términos de morbilidad, la TAVI TS destaca positivamente con menos transfusiones, menor tiempo de ventilación, y menos fibrilación auricular postoperatoria21. Sin embargo, la posibilidad de accidentes cerebrovasculares es una constante preocupación, con un riesgo del 6,1% según el registro de terapia de válvula transcatéter (TVT) y del 6,5% en el ensayo Pivotal CoreValve US5,22.
TAVI transcarotídea (TC-TAVI): consideraciones técnicas y riesgos asociadosHistoriaEl acceso TC para la TAVI fue descrito por primera vez en 2010 por Modine et al.23, mientras que el acceso a través del tronco braquiocefálico (TBC) fue descrito en el año 2012 por Philipsen et al.24.
ProcedimientoEl abordaje a la arteria carótida común (ACC) se realiza mediante una pequeña incisión de 4-5cm a lo largo del borde medial del músculo esternocleidomastoideo cerca de la escotadura esternal (fig. 2C). Este método es relativamente sencillo debido a la ubicación superficial de la ACC, incluso en pacientes con obesidad. Además, las ACC a menudo están libres de enfermedad ateromatosa, a diferencia de las arterias carótidas internas, y suelen estar menos afectadas en comparación con las arterias femorales, incluso en pacientes con múltiples factores de riesgo cardiovascular y enfermedad vascular periférica grave20,25.
El procedimiento se puede realizar bajo anestesia general o sedación consciente con anestesia local26.
El acceso TC se considera factible si el diámetro luminal mínimo de la ACC es ≥6mm. La presencia de estenosis contralateral significativa (≥70%) u oclusión de la ACC o arteria carótida interna contralateral se considera una contraindicación absoluta para el procedimiento27,28. Generalmente se prefiere el lado izquierdo, ya que la ACC izquierda ofrece una alineación coaxial superior entre la raíz aórtica y el sistema de liberación de la válvula transcatéter, pero ambos lados pueden utilizarse.
Para ser elegible para el acceso a la arteria braquiocefálica en la TAVI (fig. 2D), se deben cumplir varias condiciones24,29:
- •
Calibre mínimo recomendado 8mm, asegurando una relación de calibre introductor/arteria de menos de 1. El TBC suele presentar la ventaja de ser de mayor calibre que las ACC y, por tanto, no ser oclusivo el introductor.
- •
Distancia mínima recomendable (sobre todo con prótesis autoexpandibles) del punto de acceso en el TBC al anillo aórtico de, al menos, 6cm. En esta vía, la mayor proximidad al plano del anillo aórtico supone una desventaja por la mayor incomodidad con sistemas de liberación e introductores largos.
- •
Relación entre el origen del TBC con el esternón. Si la bifurcación del TBC alcanza el nivel del tercio superior del manubrio esternal, se puede acceder al TBC a través de una incisión supraesternal. En caso de una bifurcación más caudal, situada detrás del esternón, se puede realizar una esternotomía superior en forma de J parcial al 2.° espacio intercostal, sin abrir la cavidad pericárdica o pleural.
- •
Relación con estructuras circundantes del TBC: un tiroides agrandado o retracción de tejidos blandos después de cirugía cervical o radioterapia previa puede impedir el acceso al TBC, pero no son contraindicaciones absolutas.
Tanto en el acceso TC como a través del TBC, es fundamental monitorizar e identificar precozmente cualquier alteración de la perfusión cerebral. Por ello, la monitorización intraoperatoria incluye el empleo de un sistema de índice biespectral bilateral y de pulsioximetría cerebral bilateral.
La ACC proximal se ocluye inicialmente durante 2min, mientras se monitoriza la presión arterial distal y la oxímetría cerebral. Los signos de alerta durante este procedimiento incluyen una caída en la presión arterial media retrógrada a menos de 30mmHg o una disminución mayor al 50% en la oximetría cerebral. En casos donde se sospecha un compromiso de la perfusión cerebral debe reconsiderarse una vía de acceso vascular alternativa. Si la alteración de la perfusión cerebral ocurre después de la colocación del introductor, se podría usar un shunt femoro-carotídeo temporal para asegurar una perfusión cerebral adecuada, aunque esto rara vez es necesario.
Consideraciones y complicacionesLa principal preocupación al utilizar la vía TC para la TAVI es el riesgo potencial de ACV tanto inherente a la propia técnica de implante transcatéter de la válvula aórtica como a la manipulación quirúrgica de una de las ACC. Sin embargo, como veremos más adelante, la tasa de ACV asociada a la vía TC no es superior a la reportada en otros accesos vasculares20,30. De hecho, distintos autores22,31 han reportado que los eventos neurológicos no siempre ocurren en el mismo lado que la ACC usada en el procedimiento TAVI. Esto indica que, además de la manipulación de la arteria carótida, otros factores como la fibrilación auricular posprocedimiento, la hipotensión durante el procedimiento, la insuficiente perfusión de la carótida contralateral y el despliegue de la válvula transcatéter pueden influir en la aparición de estos eventos neurológicos31.
El riesgo de lesión del nervio vago durante la TAVI TC es bajo entre el 1,3 y el 2,4%3,32. Los factores que pueden aumentar el riesgo incluyen la edad avanzada, la presencia de enfermedades crónicas como la diabetes, el tamaño de la válvula aórtica artificial, y la experiencia del cirujano. En la mayoría de los casos, la lesión del nervio vago es temporal y los síntomas se resuelven por sí solos en unas semanas. Sin embargo, en algunos casos, la lesión puede ser permanente y provocar problemas como la disfonía, la disfagia o la bradicardia.
El acceso TC para la TAVI tiene algunas limitaciones que pueden dificultar su adopción generalizada, incluyendo la necesidad de una incisión quirúrgica, el riesgo de complicaciones en el manejo de las vías respiratorias y la necesidad de evaluaciones preoperatorias detalladas de la circulación cerebral. Además, en pacientes con funcionalidad limitada del polígono de Willis, puede ser necesario el uso de un shunt externo fémoro-carotídeo durante la operación, lo que añade complejidad al procedimiento.
ResultadosLas tasas de mortalidad a 30 días oscilan del 3 al 8%, mientras que la tasa de mortalidad a un año varía del 13 al 17% después de la TAVI TC26,33,34.
En un subanálisis del registro FRANCE TAVR, comparando la TAVI TC con la TAVI TS, la vía TC se asoció con una tasa significativamente menor de complicaciones vasculares, pero una mayor tasa de sangrado mayor y lesión renal aguda35. No obstante, la tasa de ACV fue similar entre ambos accesos con un 3,6% en el grupo TC y un 5% en el grupo TS35.
En un estudio de Kirker et al.34, del registro STS/ACC TVT, se compararon pacientes sometidos a la TAVI por vías TC y TS. Aunque la mayoría de los resultados intrahospitalarios fueron similares entre los 2 grupos, la vía TC tuvo una tasa significativamente menor de accidentes cerebrovasculares comparada con la TS (4,2 vs. 7,4%)34.
En un reciente metaanálisis, Abraham et al.30, compararon diferentes métodos de acceso para la TAVI, encontrando que el acceso TC presentó una mayor tasa de mortalidad al mes respecto al TF, pero menos complicaciones vasculares mayores durante la hospitalización. Comparado con el acceso TS, tuvo menos complicaciones vasculares, pero más hemorragias mayores30. La TAVI TAo mostró tasas de mortalidad intrahospitalaria y a 30 días más altas que la TC30. En comparación con el acceso TA, el TC redujo numéricamente la mortalidad y las complicaciones, aunque sin significación estadística30. No obstante, el hallazgo más importante de ese metaanálisis es que no se encontró un aumento en el riesgo de ACV con el acceso TC comparado con el TF u otros accesos alternativos30.
ConclusionesDe acuerdo con el registro STS/ACC TVT, hasta el año 2019, más del 50% de los casos no-TF se realizaron mediante un enfoque IT36. Sin embargo, el uso de accesos IT ha disminuido gradualmente en los últimos 5 años debido a la aparición de los enfoques ET36. Alrededor del año 2017, el acceso TS comenzó a superar a los abordajes IT34,36. Posteriormente, los datos del año 2019 del registro STS/ACC TVT indicaron que el acceso TC emergió como una primera alternativa no-TF particularmente atractiva34,36.
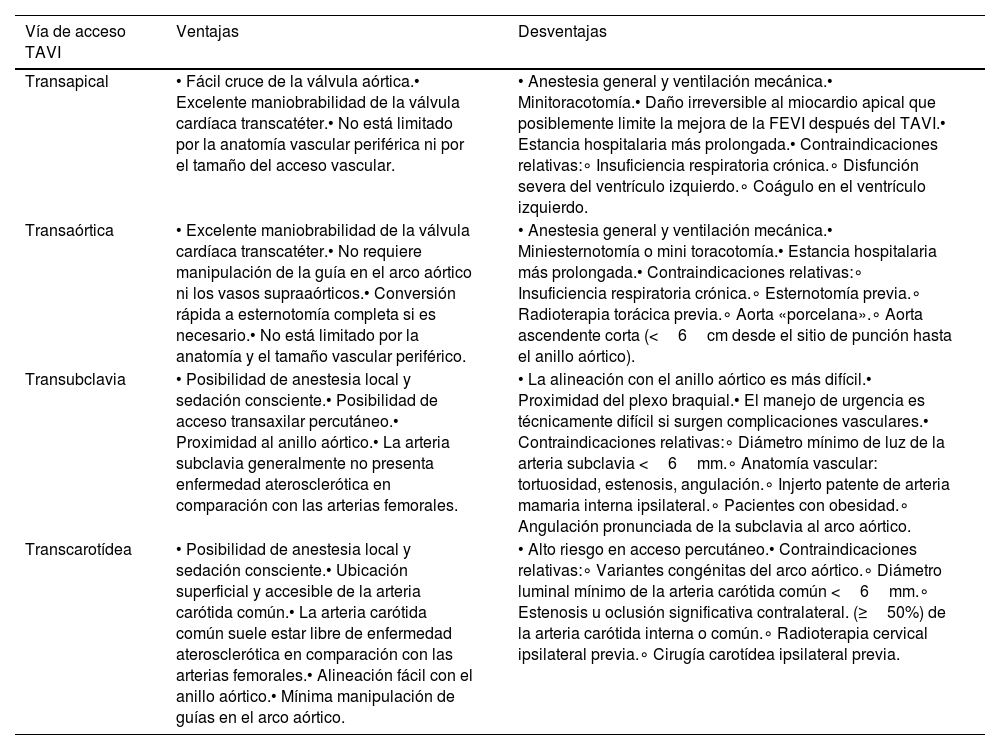
La evidencia de estudios grandes no aleatorizados indica una menor morbimortalidad en los accesos a la TAVI realizados por vía ET, tanto TC como TS, comparados con los accesos IT (TA/TAo)20,21,37. La tabla 1 resume las principales ventajas e inconvenientes de los accesos presentados en este artículo.
Ventajas y desventajas relativas asociadas con los diferentes enfoques TAVI
| Vía de acceso TAVI | Ventajas | Desventajas |
|---|---|---|
| Transapical | • Fácil cruce de la válvula aórtica.• Excelente maniobrabilidad de la válvula cardíaca transcatéter.• No está limitado por la anatomía vascular periférica ni por el tamaño del acceso vascular. | • Anestesia general y ventilación mecánica.• Minitoracotomía.• Daño irreversible al miocardio apical que posiblemente limite la mejora de la FEVI después del TAVI.• Estancia hospitalaria más prolongada.• Contraindicaciones relativas:∘ Insuficiencia respiratoria crónica.∘ Disfunción severa del ventrículo izquierdo.∘ Coágulo en el ventrículo izquierdo. |
| Transaórtica | • Excelente maniobrabilidad de la válvula cardíaca transcatéter.• No requiere manipulación de la guía en el arco aórtico ni los vasos supraaórticos.• Conversión rápida a esternotomía completa si es necesario.• No está limitado por la anatomía y el tamaño vascular periférico. | • Anestesia general y ventilación mecánica.• Miniesternotomía o mini toracotomía.• Estancia hospitalaria más prolongada.• Contraindicaciones relativas:∘ Insuficiencia respiratoria crónica.∘ Esternotomía previa.∘ Radioterapia torácica previa.∘ Aorta «porcelana».∘ Aorta ascendente corta (<6cm desde el sitio de punción hasta el anillo aórtico). |
| Transubclavia | • Posibilidad de anestesia local y sedación consciente.• Posibilidad de acceso transaxilar percutáneo.• Proximidad al anillo aórtico.• La arteria subclavia generalmente no presenta enfermedad aterosclerótica en comparación con las arterias femorales. | • La alineación con el anillo aórtico es más difícil.• Proximidad del plexo braquial.• El manejo de urgencia es técnicamente difícil si surgen complicaciones vasculares.• Contraindicaciones relativas:∘ Diámetro mínimo de luz de la arteria subclavia <6mm.∘ Anatomía vascular: tortuosidad, estenosis, angulación.∘ Injerto patente de arteria mamaria interna ipsilateral.∘ Pacientes con obesidad.∘ Angulación pronunciada de la subclavia al arco aórtico. |
| Transcarotídea | • Posibilidad de anestesia local y sedación consciente.• Ubicación superficial y accesible de la arteria carótida común.• La arteria carótida común suele estar libre de enfermedad aterosclerótica en comparación con las arterias femorales.• Alineación fácil con el anillo aórtico.• Mínima manipulación de guías en el arco aórtico. | • Alto riesgo en acceso percutáneo.• Contraindicaciones relativas:∘ Variantes congénitas del arco aórtico.∘ Diámetro luminal mínimo de la arteria carótida común <6mm.∘ Estenosis u oclusión significativa contralateral. (≥50%) de la arteria carótida interna o común.∘ Radioterapia cervical ipsilateral previa.∘ Cirugía carotídea ipsilateral previa. |
FEVI: fracción de eyección del ventrículo izquierdo; TAVI: implante valvular aórtico transcatéter.
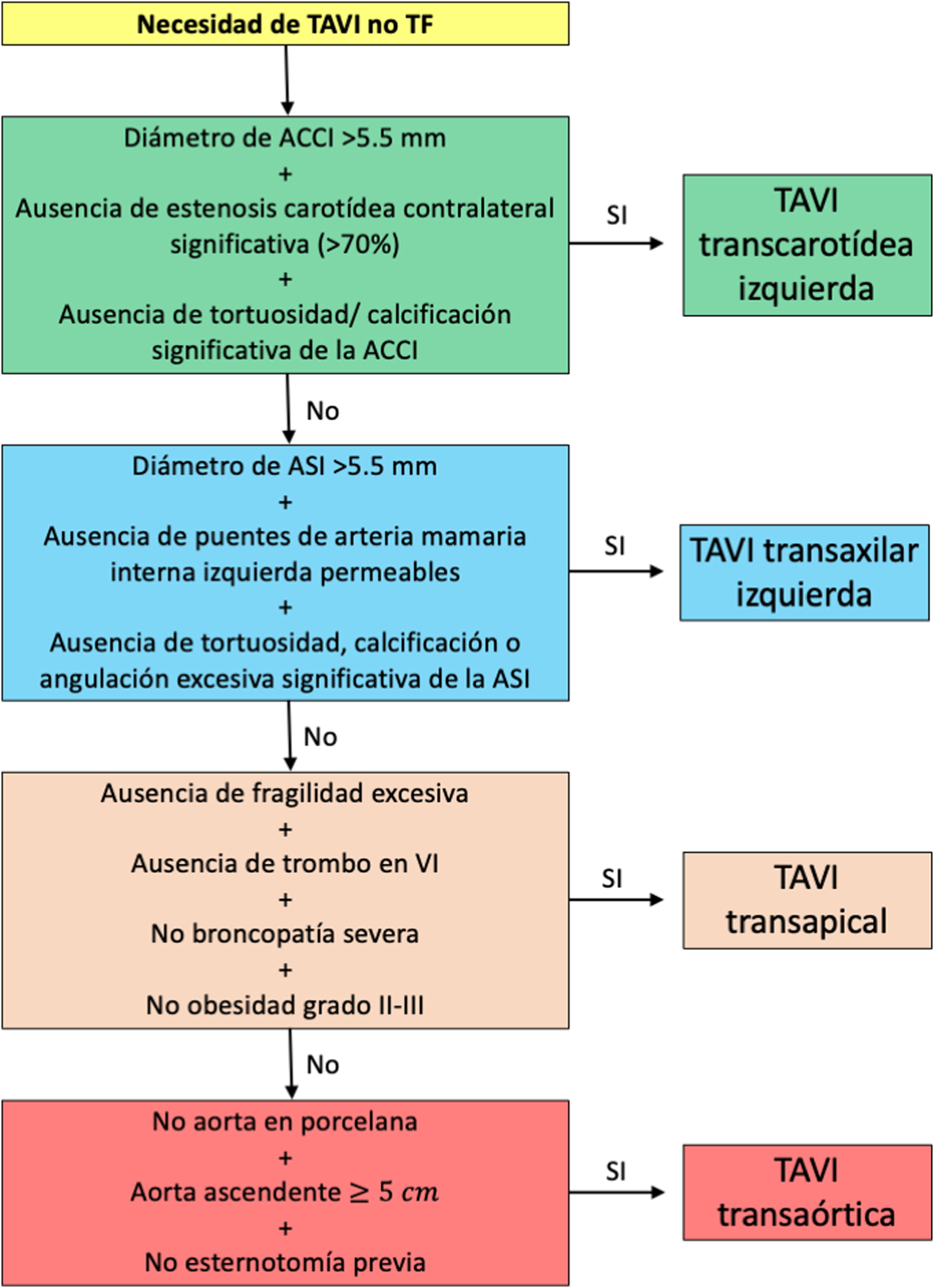
La evidencia científica actual expuesta en esta revisión, junto con los resultados de nuestra institución, han condicionado que nuestro algoritmo actual para la TAVI no-TF sea el representado en la figura 3.
Algoritmo de decisión para la selección del acceso no transfemoral en la implantación de válvula aórtica mediante catéter en el Servicio de Cirugía Cardiaca del Complejo Hospitalario Universitario de A Coruña. ACCI: arteria carótida común izquierda; ASI: arteria subclavia izquierda; TF: transfemoral.
A pesar de los claros beneficios de los accesos ET TAVI, su adopción global no ha sido tan amplia como se esperaba. Con el aumento de candidatos a la TAVI, especialmente de bajo riesgo, surge la necesidad urgente de accesos no-TF alternativos seguros que repliquen los resultados de la TAVI TF. El acceso alternativo óptimo aún está por determinarse, y las comparaciones directas entre las distintas estrategias no-TF deben interpretarse con precaución, aunque pueden ofrecer orientación sobre las ventajas y desventajas relativas de cada abordaje. La elección del sitio de acceso debe ser personalizada para cada paciente por un Heart Team experto, y los centros de la TAVI deberían dominar al menos 2 opciones no-TF, adaptando el tratamiento a las condiciones específicas del paciente y la experiencia del centro. Aunque en nuestra experiencia los resultados de los accesos ET son sobresalientes, hemos conservado el acceso TA para aquellos pacientes con enfermedad arterial periférica extensa en los que el acceso supraaórtico no sea viable.
Finalmente, cabe recordar que los accesos no-TF se reservan generalmente como alternativas secundarias cuando el acceso TF no es adecuado, complicando la evaluación de resultados post-TAVI. La falta de ensayos clínicos aleatorizados en esta área es una limitación notable, y se necesita más investigación comparativa entre abordajes TF con anatomía vascular de alto riesgo y alternativas ET para la TAVI.
Conflicto de interesesEl autor es proctor de Edwards Lifesciences.