La perforación aórtica secundaria a ingesta de espina de pescado es una rara y mortal afección; representa entre el 0,08 y el 0,1% de todos los casos de ingesta de cuerpos extraños. Su baja incidencia hace que su diagnóstico sea complicado, ya que no se piensa en esta insólita lesión. El diagnóstico y tratamiento temprano es definitivo en el pronóstico. Describimos detalladamente el manejo quirúrgico y anestésico con el cual se manejó el caso exitosamente, sin presentar daño neurológico ni medular. Este es un reporte de caso de un paciente con fístula aortoesofágica y mediastinitis secundaria a la deglución de un cuerpo extraño, y una revisión de la literatura actual, ya que es una afección mortal y de poca prevalencia.
Aortic perforation secondary to ingestion of a fish bone is a rare and fatal condition that occurs in between 0.08 and 0.1% of all cases of foreign body ingestion. Its low incidence makes its diagnosis complicated, since this unusual injury is often not considered. Early diagnosis and treatment are definitive in prognosis. The details are presented of the surgical and anaesthetic management of a case that was successfully managed without neurological or medullar damage. The case is presented of an aortoesophageal fistula and mediastinitis secondary to the swallowing of a foreign body, as well as a review of the current literature due to it being a low prevalence condition with a fatal outcome.
La ingesta de cuerpos extraños tiene una baja frecuencia en la población adulta (0,66 por 100.000 personas)1,2, siendo las espinas de pescado uno de los cuerpos extraños de mayor frecuencia3. La mayor parte de ellos pasa por el tubo digestivo y es eliminada con las heces sin ser detectada; sin embargo, ocasionalmente logran impactarse en algún sitio del tracto aerodigestivo, donde existe una alta probabilidad de producir complicaciones, como fístulas aortoesofágicas4.
En este reporte de caso presentamos el manejo quirúrgico y anestésico de una paciente con perforación aórtica secundaria a la ingesta de una espina de pescado.
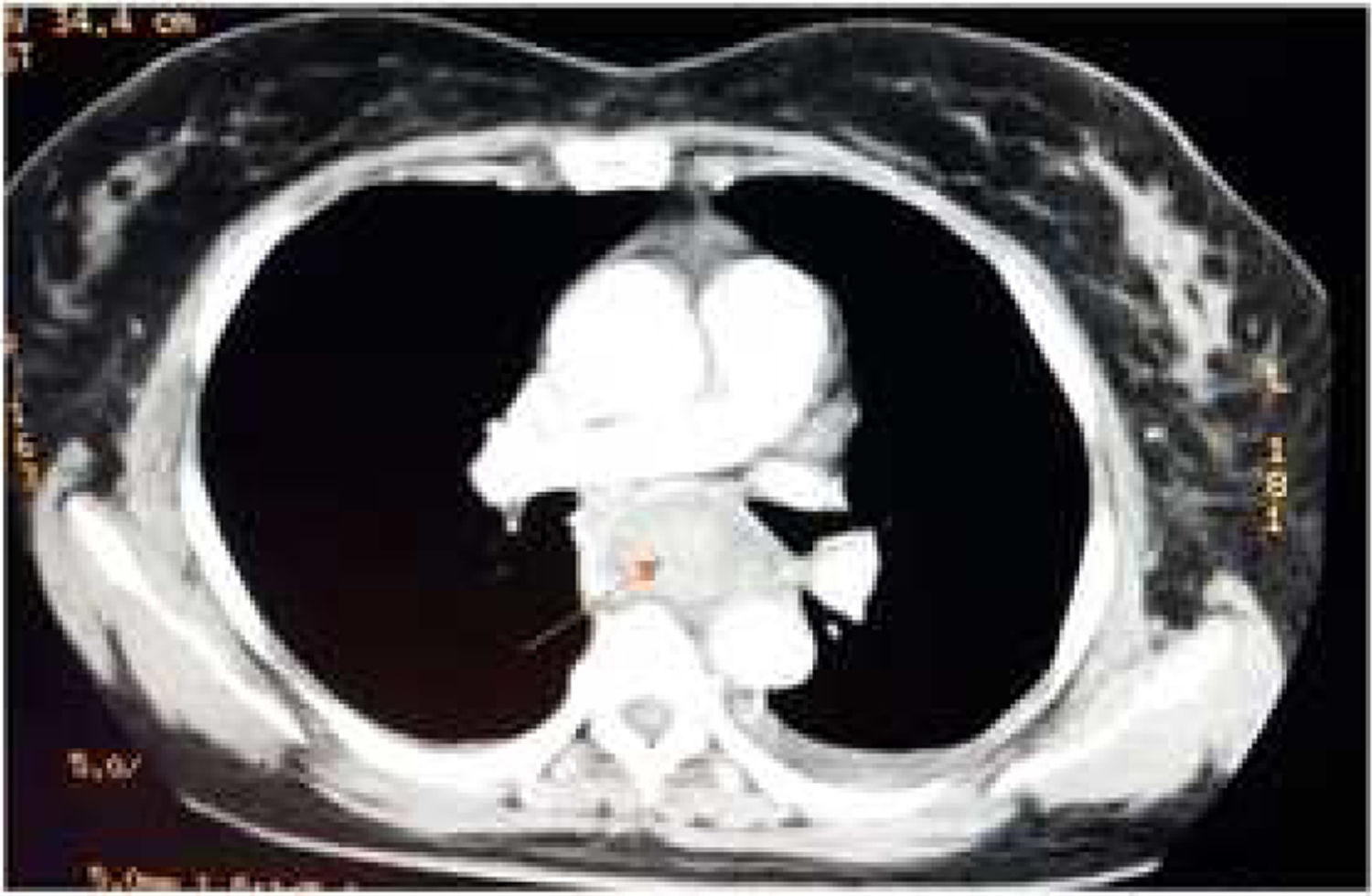
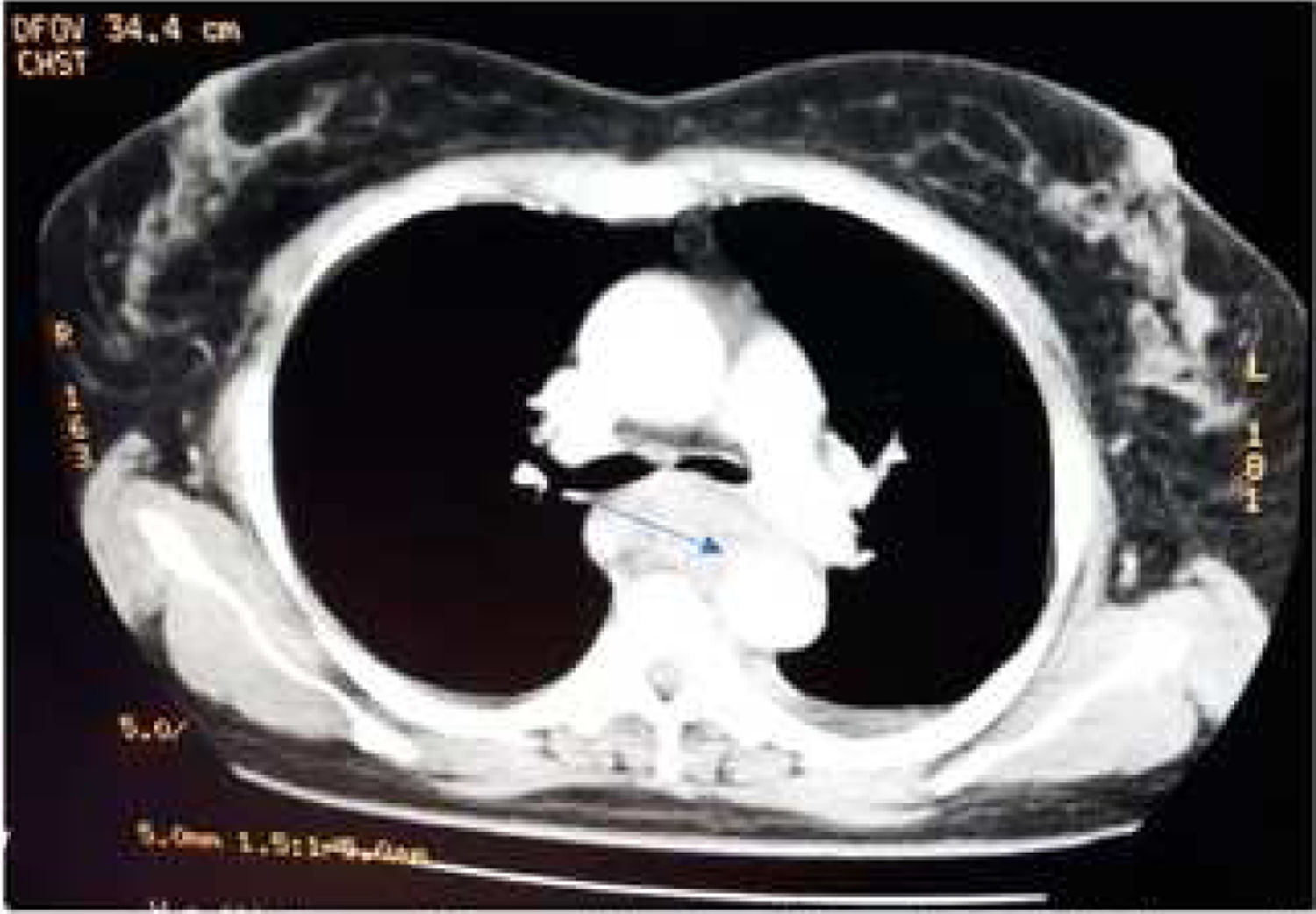
Caso clínicoPaciente femenino de 58 años, procedente de Supatá, Cundinamarca, ama de casa, sin antecedentes patológicos ni quirúrgicos de relevancia. Ingresó al hospital de tercer nivel por un cuadro de 6 días de evolución de disfagia secundaria a ingesta de cuerpo extraño (espina de pescado). En esa institución realizan una endoscopia de vías digestivas altas, que evidencia un cuerpo extraño a 25cm de la arcada dentaria, y realizan manejo mediante avance de este hasta cámara gástrica con posterior egreso hospitalario. Reingresa por episodio de dolor toracoabdominal, elevación de las cifras tensionales, hematemesis y melenas. Realizan toma de hemograma, donde se evidencia leucocitosis y anemia severa con requerimiento de transfusión de 2UI de glóbulos rojos; toman TAC de tórax, que mostró colección mediastinal en el tercio medial y distal esofágico con colección de aproximadamente 2cm con imagen de gas en su interior, compatible con absceso, además de alteración del contorno aórtico a la altura de la carina, sospechosa de lesión del espacio intramural o hematoma localizado (figs. 1 y 2), por lo que consideran perforación con lesión de aorta adyacente y remiten a nuestra institución para manejo por Cirugía Cardiovascular.
El día 22/04/2020 ingresó a la Unidad de Cuidados Intensivos de nuestra institución con presión arterial de 155/78mmHg, frecuencia cardiaca de 81lpm y temperatura de 36,6°C. Con el reporte de imágenes descritas, se tomaron nuevos paraclínicos con leucocitosis 19,5×103, Hb 9,3mg/dl, plaquetas 210×103, electrólitos con hipocalemia leve (K+ 3,3mEq/l), pruebas de función renal y gases arteriales dentro de los límites normales. Se inició manejo antibiótico con piperacilina-tazobactam 4,5g iv cada 6h, con indicación de infusión de nitroglicerina 0,5μg/kg/min para el mantenimiento de presiones arteriales medias objetivas entre 60-65mmHg, y gastroprotección con omeprazol 40mg.
Al siguiente día del ingreso se realiza nueva endoscopia de vías digestivas altas, con evidencia de fístula aortoesofágica con sangrado activo escaso. El manejo terapéutico consistió en la inserción endoscópica de stent esofágico metálico autoexpandible por el servicio de Gastroenterología, sin complicaciones. Se llevó a junta quirúrgica, donde en primera instancia se consideró manejo conservador con tratamiento antibiótico y manejo quirúrgico mediante endoprótesis; sin embargo, ante el deterioro clínico y hematológico dados por el empeoramiento de la anemia y el requerimiento transfusional, se decidió en junta médica quirúrgica realizar manejo quirúrgico vía abierta por parte de Cirugía Cardiovascular.
Se realizó manejo anestésico con monitorización invasiva con línea arterial radial derecha y femoral izquierda, catéter venoso central yugular interno derecho, inducción anestésica con midazolam 4mg, fentanilo 200μg, rocuronio 50mg, tubo doble luz izquierdo número 35, colocación de catéter intradural para monitorización de la presión intraespinal, drenaje de líquido cefalorraquídeo en caso de presión superior a 10mmHg, mantenimiento con sevoflurano 1MAC y fentanilo 2μg/kg/h, ácido tranexámico en infusión a 1μg/kg/h. Se tomó un ecocardiograma transesofágico, sin encontrar alteraciones estructurales cardiacas, y fracción de eyección conservada.
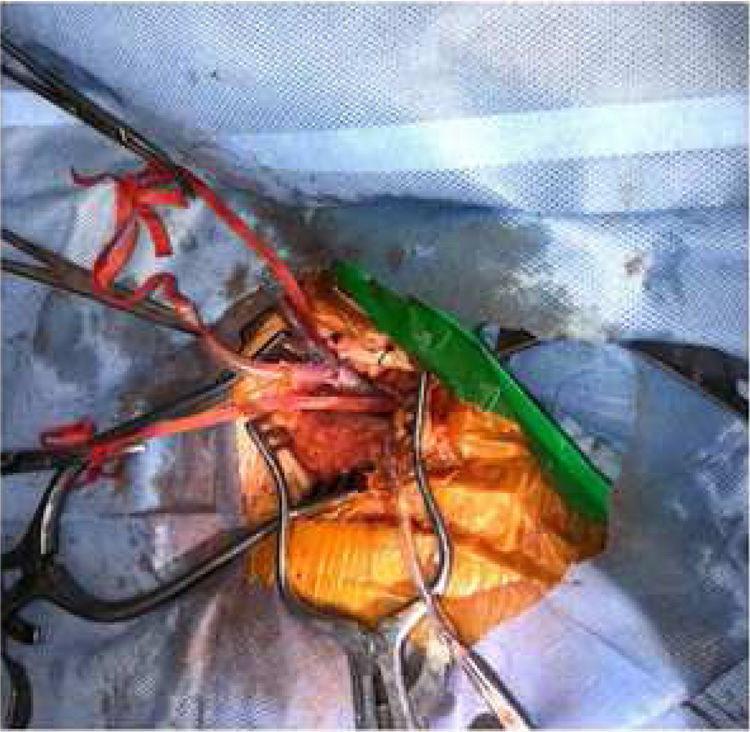
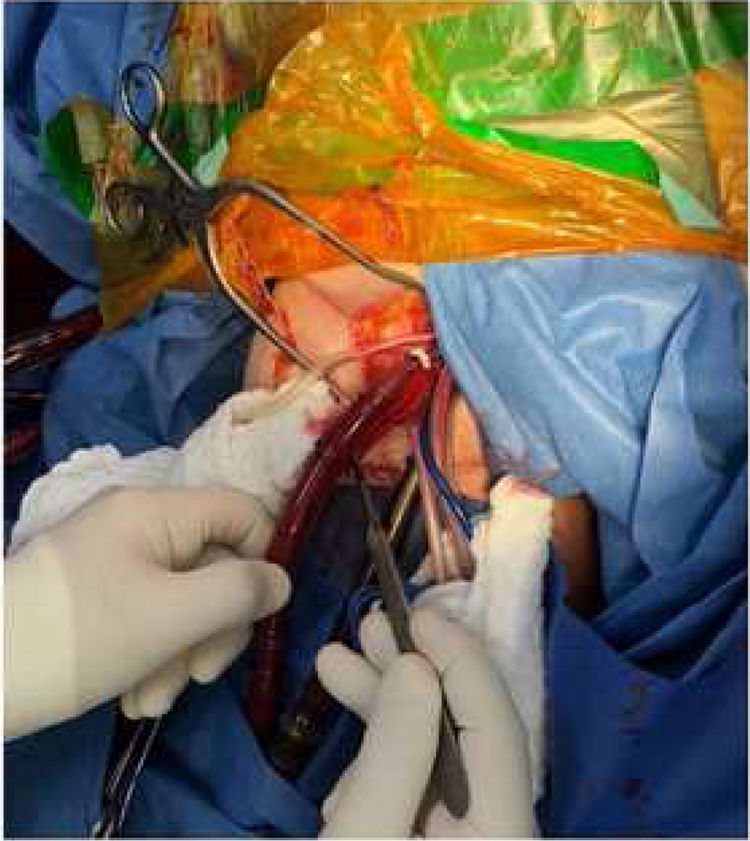
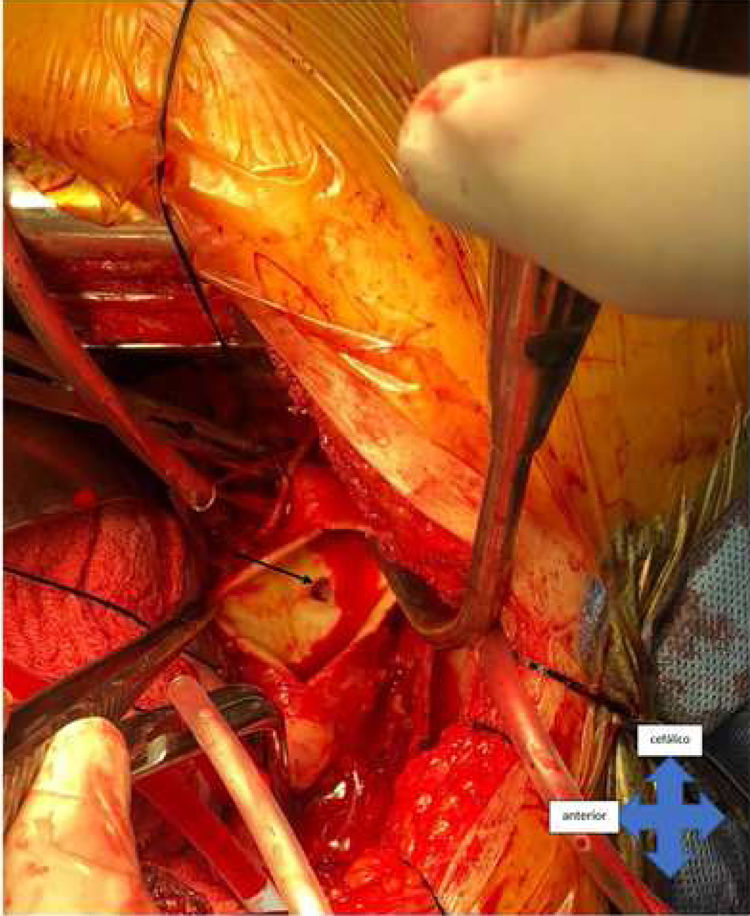
El manejo quirúrgico consistió en realizar doble canulación arterial (axilar y femoral) (figs. 3 y 4) y venosa única (femoral), abordaje mediante toracotomía posterolateral izquierda, disección de aorta torácica y control proximal y distal de la aorta respecto al segmento comprometido por proceso inflamatorio periaórtico. Se utilizó circulación extracorpórea e hipotermia moderada a 30°C, con doble pinzamiento de la aorta torácica, proximal por debajo de la arteria subclavia izquierda (T3) y distal (T6) lo más proximal posible, evitando comprometer la circulación de la médula espinal (T9-T12), logrando una adecuada exploración aórtica, donde se evidenció la rotura de la pared aórtica y una fístula aortoesofágica localizada a nivel de T4 (fig. 5), con proceso inflamatorio que comprometía un segmento de 10cm de la aorta torácica descendente. Al tener varios días de evolución el tejido aórtico inflamatorio, se decidió realizar reemplazo del segmento aórtico con una prótesis de dacrón de 24mm×10cm, control de los vasos intercostales y sutura del borde aórtico al tubo protésico para lograr el control hemostático, técnica de inclusión para evitar incrementar el daño al esófago. El tiempo de isquemia medular fue de 80min, y el de circulación extracorpórea, de 226min.
La paciente continuó el tratamiento en la Unidad de Cuidados Intensivos; 3 días después de la cirugía se retiró el soporte vasopresor, inotrópico y ventilatorio de forma exitosa, con una adecuada evolución clínica. Posteriormente se trasladó a hospitalización general, donde completó esquema antibiótico, inhaloterapia y rehabilitación cardiovascular.
Transcurridas 3 semanas se retira el stent esofágico sin complicaciones y se realiza control del esofagograma; se reinicia dieta y se da egreso nuevamente.
La paciente firmó el consentimiento informado para la publicación del caso.
DiscusiónLa fístula aortoesofágica es una rara complicación de la ingesta de cuerpos extraños, con incidencias que varían entre el 0,08 y el 0,1%5, sin embargo, presenta una elevada morbimortalidad. Entre las causas más comunes de esta se destaca la ingesta de cuerpos extraños con cerca del 19%, ocupando el segundo lugar por detrás de los aneurismas de aorta torácicos6. Teniendo en cuenta la alta mortalidad causada por la hemorragia masiva de las fístulas aortoesofágicas, la rápida actuación multidisciplinaria ante el diagnóstico es la clave de la supervivencia, por lo que estos casos deben ser manejados en instituciones de alto nivel de complejidad7. El tratamiento de esta rara afección se debe dar de manera inmediata tras el diagnóstico8.
Se ha evidenciado que el manejo conservador no tiene sobrevida a largo plazo9,10. Incluso el manejo convencional quirúrgico como intervención primaria no ha tenido resultados gratificantes9,11. Con el manejo quirúrgico abierto se han reportado tasas de mortalidad de entre el 0,30 y el 80%, mientras que con reparación endovascular torácica aórtica aislada estas se encuentran entre el 38,80 y el 100%.
En 1967 se describió la reparación anatómica con cierre del esófago en 2 planos y rafia en el defecto aórtico, pero es en 1969 cuando Yonago et al. reportan el primer superviviente con múltiples intervenciones de rafias aórticas hasta que finalmente se reemplazó con tubo de dacrón y cierre esofágico. En 1975 Laforet reporta el primer reparo definitivo6. En 1980, Ctercteko y Mok describieron una reparación exitosa esofágica y aórtica con pinzamiento secundario a un trauma esofágico aórtico por espina de pescado2. En 1991 con Parodi se pone en marcha el uso de prótesis endovasculares en la aorta que con el tiempo han tomado auge en tratamientos aórticos. En los casos de fístula aortoesofágica, se pueden realizar mediante vía endovascular y endoscópica; se han descrito casos exitosos en los cuales se despliega una endoprótesis en la aorta torácica y una prótesis recubierta a nivel esofágico en conjunto con tratamiento antibiótico7,10. La combinación entre manejo quirúrgico convencional y terapia endovascular, primero reparación endovascular torácica aórtica seguida de reparo quirúrgico abierto, mejora el pronóstico, con una mortalidad reportada de 25-37%9.
Actualmente el manejo antibiótico de amplio espectro, al igual que la reanimación hídrica y el manejo de transfusiones, es muy importante para llevar al paciente a cirugía en las mejores condiciones y evitar la expansión de la infección al mediastino y en el postoperatorio para prevenir la infección del injerto7,9,10. Varios grupos en el mundo recomiendan hoy en día el tratamiento endovascular, ya que permite controlar el sangrado inmediato en pacientes con o sin inestabilidad hemodinámica9,11,12.
Kubota et al. recomiendan que el primer paso para el manejo de la fístula aortoesofágica sea la realización inmediata de una reparación endovascular torácica aórtica en pacientes inestables, en principio como terapia puente y en algunos casos como terapia definitiva, como por ejemplo en los pacientes que no presenten contaminación por absceso. Sin embargo, es ampliamente aceptado que cualquier lesión penetrante en el esófago es un foco infeccioso, por lo cual algunos grupos consideran que en la gran mayoría de los pacientes la cirugía abierta debe ser realizada para el control infeccioso, que es de vital importancia en esta afección9.
Ha habido casos que incluso tras el manejo percutáneo por razones infecciosas han requerido una resección concomitante del esófago y el reemplazo protésico de la aorta con ascenso gástrico concomitante, con resultados exitosos9.
El manejo quirúrgico representa un gran desafío para el grupo, ya que se trata de una dolencia con una elevada mortalidad, motivo por el que se debe realizar una valoración multidisciplinaria y definir la conducta más adecuada para cada caso en particular. Se han reportado pocos casos exitosos con manejo quirúrgico abierto, siendo un procedimiento de alta dificultad técnica, con alto riesgo de paraplejia y muerte13.
La cirugía convencional incluye prótesis anatómicas, extraanatómicas, asociadas a reconstrucciones esofágicas (exclusión, reparo primario). La esternotomía con pinzamiento de la aorta ha mostrado pésimos resultados. El reparo primario del esófago solo es factible en lesiones muy pequeñas; en la mayoría de los casos se debe realizar esofaguectomía con interposición de flap de músculo intercostal pediculado, ubicado entre la aorta y el esófago. Assink et al. recomiendan que el manejo sea en este orden: control con tubo de Sengstaken-Blakemore, stent aórtico y, por último, reparación del esófago12.
En nuestro caso en particular se plantearon las diferentes posibilidades entre tratamiento conservador, manejo con stent esofágico y stent vascular, y cirugía convencional, que fue la decisión tomada por el grupo ante la reincidencia de sangrado y el posible desenlace fatal con hemorragia masiva. Se optó por el manejo por parte del servicio de Cirugía Cardiovascular, teniendo en cuenta como el objetivo principal, una vez controlado el compromiso esofágico con stent, el abordaje y control de la perforación a nivel de la aorta. Para esto se planteó la siguiente estrategia: minimizar el daño neurológico por compromiso medular, para lo que se decidió realizar el procedimiento en circulación extracorpórea con hipotermia moderada, la cual es otra de las estrategias utilizadas para la preservación de tejidos, ya que disminuye el consumo de oxígeno y adiciona protección neurológica14,15, como fue el caso de nuestra paciente, que se llevó a 30°C; adicionalmente se realizó perfusión medular por arteria vertebral vía arteria subclavia izquierda y vía femoral a la porción inferior de la aorta torácica durante el pinzamiento de la aorta; el pinzamiento se debe realizar lo más reducido posible en términos de extensión y tiempo para comprometer la menor cantidad posible de flujo medular. De esta forma disminuye de manera significativa la posibilidad de isquemia medular.
Así mismo, se debe destacar el manejo anestésico para este tipo de cirugía, debido al número de variables a manejar para obtener resultados postoperatorios satisfactorios. Factores como el compromiso orgánico transoperatorio, el elevado recambio de líquidos, la anemia, el requerimiento de vasopresores, el pinzamiento aórtico, entre otros, obligan a tener una valoración prequirúrgica completa (siempre que la estabilidad del paciente lo permita, incluyendo paraclínicos donde se evalué la función hematológica, renal y respiratoria) y una monitorización hemodinámica y de la presión de perfusión medular, considerando una tasa importante de complicaciones cardiovasculares y neurológicas derivadas de la alteración del flujo sanguíneo (como la paraplejia, la insuficiencia renal, el accidente cerebrovascular, la disfunción ventricular, el infarto agudo de miocardio y la muerte)16,17. Los objetivos anestésicos se centran en los momentos quirúrgicos de pinzamiento («clamp») y liberación aórtica, impidiendo las fluctuaciones hemodinámicas para evitar el sangrado por rotura o disección de la pared aórtica. Todos los esfuerzos quirúrgicos deben estar dirigidos a minimizar el tiempo de isquemia de órganos vitales durante el procedimiento; dentro de las estrategias se encuentran la perfusión aórtica distal con derivación cardiaca izquierda, el pinzamiento aórtico secuencial, la hipotermia sistémica permisiva y medidas neuroprotectoras para monitorizar la presión de perfusión medular14,17.
La monitorización debe incluir medidas no invasivas e invasivas; también se recomienda la monitorización neurológica con la medición de la presión intramedular y en ocasiones con potenciales evocados; la colocación de un catéter intrarraquídeo para medir la presión de perfusión medular se indica en todas las intervenciones aórticas abiertas o endovasculares de acuerdo con la recomendación del ACC/AHA. Se debe fijar de 8 a 10cm dentro del espacio intratecal15,18,19.
La intubación se debe realizar con un tubo endotraqueal de doble luz, siempre confirmando su ubicación por fibrobroncoscopio antes y después del posicionamiento definitivo del paciente, teniendo en cuenta el aislamiento pulmonar necesario para una toracotomía16,17.
El ecocardiograma transesofágico se utiliza para la evaluación directa y en tiempo real de la función miocárdica, así como para diagnosticar disecciones agudas y/o disfunciones valvulares aórticas. En el caso de la paciente se realizó tras la inducción, sin encontrar alteraciones cardiacas estructurales16,20.
En cuanto al uso de antifibrinolíticos como el ácido tranexámico a dosis de 30mg/kg para disminuir el requerimiento de transfusión durante la circulación extracorpórea, en nuestro caso se usó una infusión continua de ácido tranexámico, con buenos resultados16,17.
En el postoperatorio se debe establecer una evaluación neurológica temprana continua y en caso de no presentar deterioro neurológico se debe mantener la vigilancia incluso hasta 48h después de la cirugía.
ConclusionesEn esta infrecuente afección se han descrito múltiples posibilidades terapéuticas todas con mortalidad considerable a pesar de realizarse por personal idóneo.
El diagnóstico y abordaje es un reto para todo el equipo médico.
En este reporte se quiere proponer una vía de abordaje segura y exitosa utilizando bypass cardiopulmonar y colocando una prótesis de dacrón con técnica de inclusión. Destacamos el uso de medidas de valoración de la presión de perfusión medular con el fin de mejorar la morbimortalidad, influyendo en una variable determinante en este tipo de cirugía, dado que la anatomía de la circulación medular es más susceptible a isquemias.
Proponemos esta estrategia, que es una alternativa de abordaje segura y viable en muchas instituciones.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses con respecto al contenido del artículo.