La endocarditis infecciosa (EI) es una patología que conlleva una elevada morbimortalidad y representa un problema creciente de salud pública. El tratamiento quirúrgico es necesario en más de la mitad de los casos, y su principal finalidad es eliminar totalmente el tejido infectado y reconstruir la anatomía cardiaca normal, incluyendo la reparación o la sustitución de la/s válvula/s afectada/s.
Objetivo y métodosEl presente estudio se centra en describir el procedimiento más apropiado para la cirugía de reparación mitral en casos de EI, atendiendo a la literatura y a la amplia experiencia adquirida por parte del equipo quirúrgico. De igual modo, hemos recopilado a través de una búsqueda sistemática de la literatura los resultados que se han ido reportando sobre la cirugía reparadora en comparación con el reemplazo valvular mitral.
ResultadosLa técnica quirúrgica descrita requiere de un estudio minucioso del grado de afectación y desestructuración de los distintos segmentos valvulares. Consideramos que la resección con interposición de parche de pericardio y/o implante de neocuerdas de Goretex® es la técnica estándar que permite obtener resultados reproducibles. La revisión estructurada de las evidencias científicas disponibles verifica la seguridad de la reparación mitral para el tratamiento de la EI, aportando beneficios significativos en comparación con el reemplazo valvular.
ConclusiónLos resultados quirúrgicos evaluados sugieren que la cirugía de reparación mitral debería ser considerada el procedimiento de elección para el tratamiento quirúrgico de la EI, siempre que sea técnicamente posible.
Infective endocarditis (IE) is a pathology with a high morbidity and mortality rate and represents a growing public health problem. Surgical treatment is necessary in more than half of the cases, and its main purpose is to completely remove the infected tissue and reconstruct normal cardiac anatomy, including repair or replacement of the affected valve(s).
Objectives and methodsThe present study focuses on describing the most appropriate procedure for mitral repair surgery in cases of IE, based on the literature and the extensive experience gained by the surgical team. Likewise, we have compiled through a systematic search of the literature the results that have been reported on reparative surgery compared to mitral valve replacement.
ResultsThe surgical technique described requires a thorough study of the degree of involvement and destructuring of the different valve segments. We consider resection with pericardial patch interposition and/or Goretex® neochord implantation to be the standard technique that allows reproducible results. The structured review of the available scientific evidence verifies the safety of mitral repair for the treatment of IE, providing significant benefits compared to valve replacement.
ConclusionThe evaluated surgical results suggest that mitral repair surgery should be considered the procedure of choice for the surgical treatment of IE, whenever technically feasible.
La endocarditis infecciosa (EI) es una entidad nosológica relativamente poco frecuente, con una incidencia estimada de entre 3,1 a 7,9 casos por cada 100.000 habitantes/año. Sin embargo, conlleva una elevada morbimortalidad y un alto coste sanitario asociado1, lo que la convierte en un verdadero problema creciente de salud pública. De hecho, el análisis de los estudios publicados entre los años 2000 y 2020 señala que la incidencia de EI se ha duplicado a lo largo de esas dos décadas debido a múltiples causas, como podría ser el envejecimiento poblacional o el aumento de implantes de dispositivos, entre otras2.
El tratamiento quirúrgico es necesario en más de la mitad de los casos de EI3, principalmente cuando se acompañan de insuficiencia cardiaca, ante una infección no controlada o para la prevención de fenómenos embólicos4,5. El principal objetivo del procedimiento es eliminar totalmente el tejido infectado y reconstruir la anatomía cardiaca normal, incluyendo la reparación o la sustitución de la/s válvula/s afectada/s5. En este sentido, si la endocarditis afecta a las válvulas mitral o tricúspide, se ha de promover la reparación valvular, sobre todo cuando la infección se encuentra circunscrita a los velos y no hay una destrucción tisular significativa de estructuras adyacentes5. De hecho, una mayor extensión local de la infección, o la presencia de abscesos anulares o en la continuidad mitroaórtica no implica necesariamente una contraindicación para llevar a cabo una cirugía reparadora valvular. En centros con amplia experiencia, la reparación valvular mitral es una opción que proporciona buenos resultados quirúrgicos, llegando a realizarse con éxito hasta en el 80% de los casos6.
Sin embargo, debe señalarse que el tratamiento quirúrgico de la EI, principalmente si es urgente-emergente, presenta un elevado riesgo de morbimortalidad. Por ello, es esencial una correcta evaluación del riesgo-beneficio para asegurar el objetivo principal de la cirugía, que es la supervivencia del enfermo en ausencia de complicaciones, secuelas o cardiopatía estructural residual7. De esta forma, en primer lugar hay que estudiar la idoneidad del paciente para someterse a una cirugía reparadora, entendiendo que esta es más compleja que la sustitución valvular. Dos aspectos principales a considerar son la extensión de la infección y el grado de deterioro estructural, ya que un contexto desfavorable puede conducir a una insuficiencia mitral residual significativa.
El presente trabajo se centra en describir el procedimiento más apropiado para la cirugía de reparación mitral en casos de EI, atendiendo a la literatura y a la amplia experiencia adquirida por parte del equipo quirúrgico, así como a recopilar los resultados que se han ido reportando sobre la cirugía reparadora en comparación con el reemplazo valvular.
MétodosLa concreción de una técnica optimizada para la reparación mitral se ha fundamentado en un exhaustivo estudio de la literatura con la finalidad de recopilar todos los detalles principales del procedimiento8–12. Sobre estos, hemos incorporado detalles derivados de la amplia experiencia que ha ido adquiriendo nuestro equipo quirúrgico a lo largo del tiempo. Por otro lado, para analizar los resultados que se han ido reportando sobre la cirugía reparadora en comparación con el reemplazo valvular se llevó a cabo una revisión sistemática atendiendo a la declaración PRISMA 202013, realizando búsquedas en PubMed, Scopus y The Cochrane Library, empleando combinaciones de los términos «infective endocarditis», «mitral valve», «repair» y «replacement», para recopilar los estudios publicados entre enero de 2000 y junio de 2022 que se centran en comparar los resultados obtenidos con la reparación mitral frente a la sustitución valvular en pacientes con EI. Además, los artículos tenían que presentar al menos un indicador que permita comparar cuantitativamente los resultados proporcionados por ambas técnicas, tales como tasas supervivencia de cualquier naturaleza, de reintervención o estancia hospitalaria, entre otras. Del conjunto de estudios seleccionados inicialmente fueron excluidos los artículos basados en la revisión de la literatura, metaanálisis, resúmenes de congresos, revisiones de casos y cartas, así como publicaciones sobre la válvula aórtica, o aquellos que presentan factores de confusión de tipo diagnóstico y/o metodológico.
ResultadosTécnica quirúrgicaEl objetivo principal de la cirugía es la exéresis de todo el tejido infectado y la reconstrucción de la anatomía valvular, a través de una adecuada estandarización de la técnica de reparación que permita obtener resultados estables y reproducibles a corto, medio y largo plazo. Durante la evaluación de la válvula mitral debemos estudiar minuciosamente el grado de afectación y desestructuración de los distintos segmentos valvulares. Una afectación de un único velo, tanto de velo posterior como de velo anterior, es reconstruible con garantías suficientes para no incrementar el riesgo potencial de un reclampaje aórtico por fracaso de la técnica o de una insuficiencia mitral residual significativa en el postoperatorio.
La afectación de ambos velos o con presencia de abscesos anulares o de la continuidad mitroaórtica precisa de gran experiencia reparadora y de la interposición de una mayor cantidad de material de reconstrucción, lo que podría reducir de forma importante la tasa de éxito de la técnica y minimizar el potencial efecto beneficioso de la reparación en comparación con la sustitución valvular.
Nuestro grupo realiza de forma sistemática la reparación valvular mitral en los casos de EI con afectación del velo posterior o del velo anterior, tanto en adultos como en población infantil. La reparación, en caso de presentar una extensión local mayor de la enfermedad, se realiza en función de otros factores: edad del paciente, situación clínica, prioridad de la cirugía (emergente, urgente, urgencia diferida o programada), agente microbiológico implicado, enfermedad valvular previa (degenerativa o reumática), comorbilidades asociadas (procesos oncológicos activos o necesidad de otros procedimientos quirúrgicos), etc.
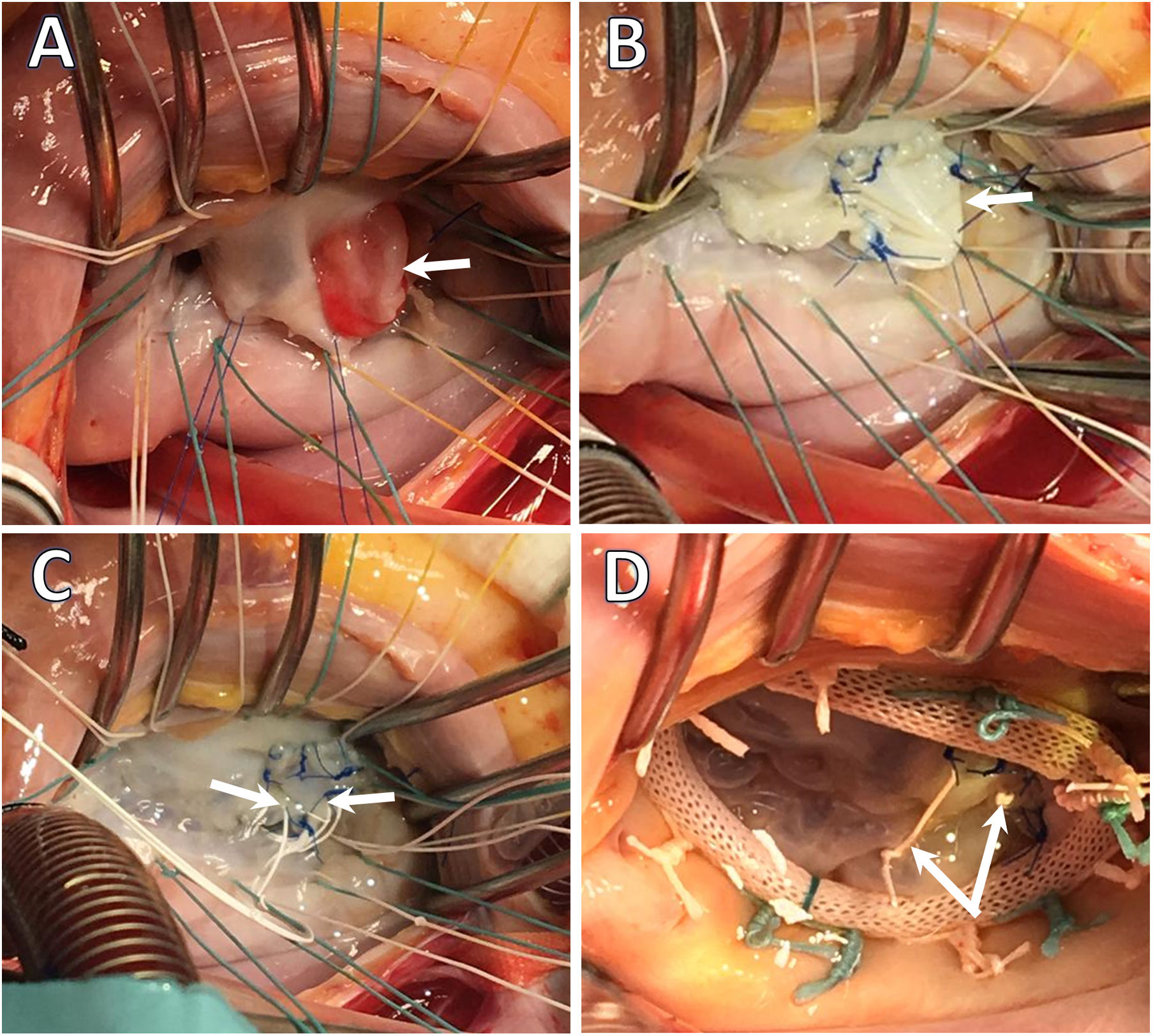
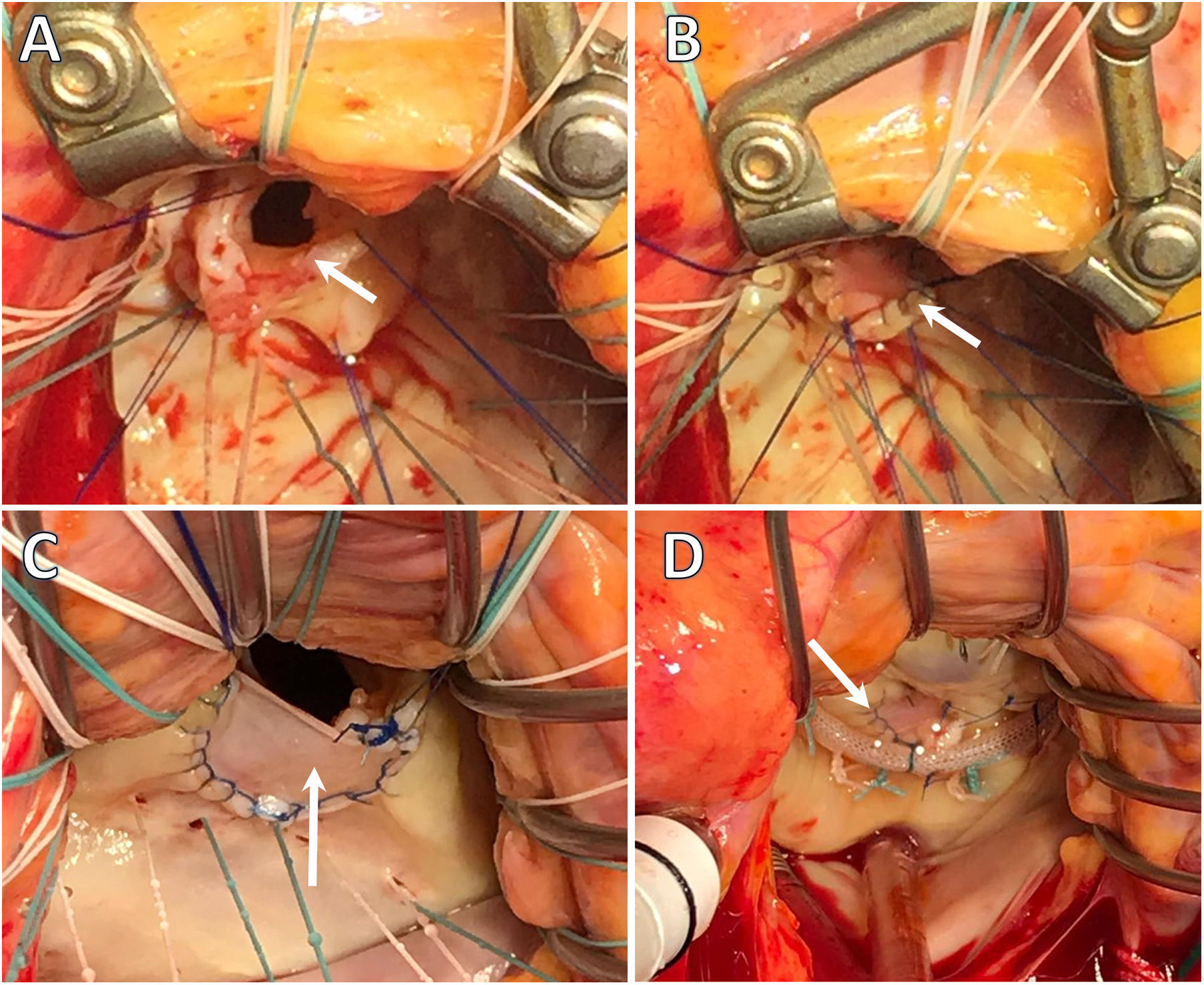
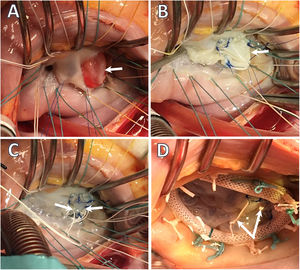
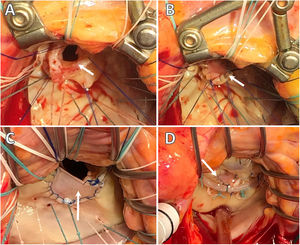
Atendiendo a nuestra experiencia en el procedimiento, consideramos que la resección con interposición de parche de pericardio y/o implante de neocuerdas de Goretex® es la técnica estándar que permite resultados reproducibles entre los cirujanos (figs. 1 y 2).
Endocarditis infecciosa. Imágenes intraoperatorias. Servicio de Cirugía Cardiovascular del HU Virgen de las Nieves. A) EI afectando al velo anterior. La flecha blanca señala la presencia de una gran vegetación que afecta a los segmentos A2 y A3. B) Reconstrucción del velo anterior tras la exéresis del tejido infectado mediante interposición de parche de pericardio equino (Matrix PatchTM), incluyendo el borde libre de A2/A3. C) Interposición de neocuerdas de Goretex 4/0 en el borde libre del neovelo para corregir el prolapso valvular. D) «Water-test» tras la reparación valvular con detalle de dos neocuerdas de Goretex 4/0.
Endocarditis infecciosa. Imágenes intraoperatorias. Servicio de Cirugía Cardiovascular del HU Virgen de las Nieves. A) Resección de tejido infectado de A2 con preservación del borde libre y cuerdas de primer orden normofuncionantes. B) Reconstrucción de la solución de continuidad postexéresis de velo anterior mediante interposición de parche de pericardio bovino. C) Reconstrucción de velo posterior, tras exéresis de tejido infectado de P2, mediante interposición de parche de pericardio bovino (detalle de sutura continua bloqueada polipropilene 5/0. D) «Water-test» tras la reconstrucción valvular e interposición de neocuerdas de Goretex 4/0 en el borde libre de neovelo.
En el caso de afectación de velo posterior, si el tejido afectado condiciona la exéresis de un fragmento inferior a la mitad de la anchura de un segmento del velo, procedemos a la resección triangular o cuadrangular del segmento, plicatura del anillo si precisa y reconstrucción directa del velo mediante sutura interrumpida en 8 de polipropilene 5/0.
Si el tejido afectado condiciona la exéresis de una mayor proporción de tejido (mayor o igual que la mitad de la anchura del segmento del velo) preferimos no condicionar el normal movimiento del velo con una técnica restrictiva que implica además una potencial plicatura excesiva del anillo posterior. En este caso tenemos que prestar atención a la implicación del borde libre del velo en la zona afectada y a la integridad y normal anatomía de las cuerdas tendinosas de primer orden. Así, si se presenta un borde libre íntegro con preservación de cuerdas tendinosas normofuncionales procedemos a resecar la parte afectada del velo posterior, preservando el borde libre y las cuerdas funcionales de primer orden. Seguidamente, se reconstruye la solución de continuidad con un parche de pericardio (bovino, equino o autólogo), empleando para ello una sutura continúa bloqueada de polipropilene 5/0.
En caso de que el borde libre se encuentre afectado por la extensión de la enfermedad, la resección del segmento implicado debe ser completa, procediendo a la reconstrucción del velo mediante la interposición de parche de pericardio (bovino, equino o autólogo), mediante una sutura continua bloqueada de polipropilene 5/0. Posteriormente y, tras verificar el probable prolapso del segmento reparado, se procede a implantar el número necesario de neocuerdas de Goretex® 4/0, para recuperar la coaptación duradera de los velos.
Si nos encontramos ante una afectación del velo anterior, el procedimiento irá dirigido a la exéresis y la reconstrucción con parche de pericardio (bovino, equino o autólogo) mediante sutura bloqueada 5/0 o 6/0. Durante el proceso, intentaremos preservar el borde libre y las cuerdas de primer orden anatómicamente funcionales. Si no es posible, y tras verificar el probable prolapso del velo, se procede a implantar el número necesario de neocuerdas de Goretex® 4/0 para recuperar la coaptación duradera de los velos.
Revisión sistemáticaLa revisión sistemática dirigida a recopilar los resultados de la cirugía reparadora en comparación con el reemplazo valvular nos proporcionó inicialmente 580 referencias, de las cuales quedaron 265 tras la eliminación de los documentos duplicados. Tras el estudio del título, resúmenes y texto completo, en su caso, aplicando los criterios de inclusión y exclusión referidos anteriormente seleccionamos finalmente siete estudios.
Los aspectos principales de los siete estudios se resumen en la tabla 1. Hemos podido constatar a través de las evidencias proporcionadas por los diferentes trabajos, que los resultados son más favorables hacia la cirugía de reparación mitral en comparación con la sustitución valvular. Así, los estudios realizados por Solari et al.14, Lee et al.15 y Ruttmann et al.16 encuentran una mayor supervivencia global, y una reducción de la mortalidad intrahospitalaria a corto y largo plazo, y del riesgo de accidente cerebrovascular, una menor tasa de transfusión de hemoderivados y una menor frecuencia de recurrencia infecciosa. En suma a lo anterior, no se describen resultados operativos contrarios a la reparación valvular mitral en los otros tres trabajos seleccionados. Los estudios realizados por Tepsuwan et al.17, Wang et al.18 y Jung et al.19 encuentran resultados similares en cuanto a mortalidad, supervivencia libre de reintervención y morbilidad asociada al tratamiento. Además, encuentran una mayor tasa de reinfección en los pacientes sometidos a cirugía de sustitución valvular, aunque las diferencias no alcanzaron significación estadística.
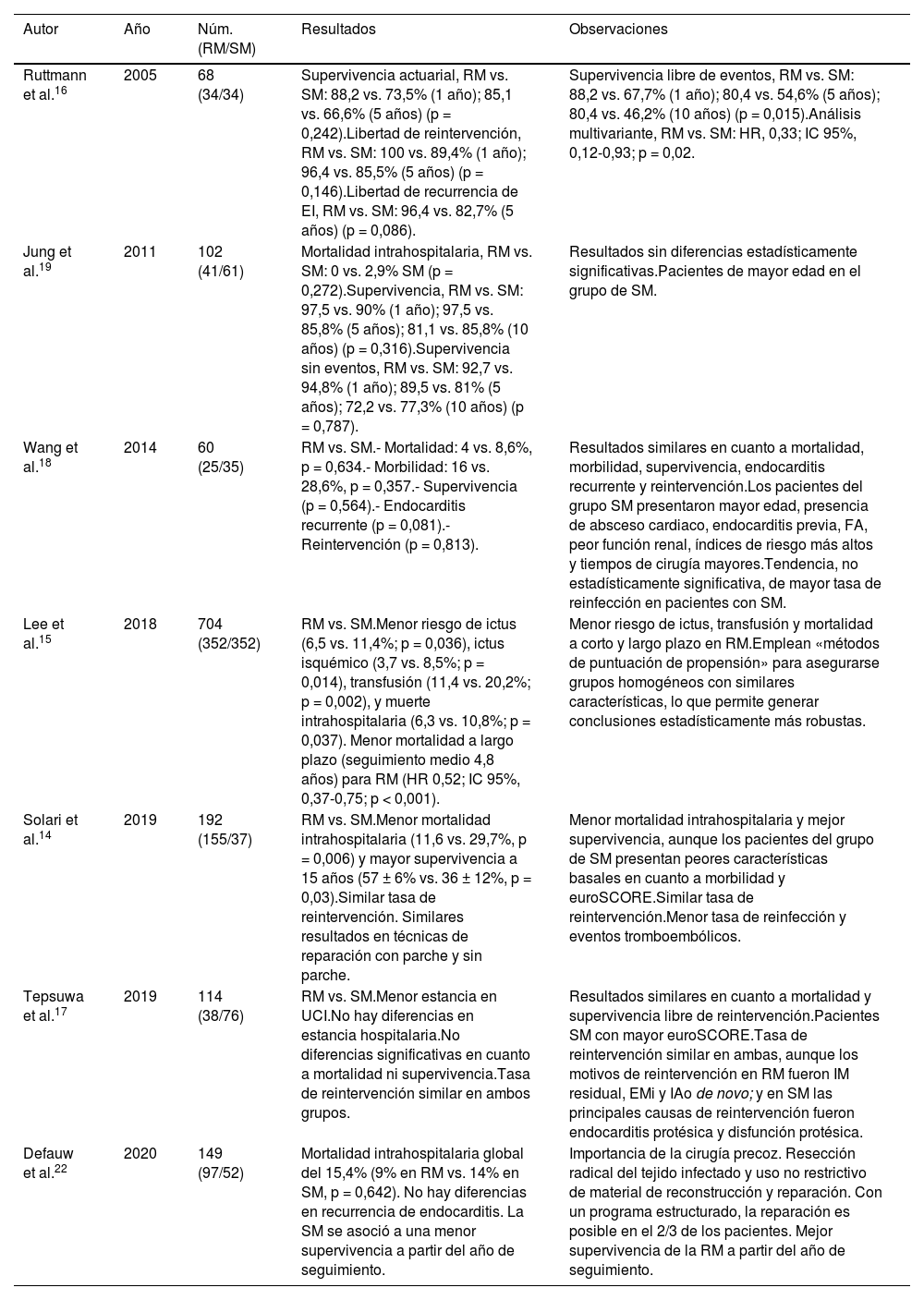
Descriptores generales y conclusiones principales de los siete estudios seleccionados a través de la revisión dirigida a comparar los resultados obtenidos mediante RM y SM
| Autor | Año | Núm. (RM/SM) | Resultados | Observaciones |
|---|---|---|---|---|
| Ruttmann et al.16 | 2005 | 68 (34/34) | Supervivencia actuarial, RM vs. SM: 88,2 vs. 73,5% (1 año); 85,1 vs. 66,6% (5 años) (p = 0,242).Libertad de reintervención, RM vs. SM: 100 vs. 89,4% (1 año); 96,4 vs. 85,5% (5 años) (p = 0,146).Libertad de recurrencia de EI, RM vs. SM: 96,4 vs. 82,7% (5 años) (p = 0,086). | Supervivencia libre de eventos, RM vs. SM: 88,2 vs. 67,7% (1 año); 80,4 vs. 54,6% (5 años); 80,4 vs. 46,2% (10 años) (p = 0,015).Análisis multivariante, RM vs. SM: HR, 0,33; IC 95%, 0,12-0,93; p = 0,02. |
| Jung et al.19 | 2011 | 102 (41/61) | Mortalidad intrahospitalaria, RM vs. SM: 0 vs. 2,9% SM (p = 0,272).Supervivencia, RM vs. SM: 97,5 vs. 90% (1 año); 97,5 vs. 85,8% (5 años); 81,1 vs. 85,8% (10 años) (p = 0,316).Supervivencia sin eventos, RM vs. SM: 92,7 vs. 94,8% (1 año); 89,5 vs. 81% (5 años); 72,2 vs. 77,3% (10 años) (p = 0,787). | Resultados sin diferencias estadísticamente significativas.Pacientes de mayor edad en el grupo de SM. |
| Wang et al.18 | 2014 | 60 (25/35) | RM vs. SM.- Mortalidad: 4 vs. 8,6%, p = 0,634.- Morbilidad: 16 vs. 28,6%, p = 0,357.- Supervivencia (p = 0,564).- Endocarditis recurrente (p = 0,081).- Reintervención (p = 0,813). | Resultados similares en cuanto a mortalidad, morbilidad, supervivencia, endocarditis recurrente y reintervención.Los pacientes del grupo SM presentaron mayor edad, presencia de absceso cardiaco, endocarditis previa, FA, peor función renal, índices de riesgo más altos y tiempos de cirugía mayores.Tendencia, no estadísticamente significativa, de mayor tasa de reinfección en pacientes con SM. |
| Lee et al.15 | 2018 | 704 (352/352) | RM vs. SM.Menor riesgo de ictus (6,5 vs. 11,4%; p = 0,036), ictus isquémico (3,7 vs. 8,5%; p = 0,014), transfusión (11,4 vs. 20,2%; p = 0,002), y muerte intrahospitalaria (6,3 vs. 10,8%; p = 0,037). Menor mortalidad a largo plazo (seguimiento medio 4,8 años) para RM (HR 0,52; IC 95%, 0,37-0,75; p < 0,001). | Menor riesgo de ictus, transfusión y mortalidad a corto y largo plazo en RM.Emplean «métodos de puntuación de propensión» para asegurarse grupos homogéneos con similares características, lo que permite generar conclusiones estadísticamente más robustas. |
| Solari et al.14 | 2019 | 192 (155/37) | RM vs. SM.Menor mortalidad intrahospitalaria (11,6 vs. 29,7%, p = 0,006) y mayor supervivencia a 15 años (57 ± 6% vs. 36 ± 12%, p = 0,03).Similar tasa de reintervención. Similares resultados en técnicas de reparación con parche y sin parche. | Menor mortalidad intrahospitalaria y mejor supervivencia, aunque los pacientes del grupo de SM presentan peores características basales en cuanto a morbilidad y euroSCORE.Similar tasa de reintervención.Menor tasa de reinfección y eventos tromboembólicos. |
| Tepsuwa et al.17 | 2019 | 114 (38/76) | RM vs. SM.Menor estancia en UCI.No hay diferencias en estancia hospitalaria.No diferencias significativas en cuanto a mortalidad ni supervivencia.Tasa de reintervención similar en ambos grupos. | Resultados similares en cuanto a mortalidad y supervivencia libre de reintervención.Pacientes SM con mayor euroSCORE.Tasa de reintervención similar en ambas, aunque los motivos de reintervención en RM fueron IM residual, EMi y IAo de novo; y en SM las principales causas de reintervención fueron endocarditis protésica y disfunción protésica. |
| Defauw et al.22 | 2020 | 149 (97/52) | Mortalidad intrahospitalaria global del 15,4% (9% en RM vs. 14% en SM, p = 0,642). No hay diferencias en recurrencia de endocarditis. La SM se asoció a una menor supervivencia a partir del año de seguimiento. | Importancia de la cirugía precoz. Resección radical del tejido infectado y uso no restrictivo de material de reconstrucción y reparación. Con un programa estructurado, la reparación es posible en el 2/3 de los pacientes. Mejor supervivencia de la RM a partir del año de seguimiento. |
EMI: estenosis mitral; FA: fibrilación auricular; HR: riesgo relativo; IAo: insuficiencia aórtica; RM: reparación mitral; SM: sustitución valvular mitral.
La cirugía de reparación mitral en pacientes con EI es una estrategia quirúrgica segura, que proporciona resultados globales superiores a la sustitución valvular. Los estudios más relevantes realizados y seleccionados en el presente trabajo muestran una ventaja significativa en los resultados quirúrgicos de los pacientes sometidos a reparación mitral, con una menor mortalidad y una mayor supervivencia libre de eventos, tales como recurrencia de la endocarditis, reintervención, etc.14,16–18
Si bien es cierto que podemos apreciar cierta discrepancia en dichas publicaciones, ninguno de los estudios muestra resultados inferiores en los brazos de pacientes tratados mediante reparación. Este hecho es de gran importancia, pues evidencia de forma clara el gran perfil de seguridad del procedimiento quirúrgico reparador en grupos expertos (tabla 1).
Hay que tener en cuenta que en algunos trabajos aparece un sesgo de selección, ya que los pacientes sometidos a cirugía de sustitución valvular presentan tanto escalas de riesgo más elevadas, como una mayor comorbilidad y mayor edad14,17. Sin embargo, el estudio realizado por Lee et al.15 aporta datos concluyentes derivados de un diseño que presenta una objetiva homogeneidad en los grupos pacientes con EI comparados. Además, cuenta con el tamaño muestral más grande de entre todas las publicaciones seleccionadas (704 pacientes), e incorporar «métodos de puntuación de propensión», lo que asegura un preciso ajuste de características basales y comorbilidades entre ambos brazos de pacientes20. Los resultados mostrados por dicho grupo son más favorables a la reparación mitral, en términos de complicaciones periprocedimiento y mortalidad a corto y largo plazo.
Por otro lado, el análisis global de la evidencia refleja una menor tendencia a la reinfección y a la presencia de endocarditis recurrente, lo que probablemente se deba a una menor utilización de material protésico, tal y como señala Dreyfus et al.21. El metaanálisis de He et al.7 señala que la reparación valvular mitral puede ser la primera opción terapéutica, siendo la técnica de elección para el tratamiento quirúrgico de la EI mitral siempre que sea anatómicamente posible7. Autores como Defauw22 o el grupo de El Koury23 señalan, además, que una cirugía precoz de la endocarditis es un aspecto clave para conseguir una elevada tasa de reparabilidad.
A pesar de ello debemos señalar que la reparación mitral en pacientes con EI implica la realización de técnicas resectivas y reconstructivas que pueden ser de alta complejidad, y que requieran de tiempos de isquemia y de circulación extracorpórea elevados. Hay múltiples técnicas descritas para estos pacientes, lo que conjuntamente representa una amplia variabilidad metodológica. Este hecho no es más que el reflejo de la diversidad de patrones de afectación anatómica y de extensión que la endocarditis produce en la válvula mitral y en los tejidos adyacentes. Dentro de las técnicas que se emplean en centros con amplia tasa de reparación, las más frecuentes descritas por Solari et al.23 son las reconstrucciones con parche de pericardio bovino o autólogo, transferencia de P2 («flip over») para defectos de A2, autoinjertos de válvula tricúspide o la utilización de homoinjertos totales o parciales de válvula mitral.
La complejidad de los programas de reparación mitral en endocarditis se incrementa si tenemos en cuenta la variabilidad técnica y la reducida incidencia anual de esta patología, lo que justifica en gran medida que la indicación de reparación mitral en endocarditis continúe siendo baja23. Por este motivo, la mayor parte de los estudios disponibles tienen un rango temporal de inclusión de pacientes de más de 15 años, con un número relativamente bajo de casos.
Ante la situación de infrautilización de la cirugía reparadora mitral en la EI en nuestro medio, se debe proceder a la estandarización de la técnica a nivel de cada servicio asistencial, reduciendo en la medida de lo posible el componente operador-dependiente. El diseño tiene que contemplar las actuales técnicas de reparación valvular mitral basadas en el implante de neocuerdas de Goretex® y la reconstrucción de los defectos tisulares mediante interposición de parche de pericardio. Aunque se ha teorizado que el uso de parches puede favorecer la recurrencia de la endocarditis, diversos trabajos, como el de Solari et al.14 demuestran que no hay mayor tasa de recurrencia ni de insuficiencia mitral residual significativa a lo largo del tiempo con el uso de parches de pericardio.
La aparición de nuevos biomateriales con propiedades físicas y hemodinámicas altamente compatibles puede contribuir a reducir el número de técnicas aplicables, y a simplificar el abordaje de la cirugía reparadora en la mayor parte de las ocasiones (resección ± parche ± neocuerdas). Dentro de los nuevos biomateriales destacamos el Matrix PatchTM. Este parche de pericardio equino descelularizado es un material muy flexible con una elevada adaptabilidad a las estructuras valvulares, y presenta una potencial capacidad de convertirse en scaffold para la repoblación celular24,25. Sus propiedades físicas permiten que podamos llevar a cabo una reconstrucción del velo sin alterar su flexibilidad ni condicionar una restricción cicatricial de su movilidad. Además, presenta un alto grado de resistencia al desgarro por estrés mecánico, por lo que, en caso de formar parte del nuevo borde libre del velo reconstruido, es posible utilizarlo para el anclaje de neocuerdas Goretex®. El resto de las técnicas, incluido el «flip over» o transferencia de P2 para los defectos de A2, las consideramos menos reproducibles y con una mayor probabilidad de fracaso.
Un aspecto a tener en cuenta es que en la actualidad no contamos con un algoritmo estandarizado que nos permita decidir con seguridad en el resultado cuándo y cómo se debe llevar a cabo el tratamiento quirúrgico. En este sentido, Nappi et al. proponen una sistematización para el tratamiento de la endocarditis valvular mediante la aplicación de un algoritmo de decisión, dirigido a la selección previa de aquellos pacientes que son candidatos a reparación mitral frente aquellos en los que la cirugía de sustitución valvular es la opción más recomendable. Los principales elementos de decisión se basan en el grado anatómico de afectación valvular y en la presencia de patología previa. Simplifica el abordaje reparador mediante la selección de aquellos pacientes que presentan vegetaciones de menor tamaño, afectación circunscrita preferentemente a los velos, destacando la opción reparadora si afecta a un único segmento o un solo velo26.
La estandarización exige que el algoritmo planteado pueda ser aplicado de forma general, por lo que se seleccionan para reparación los casos más sencillos y reproducibles. Sin embargo, estas limitaciones pudieran no ser aplicables en centros con gran experiencia y volumen de reparación valvular en los que la actividad quirúrgica específica se concentre en pocos cirujanos.
Nappi et al. también pretenden aportar claridad probablemente en el hecho más trascendental y generador de incertidumbre: ¿cuándo operar? Las variables que utiliza para estratificar el tiempo quirúrgico en electivo, urgente o emergente se basan en criterios clínicos y ecocardiográficos26. Destacamos la inestabilización clínica a pesar del tratamiento médico óptimo, la presencia en enfermedad local avanzada o de rápida expansión evidenciada por ecocardiografía, o la presencia de infección no controlada con persistencia de fiebre más de cinco días. El planteamiento realizado puede resultar útil, ya que además de destacar expresamente que un equipo multidisciplinar bien organizado es el mejor instrumento diagnóstico-terapéutico frente a la endocarditis, permite estructurar sistemáticamente los ítems a valorar en cada caso, con un adecuado escalonamiento, y sin obviar aquellas variables más significativas para la evolución del paciente. A pesar de ello, aunque el árbol de decisión planteado se soporte en la evidencia científica disponible, la incertidumbre asociada es elevada, probablemente por la heterogeneidad de las formas de presentación, agentes microbiológicos, cardiopatías predisponentes o situación clínica previa. Sin embargo, nos parece una herramienta factible para su validación en los distintos servicios de cirugía cardiovascular, sobre todo en aquellos en los que los resultados globales en el tratamiento de la endocarditis pueden ser más comprometidos y donde encontremos una excesiva variabilidad de la práctica clínica no justificada.
En conclusión, las evidencias científicas disponibles sugieren que la cirugía de reparación mitral debería ser considerada el procedimiento de elección para el tratamiento quirúrgico de la EI, siempre que sea técnicamente posible. La mejor supervivencia intrahospitalaria y a largo plazo, la menor recurrencia de infección, y las ventajas asociadas a la preservación de la válvula nativa la convierten en la mejor opción posible en el tratamiento quirúrgico de la EI. La limitación más importante que encontramos dentro de la cirugía de reparación mitral es la elevada variabilidad de técnicas y materiales empleados para la reconstrucción valvular. Por ello, la estandarización de la técnica mediante el uso de neocuerdas de Goretex®, y la utilización de los nuevos biomateriales disponibles puede contribuir a la expansión de la técnica como primera opción terapéutica..
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.