El Comité Español del Antibiograma (COESANT) presenta en este documento una serie de recomendaciones cuya finalidad es unificar la forma en la que los Servicios y Unidades de Microbiología Clínica españoles realizan los informes de sensibilidad acumulada de las bacterias, aisladas en muestras clínicas, frente a los antimicrobianos. Las recomendaciones se fundamentan en las recogidas en el Procedimiento de Microbiología Clínica n° 51, «Preparación de informes acumulados de sensibilidad a los antimicrobianos» de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (SEIMC), publicado en 2014, y recoge las modificaciones en las definiciones de las interpretaciones de las categorías clínicas publicadas en el año 2019 por el European Committee on Antimicrobial Susceptibility Testing (EUCAST). Su objetivo final es establecer una forma homogénea de elaborar estos resúmenes para poder comparar resultados de diferentes centros o sumar su información y así realizar una adecuada vigilancia local o incluso nacional de la evolución de la sensibilidad a los antimicrobianos.
The Spanish Antibiogram Committee (Comité Español del Antibiograma, COESANT) presents in this document a series of recommendations intending to unify how cumulative antibiogram reports must be made in Clinical Microbiology Spanish laboratories. This article is based on the information included in the Clinical Microbiology Procedure No. 51, «Preparation of cumulative reports on antimicrobial susceptibility» of the Spanish Society of Infectious Diseases and Clinical Microbiology (SEIMC), published in 2014. The recommendations also include the modifications in the definition of clinical interpretive categories recently published by the European Committee on Antimicrobial Susceptibility Testing (EUCAST) in 2019. Its final objective is to establish a homogeneous way of preparing these summaries to compare results from different centers or aggregate the information from these in order to carry out an adequate local or even national surveillance regarding the evolution of antimicrobial susceptibility.
El análisis conjunto de los datos procedentes del estudio de la sensibilidad a los antimicrobianos de las bacterias aisladas en los laboratorios de Microbiología es de gran valor epidemiológico y clínico, ya que permite conocer variaciones temporales en las tendencias de sensibilidad y resulta de gran ayuda en la selección del tratamiento empírico en los pacientes infectados1–4. La necesidad de conocer la proporción de microorganismos sensibles a los antimicrobianos, junto al aumento en los últimos años de la multirresistencia, hacen indispensable una vigilancia global que sobrepase los límites de un único centro. Un ejemplo de esto es la Red de Vigilancia Microbiológica de la Comunitat Valenciana (RedMIVA)5, el programa de Vigilancia de la Infección Nosocomial en Cataluña (VINCat)6 o la reciente creación de la Red de Laboratorios para la Vigilancia de los Microorganismos Resistentes (RedLabRA)7 constituida en el seno del Plan Nacional frente a la Resistencia a Antibióticos (PRAN).
Las recomendaciones generales recogidas en el Procedimiento de Microbiología Clínica n° 51, «Preparación de informes acumulados de sensibilidad a los antimicrobianos» de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (SEIMC)8–10, publicado en 2014 siguen vigentes y se resumen en este artículo, con algunas modificaciones derivadas principalmente de las nuevas directrices establecidas por el European Committee on Antimicrobial Susceptibility Testing (EUCAST) en el año 2019 respecto a las definiciones de las categorías clínicas utilizadas en la interpretación de los resultados de sensibilidad (tabla 1). Adicionalmente, se referirán los puntos clave para tener en cuenta a la hora de realizar el informe de sensibilidad acumulada, así como una serie de aspectos estadísticos relevantes para su consideración.
Diez pasos fundamentales para tener en cuenta a la hora de elaborar el informe de sensibilidad acumulada
| 1. Adherirse a las recomendaciones EUCAST en cuanto a la realización de los antibiogramas y su lectura interpretada.2. Si sólo se informa una categoría, combinar S e I, dado que aporta información más clara en cuanto a la elección del tratamiento empírico. Referir adicionalmente el porcentaje de la presencia de mecanismos de resistencia de interés epidemiológico.3. Presentar el informe con un mínimo de periodicidad anual.4. Incluir sólo resultados validados por el microbiólogo clínico.5. Incluir sólo aislados de muestras enviadas para diagnóstico clínico de infecciones.6. Informar resultados de sensibilidad a nivel de especie, incluyendo sólo aquellas con ≥ 30 aislados, precisando el número absoluto de aislados.7. Eliminar duplicados, incluyendo sólo el primer aislado de una especie por cada paciente.8. Incluir los antimicrobianos que se recogen habitualmente en el informe clínico del estudio de sensibilidad.9. En el caso de combinaciones antibiótico-microorganismo cuyo resultado depende del cuadro clínico de origen, especificar todos los supuestos.10. Detallar con precisión el algoritmo de cálculo utilizado para la generación del informe acumulado. |
- 1.
Adherirse a las recomendaciones del EUCAST11,12 en cuanto a la realización de los antibiogramas y su lectura interpretada para garantizar la estandarización y homogeneidad en la metodología seguida en el estudio de sensibilidad.
- 2.
Aunque en los resúmenes de sensibilidad ha sido una práctica habitual combinar las categorías clínicas «Resistente» e «Intermedio» como no-sensible, esta no es adecuada desde la redefinición de categorías clínicas efectuada en 2019 por el EUCAST13,14. Se modifica la definición del término «Intermedio» que pasa a considerarse «I» (Sensible, cuando se incrementa la exposición), siendo la única diferencia entre «S» (sensible con dosis estándar) e «I» la cantidad de fármaco que es necesaria en el lugar de la infección para alcanzar una respuesta clínica adecuada. Se recomienda presentar las tres categorías de forma independiente y en caso de necesidad, combinar S e I y marcar en el pie de tabla aquellos casos en que existan dos dosificaciones (tablas 2 y 3), dado que aporta una información clínica más clara en cuanto a la elección del tratamiento empírico. En algunos microorganismos es conveniente informar adicionalmente del porcentaje de presencia de mecanismos de resistencia de especial interés epidemiológico. Por ejemplo, «porcentaje de pacientes con Klebsiella pneumoniae productora de betalactamasa de espectro extendido (BLEE)».
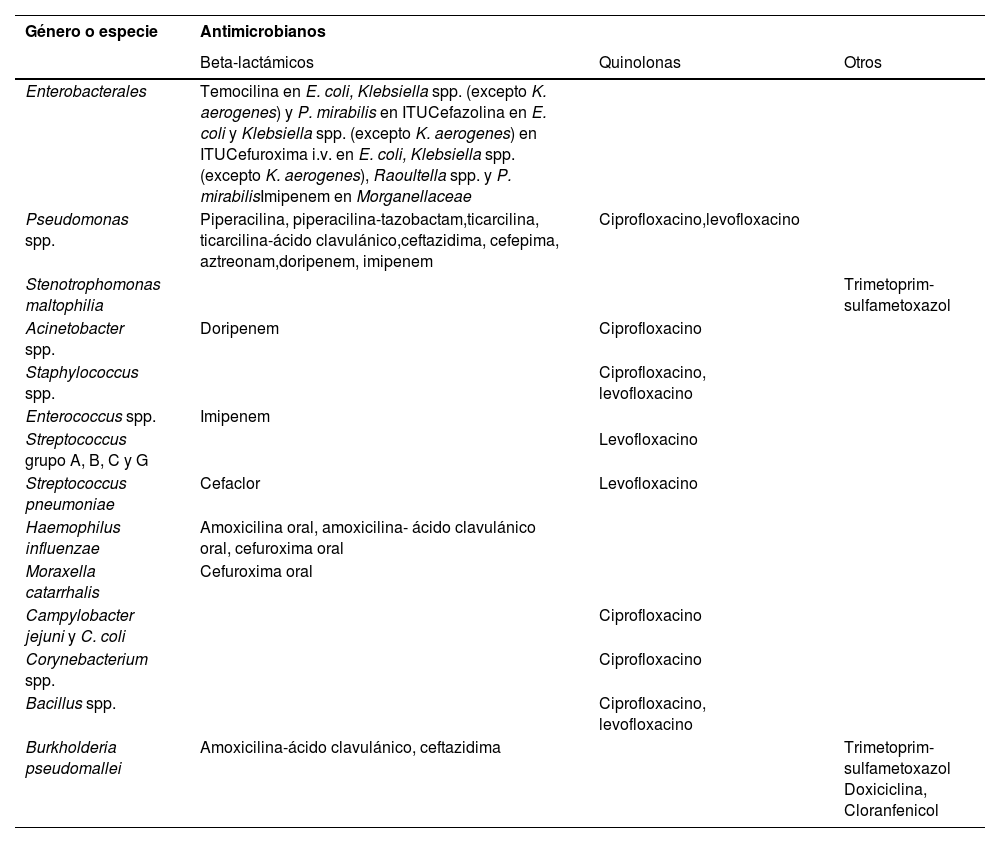
Tabla 2.Antimicrobianos para los que EUCAST ha introducido puntos de corte que clasifican a los microorganismos de tipo silvestre (organismos sin mecanismos de resistencia adquiridos fenotípicamente detectados para el agente) siempre como «Sensible cuando se incrementa la exposición (I)» en lugar de «Sensible en régimen de dosificación estándar (S)»23
Género o especie Antimicrobianos Beta-lactámicos Quinolonas Otros Enterobacterales Temocilina en E. coli, Klebsiella spp. (excepto K. aerogenes) y P. mirabilis en ITUCefazolina en E. coli y Klebsiella spp. (excepto K. aerogenes) en ITUCefuroxima i.v. en E. coli, Klebsiella spp. (excepto K. aerogenes), Raoultella spp. y P. mirabilisImipenem en Morganellaceae Pseudomonas spp. Piperacilina, piperacilina-tazobactam,ticarcilina, ticarcilina-ácido clavulánico,ceftazidima, cefepima, aztreonam,doripenem, imipenem Ciprofloxacino,levofloxacino Stenotrophomonas maltophilia Trimetoprim-sulfametoxazol Acinetobacter spp. Doripenem Ciprofloxacino Staphylococcus spp. Ciprofloxacino, levofloxacino Enterococcus spp. Imipenem Streptococcus grupo A, B, C y G Levofloxacino Streptococcus pneumoniae Cefaclor Levofloxacino Haemophilus influenzae Amoxicilina oral, amoxicilina- ácido clavulánico oral, cefuroxima oral Moraxella catarrhalis Cefuroxima oral Campylobacter jejuni y C. coli Ciprofloxacino Corynebacterium spp. Ciprofloxacino Bacillus spp. Ciprofloxacino, levofloxacino Burkholderia pseudomallei Amoxicilina-ácido clavulánico, ceftazidima Trimetoprim-sulfametoxazol Doxiciclina, Cloranfenicol ITU: infección del tracto urinario.
Tabla 3.Antimicrobianos para los que existen dos dosificaciones y por tanto la categoría de Sensible a exposición incrementada (antiguo intermedio)23
Género o especie Antimicrobianos Beta-lactámicos Quinolonas Otros Enterobacterales Ticarcilina, ticarcilina-ácido clavulánicoCefepime y ceftazidimaCeftriaxona en indicación diferente a meningitisDoripenem, imipenem (enterobacterales excepto Morganellaceae), meropenem en indicación diferente a meningitisAztreonam Ciprofloxacino,levofloxacino, ofloxacino Trimetoprim-sulfametoxazol Pseudomonas spp. Meropenem en indicación diferente a meningitis Acinetobacter spp. ImipenemMeropenem en indicación diferente a meningitis Levofloxacino Trimetoprim-sulfametoxazol Staphylococcus spp. Ceftarolina en S. aureus e indicación diferente a neumonía Claritromicina, eritromicina,roxitromicina Quinupristina-dalfopristinaDoxiciclina, tetraciclinaTrimetoprim-sulfametoxazol Enterococcus spp. Ampicilina, ampicilina-sulbactam, amoxicilina y amoxicilina-ácido clavulánico Quinupristina-dalfopristina en E. faecium Streptococcus grupo A, B, C y G Azitromicina, claritromicina, eritromicina,roxitromicina, telitromicinaTetraciclinaTrimetoprim-sulfametoxazol Streptococcus pneumoniae Benzilpenicilina, ampicilina, cefotaxima y ceftriaxona en indicación diferente a meningitisAmoxicilina y amoxicilina-ácido clavulánico por vía oralCefpodoxima y cefepimeCefuroxima por vía i.v. y oral Azitromicina, claritromicina, eritromicina,roxitromicina,telitromicinaTetraciclina, doxiciclinaTrimetoprim-sulfametoxazol S. grupo viridans Benzilpenicilina, ampicilina, amoxicilina Haemophilus influenzae Cefuroxima por vía i.v. DoxiciclinaTrimetoprim-sulfametoxazol Moraxella catarrhalis Cefixima, cefotaxima, ceftriaxona, cefuroxima por vía i.v. Azitromicina, claritromicina, eritromicina,roxitromicina, telitromicinaDoxiciclinaTrimetoprim-sulfametoxazol Neissera gonorrhoeae Benzilpenicilina Ciprofloxacino, ofloxacino Neisseria meningitidis Ampicilina y amoxicilina en indicación diferente a meningitis Helicobacter pylori Claritromicina Corynebacterium spp. Rifampicina Aeromonas spp. Cefepima, ceftazidima, aztreonam Ciprofloxacinolevofloxacino Trimetoprim-sulfametoxazol Achromobacter xylosoxidans Meropenem ITU: infección del tracto urinario; iv: formulación intravenosa.
Algunos antimicrobianos como teicoplanina, fosfomicina en formulación intravenosa, ácido fusídico y metronidazol tiene dos dosis en las tablas de EUCAST, pero no categoría intermedia (dosis y/o puntos de corte en revisión por EUCAST).
- 3.
Presentar el informe, como mínimo, con una periodicidad anual.
- 4.
Incluir sólo resultados validados por el microbiólogo clínico, no la información cruda que se obtiene del antibiograma.
- 5.
Incluir sólo aislados de muestras enviadas para diagnóstico clínico, excluyendo los aislados de cultivos de vigilancia epidemiológica o de muestras ambientales.
- 6.
Informar resultados de sensibilidad a nivel de especie, incluyendo sólo aquellas con ≥ 30 aislados. Se debe indicar el número absoluto de aislados que se tienen en cuenta en el informe.
- 7.
Eliminar duplicados siguiendo una estrategia que responda a las necesidades clínicas15. Se debe incluir sólo el primer aislado de una especie determinada por paciente y período de análisis, con independencia del sitio anatómico de recogida o perfil de sensibilidad a los antimicrobianos, ya que permite guiar la selección de tratamientos empíricos. Es una forma sencilla y evita sesgos introducidos por el observador, siendo un método más objetivo y reproducible. No obstante, de esta forma podría infraestimarse el nivel de resistencia en aquellas especies en que existe el riesgo de adquisición o desarrollo de esta durante el tratamiento (Pseudomonas aeruginosa, que puede exhibir una heterogeneidad significativa en los fenotipos de resistencia como resultado de mutación, coinfección o colonización con múltiples clones). Cuando se quiera analizar esta circunstancia específicamente, puede ser más conveniente eliminar duplicados excluyendo aislados con un cambio de falsa sensibilidad (resultado erróneo de S en lugar de R; very major error) o de falsa resistencia (R en lugar de S; major error) de algún antibiótico de entre los definidos previamente como marcadores o antibióticos clave en esa especie bacteriana. La consideración de cambios menores (S por I, I por S, I por R o R por I) es muy discutida porque pueden reflejar variantes fenotípicas de expresión o problemas metodológicos. El criterio seguido, por tanto, puede influir en el resultado final por lo que es importante detallar en el informe cómo se ha llevado a cabo la eliminación de duplicados.
- 8.
Se deben incluir los antimicrobianos que se informan habitualmente en el informe clínico de sensibilidad. Se deben excluir los antibióticos suplementarios incluidos para detectar mecanismos de resistencia en el contexto de la lectura interpretada del antibiograma. Por ejemplo, cefoxitina en Staphylococcus aureus, cefotaxima-ácido clavulánico en Enterobacterales o norfloxacino en Streptococcus pneumoniae.
- 9.
En el caso de combinaciones antibiótico-microorganismo cuyo resultado depende del cuadro clínico de origen, se recomienda especificar todos los supuestos (Escherichia coli y amoxicilina-clavulánico en infección urinaria y Streptococcus pneumoniae y penicilina en meningitis o no meningitis).
- 10.
Detallar con precisión el algoritmo de cálculo utilizado para la generación del informe acumulado16,17 para facilitar la comparabilidad de los informes en diferentes periodos o diferentes centros. Es decir, precisar si se han sumado categorías e indicar el método seguido para eliminar duplicados cuando no sea el recomendado.
- 1.
Aunque no hay un modelo estandarizado, puede ser conveniente emplear el formato de tablas y/o figuras, en las que se incluyan microorganismos y antimicrobianos, indicando el n° de aislados incluidos en cada especie y los correspondientes porcentajes de sensibilidad, considerando estos como la suma de S + I, con el fin de reflejar los porcentajes de microorganismos tratables con el antimicrobiano estudiado, en lugar de la detección de mecanismos de resistencia.
- 2.
Pueden emplearse diversos criterios para listar los microorganismos del informe: alfabéticamente, por grupo taxonómico o por prevalencia. En el PNT-IASA-1 del procedimiento n° 51 de la SEIMC figura la información mínima imprescindible que hay que incluir en el informe sobre microorganismos y antimicrobianos de especial interés epidemiológico y clínico.
- 3.
Para reflejar las tendencias temporales de sensibilidad resulta más útil la presentación de los datos en forma de figura (histograma).
- 4.
Utilizar en las tablas abreviaturas referenciadas para los antimicrobianos18.
- 5.
Como norma general es recomendable separar en las tablas de sensibilidad al menos los aislados obtenidos de hemocultivos y a partir de urocultivos, siguiendo los mismos criterios recomendados en las normas generales para la eliminación de duplicados.
- 6.
Separar en las tablas de sensibilidad los aislados según el tipo de paciente (hospitalizados, Medicina Intensiva, Pediatría, Atención Primaria, y otros que puedan ser de interés clínico)19–21.
- 7.
Aportar porcentajes de pacientes con microorganismos con mecanismos de resistencia de especial relevancia clínica, como Staphylococcus aureus resistente a meticilina, enterococos resistentes a glucopéptidos, enterobacterias productoras de BLEE o carbapenemasas y Acinetobacter baumannii y Pseudomonas aeruginosa multirresistentes o extremadamente resistentes22.
En el PNT-IASA-2 se ofrece una herramienta para facilitar el cálculo de los valores estadísticos propuestos en el procedimiento n° 51 de la SEIMC sobre hojas Excel (IC 95% del % S, comparación de porcentajes con el IC 95% de la diferencia) y el análisis de tendencias. El libro Excel se puede descargar desde el enlace www.seimc.org/contenidos/documentoscientificos/procedimientosmicrobiologia/seimc-procedimientomicrobiologia51.pdf
- 1.
Los porcentajes de sensibilidad permiten una estimación mejor de la verdadera proporción en la población real de aislados. No es necesario incluir en el informe los valores de los intervalos de confianza que señalan la precisión del porcentaje presentado para no restar claridad al informe. No obstante, estos deben estar a disposición de cualquier persona que necesite conocerlos mediante consulta específica al Servicio/Unidad de Microbiología.
- 2.
La significación estadística de la diferencia entre porcentajes de sensibilidad de dos periodos de tiempo debe distinguirse de la importancia (o relevancia) clínica o epidemiológica.
- 3.
El análisis de tendencias de sensibilidad a lo largo del tiempo presupone que la base de datos original contenga los valores reales de las concentraciones mínimas inhibitorias (CMI) o de diámetro de halo, para poder hacer reinterpretación de los resultados, dado que los puntos de corte clínicos pueden variar a lo largo del periodo que se pretende estudiar.
Tradicionalmente los informes de sensibilidad acumulada se han presentado en formato papel, muchas veces en forma de trípticos con el fin de ser consultados en el día a día por los clínicos y con ello contribuir a la adecuación de los tratamientos empíricos. Hoy en día y con las nuevas herramientas informáticas, dichos informes pueden ser colgados en distintos lugares o plataformas como la intranet de los hospitales o incluso en los visores de resultados microbiológicos. Respecto a esto último, cuando se emite un resultado microbiológico con la identificación de un microorganismo del que aún no se conoce el resultado de su sensibilidad antimicrobiana, es de gran utilidad introducir un enlace que lleve directamente al informe de sensibilidad acumulada del hospital y en el cual el clínico pueda conocer la sensibilidad habitual del microorganismo y elegir por tanto de forma más precisa y ágil la mejor terapia empírica para dicho microorganismo. Dicha funcionalidad es posible hoy en día en algunos sistemas informáticos de laboratorio y permite hacer más prácticos y extensibles a muchos más profesionales los informes de sensibilidad acumulada.
ConclusionesLa necesidad de conocer la proporción de microorganismos sensibles a los antimicrobianos, junto al aumento en los últimos años de la multirresistencia, hacen indispensable una vigilancia global que sobrepase los límites de un único centro.
Para poder trabajar con datos de forma conjunta es fundamental que los informes de sensibilidad se elaboren de forma homogénea y estandarizada en todos los centros.
Estos informes han de ser fácilmente accesibles a los profesionales cuya actividad está relacionada con el uso de antibióticos contribuyendo así a una mejor optimización de este tipo de tratamientos y a la preservación de su actividad, evitando la generación de resistencias por un uso inadecuado.
FinanciaciónPara la realización de este documento no se ha contado con financiación específica. Las actividades del COESANT están parcialmente financiadas por la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (SEIMC) y la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS).
El Plan Estatal de Investigación Científica y Técnica y de Innovación 2017-2020 y el Instituto de Salud Carlos III, Subdirección General de Redes y Centros de Investigación Cooperativa, Ministerio de Ciencia e Innovación, financia la investigación de MNL, RC, FFC, LMM y AO a través de la Red de Investigación en Patología Infecciosa (REIPI) y el CIBER en Enfermedades Infecciosas (CIBERINFEC) y de EC, JFD y JG a través del CIBER de Enfermedades Respiratorias (CIBERES).
Conflicto de interesesLos autores declaran no tener conflicto de intereses.