El uso de anticoagulantes orales es controvertido en pacientes con antecedentes de fibrilación auricular (FA) y hemorragia intracraneal (HIC), por riesgo de recurrencia de ictus hemorrágico. Presentamos la experiencia de nuestro centro en relación con la seguridad y la eficacia del cierre percutáneo de orejuela (CPO), una alternativa a la anticoagulación en dicho contexto.
MétodosEstudio observacional, retrospectivo y unicéntrico. El CPO se realizó en pacientes con antecedentes de HIC y FA no valvular. El riesgo de eventos isquémicos y hemorrágicos se estimó usando las escalas CHA2DS2Vasc y HAS-BLED. Se registraron: complicaciones periprocedimiento, recurrencia de HIC, embolismo cerebral/sistémico, mortalidad tras el cierre y al seguimiento y uso de antitrombóticos tras el procedimiento.
ResultadosEl CPO se realizó en 9 pacientes (7 hombres, 2 mujeres). Se utilizó en 7 casos el dispositivo Amplatzer Amulet y en 2 el Amplatzer Cardiac Plug. La media de edad fue 72,7 ± 8,2 años. El tiempo entre la HIC y el CPO fue menor de un mes en 5 pacientes y mayor en 4. La mediana y el rango intercuartil para la escala CHA2DS2Vasc fueron de 4 y 2,5, respectivamente, siendo de 3 y 0 para la escala HAS-BLED. No hubo complicaciones periprocedimiento. Todos recibieron antiagregación simple tras el procedimiento (5 clopidogrel y 4 aspirina); en 5 se mantuvo 6 meses, en 4 indefinidamente. Durante el seguimiento (15 meses de promedio) no se registraron eventos isquémicos ni hemorrágicos.
ConclusionesEn nuestra serie, el CPO supone una alternativa segura y eficaz en pacientes que han presentado HIC y que precisan ser anticoagulados por FA.
The use of oral anticoagulants in patients with a history of atrial fibrillation (AF) and intracranial haemorrhage (ICH) is controversial on account of the risk of haemorrhagic stroke recurrence. This study presents our experience regarding the safety and efficacy of percutaneous left atrial appendage closure (LAAC), an alternative to anticoagulation in these patients.
MethodsWe conducted a retrospective, single-centre, observational study. LAAC was performed in patients with a history of ICH and non-valvular AF. Risk of ischaemic and haemorrhagic events was estimated using the CHA2DS2-VASc and HAS-BLED scales. We recorded periprocedural complications, IHC recurrence, cerebral/systemic embolism, mortality and use of antithrombotic drugs following the procedure.
ResultsLAAC was performed in 9 patients (7 men, 2 women) using the AMPLATZER Amulet device in 7 cases and the AMPLATZER Cardiac Plug device in 2. Mean age was 72.7±8.2 years. Time between ICH and LAAC was less than one month in 5 patients and more than one month in 4 patients. Median CHA2DS2-VASc score was 4 (interquartile range of 2.5). Median HAS-BLED score was 3 (interquartile range of 0). No periprocedural complications were recorded. All patients received single anti-platelet therapy (clopidogrel in 5 patients, aspirin in 4) after the procedure; 5 patients received this treatment for 6 months and 4 received it indefinitely. No ischaemic or haemorrhagic events were recorded during follow-up (mean duration of 15 months).
ConclusionsIn our series, LAAC was found to be safe and effective in patients with a history of ICH who required anticoagulation due to AF.
Una de las complicaciones más temidas asociadas a la anticoagulación oral (ACO) es la hemorragia intracraneal (HIC). Los nuevos ACO parecen disminuir los eventos hemorrágicos con respecto a los clásicos1. Sin embargo, esto no se ha demostrado en pacientes que ya han presentado una HIC, donde la anticoagulación es especialmente controvertida2–4. Cabe destacar que hasta el 13% de los pacientes con antecedente de HIC tienen criterios de anticoagulación5. Por tanto, el clínico se encuentra con frecuencia ante la difícil disyuntiva de tener que escoger entre anticoagular a un paciente con fibrilación auricular (FA) y antecedentes de HIC (con el consiguiente riesgo de sangrado) o antiagregar e incluso no tratar de ningún modo, asumiendo entonces un importante riesgo de eventos isquémicos.
Frente a este dilema terapéutico, el cierre percutáneo de la orejuela auricular (CPO) se presenta como una tercera vía. Así pues, el CPO sería una alternativa en pacientes con FA y contraindicación al tratamiento con ACO por ictus hemorrágico previo; de este modo, se evitarían simultáneamente los eventos isquémicos y hemorrágicos secundarios a la anticoagulación.
Existen ensayos clínicos y metaanálisis que comparan el CPO con ACO en pacientes con FA e ictus isquémico6. Sin embargo, no existen ensayos clínicos en el caso de presentar antecedente de HIC. Tan solo 3 estudios observacionales han indicado que el CPO sea una opción segura y eficaz7–9.
De este modo, son necesarios nuevos estudios que demuestren la eficacia y la seguridad del CPO en este perfil de pacientes. Presentamos en este estudio los resultados de nuestro centro.
MétodosSe trata de un estudio observacional, unicéntrico, de casos consecutivos y retrospectivo (con recogida de datos prospectiva durante el seguimiento) realizado entre los años 2013 y 2016. En nuestro centro, el CPO se realiza desde 2012 con un total de 66 procedimientos hasta la fecha, 9 de los cuales se llevaron a cabo por HIC (los otros 57 CPO se realizaron en pacientes con hemorragias no intracraneales —fundamentalmente gastrointestinales— en contexto de toma de ACO).
Se registraron de manera prospectiva variables demográficas (edad, sexo), factores de riesgo cardiovascular (hipertensión, diabetes, dislipidemia), hábitos tóxicos (tabaquismo, enolismo), tipo de HIC (intraparenquimatosa, subaracnoidea o subdural) y causa de HIC, puntuación en la escala National institute of Health Stroke Scale (NIHSS) preprocedimiento, escala de Rankin modificada tras la HIC, el tratamiento anticoagulante y antiagregante previo a la HIC y tras el CPO, y el riesgo isquémico y hemorrágico sobre la base de las escalas CHA2DS2Vasc y HASBLED. Los criterios de inclusión consistieron en haber presentado FA con indicación de ACO y antecedente de HIC. Se excluyó a aquellos pacientes con un mal estado funcional (escala de Rankin de 4 o más al año de la HIC).
El seguimiento se realizó durante 15 meses de promedio (con un máximo de 2 años y un mínimo de 3 meses) y todos los pacientes firmaron un consentimiento informado estandarizado previo al CPO en el que accedían a realizarse dicho procedimiento y a ser incluidos en el estudio. Además, tanto el procedimiento como el protocolo del estudio cuentan con la aprobación del comité ético local.
Las complicaciones se definieron de acuerdo con el estudio PROTECT AF6 y se consideraron como complicaciones mayores: ictus isquémico o hemorrágico, muerte, pericarditis o embolización del dispositivo. Fueron consideradas complicaciones menores el pseudoaneurisma inguinal, la fístula arteriovenosa, hematomas, formación de un trombo sobre el dispositivo o sangrados menores que no requirieron reintervención. Los métodos estadísticos utilizados han sido exclusivamente descriptivos, utilizando medias, desviación estándar y rangos intercuartil en el caso de variables cuantitativas continuas, y medianas para variables cuantitativas ordinales.
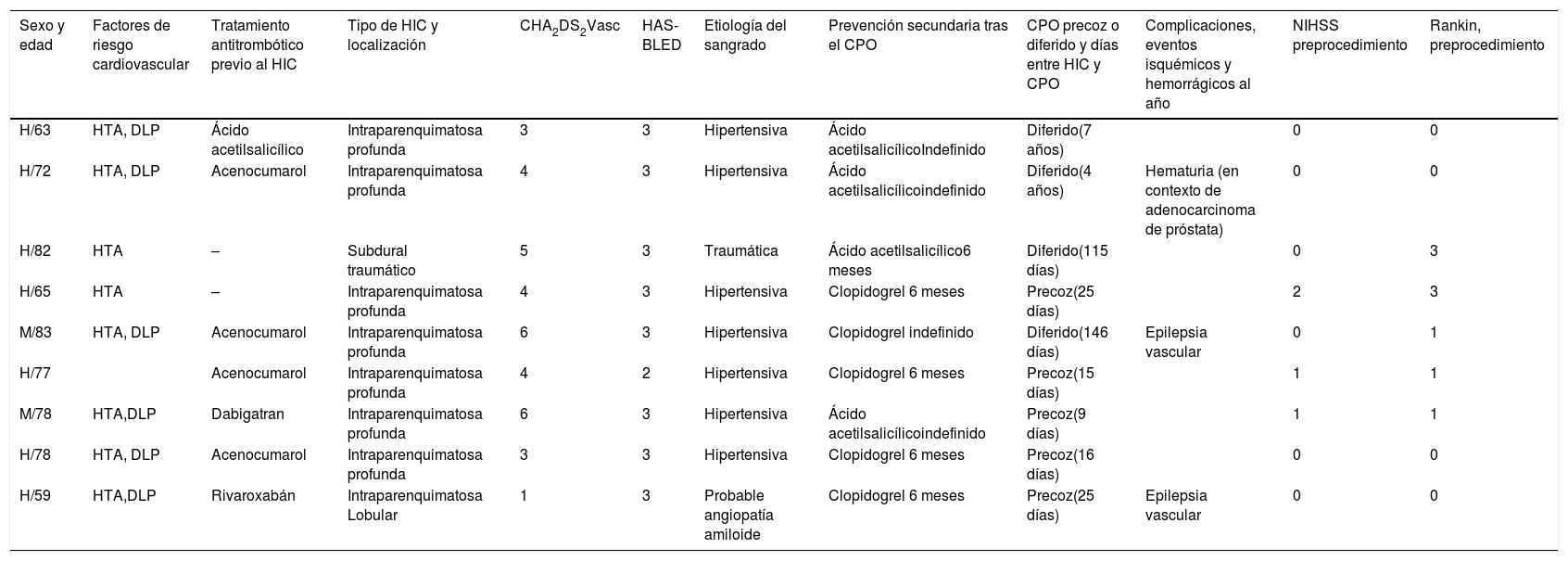
ResultadosDe los 49 pacientes que presentaron HIC y FA entre 2013 y 2016, el CPO se llevó a cabo en 9, de los cuales 7 eran hombres y 2 mujeres. Las características de los mismos se detallan en la tabla 1.
Resumen de los datos clínicos de los 9 pacientes
| Sexo y edad | Factores de riesgo cardiovascular | Tratamiento antitrombótico previo al HIC | Tipo de HIC y localización | CHA2DS2Vasc | HAS-BLED | Etiología del sangrado | Prevención secundaria tras el CPO | CPO precoz o diferido y días entre HIC y CPO | Complicaciones, eventos isquémicos y hemorrágicos al año | NIHSS preprocedimiento | Rankin, preprocedimiento |
|---|---|---|---|---|---|---|---|---|---|---|---|
| H/63 | HTA, DLP | Ácido acetilsalicílico | Intraparenquimatosa profunda | 3 | 3 | Hipertensiva | Ácido acetilsalicílicoIndefinido | Diferido(7 años) | 0 | 0 | |
| H/72 | HTA, DLP | Acenocumarol | Intraparenquimatosa profunda | 4 | 3 | Hipertensiva | Ácido acetilsalicílicoindefinido | Diferido(4 años) | Hematuria (en contexto de adenocarcinoma de próstata) | 0 | 0 |
| H/82 | HTA | – | Subdural traumático | 5 | 3 | Traumática | Ácido acetilsalicílico6 meses | Diferido(115 días) | 0 | 3 | |
| H/65 | HTA | – | Intraparenquimatosa profunda | 4 | 3 | Hipertensiva | Clopidogrel 6 meses | Precoz(25 días) | 2 | 3 | |
| M/83 | HTA, DLP | Acenocumarol | Intraparenquimatosa profunda | 6 | 3 | Hipertensiva | Clopidogrel indefinido | Diferido(146 días) | Epilepsia vascular | 0 | 1 |
| H/77 | Acenocumarol | Intraparenquimatosa profunda | 4 | 2 | Hipertensiva | Clopidogrel 6 meses | Precoz(15 días) | 1 | 1 | ||
| M/78 | HTA,DLP | Dabigatran | Intraparenquimatosa profunda | 6 | 3 | Hipertensiva | Ácido acetilsalicílicoindefinido | Precoz(9 días) | 1 | 1 | |
| H/78 | HTA, DLP | Acenocumarol | Intraparenquimatosa profunda | 3 | 3 | Hipertensiva | Clopidogrel 6 meses | Precoz(16 días) | 0 | 0 | |
| H/59 | HTA,DLP | Rivaroxabán | Intraparenquimatosa Lobular | 1 | 3 | Probable angiopatía amiloide | Clopidogrel 6 meses | Precoz(25 días) | Epilepsia vascular | 0 | 0 |
Con respecto a los 40 pacientes en los que se desestimó el CPO como alternativa terapéutica, encontramos los siguientes criterios de exclusión: fallecimiento (20 pacientes), Rankin igual o superior a 4 (18 pacientes) o negación del paciente (2 pacientes).
La edad media fue de 72,7 ± 8,2 años. La etiología de las mismas se determinó sobre la base del sistema H-ATOMIC10. Siete de estas hemorragias fueron profundas e hipertensivas, una de ellas fue un hematoma subdural traumático y otra fue lobular, de probable etiología amiloide.
La mediana de CHA2DS2Vasc fue de 4, con un rango intercuartil de 2,5. La mediana de HAS-BLED fue de 3, con un rango intercuartil de 0.
Antes de la HIC, 4 pacientes estaban anticoagulados con acenocumarol, uno con dabigatran, otro con rivaroxabán, otro estaba antiagregado con ácido acetilsalicílico y 2 sin tratamiento.
El tratamiento antitrombótico tras el CPO consistió en AAS o clopidogrel durante 6 meses en 5 de los casos e indefinido en el resto, dependiendo de las características del paciente (ser portador de stent, diabético, etc.). Dicha elección fue tomada por parte del servicio de cardiología.
Ningún paciente presentó complicaciones mayores o menores periprocedimiento. No se registró ninguna complicación mayor o menor durante el seguimiento. Un paciente presentó hematuria en contexto de un adenocarcinoma de próstata y otros 2 presentaron crisis comiciales de etiología vascular.
El tiempo hasta el CPO desde la hemorragia fue muy variado, con un promedio de 361 días y una desviación estándar de 479 días, dividiéndose los pacientes en 2 grupos: aquellos que se sometieron al procedimiento precozmente (5 pacientes en los que el CPO se realizó en menos de un mes desde la HIC con una media de 18 días) y aquellos que lo hicieron diferido de manera ambulatoria (4 pacientes, con una media de 2 años y 2 meses entre la HIC y el CPO).
Los pacientes que fueron sometidos al CPO presentaban un buen estado funcional preprocedimiento (mRS igual o menor de 3) y una puntuación NIHSS menor de 3.
DiscusiónSobre la base de autopsias y estudios ecocardiográficos se ha observado que la orejuela izquierda es el origen del 90% de trombos en pacientes con FA no valvular5. Por tanto, una forma de evitar eventos isquémicos es aislar la zona donde se genera el trombo en la orejuela izquierda, su embolización y la necesidad, por tanto, de anticoagulación7,11,12. En nuestro centro, entre los años 2013 y 2016 se han llevado a cabo 9 CPO en pacientes con antecedentes de FA e HIC, sin registrarse complicaciones mayores o menores durante el seguimiento.
La coexistencia de FA con criterios de anticoagulación e HIC es un hecho frecuente en la práctica clínica. De hecho, hasta el 13% de los pacientes que han presentado una HIC son tributarios a ser anticoagulados5. Sin embargo, la continuación de la anticoagulación tras una HIC incrementa significativamente el riesgo de recurrencia de hemorragia13. Si bien es cierto que los nuevos anticoagulantes han demostrado un menor riesgo de HIC a priori con respecto a los anticoagulantes clásicos1, se desconoce si poseen un menor riesgo de recurrencia en aquellos pacientes que ya han presentado un evento hemorrágico.
Hasta la fecha existen pocos estudios que analicen cuál es la actitud a seguir frente a un paciente que ha presentado una HIC y precisa continuar anticoagulándose, ni tampoco a partir de qué momento es correcto iniciar la anticoagulación2,3,14. Algunos de estos estudios señalan que únicamente sería recomendable anticoagular a aquellos pacientes que tengan un CHA2DS2Vasc igual o mayor de 6, no recomendando antiagregar por incrementar el riesgo de sangrado sin proteger de eventos isquémicos15.
Las guías de la Sociedad Española de Neurología contraindican la anticoagulación en el caso de las hemorragias lobulares, dado el importante riesgo teórico de recurrencia hemorrágica. En el caso de las hemorragias profundas de etiología hipertensiva, únicamente se permite el uso de ACO en el caso de que exista un óptimo control tensional4.
Con respecto a la elección terapéutica, los nuevos anticoagulantes orales presentan frente a los clásicos un menor riesgo de ictus, de embolismo sistémico y de ictus hemorrágico. Sin embargo, una vez se ha presentado la HIC no se ha demostrado que el pronóstico sea diferente con respecto a aquellos pacientes tratados con anticoagulantes clásicos. Por otra parte, presentan un mayor riesgo de hemorragia gastrointestinal1.
Si bien es cierto que existen ensayos clínicos en relación al CPO frente a los ACO6, esto no se da en el caso de los pacientes con HIC.
En el metaanálisis de los estudios PROTECT AF y PREVAIL (en el que se incluyeron más de 2.400 pacientes con FA) se objetivó una eficacia comparable entre la warfarina y el dispositivo WATCHMAN en la prevención global de eventos neurovasculares (sin diferenciar isquémico y hemorrágico), con menores tasas de HIC y menor mortalidad en el grupo en el que se realizó el CPO; sin embargo, este grupo también mostró una mayor tasa de ictus isquémico6. Cabe destacar que, mientras que la ACO conlleva complicaciones a largo plazo, el CPO se asocia a complicaciones principalmente durante el procedimiento (embolización del dispositivo, ictus periprocedimiento, muerte, derrame pericárdico) y a corto plazo1. Con respecto a dichas complicaciones, se han objetivado un 7,4% en el estudio PROTECT AF y un 4,2% en el estudio PREVAIL.
La escasa literatura médica existente compara únicamente anticoagular frente a antiagregar o la abstención terapéutica15,16, no contemplándose la posibilidad del CPO, y aconsejando anticoagular en caso de presentar un alto riesgo de eventos isquémicos. Así pues, el objetivo de nuestro estudio es abordar la difícil decisión de qué hacer para evitar eventos isquémicos en pacientes con FANV e HIC previa.
Únicamente existen 3 estudios descriptivos que analicen la seguridad y eficacia del CPO en pacientes con antecedentes de HIC7–9 y ninguno de ellos realiza una comparativa con respecto al resto de opciones terapéuticas. Con respecto a los 3 estudios en los que se ha incluido a pacientes con HIC, en el primero de ellos (publicado en 2014) se llevó a cabo el CPO en 20 pacientes con HIC previa, sin observar complicaciones periprocedimiento ni eventos isquémicos o hemorrágicos con un seguimiento medio de 13,8 meses. Únicamente se detectaron cuatro complicaciones menores7. En el segundo (publicado en 2016), se realizó el CPO en 24 pacientes con antecedente de HIC y en 2 con hemorragia intraocular previa, observándose 3 complicaciones durante un seguimiento medio de 11 ± 9 meses: un AIT de causa desconocida, un fallecimiento no relacionado con el procedimiento y una embolización del dispositivo que pudo resolverse percutáneamente8. En el tercero (publicado en 2016), el CPO se realizó en 46 pacientes con antecedente de HIC; se registraron un 6% de complicaciones periprocedimiento y 3 muertes durante un seguimiento de 12 meses (una de ellas por HIC, otra por fracaso multiorgánico y otra de causa desconocida)9.
En nuestros 9 pacientes no objetivamos complicaciones menores o mayores periprocedimiento, ni tampoco eventos isquémicos o hemorrágicos durante el seguimiento. Cabe destacar que, sobre la base de las escalas CHA2DS2Vasc y HASBLED, se calculó un riesgo anual de ictus y complicaciones hemorrágicas entre el 4-6,7 y el 1,8-3,7%, respectivamente.
En nuestro caso, el porcentaje de eventos isquémicos y hemorrágicos cerebrales fue del 0%. Como novedad frente a los estudios realizados acerca del CPO, no hemos encontrado diferencias entre los pacientes que se sometieron al CPO durante el ingreso causado por la HIC y aquellos en los que se realizó de manera ambulatoria (como puede observarse en la tabla 1, no existen diferencias con respecto a las complicaciones del procedimiento, el tratamiento posterior o la presencia de eventos isquémicos o hemorrágicos posteriores). Por tanto, de este modo disminuimos el tiempo en el que el paciente no se encuentra protegido frente a eventos isquémicos.
Sin embargo, no se pueden establecer conclusiones firmes al respecto dado el diseño del mismo (retrospectivo y unicéntrico), el limitado número de pacientes en el que se basa, el corto seguimiento y la heterogeneidad de los mismos. Serían necesarios para confirmar nuestros hallazgos estudios observacionales multicéntricos con un mayor número de paciente y la realización de ensayos clínicos que comparen la eficacia y seguridad del CPO en comparación con la antiagregación o la anticoagulación. A la espera de datos definitivos, nuestro estudio aporta datos que indican que el CPO podría ser una buena alternativa a la ACO en pacientes con HIC a la hora de prevenir eventos vasculares isquémicos y hemorrágicos.
Conflicto de interesesNo hay conflicto de intereses a declarar
El presente trabajo no ha sido presentado en la Reunión Anual de la SEN o en otras reuniones o congresos.