Se han descrito diversas manifestaciones neurológicas asociadas a alteraciones glucémicas, siendo bien conocida la hipoglucemia como causa de crisis epilépticas1. Sin embargo, es menos conocido que la hiperglucemia puede presentarse inicialmente con clínica neurológica2, siendo una de las formas características la epilepsia parcial continúa, normalmente con crisis focales motoras, a diferencia de la hipoglucemia3. La hiperglucemia hiperosmolar no cetósica es el tipo de hiperglucemia más frecuentemente asociada con este tipo de síntomas, siendo en ocasiones el inicio clínico de una diabetes mellitus no conocida previamente4. El mecanismo fisiopatológico concreto por el que esto ocurre no es del todo conocido, pudiendo tener la cetosis un papel protector en casos de hiperglucemia para el desarrollo de síntomas comiciales4. Presentamos un caso de epilepsia parcial continua con semiología occipital, en contexto de una hiperglucemia no cetósica, resuelta tras control metabólico, recordando la necesidad de tener en cuenta esta entidad, que si bien es poco frecuente, tiene importantes implicaciones terapéuticas y pronósticas.
Varón de 61 años, hipertenso, dislipémico y diabético tipo 2 no insulinodependiente, con buen control previo, en tratamiento con telmisartan, simvastatina, fenofibrato, metformina, Adiro® y omeprazol, sin antecedentes de crisis epilépticas ni otros antecedentes de interés. Comienza de manera brusca a presentar episodios de duración variable, desde segundos hasta horas, consistentes en alucinaciones visuales simples con visión de destellos luminosos, binoculares, referidos en todo el campo visual, que persisten pese al cierre ocular. Al inicio del cuadro, además, presentó fenómeno de metamorfopsia invertida, que se resolvió espontáneamente. No déficit campimétrico objetivado, cefalea ni otra focalidad neurológica. Esta sintomatología se mantuvo durante al menos 20 días antes de consultar, durante los cuales la frecuencia de los mismos fue variable, ocurriendo todos los días, con una frecuencia de entre 5 y 20 episodios, sin un patrón temporal ni circadiano definido.
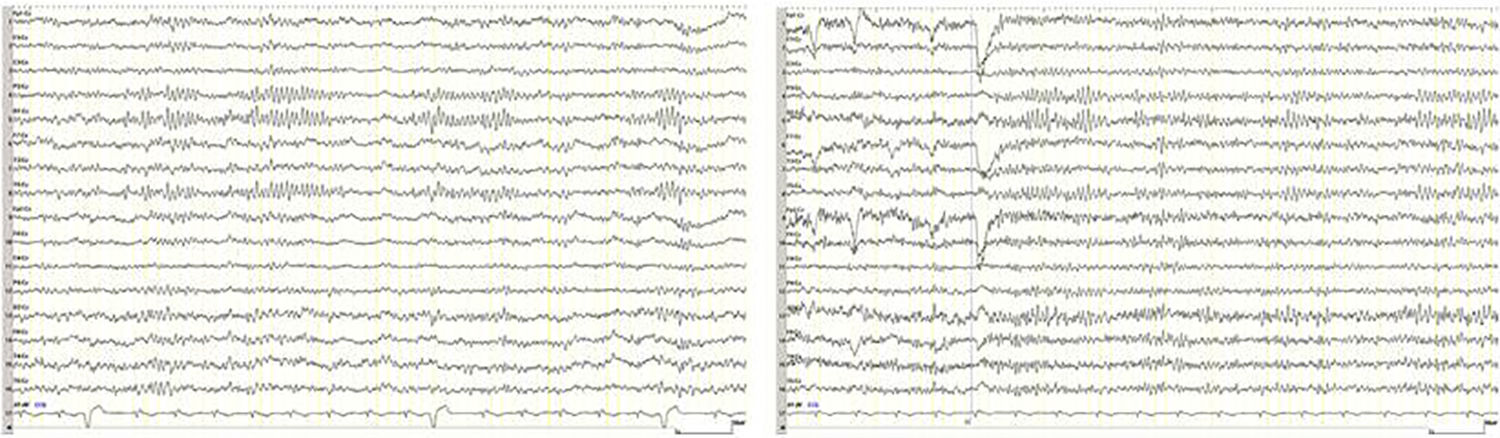
La exploración neurológica no mostró déficits focales. Se realizó analítica completa de sangre mostrando una glucemia de 382mg/dl y una hemoglobina glicada del 14%. Sin otras alteraciones analíticas salvo hipertrigliceridemia conocida. Cuerpos cetónicos negativos. Se realizó un electroencefalograma que mostró asimetría con ritmo alfa occipital derecho, peor configurado que el contralateral (fig. 1). La resonancia magnética craneal evidenció hiperintensidad en T2 y restricción en secuencia de difusión en córtex occipital derecho, además de hipointensidad en región subcortical adyacente (fig. 2). Se completó estudio con angio-RM de cuello e intracraneal, y con ecografía-doppler de troncos supraaórticos y transcraneal, que no mostraron hallazgos relevantes. Tras comenzar insulinoterapia, el cuadro perceptivo visual remitió en horas, sin volver a ocurrir de nuevo en 15 meses de seguimiento, durante los cuales ha existido un óptimo control glucémico. Asimismo, el electroencefalograma y la resonancia magnética se normalizaron en controles sucesivos (figs. 1 y 2). En ningún momento se inició tratamiento con anticomiciales.
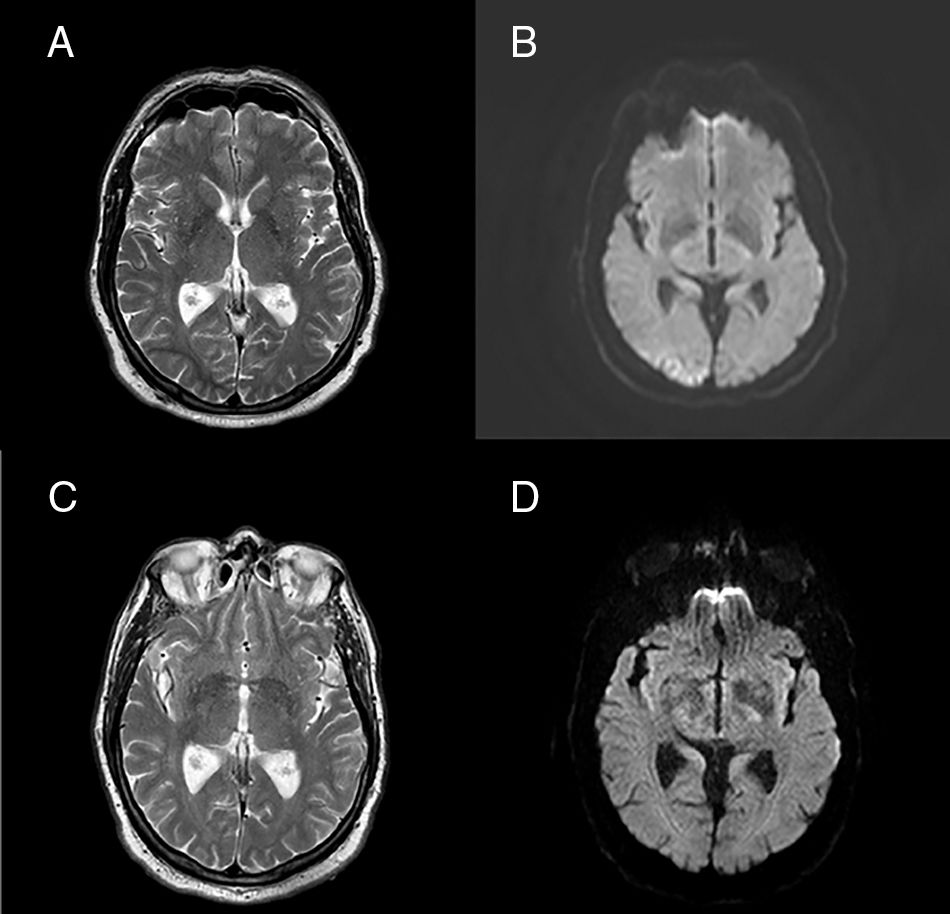
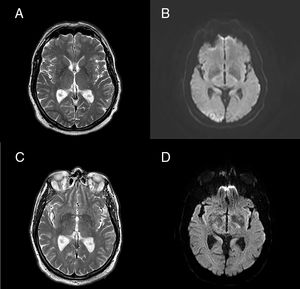
A) RM craneal, secuencia T2, discreta hiperintensidad cortical en corteza visual derecha, con hipointensidad de señal subcortical adyacente. B) Secuencia de difusión que muestra un área de restricción de señal en corteza visual derecha. C y D) Imágenes de RM craneal en secuencias T2 y difusión tras inicio de insulinoterapia, con total resolución de las alteraciones previas.
Las crisis epilépticas occipitales en contexto de hiperglucemia, son un cuadro poco frecuente5, que se ha relacionado en los últimos años con hallazgos característicos en resonancia magnética, como hipointensidad subcortical en secuencia T2 y restricción cortical en secuencias de difusión en lóbulos occipitales6–8. El mecanismo fisiopatológico continúa siendo desconocido, aunque se postula que el depósito anormal de hierro esté relacionado6. La normalización clínica, eléctrica y radiológica tras tratamiento diabetológico son claves para el diagnóstico, evitando exploraciones complementarias innecesarias y el inicio de tratamiento anticomicial crónico, con las consecuencias que ello conlleva.
Al paciente y a su familia por su colaboración.
Trabajo presentado como póster en la XV Reunión anual de la Asociación Madrileña de Neurología (AMN), octubre de 2017.