Describir los tipos de demencia en una serie de pacientes valorados en una clínica psicogeriátrica y estimar el grado de acuerdo entre el diagnóstico clínico y el anatomopatológico.
Material y métodosRealizamos un análisis descriptivo de la prevalencia de los tipos de demencia entre los pacientes valorados en nuestro centro y establecemos el grado de concordancia entre el diagnóstico clínico y el anatomopatológico. Los diagnósticos se establecieron en función de los criterios diagnósticos vigentes en cada momento.
ResultadosCiento catorce casos cumplieron los criterios de inclusión. Los diagnósticos más frecuentes tanto a nivel clínico como anatomopatológico fueron enfermedad de Alzheimer y demencia mixta, pero la prevalencia se invirtió pasando de un 39% y 18% a nivel clínico a un 22% y 34% a nivel anatomopatológico respectivamente. La concordancia entre el diagnóstico clínico y el anatomopatológico fue de un 62% (IC 95%: 53-72%).
ConclusionesCasi un tercio de nuestros pacientes no tenía un diagnóstico certero en vida, fundamentalmente a expensas del infradiagnóstico a nivel clínico de la enfermedad cerebrovascular.
The aim of our study is to describe the types of dementia found in a series of patients and to estimate the level of agreement between the clinical diagnosis and post-mortem diagnosis.
Material and MethodsWe conducted a descriptive analysis of the prevalence of the types of dementia found in our series and we established the level of concordance between the clinical and the post-mortem diagnoses. The diagnosis was made based on current diagnostic criteria.
Results114 cases were included. The most common clinical diagnoses both at a clinical and autopsy level were Alzheimer disease and mixed dementia but the prevalence was quite different. While at a clinical level, prevalence was 39% for Alzheimer disease and 18% for mixed dementia, in the autopsy level, prevalence was 22% and 34%, respectively. The agreement between the clinical and the autopsy diagnoses was 62% (95% CI 53-72%).
ConclusionsAlmost a third of our patients were not correctly diagnosed in vivo. The most common mistake was the underdiagnosis of cerebrovascular pathology.
Las demencias tienen graves consecuencias sobre los pacientes y sus familias en particular, y sobre el sistema sanitario y la economía de cada país en general.
La enfermedad de Alzheimer (EA) ha sido considerada la causa más frecuente de demencia en los países occidentales. Sin embargo, recientes estudios indican que la demencia vascular (DV), sola o asociada a la EA, puede ser al menos tan frecuente1,2.
En la práctica diaria el diagnóstico de demencia se basa en los hallazgos clínicos y no en la anatomía patológica (AP). Es frecuente que los hallazgos de AP sean mucho más heterogéneos de lo que se podría suponer. Casi el 46% de los cerebros de una muestra de personas con diagnóstico clínico de EA evidenciaban la presencia de varias entidades patológicas, aunque una predominase claramente sobre la otra3.
En este artículo mostramos la distribución de tipos de demencia entre pacientes de nuestro centro a los que se les solicitó y accedieron a la donación del tejido neurológico. Evaluamos también la concordancia entre el diagnóstico clínico y el AP y discutimos las similitudes y diferencias entre nuestros datos y los de otros estudios.
Material y métodosSujetos del estudio y evaluación clínicaLos cerebros analizados procedían de 114 pacientes valorados en nuestro centro, diagnosticados de demencia o deterioro cognitivo leve (DCL), y que tras ser consultados, ellos o sus familias, habían accedido a la donación. Se les informó del procedimiento, de su finalidad y de las posibles implicaciones, y cumplimentaron el formulario de consentimiento informado vigente.
En la base de datos incluimos: sexo, antecedentes familiares de demencia, edad al inicio de los síntomas, al diagnóstico y al exitus, diagnóstico inicial, final y AP y pruebas complementarias realizadas (exploración neuropsicológica [ENP], puntuación del mini-examen cognoscitivo4 [MEC], tomografía axial computarizada craneal [TAC], resonancia magnética nuclear cerebral [RMN], tomografía computarizada de emisión monofotónica y electroencefalograma).
Como diagnóstico inicial se consideró el realizado tras la primera valoración, fuera o no en nuestro centro, y el diagnóstico final fue el que establecimos tras nuestra valoración y seguimiento. Se estableció el diagnóstico de demencia en función de los criterios DSM-IV5. Para determinar el tipo de demencia se usaron los criterios NINCDS-ADRA para el diagnóstico de posible y probable EA6. Los criterios NINDS también se usaron para el diagnóstico de DV y EA con DV. Las otras demencias se diagnosticaron en función de los criterios habituales vigentes en cada momento. El diagnóstico de DCL se basó en los criterios de Petersen7.
Establecimos que existía concordancia entre diagnóstico clínico y el AP no solo cuando ambos coincidían, sino también cuando, aunque existiesen hallazgos AP de diferentes enfermedades, una predominaba claramente sobre las demás y el diagnóstico clínico era el acertado en función de los datos clínicos y las exploraciones complementarias disponibles. No considerábamos que existiese concordancia cuando el diagnóstico final y el AP no coincidían, o cuando no se había investigado o considerado la comorbilidad vascular cerebral en el diagnóstico clínico final, y sin embargo sí existía en el AP.
En referencia al DCL consideramos que existía concordancia cuando los hallazgos en la AP no presentaban la entidad suficiente para cumplir los criterios de ninguno de los tipos de demencia, y mantuvimos la denominación de DCL en el diagnóstico AP de esos casos.
Los criterios de inclusión fueron: haber sido diagnosticado en vida de demencia o DCL, habérseles solicitado y haber accedido a la donación del cerebro, no haber precisado autopsia judicial y disponer del informe AP final.
Obtención y procesamiento del tejidoEl protocolo de estudio neuropatológico incluyó técnicas básicas y procedimientos específicos siguiendo las guías de la red europea BrainNet8.
Contamos con 114 cerebros. Se excluyeron 5 casos, 3 de ellos porque no disponíamos del resultado AP y otros 2 porque se trataba de pacientes sin diagnóstico de demencia o deterioro cognitivo en vida.
Análisis estadísticoRealizamos un análisis descriptivo para conocer la media de edad al inicio de la enfermedad, al diagnóstico y al exitus, la prevalencia de sexo y antecedentes familiares de demencia y las pruebas diagnósticas realizadas.
Además, analizamos los datos de frecuencia absoluta y relativa de cada tipo de demencia en el momento de diagnóstico inicial, final y anatomopatológico.
Finalmente realizamos una estimación puntual y por intervalo de confianza al 95% (IC 95%) de la concordancia entre el diagnóstico clínico y la AP, así como un análisis multivariante para determinar qué variables de las estudiadas podían ayudar a aumentar dicha concordancia.
ResultadosCiento catorce casos cumplieron los criterios de inclusión. La edad media al inicio de la enfermedad era 77±8 años, al diagnóstico 79±8 años y en el momento del exitus 84±8 años, con una supervivencia promedio de 7 años. Un 75% fueron diagnosticados en los 3 primeros años desde el inicio de los síntomas. Mayoritariamente fueron mujeres (60,5%). En el 30% constaba la presencia de antecedentes familiares de demencia.
Contamos con una ENP completa en el 89,5% de los casos. La puntuación media del MEC al diagnóstico fue de 20±6 puntos. Se disponía de TAC en el 79%, pero RMN solo en el 19%. En cuanto a la tomografía computarizada de emisión monofotónica y elelectroencefalograma se realizaron en un 14% y 17% respectivamente. El 75% de los pacientes tenía hecha una ENP completa y una prueba de neuroimagen (TAC o RMN) en el momento del diagnóstico final.
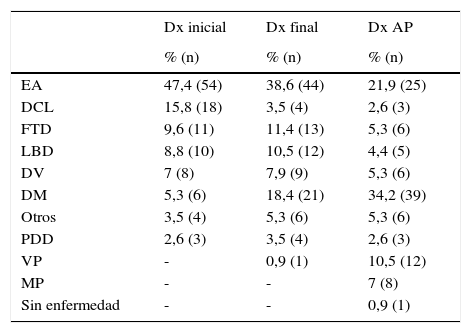
En la tabla 1 reflejamos la prevalencia del tipo de demencia en el momento del diagnóstico inicial, final y AP. Para simplificar el análisis de los resultados decidimos incluir dentro de la categoría de demencia frontotemporal tanto los casos de la variante conductual como los de parálisis supranuclear progresiva o degeneración corticobasal. Englobamos en el término vascular plus (VP) los casos de enfermedad cerebrovascular con afectación neurodegenerativa distinta de EA, y en el término multiproteínas (MP) aquellos en los que existía depósito de 2 o más proteínas.
Prevalencia diagnóstica al inicio (Dx inicial), al exitus (Dx final) y en la necropsia (Dx AP)
| Dx inicial | Dx final | Dx AP | |
|---|---|---|---|
| % (n) | % (n) | % (n) | |
| EA | 47,4 (54) | 38,6 (44) | 21,9 (25) |
| DCL | 15,8 (18) | 3,5 (4) | 2,6 (3) |
| FTD | 9,6 (11) | 11,4 (13) | 5,3 (6) |
| LBD | 8,8 (10) | 10,5 (12) | 4,4 (5) |
| DV | 7 (8) | 7,9 (9) | 5,3 (6) |
| DM | 5,3 (6) | 18,4 (21) | 34,2 (39) |
| Otros | 3,5 (4) | 5,3 (6) | 5,3 (6) |
| PDD | 2,6 (3) | 3,5 (4) | 2,6 (3) |
| VP | - | 0,9 (1) | 10,5 (12) |
| MP | - | - | 7 (8) |
| Sin enfermedad | - | - | 0,9 (1) |
DCL: deterioro cognitivo leve; DV: demencia vascular; EA: enfermedad de Alzheimer; FTD: demencia frontotemporal; LBD: demencia con cuerpos de Lewy; PDD: demencia asociada a la enfermedad de Parkinson. VP: vascular plus; MP: multiproteínas.
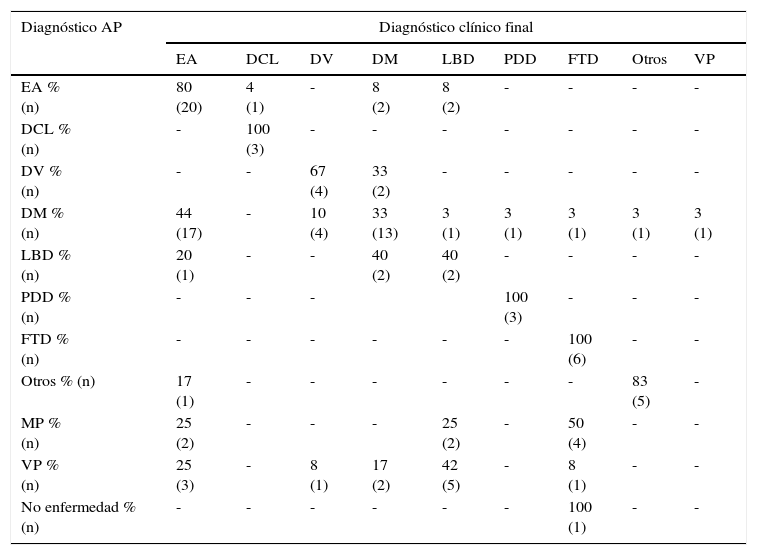
La concordancia entre el diagnóstico clínico final y el diagnóstico AP fue de un 62,3% (IC 95%: 53-72%). En la tabla 2 mostramos de manera detallada los datos de concordancia en cada tipo de demencia, pero intentando poner de manifiesto hacia dónde se producen los errores en el diagnóstico clínico, teniendo en cuenta el diagnóstico AP.
Correspondencia entre el diagnóstico anatomopatológico y el clínico
| Diagnóstico AP | Diagnóstico clínico final | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| EA | DCL | DV | DM | LBD | PDD | FTD | Otros | VP | |
| EA % (n) | 80 (20) | 4 (1) | - | 8 (2) | 8 (2) | - | - | - | - |
| DCL % (n) | - | 100 (3) | - | - | - | - | - | - | - |
| DV % (n) | - | - | 67 (4) | 33 (2) | - | - | - | - | - |
| DM % (n) | 44 (17) | - | 10 (4) | 33 (13) | 3 (1) | 3 (1) | 3 (1) | 3 (1) | 3 (1) |
| LBD % (n) | 20 (1) | - | - | 40 (2) | 40 (2) | - | - | - | - |
| PDD % (n) | - | - | - | 100 (3) | - | - | - | ||
| FTD % (n) | - | - | - | - | - | - | 100 (6) | - | - |
| Otros % (n) | 17 (1) | - | - | - | - | - | - | 83 (5) | - |
| MP % (n) | 25 (2) | - | - | - | 25 (2) | - | 50 (4) | - | - |
| VP % (n) | 25 (3) | - | 8 (1) | 17 (2) | 42 (5) | - | 8 (1) | - | - |
| No enfermedad % (n) | - | - | - | - | - | - | 100 (1) | - | - |
DCL: deterioro cognitivo leve; DV: demencia vascular; EA: enfermedad de Alzheimer; FTD: demencia frontotemporal; LBD: demencia con cuerpos de Lewy; PDD: demencia asociada a la enfermedad de Parkinson. VP: vascular plus; MP: multiproteínas.
No evidenciamos que disponer de más pruebas complementarias, el sexo del sujeto, el menor deterioro cognitivo al diagnóstico (en función de la puntuación del MEC) o un diagnóstico más precoz mejoraran nuestra concordancia diagnóstica.
DiscusiónAl analizar nuestros datos de prevalencia AP de tipos de demencia encontramos diferencias importantes respecto a estudios similares9. Nos llamó la atención la alta prevalencia de DM, del 34% frente al 4-21%, y la baja prevalencia de EA, del 22% frente al 42-65%9. A estas diferencias pudo contribuir que la elevada edad media de nuestra muestra hacía aumentar la comorbilidad cerebral3.
Nuestra comorbilidad fue mayoritariamente a expensas de enfermedad cerebrovascular. Hasta en el 53% de los casos constatamos la presencia de lesiones vasculares en la AP solas o asociadas al depósito de diversas proteínas. En estudios previos se había estimado la presencia de lesiones vasculares en un 29-41% de las necropsias de los casos de demencia en la comunidad10.
En un 11% de los casos había depósito de cuerpos de Lewy, bien en combinación con lesiones vasculares, bien con otras proteínas (casos incluidos en las categorías VP o MP respectivamente). Además, hasta en el 7% se evidenciaba el depósito de al menos 2 proteínas (MP) y en un 3% de 2 proteínas y lesiones vasculares (englobados en la categoría VP). Ya se había evidenciado la presencia de cuerpos de Lewy en el 10-20% de los cerebros de pacientes con demencia11.
El desarrollo de la inmunohistoquímica permitió clasificar las enfermedades neurodegenerativas en función del depósito cerebral de una proteína que sería la responsable de la activación de diferentes mecanismos patogénicos y diferente sintomatología. No obstante, tanto en nuestro estudio como en previos se ha puesto de manifiesto que lo infrecuente es la existencia de un tipo de lesión aislado11.
Nuestra concordancia estuvo muy lejos del 97% alcanzado en otros estudios12, y no aumentaba a más pruebas complementarias realizadas, como constatamos en el análisis multivariante. La comparativa se realizó entre el diagnóstico clínico final y el AP. No analizamos los motivos de cambio entre el diagnóstico inicial y el final, pero es bien conocida la progresión del DCL a demencia o la posibilidad de eventos cerebrovasculares sobrevenidos. Además, con frecuencia la aparición de nuevos síntomas o la realización de nuevas exploraciones complementarias implica cambios en el diagnóstico.
Se asemejaba más a trabajos clásicos en los que entre el 10-20% de los pacientes clínicamente diagnosticados de EA no tenía hallazgos AP de dicha enfermedad, y hasta un 40% tenía hallazgos AP de EA sin haber sido diagnosticados13.
El haber empleado mayoritariamente la TAC como prueba de neuroimagen pudo contribuir a infravalorar el componente cerebrovascular14. Otros estudios demostraron que contar con una prueba de neuroimagen estructural como parte del proceso diagnóstico aumentaba la sensibilidad y la especificidad en ciertos tipos de demencia14.
Nuestros bajos datos de concordancia también pueden ser justificados porque con frecuencia eran los pacientes con manifestaciones clínicas atípicas a los que se les solicitó la donación del tejido neurológico, y se trataba de una serie de casos de la práctica clínica, donde no era infrecuente que las exploraciones y valoraciones realizadas estuvieran incompletas. Además, no podemos olvidar que el nuestro es un centro psicogeriátrico, por lo que la edad de los pacientes es muy avanzada y el motivo de ingreso o valoración más habitual son graves trastornos de conducta.
ConclusiónCasi un tercio de nuestros pacientes no tenía un diagnóstico certero en vida, a pesar de nuestros esfuerzos y conocimientos, del uso de las guías de práctica clínica y de las exploraciones complementarias realizadas.
Aunque no dispongamos de fármacos con un impacto drástico sobre el curso de la enfermedad, sabemos que un correcto manejo terapéutico de las demencias ayuda a enlentecer la progresión, y eso además de una mejora en la calidad de vida del paciente tiene importantes repercusiones económicas15.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Los autores quieren expresar su agradecimiento a todos los trabajadores sanitarios y no sanitarios de la Clínica Josefina Arregui por su compromiso con la excelencia, y muy especialmente a los pacientes y sus familias por su confianza en nuestro centro y su altruista colaboración para que este trabajo fuera posible.