El tratamiento con colagenasa Clostridium histolyticum (CCH) ocupa hoy en día una alternativa para la contractura de Dupuytren. Nuestro objetivo es valorar su eficacia a un año en una serie de pacientes consecutivos.
Material y métodoEstudio prospectivo con seguimiento mínimo de los pacientes de un año. Valoración de resultados y efectos adversos.
ResultadosSe incluye un total de 75 articulaciones tratadas en 51 pacientes. La edad media fue de 65,18 años (DE: 7,288) y el 82,7% eran varones. La contractura media inicial de la MCF fue de 34,0 grados (DE: 27,37), de la IFP 41,5 grados (DE: 31,33) y de la afectación combinada (MCF+IFP) de 75,5 grados (DE: 35,2). Se alcanzó la eficacia en 68 pacientes (90,7%). Los efectos adversos fueron leves y autolimitados. La corrección media para la articulación MCF fue de 28,96 grados (DE: 26,90) y para la IFP fue de 28,72 grados (DE: 24,30). La tasa de recidivas fue de 18 (24,0%) articulaciones en 14 pacientes, siendo más frecuentes en los casos graves. El QuickDASH mostró mínimas diferencias medido antes de la intervención y al año.
DiscusiónNuestros resultados presentan mejor evolución en los casos leves; la evolución es más favorable y con mayor tasa de éxitos en la articulación MCF. El QuickDASH no es una herramienta útil para la valoración de la contractura de Dupuytren.
ConclusionesEl tratamiento con CCH para la CD es un tratamiento efectivo a medio plazo. Presenta peor evolución en afecciones de articulaciones combinadas, 5.o dedo, IFP y casos graves.
Aim Clostridium histolyticum collagenase (CCH) is nowadays an alternative treatment for the contracture of Dupuytren. Our objective is to assess its effectiveness at one year in a series of consecutive patients.
Material and methodProspective study with minimum follow-up of one year. Evaluation of results and adverse effects.
ResultsA total of 75 joints treated in 51 patients were included. The average age was 65.18years (SD: 7.288) and 82.7% were males. The initial mean contraction of the MCP was 34.0 degrees (SD: 27.37), PIP 41.5 degrees (SD: 31.33) and combined impairment (MCF+IFP) of 75.5 degrees (SD: 35.2). Efficacy was achieved in 68 patients (90.7%). Adverse effects were mild and self-limiting. The mean correction for the MCP joint was 28.96 degrees (SD: 26.90) and for PIP it was 28.72 degrees (SD: 24.30). The recurrence rate was 18 (24.0%) joints in 14 patients, being more frequent in severe cases. QuickDASH score showed minimal differences measured before the intervention and once a year.
DiscussionOur results show a better outcome in mild cases; the outcome was more favourable and with a higher success rate in the MCP joint. QuickDASH score is not a useful tool for the assessment of Dupuytren's contracture.
ConclusionsTreatment with CCH for Dupuytren's contracture is an effective treatment in the medium term. It has a poorer outcome in combined joint disorders, 5th finger, PIP and severe cases.
Actualmente el tratamiento con colagenasa Clostridium histolyticum (CCH) para la contractura de Dupuytren (CD) es un tratamiento aceptado y ampliamente utilizado que se ha incorporado ya de modo rutinario a los protocolos de tratamiento de esta patología1. Sin embargo, el tratamiento con CCH plantea los mismos problemas e incógnitas que los tratamientos clásicos en la CD: el ser un tratamiento no curativo de la enfermedad y la valoración de su efecto a largo plazo mediante la tasa de recidivas.
El concepto de recidiva todavía es un tema de debate. Recientemente dos artículos hacían referencia a la definición de la misma mediante un consenso de expertos2,3 que establecen el periodo mínimo de evolución para considerar como recidiva de la CD un año desde un punto de corte en el que se objetiva el resultado del tratamiento y una nueva contractura de más de 20 grados. En el caso específico del tratamiento con CCH, los estudios CORD4,5 y los estudios de seguimiento (CORDLESS)6,7 adaptaron diversas definiciones con el fin de considerar los distintos aspectos del nuevo tratamiento, entre ellos el concepto de paciente no respondedor y el concepto de no perdurabilidad para aquellos pacientes que, a pesar de la correcta administración del tratamiento, la evolución no era la deseada o podían incluirse en las evoluciones normales.
El objetivo de nuestro estudio es la valoración de nuestra serie clínica en los pacientes sometidos a tratamiento con CCH con un año de evolución con el fin de objetivar las recidivas y los fracasos de tratamiento.
Material y métodoEstudio de cohortes prospectivo unicéntrico. El periodo de estudio fue de aproximadamente 6años, y engloba desde el 7 de julio de 2011 al 2 de marzo de 2017. Se han incluido todas las infiltraciones con CCH abarcadas en el periodo de tiempo comprendido para su análisis de manera consecutiva. Todos los pacientes incluidos en el estudio firmaron el correspondiente consentimiento informado tanto para su intervención como para la inclusión en el estudio que ha sido aprobado tanto por el Comité de Ética del hospital como por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) con el código JPJ-COL-2015-01.
Los criterios de inclusión de los pacientes fueron tener una afectación de CD con una contractura ≥20 grados4 al nivel de las articulaciones metacarpofalángicas (MCF) o interfalángicas proximales (IFP) en una o ambas manos, la afectación de uno o dos radios de la mano8 y no tener alergias declaradas a la CCH o a los anestésicos locales. No se incluyó a pacientes con afectación del pulgar ni de la interfalángica distal. Los pacientes con tratamiento antiagregante suspendieron su medicación 7días antes del tratamiento. Los pacientes que tomaban anticoagulantes orales cambiaron temporalmente su tratamiento a heparinas de bajo peso molecular 5días antes de la inyección con CCH. El procedimiento tanto de inyección como de extensión del dedo se realizó según protocolo previamente descrito8.
Todos los procedimientos fueron realizados por cirujanos ortopédicos, tanto las inyecciones de CCH como las infiltraciones del anestésico local. El volumen de la inyección de CCH fue de 0,25ml para la MCF y 0,20ml para la IFP. La dosis total administrada fue de 0,58mg de CCH. Con la afectación de las articulaciones MCF e IFP combinada se ha infiltrado la más afectada en casos de más de 20 grados de diferencia; en el caso de menos de 20° de diferencia se ha optado por la infiltración de la zona correspondiente a la MCF. El procedimiento de extensión se realizó entre 24-48h después de la inyección del fármaco tras mantener al paciente con un vendaje oclusivo. Los bloqueos anestésicos se realizaron antes del momento de la extensión al nivel del pliegue proximal de la muñeca con una dosis total de 10ml de mepivacaína al 2% mediante una o dos punciones para anestesia de los nervios mediano y cubital. El efecto de la anestesia se comprobó mediante el sistema de discriminación en dos puntos (pinprick test)9.
La medición de resultados clínicos se ha realizado calculando la diferencia entre la extensión pasiva máxima antes del tratamiento y en los sucesivos controles después del mismo. El criterio definido como de efectividad del tratamiento a los 30días de evolución se ha determinado con los criterios CORD como objetivo primario (primary end point [PEP])4 con un déficit de extensión de entre 0-5 grados y el mantenimiento del mismo, medidos con un goniómetro digital (Baseline Digit®, Fabrication Entrerprises Inc., Elmsford, Nueva York, EE.UU.). La hiperextensión se consideró como valor de 0 para evitar factores confundidores. Se ha realizado un análisis posterior valorando la gravedad de la contractura, considerándose según los criterios de los estudios CORD4 (MCF leve ≤50 grados e IFP leve ≤40 grados) y en los casos correspondientes se han utilizado los criterios de la clasificación de Tubiana10.
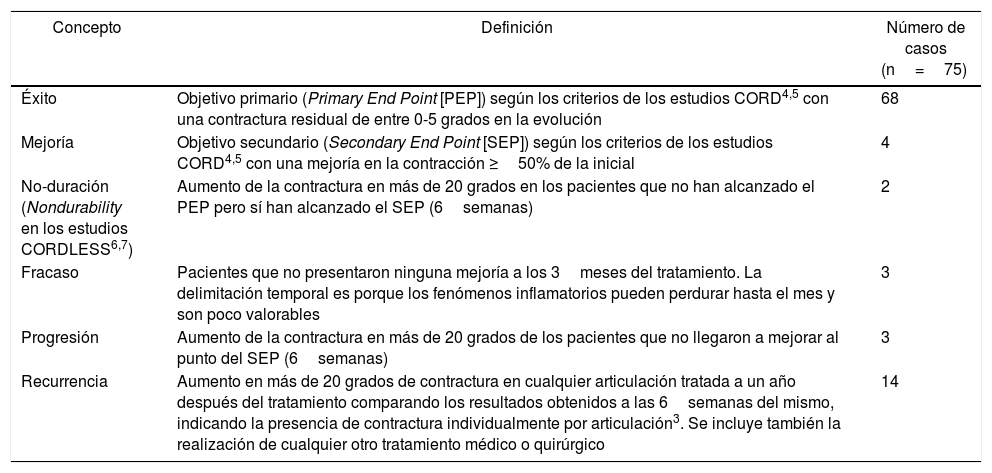
El seguimiento de los pacientes se ha realizado al mes, un año y dos años desde la intervención; en caso de laceraciones cutáneas, los pacientes han sido seguidos por la unidad de enfermería hospitalaria hasta la resolución. El criterio de recidiva se ha establecido según los criterios de consenso de Kan3, en el que se establece la recidiva en más de 20 grados de contractura en cualquier articulación tratada a un año después del tratamiento comparando los resultados obtenidos a las 6semanas del mismo, indicando la presencia de contractura individualmente por articulación. Los pacientes con evolución no satisfactoria se han clasificado de acuerdo a los criterios de los estudios CORDLESS7 (tabla 1).
Definiciones de resultados a lo largo de la evolución del tratamiento
| Concepto | Definición | Número de casos (n=75) |
|---|---|---|
| Éxito | Objetivo primario (Primary End Point [PEP]) según los criterios de los estudios CORD4,5 con una contractura residual de entre 0-5 grados en la evolución | 68 |
| Mejoría | Objetivo secundario (Secondary End Point [SEP]) según los criterios de los estudios CORD4,5 con una mejoría en la contracción ≥50% de la inicial | 4 |
| No-duración (Nondurability en los estudios CORDLESS6,7) | Aumento de la contractura en más de 20 grados en los pacientes que no han alcanzado el PEP pero sí han alcanzado el SEP (6semanas) | 2 |
| Fracaso | Pacientes que no presentaron ninguna mejoría a los 3meses del tratamiento. La delimitación temporal es porque los fenómenos inflamatorios pueden perdurar hasta el mes y son poco valorables | 3 |
| Progresión | Aumento de la contractura en más de 20 grados de los pacientes que no llegaron a mejorar al punto del SEP (6semanas) | 3 |
| Recurrencia | Aumento en más de 20 grados de contractura en cualquier articulación tratada a un año después del tratamiento comparando los resultados obtenidos a las 6semanas del mismo, indicando la presencia de contractura individualmente por articulación3. Se incluye también la realización de cualquier otro tratamiento médico o quirúrgico | 14 |
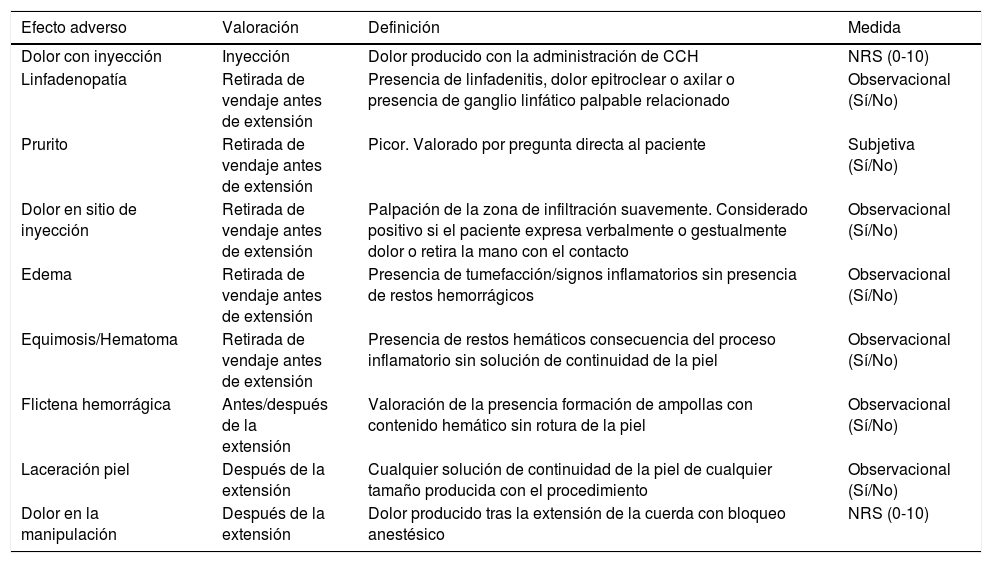
La definición de las distintas complicaciones, así como el momento de producción de las mismas y el modo de medición de cada una de las variables, se enumera en la tabla 2. Se valoró el dolor producido por el procedimiento mediante una escala Numerical Rating Score [NRS]); la escala NRS empleada presenta valores de 0 (ausencia de dolor) a 10 (peor dolor inimaginable), considerándose las valoraciones como ausencia de dolor si el valor fue de 0, dolor leve de 1-3, dolor moderado de 4-6 y dolor grave >6. Se consideró el valor de dolor patológico si el valor era ≥4.
Definición de los distintos efectos adversos a CCH considerados en el estudio, momento de producción de los mismos y escalas de medida utilizadas
| Efecto adverso | Valoración | Definición | Medida |
|---|---|---|---|
| Dolor con inyección | Inyección | Dolor producido con la administración de CCH | NRS (0-10) |
| Linfadenopatía | Retirada de vendaje antes de extensión | Presencia de linfadenitis, dolor epitroclear o axilar o presencia de ganglio linfático palpable relacionado | Observacional (Sí/No) |
| Prurito | Retirada de vendaje antes de extensión | Picor. Valorado por pregunta directa al paciente | Subjetiva (Sí/No) |
| Dolor en sitio de inyección | Retirada de vendaje antes de extensión | Palpación de la zona de infiltración suavemente. Considerado positivo si el paciente expresa verbalmente o gestualmente dolor o retira la mano con el contacto | Observacional (Sí/No) |
| Edema | Retirada de vendaje antes de extensión | Presencia de tumefacción/signos inflamatorios sin presencia de restos hemorrágicos | Observacional (Sí/No) |
| Equimosis/Hematoma | Retirada de vendaje antes de extensión | Presencia de restos hemáticos consecuencia del proceso inflamatorio sin solución de continuidad de la piel | Observacional (Sí/No) |
| Flictena hemorrágica | Antes/después de la extensión | Valoración de la presencia formación de ampollas con contenido hemático sin rotura de la piel | Observacional (Sí/No) |
| Laceración piel | Después de la extensión | Cualquier solución de continuidad de la piel de cualquier tamaño producida con el procedimiento | Observacional (Sí/No) |
| Dolor en la manipulación | Después de la extensión | Dolor producido tras la extensión de la cuerda con bloqueo anestésico | NRS (0-10) |
NRS: Numerical Rating Score (calificación por puntuación numérica).
Se han definido como individuos no participantes aquellos que cumplen todos los criterios de inclusión en el estudio pero no entran en el análisis por dos razones principalmente: pérdidas en el seguimiento por diferentes motivos (tratamientos paliativos, no ser su hospital de referencia, extranjeros, o de otras comunidades autónomas o área de salud…) o tiempo de su seguimiento insuficiente para ser incluidos en el estudio. El tiempo mínimo de seguimiento considerado para la inclusión en el estudio ha sido de 12meses.
En 34 pacientes se ha realizado un cuestionario QuickDASH para la valoración de la calidad de vida antes y al año de la intervención. La elección de este cuestionario ha venido determinada por la disponibilidad de su traducción validada al castellano.
Los datos clínicos se recopilaron en una base de datos Access® (Microsoft®, Redmond, Washington, EE.UU.). Los datos cuantitativos fueron expresados como la media y su desviación estándar (DE) o medianas y percentiles (25 y 75) para las variables de distribución normal o no. Para comparar variables cuantitativas se aplicó la prueba de la t de Student o la prueba no paramétrica de Wilcoxon. Las variables dicotómicas se analizaron mediante el test de χ2, de Pearson o la prueba exacta de Fisher, dependiendo del caso. Se aplicaron pruebas de tendencia a las variables cualitativas con más de dos categorías. Las pruebas de correlación de Pearson o Spearman se utilizaron para correlacionar variables. Para la valoración del seguimiento de los pacientes antes-después se utilizó el T-Test para muestras pareadas, pareando las muestras para su seguimiento. El análisis estadístico se realizó mediante IBM SPSS Statistics for Windows (Versión 19.0. Armonk, NY: IBM Corp®). Todas las variables fueron evaluadas previamente para la detección de factores confundidores o modificadores según los criterios de Maldonado11.
ResultadosPacientesSe han incluido todos los pacientes en los que se ha realizado tratamiento con CCH en el periodo descrito previamente. Se han realizado un total de 147 infiltraciones de CCH en 110 pacientes. Se han considerado como individuos no participantes un total de 59 individuos atendiendo al corte longitudinal del estudio en el tiempo representado que les ha impedido la cumplimentación del tiempo de seguimiento, lo que supone la pérdida de seguimiento de 72 articulaciones. Las causas de las pérdidas fueron las siguientes: 6 fallecimientos (6 articulaciones); 12 pérdidas en consulta, de las cuales 10 corresponden a pacientes extranjeros o privados (19 articulaciones), y 41 pacientes (47 articulaciones) que no llegaron al tiempo suficiente de seguimiento al realizar el corte temporal.
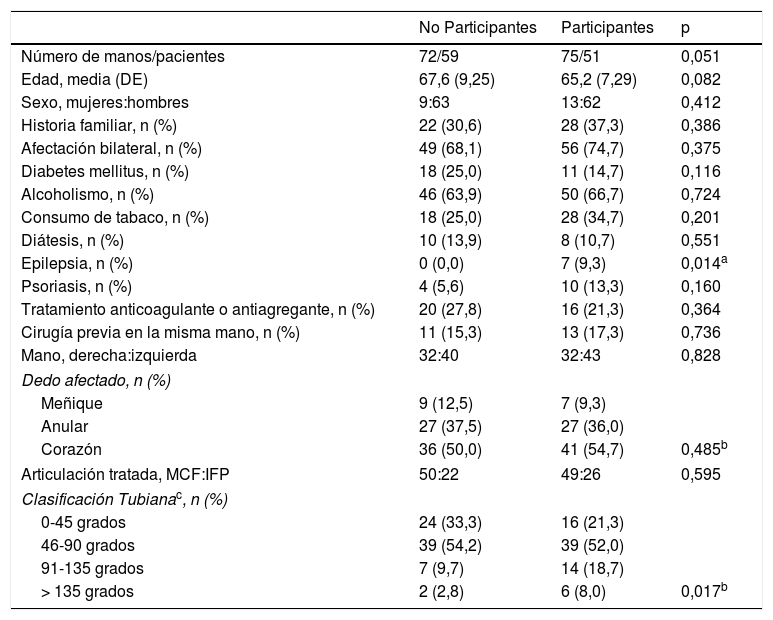
Características demográficasLas características de los pacientes que cumplieron los criterios de inclusión en el estudio se muestran en la tabla 3. Se ha incluido un total de 75 infiltraciones de CCH en 51 pacientes. La edad media de los pacientes fue de 65,18años (DE: 7.288). El porcentaje de pacientes varones fue del 82,7%. Cabe destacar la presencia de un 9,3% (7 pacientes) epilépticos con toma de fenobarbital o derivados que podrían presentar formas rápidamente recurrentes de la enfermedad. El 74,7% de los pacientes (56 tratamientos) presentaban la CD de modo bilateral, lo que también puede orientar a formas más agresivas de la enfermedad. El 21,3% (16 tratamientos) estaban anticoagulados o antiagregados.
Características de los pacientes incluidos y no incluidos en la cohorte a un año de evolución
| No Participantes | Participantes | p | |
|---|---|---|---|
| Número de manos/pacientes | 72/59 | 75/51 | 0,051 |
| Edad, media (DE) | 67,6 (9,25) | 65,2 (7,29) | 0,082 |
| Sexo, mujeres:hombres | 9:63 | 13:62 | 0,412 |
| Historia familiar, n (%) | 22 (30,6) | 28 (37,3) | 0,386 |
| Afectación bilateral, n (%) | 49 (68,1) | 56 (74,7) | 0,375 |
| Diabetes mellitus, n (%) | 18 (25,0) | 11 (14,7) | 0,116 |
| Alcoholismo, n (%) | 46 (63,9) | 50 (66,7) | 0,724 |
| Consumo de tabaco, n (%) | 18 (25,0) | 28 (34,7) | 0,201 |
| Diátesis, n (%) | 10 (13,9) | 8 (10,7) | 0,551 |
| Epilepsia, n (%) | 0 (0,0) | 7 (9,3) | 0,014a |
| Psoriasis, n (%) | 4 (5,6) | 10 (13,3) | 0,160 |
| Tratamiento anticoagulante o antiagregante, n (%) | 20 (27,8) | 16 (21,3) | 0,364 |
| Cirugía previa en la misma mano, n (%) | 11 (15,3) | 13 (17,3) | 0,736 |
| Mano, derecha:izquierda | 32:40 | 32:43 | 0,828 |
| Dedo afectado, n (%) | |||
| Meñique | 9 (12,5) | 7 (9,3) | |
| Anular | 27 (37,5) | 27 (36,0) | |
| Corazón | 36 (50,0) | 41 (54,7) | 0,485b |
| Articulación tratada, MCF:IFP | 50:22 | 49:26 | 0,595 |
| Clasificación Tubianac, n (%) | |||
| 0-45 grados | 24 (33,3) | 16 (21,3) | |
| 46-90 grados | 39 (54,2) | 39 (52,0) | |
| 91-135 grados | 7 (9,7) | 14 (18,7) | |
| > 135 grados | 2 (2,8) | 6 (8,0) | 0,017b |
IFP: articulación interfalángica proximal; MCF: articulación metacarpofalángica.
La contractura media inicial de la articulación MCF fue de 34,0 grados (DE: 27,37); la de la IFP, de 41,5 grados (DE: 31,33), y la de la afectación combinada (MCF +IFP), de 75,5 grados (DE: 35,2). Por dedos tratados, se realizaron 7 infiltraciones en el 3.er dedo (9,3%), 27 en el 4.o dedo (36%) y 41 en el 5.o (54,7%); no hubo casos que afectaran al 2.o dedo en nuestra serie. Las infiltraciones se realizaron en un 65,3% en las MCF (49 casos) y en un 34,7% en las IFP (26 casos).
El 70,7% (53 infiltraciones) se realizaron en articulaciones consideradas como graves según los criterios CORD (28 casos de las MCF [57,1%] y 25 de las IFP [96,2%]). De acuerdo con la clasificación Tubiana, 16 infiltraciones (21,3%) se realizaron sobre radios considerados como de gradoi, 39 (52%) sobre gradoii, 14 (18,7%) sobre gradoiii y 6 (8%) sobre gradoiv.
Eficacia de tratamientoSe alcanzó la eficacia en el tratamiento a 30días en 68 pacientes (90,7%). No se encontró ninguna relación estadísticamente significativa entre el resultado (consecución de la extensión primaria del dedo) y ningún factor demográfico. Por gravedad, todas las articulaciones tratadas consideradas como leves consiguieron la extensión según el objetivo primario (PEP), mientras que en 7 (13,2%) de las consideradas como graves no se alcanzó la extensión completa al mes; todas ellas se localizaron en el 5.o dedo (4 IFP y 3 MCF). De estos pacientes se consideró que 4 alcanzaron el objetivo secundario (SEP) y 3 fueron fracasos (tabla 1). Con respecto a la articulación tratada, 46 de las articulaciones MCF (93,9%) y 22 de las IFP (84,6%) consiguieron alcanzar el PEP al mes. Por dedos afectos, en el 3.er y el 4.o se consiguió una eficacia en el tratamiento del 100% (7 y 27 casos, respectivamente), y solo se observaron fracasos de tratamiento en el 5.o dedo en el 17,1% de los pacientes tratados en ese dedo (7casos) (tabla 1).
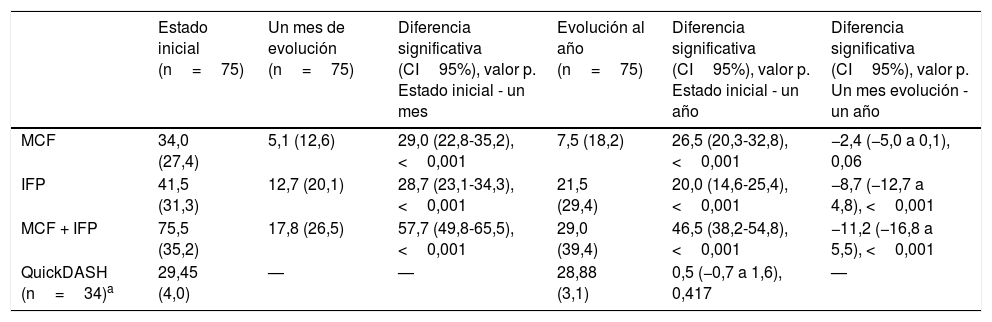
La corrección media para la articulación MCF fue de 28,96 grados (DE: 26,90) y para la IFP fue de 28,72 grados (DE: 24,30). Considerando a todos los pacientes (los que alcanzaron el PEP y los que no), el déficit de extensión al mes del tratamiento fue de 5,08 grados para la MCF (DE: 12,58) y de 12,73 grados para la IFP (DE: 20,11) (tabla 4).
Resultados clínicos y de calidad de vida tras la administración de CCH durante el tiempo de seguimiento
| Estado inicial (n=75) | Un mes de evolución (n=75) | Diferencia significativa (CI95%), valor p. Estado inicial - un mes | Evolución al año (n=75) | Diferencia significativa (CI95%), valor p. Estado inicial - un año | Diferencia significativa (CI95%), valor p. Un mes evolución - un año | |
|---|---|---|---|---|---|---|
| MCF | 34,0 (27,4) | 5,1 (12,6) | 29,0 (22,8-35,2), <0,001 | 7,5 (18,2) | 26,5 (20,3-32,8), <0,001 | −2,4 (−5,0 a 0,1), 0,06 |
| IFP | 41,5 (31,3) | 12,7 (20,1) | 28,7 (23,1-34,3), <0,001 | 21,5 (29,4) | 20,0 (14,6-25,4), <0,001 | −8,7 (−12,7 a 4,8), <0,001 |
| MCF + IFP | 75,5 (35,2) | 17,8 (26,5) | 57,7 (49,8-65,5), <0,001 | 29,0 (39,4) | 46,5 (38,2-54,8), <0,001 | −11,2 (−16,8 a 5,5), <0,001 |
| QuickDASH (n=34)a | 29,45 (4,0) | — | — | 28,88 (3,1) | 0,5 (−0,7 a 1,6), 0,417 | — |
IFP: articulación interfalángica proximal; MCF: articulación metacarpofalángica.
Los valores son medios (desviación estándar) a menos que se especifique lo contrario.
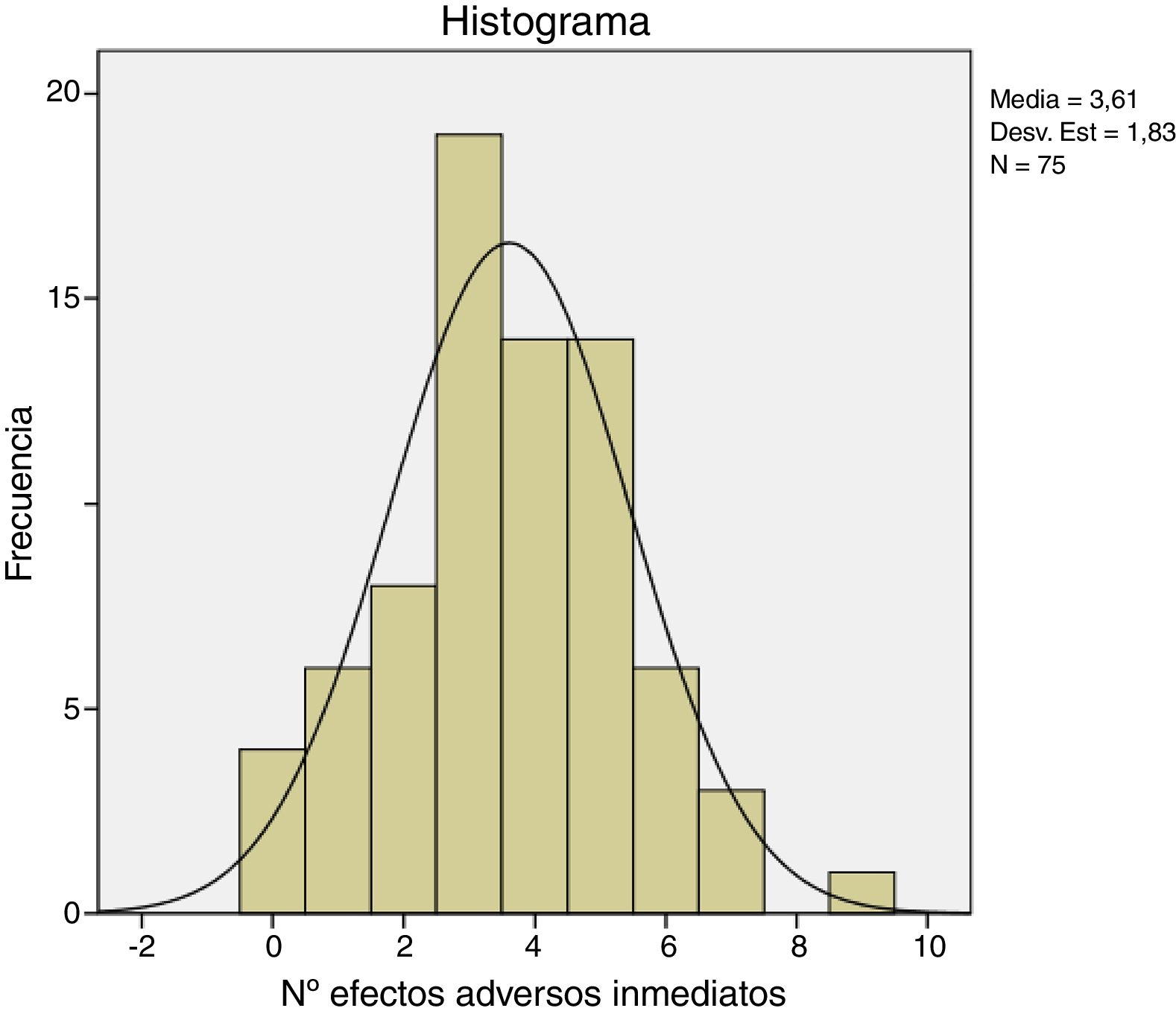
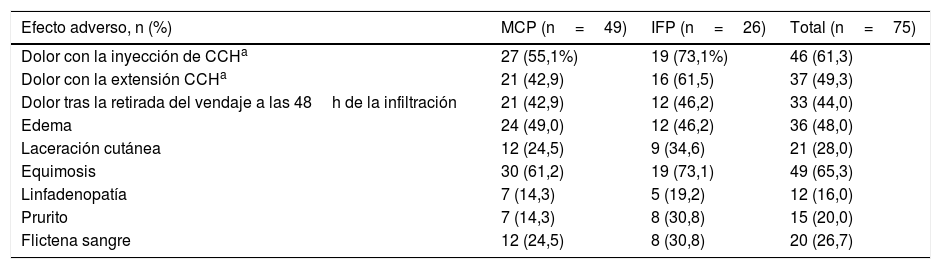
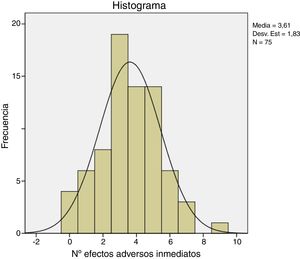
Los efectos adversos inmediatos experimentados por los pacientes fueron en general leves y autolimitados. Siete de los 75 pacientes no experimentaron ninguna complicación o efecto adverso inmediato durante o tras el tratamiento con CCH. Los pacientes presentaron una media de 3,6 (IC95%: 3,1-4,0) y una mediana de 4,0 efectos adversos por paciente. En la tabla 5 se muestran la frecuencia de los efectos adversos con el tratamiento de CCH. El dolor en cualquiera de sus manifestaciones (durante la inyección de la CCH, con la retirada del vendaje y con la extensión) y la equimosis fueron los efectos secundarios más frecuentes. La puntuación del dolor con la escala NRS varió en un rango de 0-10. El test de Kolmogorov-Smirnov mostró una distribución normal de los efectos secundarios (fig. 1).
Efectos adversos inmediatos
| Efecto adverso, n (%) | MCP (n=49) | IFP (n=26) | Total (n=75) |
|---|---|---|---|
| Dolor con la inyección de CCHa | 27 (55,1%) | 19 (73,1%) | 46 (61,3) |
| Dolor con la extensión CCHa | 21 (42,9) | 16 (61,5) | 37 (49,3) |
| Dolor tras la retirada del vendaje a las 48h de la infiltración | 21 (42,9) | 12 (46,2) | 33 (44,0) |
| Edema | 24 (49,0) | 12 (46,2) | 36 (48,0) |
| Laceración cutánea | 12 (24,5) | 9 (34,6) | 21 (28,0) |
| Equimosis | 30 (61,2) | 19 (73,1) | 49 (65,3) |
| Linfadenopatía | 7 (14,3) | 5 (19,2) | 12 (16,0) |
| Prurito | 7 (14,3) | 8 (30,8) | 15 (20,0) |
| Flictena sangre | 12 (24,5) | 8 (30,8) | 20 (26,7) |
Por articulaciones, las intervenciones sobre la IFP presentaron una media de 4,2 (IC95%: 3,4-5,0) y sobre la MCF presentaron una media de 3,3 (IC95%: 2,8-3,8) efectos secundarios, presentando diferencias estadísticamente significativas (F=4,154; p=0,045). En la aparición de efectos adversos no se encontraron diferencias significativas ni por lado ni por el dedo tratado, aunque fueron más frecuentes el 5.o dedo (n=41) que en el resto (27 en el 4.o dedo y 7 en el 3.er dedo).
Según la gravedad de la contractura inicial se encontraron diferencias significativas (F=6,30; p=0,014), con el promedio de efectos adversos por paciente de 2,8 (DE=1,7) en el caso de las contracturas consideradas como leves, o de 3,9 (DE=1,8) si eran consideradas como graves. En cuanto a la valoración de los efectos secundarios considerados individualmente, solamente se encontraron diferencias significativas (p=0,023) en el caso de las laceraciones cutáneas en el caso de que la contractura inicial era considerada como grave (n=19; 35,8%) (solamente se presentaron dos casos (9,1%) en las articulaciones tratadas consideradas como leves).
Respecto a la relación de la aparición de efectos adversos inmediatos con la eficacia del tratamiento, hubo diferencias muy significativas en el dolor en la infiltración de CCH, eficaz (n=30; 44,1%) versus ineficaz (n=7, 100%), p=0,005, y en el dolor tras la manipulación: eficaz (n=27, 39,7%) versus ineficaz (n=6, 85,7%), p=0,039.
Calidad de vidaSe ha aplicado el cuestionario QuickDASH a 34 pacientes del total antes del tratamiento, a la valoración a los 3meses y al año. Los resultados se pueden observar en la tabla 4. Las diferencias al año en la puntuación del QuickDash fueron de 1,00 (IC95%: −0,57 a 2,57; p=0,201) para MCP y de −0,80 (IC95%: −2,05 a 0,45; p=0,182) para IFP, mostrando un mínimo cambio en los valores iniciales.
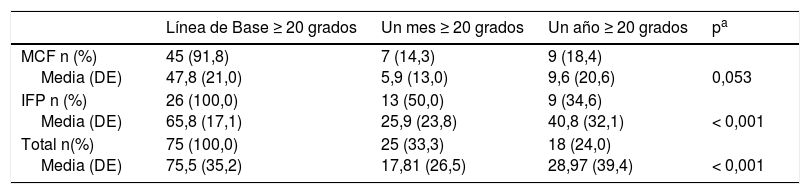
Seguimiento a un añoEl tiempo medio de seguimiento de los pacientes fue de 13,8 (IC95%: 12,7-15,0) meses. La tasa de recidivas en periodos de seguimiento a más de un año fue de 18 (24,0%) articulaciones de 14 pacientes. No hubo diferencias significativas en las recidivas producidas por el tipo de articulación intervenida (χ2 de Pearson: 2,459, p=0,117). Hubo más recidivas en las articulaciones consideradas inicialmente graves (n=16; 30,2%) que en las leves (n=2; 9,1%), aunque esta diferencia no fue significativa (p=0,07). Por articulaciones, las recidivas fueron proporcionalmente más frecuentes en la IFP (34,6%; 9 casos) que en la MCF (18,4%; 9 casos) (tabla 6). La tasa de recidivas al año fue independiente de la eficacia del tratamiento al mes (p=0,348): ineficaz (n=3; 42,9%) versus eficaz (n=15; 22,1%).
Tasa de recurrencia después de un año. Comparación con la línea de base y un mes de infiltración de CCH
| Línea de Base ≥ 20 grados | Un mes ≥ 20 grados | Un año ≥ 20 grados | pa | |
|---|---|---|---|---|
| MCF n (%) Media (DE) | 45 (91,8) 47,8 (21,0) | 7 (14,3) 5,9 (13,0) | 9 (18,4) 9,6 (20,6) | 0,053 |
| IFP n (%) Media (DE) | 26 (100,0) 65,8 (17,1) | 13 (50,0) 25,9 (23,8) | 9 (34,6) 40,8 (32,1) | < 0,001 |
| Total n(%) Media (DE) | 75 (100,0) 75,5 (35,2) | 25 (33,3) 17,81 (26,5) | 18 (24,0) 28,97 (39,4) | < 0,001 |
IFP: articulación interfalángica proximal; MCF: articulación metacarpofalángica.
Recurrencia ≥20 grados al año.
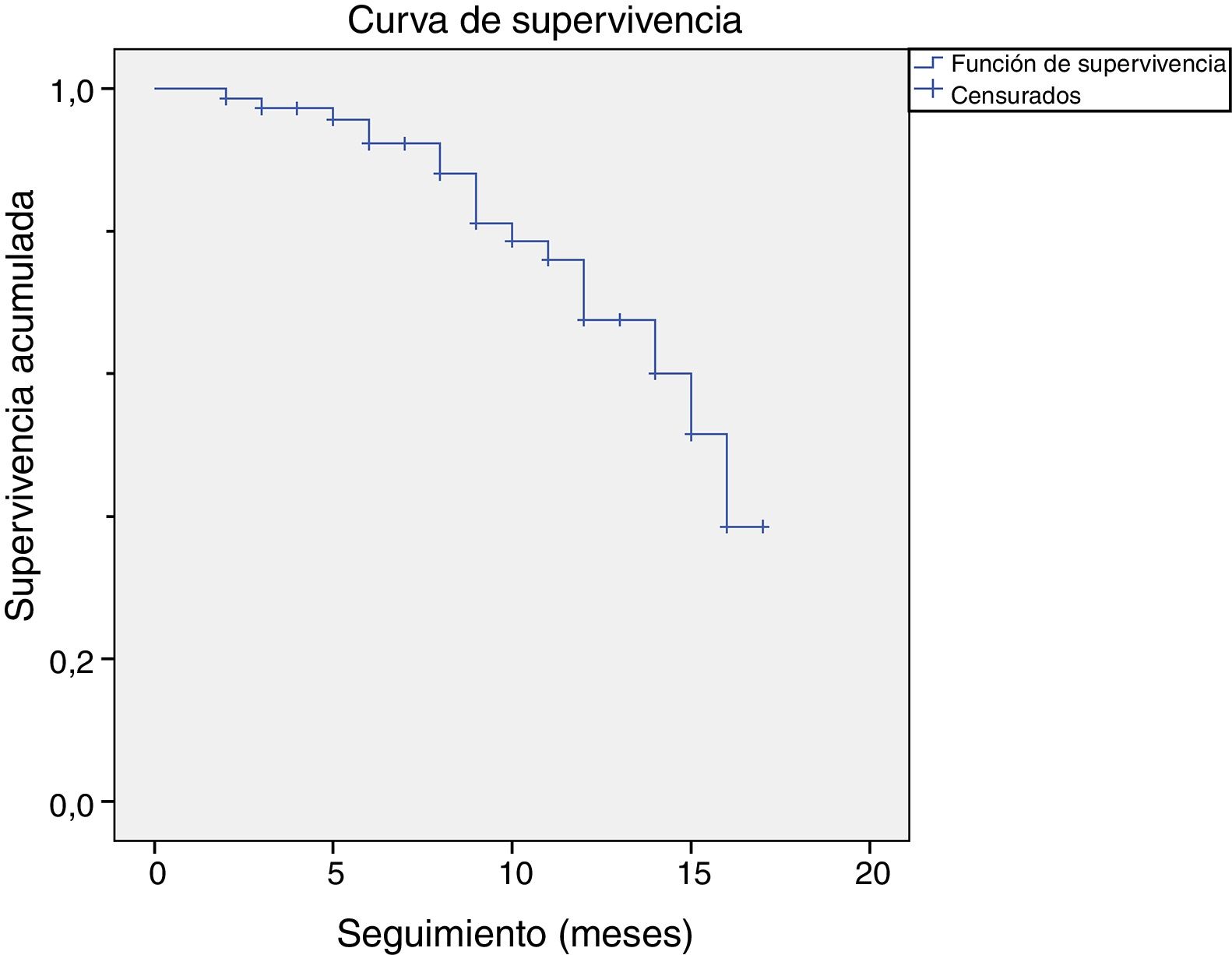
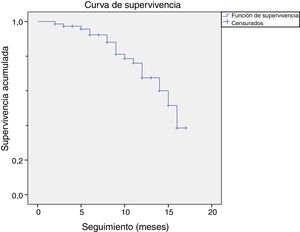
De estos 14 pacientes que sufrieron recidiva, 9 fueron considerados recidivas al haber recibido un nuevo tratamiento en el punto temporal de corte. Cinco pacientes optaron por cirugía y 4 por un nuevo tratamiento con CCH. El resto de pacientes (n=5) se consideraron recidivas por presentar una medición de más de 20 grados en una medición después del año del tratamiento con CCH. En la figura 2 se muestra la gráfica del análisis de supervivencia realizado por el método Kaplan-Meier de la cohorte, siendo la recidiva el evento principal.
De los 4 pacientes que alcanzaron una mejoría (SEP), 2 de ellos volvieron a mostrar un aumento de la contractura en los meses siguientes. De los 3 pacientes que se consideraron fracasos de tratamiento (todos ellos en la IFP del 5.o dedo), la contractura durante el periodo de evolución se consideró al menos igual que antes del tratamiento.
DiscusiónNuestros resultados son avalados por la literatura existente con respecto al tratamiento de la CD con CCH. Se presenta mejor evolución en los casos considerados como leves en la clasificación establecida en los estudios CORD4,5, y la evolución es más favorable y con mayor tasa de éxitos en la articulación MCF. La alta tasa de éxitos del tratamiento a 30días de evolución (90,7%) solo indica la correcta administración del medicamento y la consiguiente destrucción de la cuerda de la CD en mayor o menor medida, pero la eficacia real del tratamiento ha de valorarse a lo largo del tiempo, medido en forma de recidivas.
La serie presentada muestra una evolución mínima de un año, periodo considerado en las reuniones de consenso que han establecido la definición de recidiva en la CD2,3 como el tiempo a valorar para establecer el concepto de recidiva. La tasa del 24% de recidivas al año, siendo más frecuentes a nivel de los casos graves y en articulaciones IFP, es acorde a los resultados de algunas series como la de McFarlane et al.12, con un tasa del 20% en pacientes con una sola dosis, menor que la de Hansen et al.13, con una tasa de recidivas del 67% para la IFP, y mayor que la de Hurst et al.4, del 6,7% al año. El único estudio publicado con una evolución a 5años es el estudio CORDLESS6, que valora el seguimiento de los pacientes incluidos en los estudios CORD y JOINT; en este estudio se estipula una tasa de recidivas a los 2años del 20% sobre pacientes que habían alcanzado el éxito terapéutico, siendo mucho más marcada en los tratamientos sobre IFP. A nuestra tasa de recidiva hay que añadir los 2 de los 4 que aumentaron la contractura tras una mejoría parcial (SEP) (no duración del tratamiento) y los 3 en los que se consideró el tratamiento como fracaso (progresión). En total, 23 (30,6%) pacientes de nuestra serie no mantuvieron un resultado óptimo a los 13meses de seguimiento. Hemos de tener en cuenta en nuestra serie la cantidad de pacientes en los que se trataron articulaciones consideradas graves (70,7%), las articulaciones IFP (34,7%), el 5.o dedo (54,7), el casi 10% de epilépticos, el casi 75% de bilateralidad o los denominados estadiosii de Tubiana de muchas de las afectaciones combinadas (media de 75,5 grados de contractura) que realmente muestran una afectación de la IFP correspondiente a un gradoiii (contractura mayor de 45 grados), datos todos ellos que indican peor pronóstico en cuanto al tratamiento de ese tipo de articulaciones13,14 o formas de mayor agresividad. Los resultados en la serie de Syed et al.15 con pacientes seleccionados con articulación MCF única presentan mucho mejor evolución con una tasa del 100% de éxitos al año y un aumento de contractura de solo un grado. Los resultados de nuestra serie están enfocados a la valoración del uso de la CCH en la práctica diaria y engloban a pacientes desde el inicio de la comercialización del fármaco en Europa. Actualmente la postura de algunos autores se basa en la selección de pacientes para la optimización de resultados16, excluyendo IFP graves o pacientes con cuerdas muy gruesas. La utilización de una sola dosis por tratamiento también puede influir en nuestros resultados, ya que, basándonos en estudios previos de coste-utilidad17,18, la utilización de CCH es coste-efectiva con la utilización de solo un vial por tratamiento.
Uno de los problemas que plantean muchas series es la valoración de las articulaciones combinadas. La medición de resultados en este tipo de pacientes presenta invariablemente un sesgo, ya que el tratamiento con CCH está determinado para la valoración de la actuación del fármaco en una sola articulación (MCF o IFP). Hemos incluido los pacientes de este modo para mantener la uniformidad con respecto a las series publicadas a pesar de ello y se han dado los valores de la articulación más afectada19, con lo que el sesgo puede aumentar. Hayton et al.20 realizan un estudio comparando la evolución de MCF con tratamientos en articulaciones únicas y combinadas, y evidencian que el resultado en las últimas no es tan bueno como en las primeras.
Aunque no hay un sistema estandarizado para valorar los resultados en el tratamiento de la CD21, actualmente las escalas de medición de calidad de vida y de satisfacción de los pacientes, los denominados Patient Reported Outcome Measure (PROM) y Patient Reported Experience Measure (PREM), son herramientas fundamentales en la valoración de los pacientes con CD. La afectación del 5.o dedo de forma aislada, con una contractura moderada-grave, normalmente no es tan incapacitante como la afectación comisural a nivel de la zona del pulgar, por ejemplo. Hemos de tener en cuenta que la correlación entre el déficit de extensión pasivo (TPED) y la satisfacción de los pacientes, o sea, los resultados objetivos y los subjetivos, es débil22. Para la valoración de estos parámetros se han utilizado diversas escalas: Patient Evaluation Measure (PEM)23, Michigan Hand Outcomes Questionnaire (MHQ)24,25, Southampton Dupuytren's Scoring Scheme (Southampton SDSS)26, Unité Rhumatologique des Affections de la Main (URAM)12,15,22,27… De todos ellos, el SDSS y el URAM han demostrado una buena consistencia interna28,29. Nosotros hemos utilizado el QuickDASH por considerarlo cómodo y eficaz desde un primer momento; sin embargo, hemos tenido que abandonar su utilización por diversos motivos: su no validez en la CD30, la valoración del dolor como hecho cardinal no es válida para la CD31,32 y la falta de objetivación de resultados en nuestra serie (no hay diferencias en la evolución del tiempo aunque el paciente presente una franca mejoría objetiva), a pesar de que otras series sí hayan mostrado diferencias significativas en la evolución12,15,22. La utilización de cualquiera de los otros cuestionarios expuestos no ha podido realizarse por falta de validación de los mismos al castellano.
La sistemática planteada para la valoración de los efectos secundarios presenta el mismo problema que las articulaciones combinadas: los sesgos de medición. Hemos utilizado también la nomenclatura inicial establecida en los estudios CORD y seguida en la mayoría de artículos, aunque no compartamos actualmente este punto de vista33 por motivos de uniformidad. Prueba de ello es la reciente publicación de una revisión sistemática34 donde se recogen las complicaciones de los diversos tratamientos para la CD que estima la tasa de complicaciones para la CCH en el 78% mientras que para la dermofasciectomía es solo del 11,6%. No parece lógico que las técnicas quirúrgicas más complejas presenten una tasa de complicaciones tan pequeña con respecto a la CCH, y, de hecho, si analizamos únicamente las complicaciones mayores entre distintas técnicas, la tasa de complicaciones del tratamiento con CCH se asemeja mucho a la de la fasciectomía, sin presentar diferencias estadísticamente significativas entre las dos técnicas35.
En cuanto a las limitaciones de nuestro estudio, encontramos por un lado la pérdida progresiva de pacientes en el evolutivo, la consiguiente disminución del número de pacientes en la serie, el tiempo de evolución considerado como medio plazo y los posibles sesgos de medición citados anteriormente, que podrían evitarse en reuniones y consensos entre expertos unificando criterios.
En definitiva, podemos concluir que el tratamiento con CCH para la CD es un tratamiento efectivo a medio plazo con una alta tasa de éxitos y una peor evolución en afecciones de articulaciones combinadas, 5.o dedo, IFP y casos graves.
Nivel de evidenciaNivel de evidencia III.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no presentar ningún tipo de conflicto de intereses en el momento de la realización del presente trabajo.
El presente trabajo forma parte de la tesis doctoral de Rafael Sanjuán Cerveró en la Universidad de Granada.