A terapêutica de privação androgénica (TPA) é a terapêutica standard para o cancro da próstata avançado. Contudo, sabe-se que não está isenta de efeitos adversos, com impacto na qualidade de vida dos doentes e, possivelmente, também na sobrevida global. Este artigo tem como objectivos rever os principais efeitos adversos associados à terapêutica de privação androgénica e abordar os métodos para minimizar o impacto de cada um deles.
Androgen deprivation therapy (ADT) is the standard therapy for advanced prostate cancer. However, it encompasses several adverse effects, with impact on patient’s quality of life and, eventually, on overall survival. This article will review the most important side-effects associated with androgen deprivation therapy and the methods for minimizing their impact.
A neoplasia da próstata é o tumor não cutâneo mais frequente no homem. A taxa de mortalidade associada só é ultrapassada pela da neoplasia do pulmão1.
Sabe-se, há mais de um século (Hunter, 1840), que o epitélio da próstata sofre atrofia após a castração. Em 1941, Huggins (prémio Nobel da Medicina 1966) lançou a hipótese de que o epitélio prostático benigno e maligno eram bioquimicamente análogos e que responderiam da mesma forma à privação androgénica, fenómeno a que chamou de “silogismo biológico”. O bloqueio androgénico provoca a apoptose de células tumorais, levando a uma diminuição do volume tumoral e ao atraso da sua progressão. Na maior parte dos doentes, as células insensíveis aos androgénios sobrevivem e proliferam, eventualmente levando à morte do doente2.
A testosterona é a principal hormona masculina e a privação da sua acção está associada a uma série de efeitos secundários. A maioria dos estudos até à actualidade focou-se na “toxicidade sintomática” desta privação (afrontamentos, diminuição da líbido, instabilidade emocional, fadiga). Recentemente, desviou-se a atenção para toxicidades mais silenciosas mas potencialmente mais graves, que merecem monitorização específica e medidas preventivas para manter a qualidade de vida dos doentes, nomeadamente a obesidade, a sarcopénia, a osteoporose e o risco cardiovascular3.
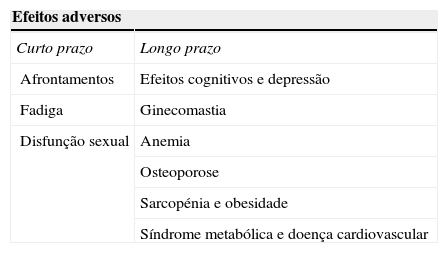
ApresentaçãoEfeitos adversosOs efeitos adversos da hormonoterapia podem ser classificados, quanto ao timing (tabela 1), em efeitos que surgem a curto e longo prazo4. Em doentes com doença metastática, os efeitos adversos são por vezes aceitáveis tendo em conta os ganhos potenciais na diminuição dos sintomas. Contudo, os efeitos a longo prazo na saúde e qualidade de vida dos homens com doença localizada podem ser inaceitáveis tendo em conta o impacto (por vezes questionável) na sobrevida5.
Classificação das complicações da terapêutica de privação androgénica quanto ao momento do seu aparecimento
| Efeitos adversos | |
|---|---|
| Curto prazo | Longo prazo |
| Afrontamentos | Efeitos cognitivos e depressão |
| Fadiga | Ginecomastia |
| Disfunção sexual | Anemia |
| Osteoporose | |
| Sarcopénia e obesidade | |
| Síndrome metabólica e doença cardiovascular |
Afectam cerca de 80% dos doentes6. Definem-se como uma sensação súbita de calor intenso na face, pescoço e porção superior do tronco, com uma duração que varia desde segundos a horas, podendo ocorrer várias vezes por dia. Podem surgir espontaneamente mas existem factores desencadeantes conhecidos: as alterações posturais, o stress, as mudanças de temperatura, os alimentos picantes ou quentes e o tabaco3. A causa deste efeito adverso está relacionada com uma estimulação inapropriada do centro termorregulador do hipotálamo, provocando uma vasodilatação periférica e consequente rubor cutâneo e sudorese7. Os afrontamentos tendem a aparecer nos primeiros três meses de tratamento e persistem a longo prazo na maioria dos doentes8.
Poucos tratamentos estão aprovados para o controlo dos afrontamentos no homem com cancro da próstata, havendo necessidade de grandes ensaios prospectivos nesta área.
Existem tratamentos a que alguns doentes recorrem e que, apesar de falta de evidências fortes, merecem atenção, tendo sido já publicadas algumas revisões sobre acunpuntura9, suplementos de óleo de peixe10, fitoestrogénios da soja (com eficácia comprovada no tratamento dos afrontamentos nas mulheres com cancro da mama sob hormonoterapia, mas não avaliados no homem11).
Actualmente, o tratamento passa pela terapêutica hormonal e antidepressivos.
- •
Os progestagénios (acetato de ciproterona 50–100 mg/ dia e medroxiprogtesterona 20 mg/dia) mostraram alguma eficácia, com 80% dos homens com evidência de melhoria com o primeiro e 84% com o segundo12. No entanto, apesar do baixo custo, apresentam efeitos adversos a ter em consideração: aumento do tecido adiposo, diminuição da HDL, aumento do apetite, sarcopénia e fadiga13,14.
- •
A venlafaxina (75mg/dia) demonstrou redução de sintomas em 47% dos homens, com o efeito benéfico nos sintomas depressivos. São também válidos fármacos da classe dos inibidores selectivos de recaptação da serotonina (ISRS), como a sertralina e o escitalopram12,15.
- •
Os estrogénios em baixa dosagem (dietilestilbestrol 0,5-1mg/dia per os e estradiol transdérmico 0,05mg/semanal) são bastante eficazes na redução dos afrontamentos, com uma resolução completa dos mesmos em 70% dos homens sob dietilestilbestrol e 83% de melhoria naqueles sob estrogénios transdérmicos. Há que ponderar este benefício versus o risco de eventos tromboembólicos ou cardiovasculares, que não se mostrou tão elevado nas dosagens mais baixas. A ginecomastia e a mastodinia são as toxicidades mais frequentes16,17.
- •
A clonidina transdérmica foi estudada num ensaio clinico (controlo vs placebo), não diminuindo de forma significativa os afrontamentos, além de apresentar efeitos adversos importantes, como a hipotensão, sonolência e a hipersensibilidade ao álcool18.
- •
A gabapentina (900 mg/dia) foi avaliada em tratamento durante 4 meses, tendo mostrado uma excelente tolerância com melhoria significativa dos sintomas19.
A fadiga é um dos principais efeitos secundários da TPA, e é também dos que provavelmente mais afectam a qualidade de vida global. Esta última é uma área complexa e difícil de investigar, já que cobre domínios como bem-estar físico e emocional, capacidade de executar tarefas diárias e funções socio-económicas e, consequentemente, de difícil quantificação3.
A TPA foi comparada com a conduta expectante (Watchfull waiting) no que respeita à qualidade de vida na doença localizada e, depois de ajustadas comorbilidades, características sociodemográficas e severidade da doença, concluiu-se que provocava maior desconforto físico, mais limitações nas actividades diárias e um score de vitalidade mais baixo. Contudo, só a diferença no desconforto físico foi estatisticamente significativa20. Apesar do impacto na qualidade de vida ser evidente, a magnitude permanece questionável, uma vez que não há ferramentas precisas para a avaliar21.
Dados recentes indicam que mudanças no estilo de vida, em especial exercício físico aeróbio e uma dieta saudável durante e após o tratamento hormonal, levaram a um aumento da massa muscular e a um aumento da vitalidade, por melhorarem o bem-estar físico e psicológico22.
Os benefícios do Ginseng (1000–2000 mg/dia) foram avaliados num ensaio clínico contra placebo, com diminuição da fadiga, sem efeitos secundários23.
3Disfunção sexualConstata-se disfunção eréctil em 80% dos doentes e perda de líbido em 95% dos doentes após o primeiro ano de tratamento. Ocorre também diminuição do volume e comprimento peniano, bem como redução da intumescência nocturna e do volume testicular24. No entanto, os efeitos negativos da TPA na função sexual não incomodam a maioria dos doentes, não necessitando de tratamento. No caso de ser necessário, o tratamento não é específico, com uma taxa de resposta à terapêutica médica (I-5PDE e alprostadilo) de 33-80% num estudo retrospectivo que avaliou a incidência de DE e a resposta ao tratamento em 395 doentes sob TPA, com um follow-up de 87,4 meses25.
Longo prazo1Efeitos cognitivos e depressãoA testosterona tem diversos efeitos neuropsicológicos no homem, intervindo ao nível da função cognitiva, humor e auto-estima26. As manifestações de alteração da cognição manifestam-se nos primeiros três a seis meses de tratamento e são aparentemente reversíveis27. É importante que se informe o doente acerca destes efeitos e que se identifiquem sinais precoces de depressão ou demência que mereçam referenciação à Psiquiatria28.
2GinecomastiaAs alterações no tecido mamário, nomeadamente a ginecomastia dependem dos agentes usados na TPA. Os antiandrogéneos não esteroides (flutamida, bicalutamida, nilutamida) provocam ginecomastia em cerca de 66% dos homens (no caso da bicalutamida) e mastodinia (hipersensibilidade mamária) em 72%, por promoverem a conversão periférica da testosterona em estradiol2.
Para prevenção da ginecomastia dolorosa está disponível a radioterapia profilática (10 Gy), não tendo efeito na ginecomastia instalada. Neste caso, as opções terapêuticas passam por lipoaspiração, mastectomia24 ou tamoxifeno29.
3AnemiaO excesso de testosterona leva a policitémia, e o seu défice provoca anemia. Contribuem não só a ausência de estimulação dos precursores eritroides pela testosterona, como também a diminuição da produção de testosterona2. A anemia, tipicamente normocítica normocrómica, afecta 90% dos doentes e com uma redução em cerca de 10% dos níveis de hemoglobina30,31. Surge precocemente após a instituição da hormonoterapia e tende a progredir até aos 24 meses de tratamento. Embora seja solucionada com a suspensão da privação androgénica, pode demorar um ano até alcançar os valores de hemoglobina pré-tratamento. É sintomática em apenas 13% dos doentes, devido à acção dos mecanismos compensatórios31.
Quanto ao tratamento, não são necessárias intervenções na dieta ou suplementos alimentares. Em caso de necessidade, a eritropoietina provoca um aumento da hemoglobina superior a 10%30.
4Efeitos no metabolismo ósseoA relação entre o hipogonadismo e a perda de massa óssea é conhecida32. Há um aumento do metabolismo ósseo e diminuição da densidade mineral óssea após TPA33. Vários estudos tentaram investigar a relação entre a perda de massa óssea e o risco de fracturas34,35, tendo-se encontrado uma redução da densidade mineral óssea e, consequentemente, um aumento do risco de fractura óssea (até 45% com TPA de longo prazo / 6 meses de duração). No entanto, estes achados não se traduziram num aumento da incidência da fractura óssea, por não existir um aumento da incidência de osteoporose36.
A avaliação dos doentes é efectuada por densitometria óssea (DEXA) da coluna lombar ou do colo do fémur, antes de iniciar a terapêutica hormonal ou após dois anos de TPA na ausência de factores de risco. Deverá ser feito o controlo anualmente ou de dois em dois anos37,38.
O tratamento engloba a alteração da dieta e do estilo de vida, estimulando a prática de exercícios de resistência, que aumentam a densidade mineral óssea em 2-5%/ano e diminuem o IMC39,40.
A suplementação com cálcio (1200–1500 mg/dia) deverá ser efectuada nos casos de deficiência do mesmo41. Este deverá ser associado à vitamina D (1000 UI/dia), com vigilância dos níveis desta última (30–40 ng/mL)42,43.
A terapêutica com bifosfonatos está indicada quando o T score na DEXA seja < −2,5 ou em caso de fractura óssea. Estão disponíveis formulações orais (ácido alendrónico 10 mg/dia ou risendronato de sódio 5 mg/dia) e endovenosas (pamidronato 45–60 mg a cada 3–4 semanas, zoledronato 4 mg trimestral ou anual44,45). Deverão ser considerados os efeitos adversos destes agentes, nomeadamente a nível gastro-intestinal e necrose da mandíbula46.
O denosumab é o anticorpo monoclonal anti-RANKL, mediador da activação, função e sobrevivência dos osteoclastos. A sua administração aumenta a densidade mineral óssea, diminui a incidência de fracturas vertebrais, atrasa o aparecimento de metástases ósseas nos doentes sem doença metastática sem, no entanto, apresentar impacto na sobrevida global47.
Os moduladores selectivos dos receptores de estrogénios (raloxifeno, toremifeno) estão também a ser avaliados para a prevenção da osteoporose nos homens sob TPA, tendo o toremifeno demonstrando, na análise interina, um aumento estatisticamente significativo da densidade mineral óssea avaliada na coluna lombar e colo do fémur48,49.
5Sarcopénia e obesidadeAs hormonas sexuais desempenham um papel importante na manutenção da massa muscular e no controlo da lipogénese. Como sarcopénia entende-se a diminuição progressiva da massa muscular, havendo muitas vezes a substituição por tecido adiposo. Este fenómeno ocorre normalmente no envelhecimento e é acelerado pela TPA. Afecta principalmente os membros, havendo um aumento de 13,8% de massa gorda nos mesmos e uma diminuição da massa magra que ronda os 2,4%, após 36 semanas de TPA50. Associado ao aumento do tecido adiposo surge a resistência periférica à insulina51.
O tratamento passa por mudanças no estilo de vida com realização de exercício físico frequente (duas vezes por semana)50, um reforço da ingestão proteica (recomendado 1–1,5 g/Kg/dia)52,53, e suplementação de aminoácidos essenciais54. A suplementação com óleo de peixe previne a sarcopénia devido à potencial redução de marcadores inflamatórios55. O músculo esquelético apresenta receptores para a vitamina D, e indivíduos mais velhos, com níveis normais de vitamina D, parecem ter menor risco de sarcopénia. Este facto justifica a suplementação com vitamina D para prevenção desta condição, em indivíduos com níveis reduzidos da mesma56.
6Síndrome metabólica e doença cardiovascularA prevalência da síndrome metabólica é superior em doentes sob TPA comparativamente aos homens não tratados, pelo desequilíbrio entre a percentagem de massa gorda e magra desencadeado pela terapêutica3. Neste contexto, a síndrome apresenta manifestações fenotípicas diferentes da síndrome original, identificando-se uma deposição preferencial da gordura no tecido subcutâneo e não visceral, um aumento do colesterol HDL e da apoproteína a, além do aumento do colesterol LDL e dos triglicéridos. Não se verifica alteração da razão abdómen/anca; não há aumento da pressão arterial sistémica ou da proteína C reactiva. A hiperglicemia é comum às duas variantes57. Isto levanta a questão se haverá, de facto, um risco aumentado de eventos e mortalidade cardiovasculares. Até à data, os dados da mortalidade cardiovascular nos doentes sob TPA permanecem inconsistentes, existindo estudos que comprovam um risco aumentado, não corroborado por outros58–60. Independentemente da argumentação, sabe-se que a doença cardiovascular é uma causa muito importante de mortalidade nos homens, nos doentes comneoplasia da próstata e nos doentes sob TPA28. Assim, recomenda-se a todos os homens sob TPA a redução do risco cardiovascular, através de alterações do estilo de vida (dieta, exercício físico, combate à obesidade e cessação de hábitos tabágicos); a introdução de estatinas61; e a suplementação com óleo de peixe (ácido eicosapentanóico (EPA) e ácido docosahexanóico (DHA) 600 mg 3id), com diminuição comprovada dos triglicéridos e um possível efeito na redução da resistência periférica à insulina62–64.
ConclusãoA terapêutica de privação androgénica é o tratamento standard para o carcinoma da próstata avançado. Contudo, está associada a vários efeitos adversos que têm um impacto negativo sobre a qualidade de vida do doente. Existem diversos métodos para minimizar os seus efeitos, incluindo medidas gerais relacionadas com alterações no estilo de vida (dieta, exercício físico), ou terapêutica farmacológica específica (tabela 2). O médico que institui a TPA deve adoptar uma atitude proactiva aquando do seguimento destes doentes, para detecção, prevenção e tratamento atempado das várias condições, nomeadamente quando a sobrevida espectável é prolongada.
Resumo das principais medidas terapêuticas aplicadas às complicações da terapêutica hormonal no cancro da próstata
| Efeitos adversos | Medidas terapêuticas |
|---|---|
| Afrontamentos |
|
| Fadiga |
|
| Disfunção sexual |
|
| Efeitos cognitivos e depressão |
|
| Ginecomastia |
|
| Anemia |
|
| Osteoporose |
|
| Sarcopénia e obesidade |
|
| Síndrome metabólica e doença cardiovascular |
|
Os autores declaram não haver conflito de interesses.