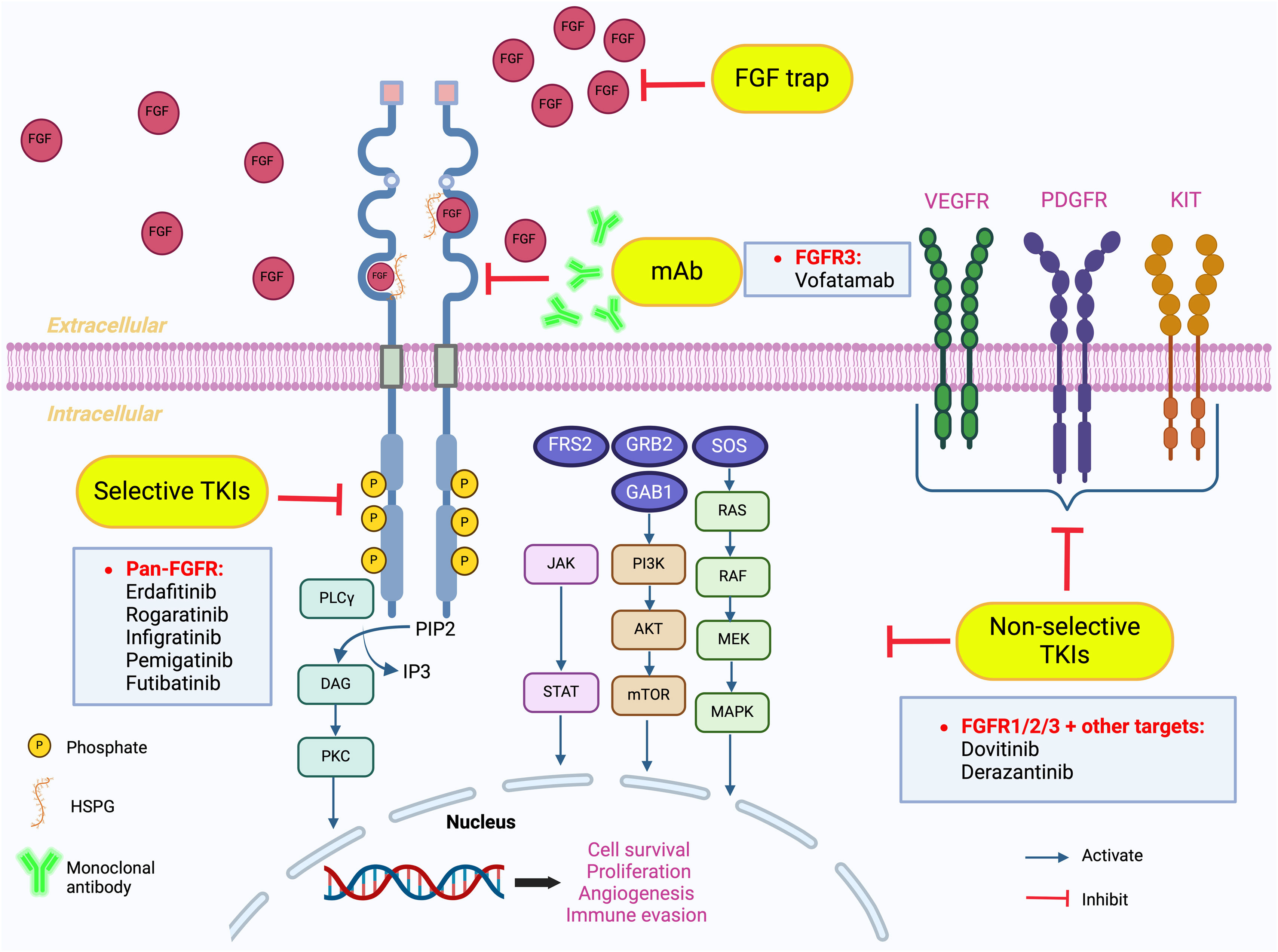
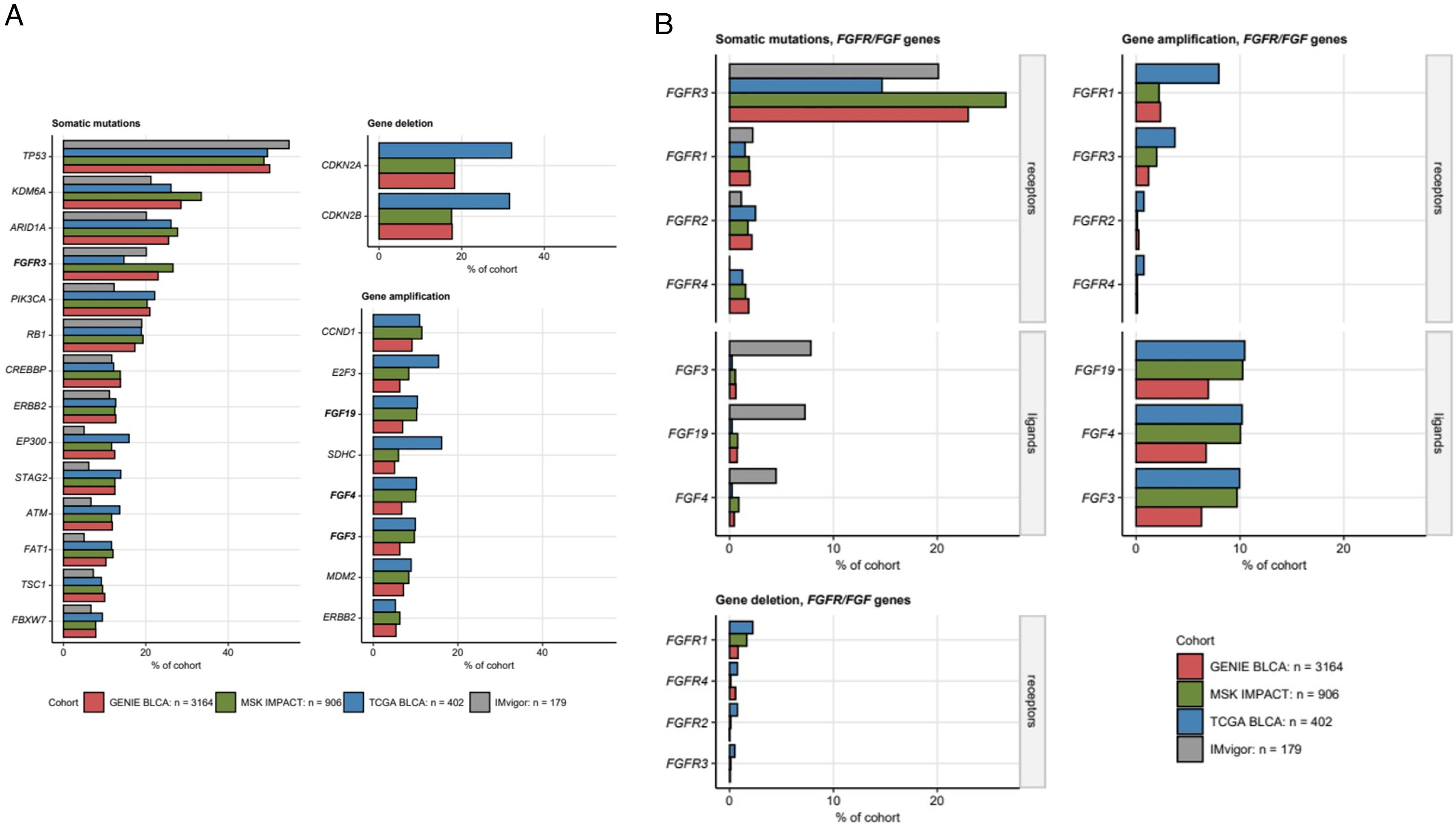
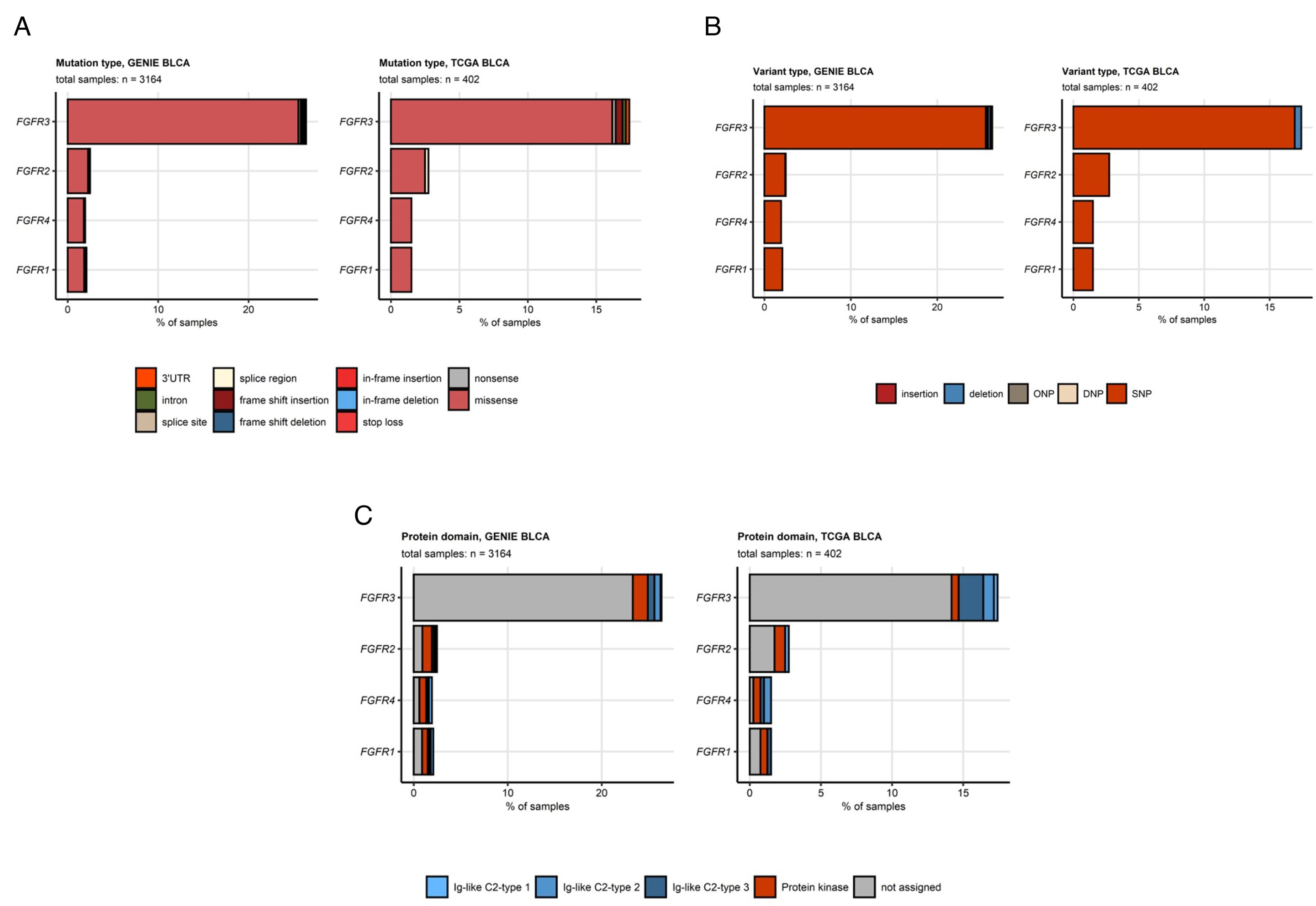
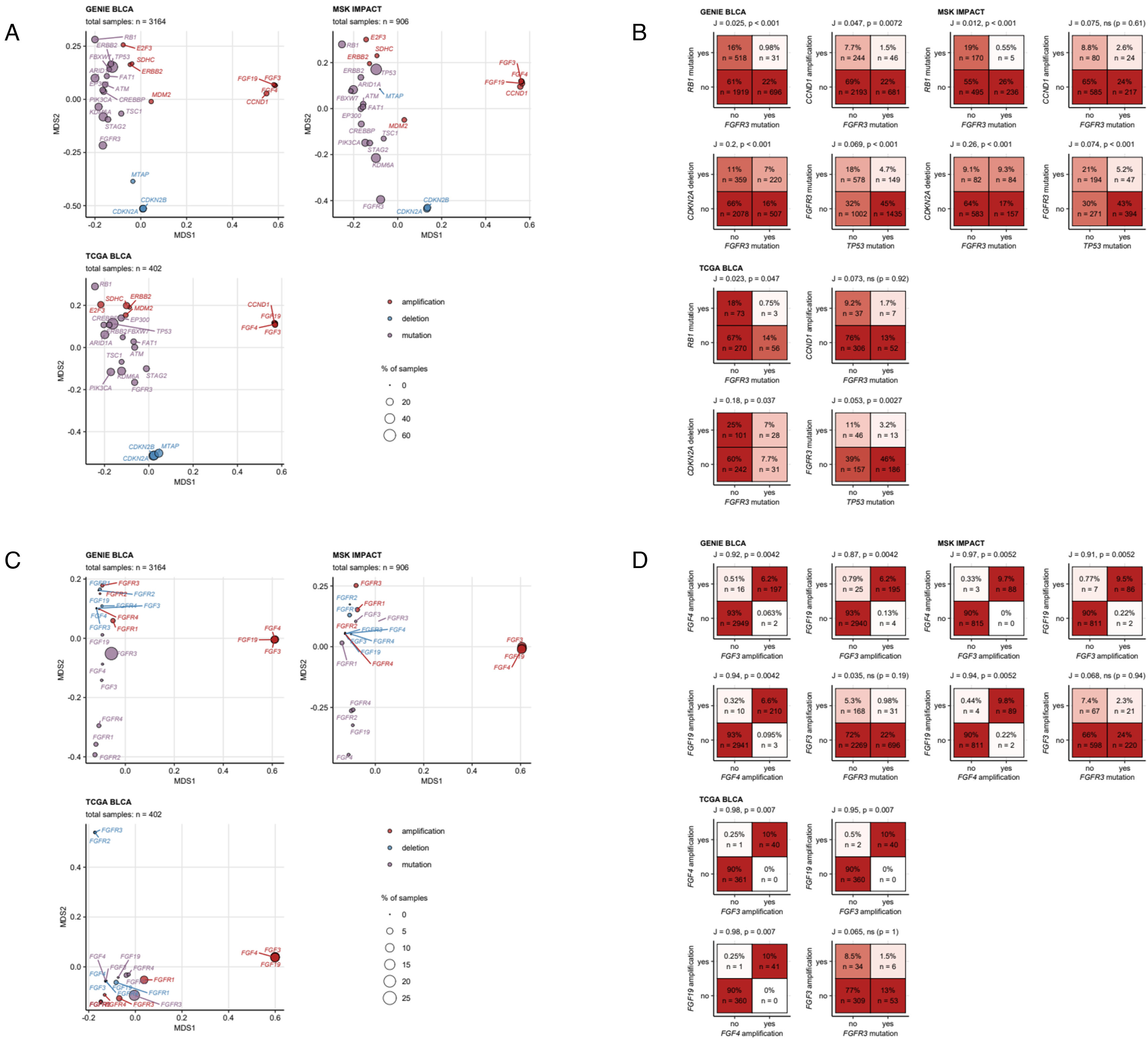
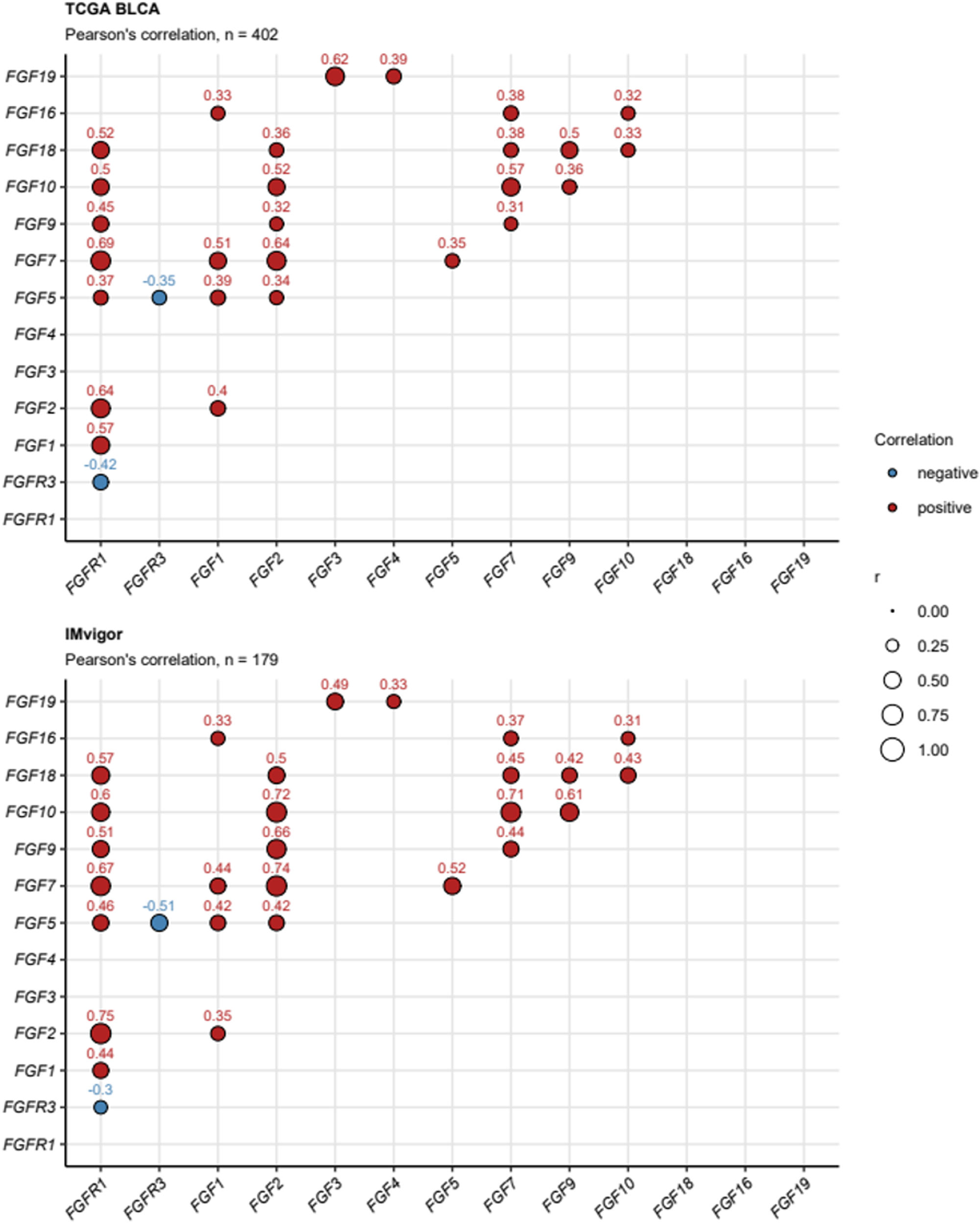
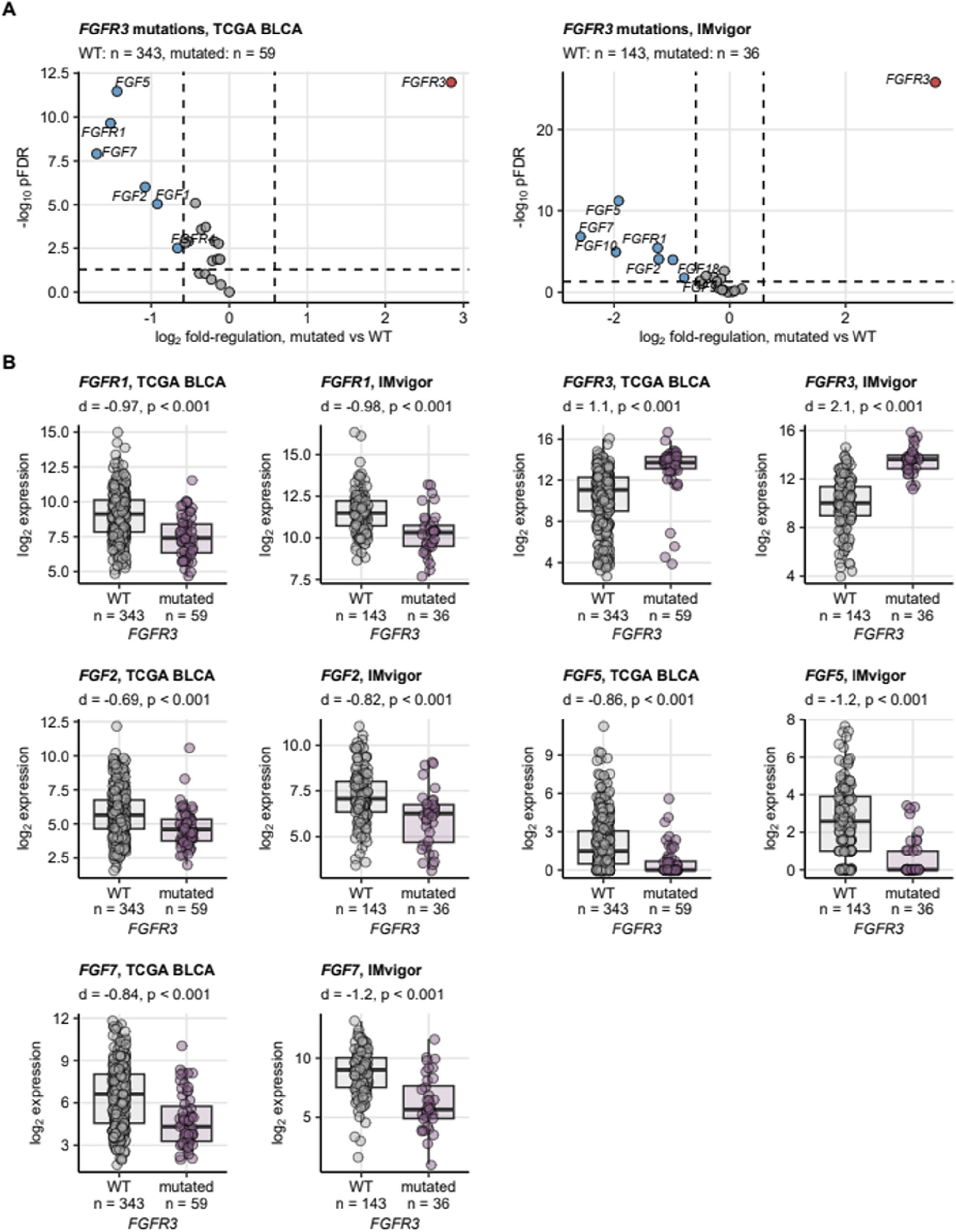
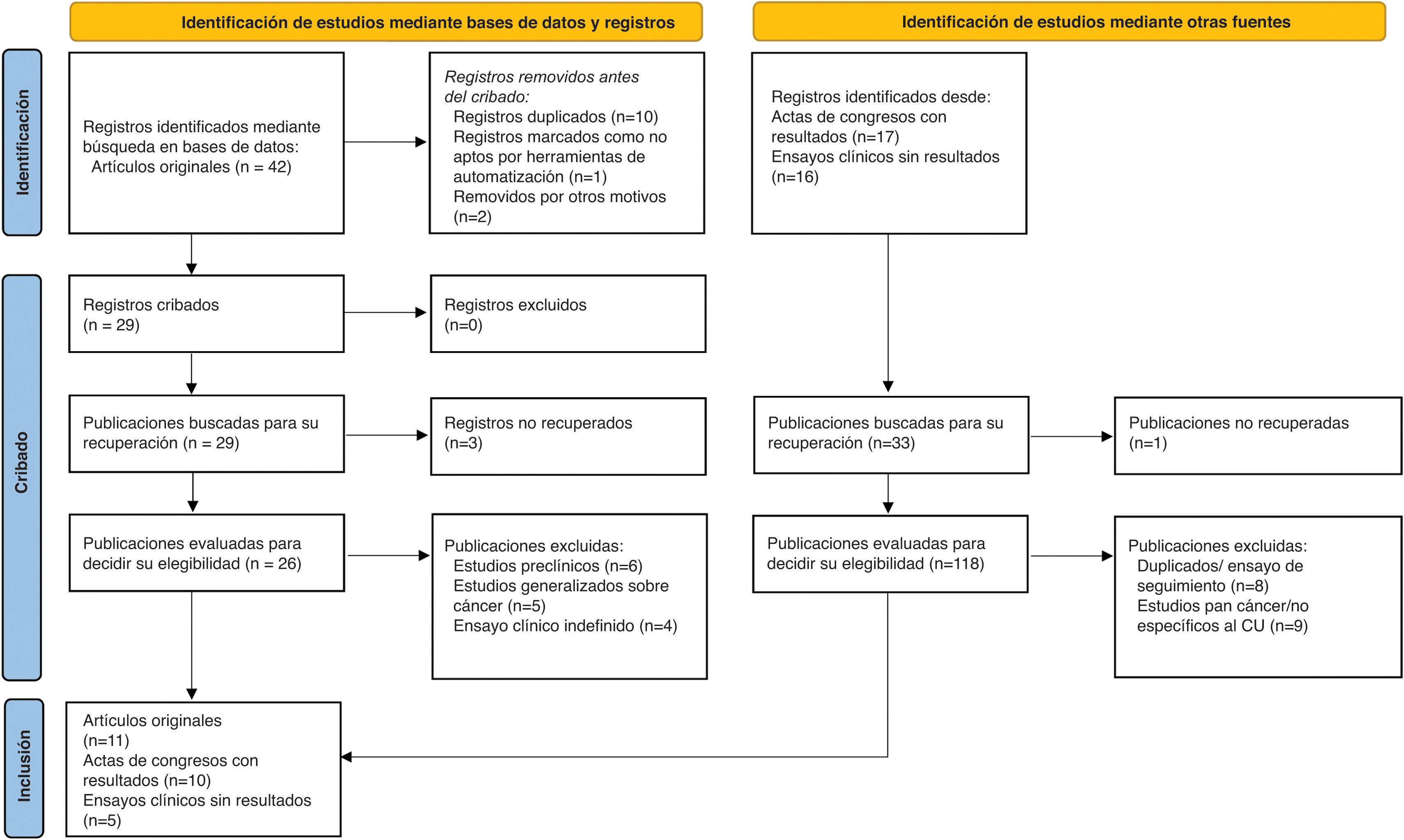
Las mutaciones del FGFR3, asociadas principalmente al subtipo papilar luminal (LumP) se encuentran entre las alteraciones genómicas más comunes en el cáncer urotelial (CU). Gracias al desarrollo de los inhibidores del receptor del factor de crecimiento de fibroblastos (FGFR), el tratamiento del CU se acerca cada vez más a la medicina personalizada. Se realizó una revisión sistemática utilizando Medline y publicaciones de congresos científicos según las directrices Preferred Reporting Items for Systematic Reviews and Meta-analyses (PRISMA) para evaluar el papel potencial de los inhibidores del FGFR utilizados en combinación con otras terapias para el tratamiento del CU. Se llevó a cabo una búsqueda sistemática en ClinicalTrials.gov para identificar ensayos clínicos en curso. En total, 11artículos a texto completo, 10resúmenes de congresos y 5ensayos fueron identificados. Según los estudios BLC2001 y THOR, erdafitinib es el único inhibidor de FGFR1-4 aprobado para el CU metastásico con alteraciones susceptibles en FGFR2/3 tras quimioterapia basada en platino.
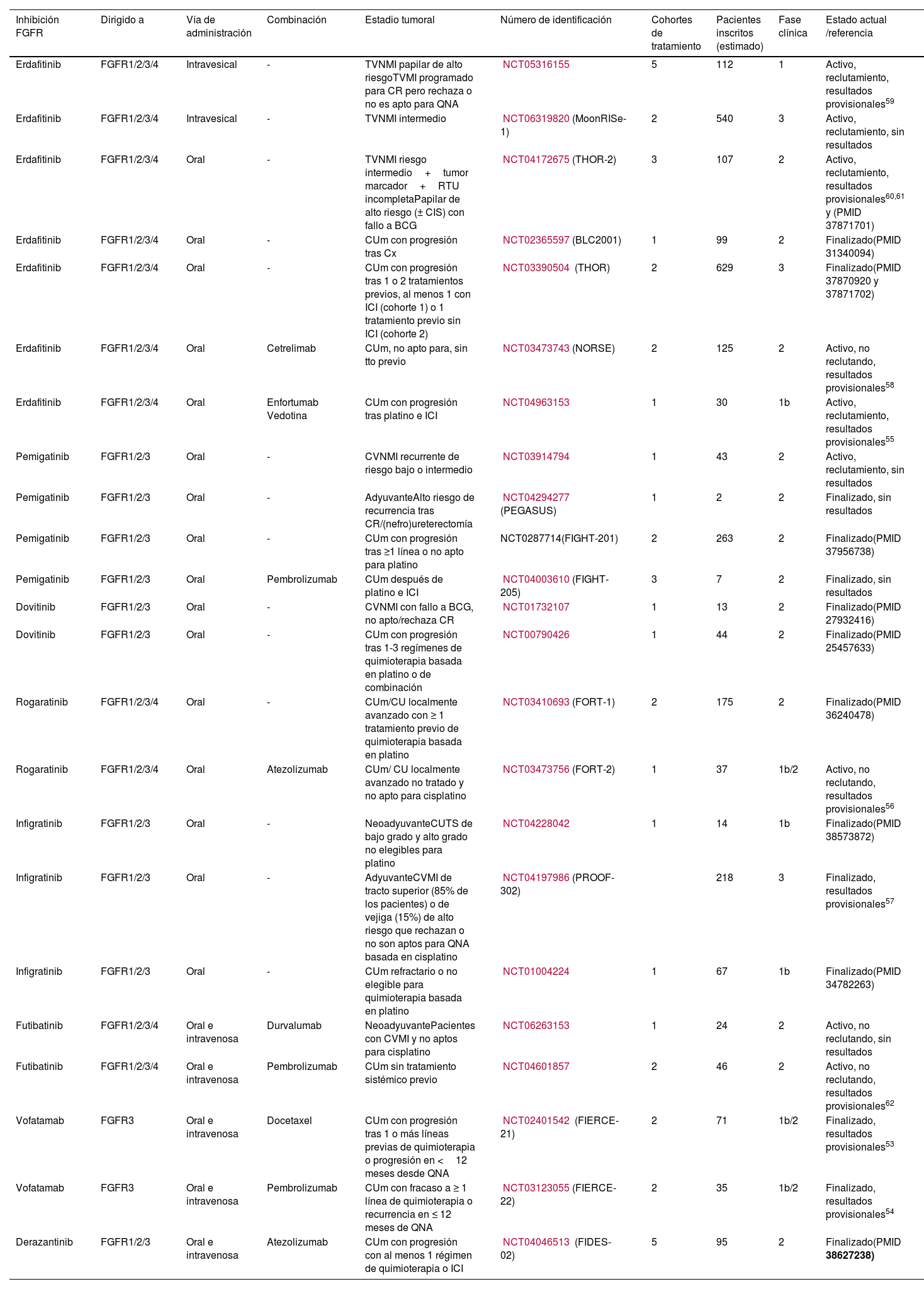
Según los datos correspondientes a la cohorte 2 del ensayo THOR, erdafitinib no debe recomendarse en pacientes aptos para recibir tratamiento con inhibidores de puntos de control inmunitario (ICI) y que no lo hayan recibido previamente. Actualmente, un ensayo de fase 3 está evaluando el sistema de administración intravesical (TAR210) en el cáncer de vejiga no músculo-invasor de riesgo intermedio con alteraciones del FGFR (MoonRISe-1). Los estudios preclínicos indican que podrían considerarse estrategias basadas en terapias combinadas para mejorar la eficacia de los inhibidores del FGFR en pacientes con CU. Nueve ensayos de fase 1b/2 están enfocados a evaluar el papel de los inhibidores del FGFR en combinación con ICI, quimioterapia o enfortumab vedotina. En el contexto de la enfermedad metastásica, estudios preliminares han revelado resultados prometedores de estas combinaciones (por ejemplo, los estudios NORSE y FORT-2). Sin embargo, ningún estudio de fase 3ha finalizado, por lo que actualmente no existen datos de nivel 1 con resultados a largo plazo que respalden la combinación de inhibidores del FGFR con ICI, quimioterapia o terapias dirigidas. Aún se requiere un mejor entendimiento de los diferentes mecanismos de acción de los inhibidores de las vías de señalización del FGFR, la selección óptima de pacientes y los enfoques terapéuticos.
FGFR3 mutations are among the most frequent genomic alterations in urothelial cancer (UC) being mainly associated with the luminal papillary (LumP) subtype. With the establishment of fibroblast growth factor receptor (FGFR) inhibitors, the treatment of UC is now shifting more and more towards personalized medicine. A systematic review using Medline and scientific meeting records was carried out according to the Preferred Reporting Items for Systematic Review and Meta-analyses guidelines to assess the potential role of FGFR inhibitors in combination with additional therapies for the management of UC. Ongoing trials were identified via a systematic search on ClinicalTrials.gov. A total of 11full-text papers, 10congress abstracts, and 5 trials on ClinicalTrials.gov were identified. Following the BLC2001 and THOR study, erdafitinib is the only approved FGFR1-4 inhibitor for metastatic UC with susceptible FGFR2/3 alterations following platinum-based chemotherapy. According to the THOR data of cohort 2, erdafitinib should not be recommended in patients who are eligible for and have not received prior immune checkpoint inhibitors (ICIs). One phase 3 trial is currently evaluating the intravesical device system (TAR210) in FGFR-altered intermediate non-muscle invasive bladder cancer (MoonRISe-1). Preclinical evidence suggests that combination-based approaches could be considered to improve the efficacy of FGFR inhibitors in patients with UC. Nine phase 1b/2 trials are focusing on the combination of FGFR inhibitors with ICIs, chemotherapy, or enfortumab vedotin. In metastatic disease, some preliminary analyses have reported promising results from these combinations (e.g. NORSE and FORT-2 trial). However, no phase 3 trial is terminated, so there is currently no level 1 evidence with long-term outcomes to support the combination of FGFR inhibitors with ICIs, chemotherapy, or targeted therapies. A better understanding of the different mechanisms of action to inhibit FGFR signaling pathways, optimal patient selection and treatment approaches is still needed.