La mortalidad por rotura de aneurismas aórticos abdominales (AAAr) sigue siendo elevada, a pesar de las mejoras en la anestesia, los cuidados intensivos postoperatorios y las técnicas quirúrgicas. Series pequeñas recientes y la experiencia de determinados centros sugieren que la reparación endovascular de los aneurismas (REVA) en caso de AAAr es factible y puede mejorar la supervivencia a corto plazo. Sin embargo, se desconoce si la REVA es aplicable en todos los casos de AAAr. El objetivo de este estudio fue investigar la idoneidad anatómica de la rotura de aneurisma para la REVA a través de tomografías axiales computarizadas. Se revisó de forma retrospectiva una serie consecutiva de AAAr presentadas en un centro terciario universitario. Se revisaron las imágenes radiográficas preoperatorias y se evaluó la idoneidad para la REVA sobre la base de los dispositivos disponibles actualmente. Los pacientes cuya morfología aneurismática presentó un diámetro de cuello>32mm, una longitud<10mm, un ángulo>60°, tortuosidad ilíaca grave, o diámetro de la arteria ilíaca externa<6mm fueron considerados no candidatos para REVA. A lo largo de un período de 10 años se trataron 47 AAAr, de los cuales el 47% de los pacientes ingresaron directamente en nuestro centro, mientras que el 60% fueron transferidos desde otros hospitales. Cinco pacientes (11%) fueron sometidos a REVA, todos ellos durante los 2 últimos años, mientras que los 42 restantes fueron tratados mediante corrección abierta. Se dispuso de imágenes preoperatorias para su revisión en 43 pacientes (91%), y las mediciones morfológicas indicaron que un 49% hubieran sido candidatos a la REVA con los dispositivos existentes en la actualidad. Los criterios que imposibilitaron una REVA en esta cohorte fueron longitud del cuello inadecuada en el 73%, abordaje ilíaco no adecuado en el 23%, gran diámetro del cuello en el 18%, y angulación severa del cuello en el 14%. La mortalidad global a los 30 días fue del 34%, y la mortalidad al año fue del 42%. Los candidatos a REVA eran hombres con mayor frecuencia que los no candidatos (95 frente a 68%, p=0,046), y presentaban diámetros del saco menores (7,0 frente a 8,5cm, p=0,02) y longitudes del cuello mayores (24,1 frente a 8,6mm, p<0,0001); tenían cuellos con angulaciones>60° (10 frente a 45%, p=0,0002), mayor diámetro de la arteria ilíaca externa (8,9 frente a 7,3mm, p=0,015), y presentaron pérdidas de sangre menores durante la corrección quirúrgica (2,4 frente a 6,0 l, p=0,02). Además, recibieron el alta domiciliaria con mayor frecuencia (71 frente a 25%, p=0,05). No se observaron diferencias en la mortalidad a los 30 días, 1 año, o global, entre los candidatos a REVA y los no candidatos. Solamente el 49% de los pacientes con AAAr de esta serie fueron considerados candidatos a la REVA con endoprótesis convencionales. Las diferencias en la demografía, morfología del aneurisma, y resultados entre candidatos y no candidatos sometidos a cirugía abierta sugieren la existencia de riesgos diferenciales en los pacientes con rotura de aneurisma. Los protocolos y los informes futuros sobre REVA en casos de AAAr deben ajustarse a estos resultados. Son necesarias modificaciones en los dispositivos y la técnica de implante para aumentar la aplicabilidad de la REVA en los AAAr.
A pesar de las mejoras en el manejo anestésico, las técnicas quirúrgicas y los cuidados postoperatorios, la mortalidad de los pacientes con rotura de aneurismas aórticos abdominales (AAAr) sigue siendo elevada y no ha mejorado de forma significativa en las tres últimas décadas1,2. La corrección quirúrgica abierta ha sido desde hace tiempo la estrategia tradicional para tratar a los pacientes con AAAr, arrojando unas tasas de mortalidad de aproximadamente el 50% tras la intervención quirúrgica3. Recientemente, la reparación endovascular de los aneurismas (REVA) ha surgido como alternativa mínimamente invasiva para el tratamiento electivo de los aneurismas asintomáticos4,5. La amplia adopción de la REVA por parte de muchos centros, así como la mejora de las técnicas y dispositivos endovasculares y su disponibilidad, han provocado un entusiasmo considerable por el abordaje endovascular de las AAAr.
Diferentes ensayos han evaluado la REVA frente a la corrección quirúrgica convencional abierta como tratamiento de AAAr, siendo la mayoría de ellos series retrospectivas, de tamaño reducido, y no aleatorizados6. En estos estudios, la REVA para la rotura de aneurismas (REVAr) ha demostrado ser factible y reducir las complicaciones perioperatorias y la mortalidad a corto plazo en comparación con la corrección quirúrgica abierta en pacientes seleccionados7-10. Solamente existe un estudio comparativo y aleatorizado que compara ambas técnicas en AAAr, que en realidad no mostró diferencias significativas en los resultados11. La mejora de los resultados observada en los estudios de menor tamaño y no aleatorizados se ha demostrado en pacientes seleccionados y generalmente es comparable a la de los controles históricos del mismo centro tratados de forma abierta. Las estrategias para la adopción generalizada de la REVA para tratar AAAr siguen redefiniéndose y dependerán de factores como la idoneidad morfológica, la comodidad del cirujano y la disponibilidad de los dispositivos.
El objetivo de este estudio fue investigar la idoneidad anatómica de la rotura de aneurismas para su reparación endovascular en una serie consecutiva de pacientes tratados principalmente con corrección abierta. Esperamos determinar si existieron diferencias demográficas, morfológicas, o de resultados en pacientes que hubiesen sido candidatos a la reparación endovascular.
Materiales y MétodosSe obtuvo la autorización del comité de evaluación del centro para revisar las historias clínicas de los pacientes. Realizamos una revisión retrospectiva de los historiales de todos los pacientes consecutivos sometidos a corrección de una AAAr en un centro terciario universitario desde julio de 1997 hasta noviembre de 2007. Se revisaron de forma retrospectiva las imágenes de las tomografías axiales computarizadas preoperatorias, cuando se dispuso de ellas, de forma ciega frente al tratamiento del paciente, el curso y el resultado, para poder evaluar la idoneidad anatómica del aneurisma del paciente para la REVA. Los criterios de idoneidad se basaron en los dispositivos comercializados actualmente y utilizados de forma habitual en nuestro centro desde enero de 2008. Un diámetro del cuello>32mm, longitud<10mm, angulación>60°, tortuosidad ilíaca severa o diámetro de la arteria ilíaca externa<6mm fueron consideradas razones por las que un paciente no podía ser candidato a una REVA. Se utilizaron los estándares de notificación habituales. Las características de la REVA se notificaron según las normas habituales establecidas por la Society for Vascular Surgery12. Otros datos demográficos, morfológicos, y de resultado obtenidos para la cohorte fueron edad, sexo, presencia de rotura libre, tipo de intervención, duración de la hospitalización, pérdida de sangre estimada, complicaciones postoperatorias, mortalidad a los 30 días y a 1 año, seguimiento a largo plazo, y traslado tras el alta (domicilio o centro de atención especializada).
Se calculó la estadística descriptiva para cada variable. Los datos continuos se presentan como media ± desviación estándar y los datos categóricos se presentan como porcentaje. Las técnicas estadísticas bivariantes, incluidos los test de suma de rangos de Wilcoxon y el test exacto de Fisher, se utilizaron cuando fue adecuado. Se utilizaron tests t de grupo independientes para comprobar las diferencias medias en los resultados entre los candidatos y los no candidatos a la REVAr. La significancia estadística se estableció en p≤0,05. Se realizó un análisis de Kaplan-Meier para determinar la supervivencia global tras la intervención quirúrgica. Los análisis estadísticos se realizaron utilizando el programa MedCalc versión 9.2.1.0 (MedCalc Software, Mariakerke, Bélgica).
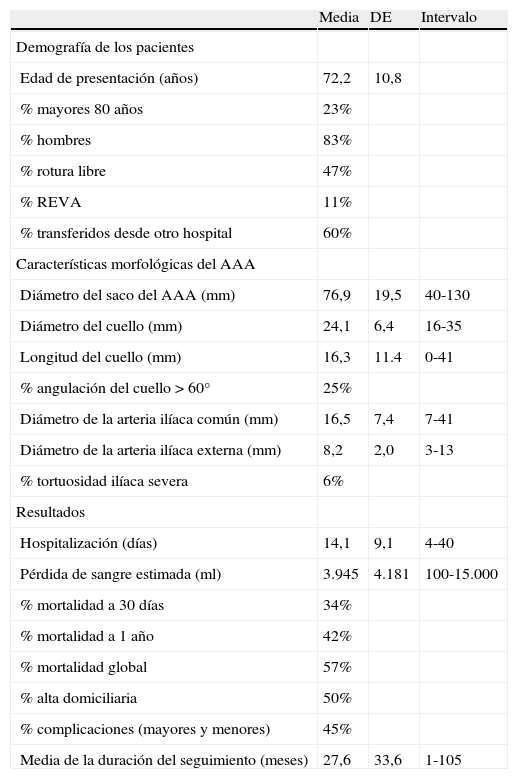
ResultadosCuarenta y siete pacientes (83% hombres) con AAAr fueron sometidos a corrección a lo largo de un período de 10 años. Las características demográficas de los pacientes y los rasgos morfológicos de sus AAA se enumeran en la tabla I. En esta cohorte de pacientes, el 47% presentó una rotura libre y el 60% fue transferido desde otro hospital. La principal cohorte del estudio estuvo formada por 43 pacientes de los que se dispusieron las imágenes de tomografías axiales computarizadas anteriores a la intervención para esta revisión retrospectiva. No se dispuso de imágenes para revisar en 4 pacientes o no fueron sometidos a estudios de tomografía axial computarizada anteriores a la intervención, y en todos ellos se realizó una corrección abierta. Cinco pacientes (11%) de los que se habían obtenido imágenes preoperatorias fueron tratados mediante REVA, todos ellos en los últimos 2 años, mientras que el resto fue sometido a corrección abierta a través de un abordaje transperitoneal. A lo largo del período de estudio de 10 años, el número anual de pacientes con AAAr no varió de forma significativa (3 a 6 por año).
Características demográficas y morfológicas de 47 AAAr consecutivas
| Media | DE | Intervalo | |
| Demografía de los pacientes | |||
| Edad de presentación (años) | 72,2 | 10,8 | |
| % mayores 80 años | 23% | ||
| % hombres | 83% | ||
| % rotura libre | 47% | ||
| % REVA | 11% | ||
| % transferidos desde otro hospital | 60% | ||
| Características morfológicas del AAA | |||
| Diámetro del saco del AAA (mm) | 76,9 | 19,5 | 40-130 |
| Diámetro del cuello (mm) | 24,1 | 6,4 | 16-35 |
| Longitud del cuello (mm) | 16,3 | 11.4 | 0-41 |
| % angulación del cuello>60° | 25% | ||
| Diámetro de la arteria ilíaca común (mm) | 16,5 | 7,4 | 7-41 |
| Diámetro de la arteria ilíaca externa (mm) | 8,2 | 2,0 | 3-13 |
| % tortuosidad ilíaca severa | 6% | ||
| Resultados | |||
| Hospitalización (días) | 14,1 | 9,1 | 4-40 |
| Pérdida de sangre estimada (ml) | 3.945 | 4.181 | 100-15.000 |
| % mortalidad a 30 días | 34% | ||
| % mortalidad a 1 año | 42% | ||
| % mortalidad global | 57% | ||
| % alta domiciliaria | 50% | ||
| % complicaciones (mayores y menores) | 45% | ||
| Media de la duración del seguimiento (meses) | 27,6 | 33,6 | 1-105 |
AAA: aneurismas aórticos abdominales; DE: desviación estándar; REVA: reparación endovascular de los aneurismas.
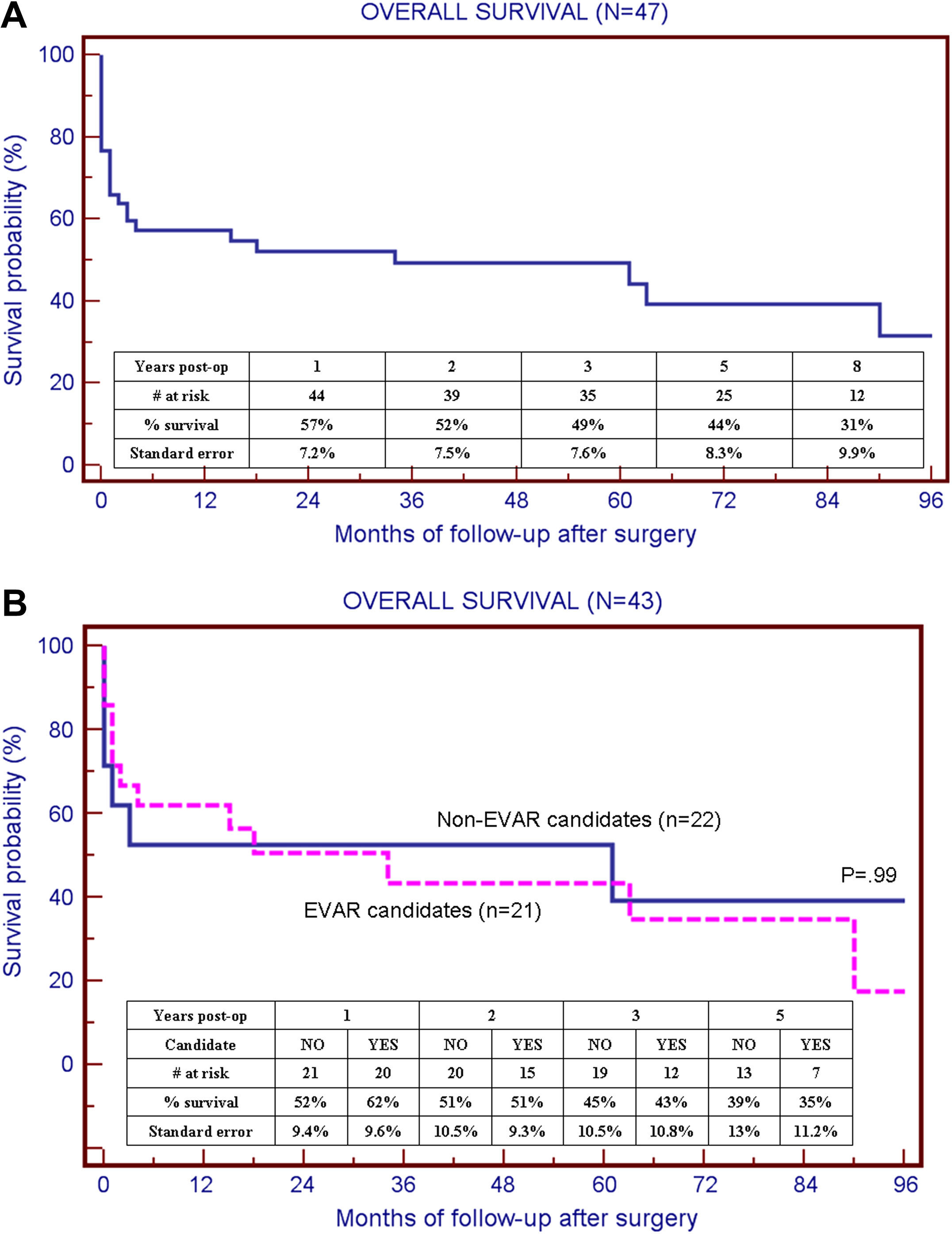
La mortalidad global a los 30 días de toda la cohorte fue del 34%, al del 42%. Con un seguimiento medio de 27,6±33,6 meses (intervalo 1-105), el 43% seguían estando vivos. De los 29 pacientes que sobrevivieron a la intervención quirúrgica por AAAr y recibieron el alta hospitalaria, el seguimiento medio fue de 42,2 meses. Las curvas de supervivencia de Kaplan-Meier para la tasa de mortalidad global se muestran en la figura 1. La media del tiempo de supervivencia de toda la cohorte fue de 34 meses. Las complicaciones perioperatorias de aquellos que sobrevivieron 30 días incluyeron el compromiso renal (21%), la insuficiencia renal (14%), la insuficiencia pulmonar (14%), la isquemia de las extremidades inferiores (14%), el infarto de miocardio (10%), y la isquemia intestinal (10%).
A Curva de supervivencia Kaplan-Meier que muestra la ausencia de mortalidad por cualquier causa y la supervivencia global tras la AAAr de toda la cohorte de pacientes (n=47). Los errores estándar de la media se muestran en la tabla hasta un seguimiento de 8 años. B Curvas de supervivencia de Kaplan-Meier comparando los candidatos a la REVA y los no candidatos que dispusieron de tomografías axiales computarizadas preoperatorias (n=43). No existen diferencias estadísticamente significativas en la supervivencia global entre los candidatos y los no candidatos (p=0,99).
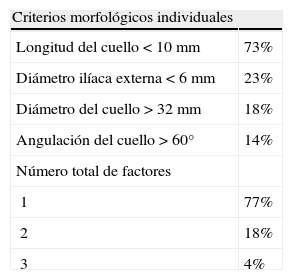
De los 43 pacientes que tenían imágenes preoperatorias, y que por tanto fueron clasificados como candidatos a la REVA, el 49% pudo haber sido tratado con los dispositivos disponibles actualmente. La otra mitad no hubiesen sido candidatos a la REVA; en la tabla II aparecen reflejadas las razones de esta clasificación. El criterio de exclusión como candidatos a REVA más habitual fue longitud corta del cuello, < 10mm (73%). Otras razones de la no idoneidad para la REVA fueron un abordaje de la arteria ilíaca externa pequeño (23%), diámetro del cuello amplio, > 32mm (18%) y angulación severa>60° (14%).
Razones de la no idoneidad de la REVA en 22 pacientes no considerados candidatos para la reparación endovascular de la AAAr
| Criterios morfológicos individuales | |
| Longitud del cuello<10mm | 73% |
| Diámetro ilíaca externa<6mm | 23% |
| Diámetro del cuello>32mm | 18% |
| Angulación del cuello>60° | 14% |
| Número total de factores | |
| 1 | 77% |
| 2 | 18% |
| 3 | 4% |
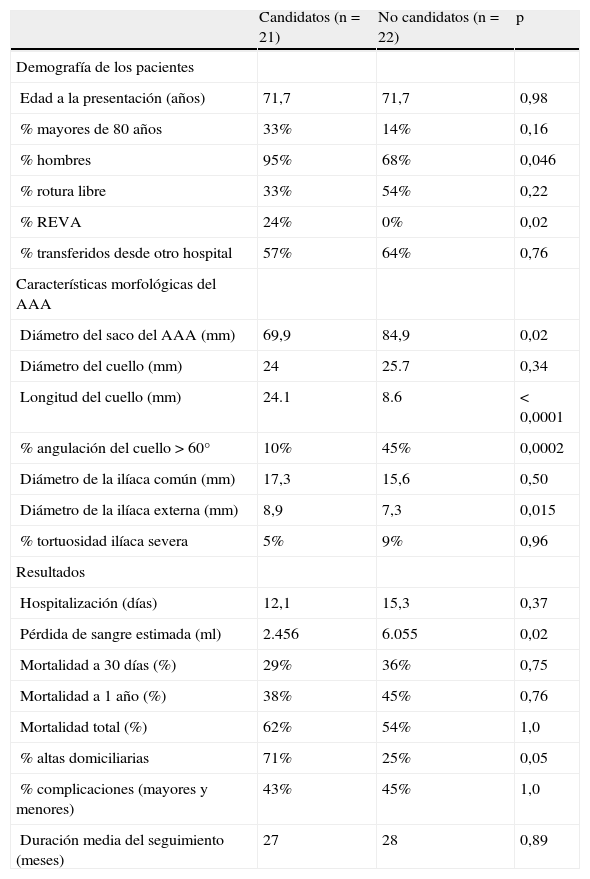
Se observaron varias diferencias importantes entre los grupos de candidatos y no candidatos a la REVA que se muestran en la tabla III. Desde el punto de vista demográfico, la edad, el porcentaje de pacientes que presentaron una rotura libre y el de transferidos desde otro centro no tuvieron ninguna importancia en la idoneidad para REVA. Los candidatos fueron hombres con mayor frecuencia (95% frente al 68%, p=0,046). Obviamente, entre los candidatos se incluyeron los 5 pacientes que fueron sometidos a una REVA en los 2 últimos años, lo que resultó estadísticamente significativo.
Comparación de la demografía, morfología del aneurisma, y resultados de toda la cohorte de 43 pacientes tratados que dispusieron de imágenes de tomografía axial computarizada preoperatorias para su revisión
| Candidatos (n=21) | No candidatos (n=22) | p | |
| Demografía de los pacientes | |||
| Edad a la presentación (años) | 71,7 | 71,7 | 0,98 |
| % mayores de 80 años | 33% | 14% | 0,16 |
| % hombres | 95% | 68% | 0,046 |
| % rotura libre | 33% | 54% | 0,22 |
| % REVA | 24% | 0% | 0,02 |
| % transferidos desde otro hospital | 57% | 64% | 0,76 |
| Características morfológicas del AAA | |||
| Diámetro del saco del AAA (mm) | 69,9 | 84,9 | 0,02 |
| Diámetro del cuello (mm) | 24 | 25.7 | 0,34 |
| Longitud del cuello (mm) | 24.1 | 8.6 | < 0,0001 |
| % angulación del cuello>60° | 10% | 45% | 0,0002 |
| Diámetro de la ilíaca común (mm) | 17,3 | 15,6 | 0,50 |
| Diámetro de la ilíaca externa (mm) | 8,9 | 7,3 | 0,015 |
| % tortuosidad ilíaca severa | 5% | 9% | 0,96 |
| Resultados | |||
| Hospitalización (días) | 12,1 | 15,3 | 0,37 |
| Pérdida de sangre estimada (ml) | 2.456 | 6.055 | 0,02 |
| Mortalidad a 30 días (%) | 29% | 36% | 0,75 |
| Mortalidad a 1 año (%) | 38% | 45% | 0,76 |
| Mortalidad total (%) | 62% | 54% | 1,0 |
| % altas domiciliarias | 71% | 25% | 0,05 |
| % complicaciones (mayores y menores) | 43% | 45% | 1,0 |
| Duración media del seguimiento (meses) | 27 | 28 | 0,89 |
AAA: aneurismas aórticos abdominales; REVA: reparación endovascular de los aneurismas.
Los candidatos son aquellos pacientes con anatomía adecuada para REVA.
Desde el punto de vista morfológico, los candidatos, en comparación con los no candidatos, presentaron diámetros del saco AAA significativamente menores (7,0 frente a 8,5cm, p=0,02), longitudes mayores del cuello (24,1 frente a 8,6mm, p<0,0001), menos angulación y mayor diámetro de la arteria ilíaca externa (8,9 frente a 7,3mm, p=0,015). Las medias del diámetro del cuello, del diámetro de la arteria ilíaca común, y de la tortuosidad ilíaca no fueron diferentes entre grupos.
Los resultados peri y postoperatorios difirieron entre los grupos de candidatos y no candidatos (tabla III). Si bien existió una tendencia a una ligera disminución de la mortalidad a los 30 días y al año en el grupo de candidatos, esta diferencia no fue estadísticamente significativa. La figura 1B muestra el análisis de Kaplan-Meier para la supervivencia global de ambos grupos, sin diferencias en los resultados a largo plazo entre los grupos (p=0,99). Sin embargo, la pérdida de sangre estimada se redujo (2,4 frente a 6,0 l, p=0,02), y el porcentaje de pacientes dados de alta domiciliaria (71 frente a 25%, p=0,05) fue significativamente mayor entre los pacientes considerados candidatos. Tras reanalizar los datos excluyendo a los 5 pacientes que habían sido sometidos a REVA y disponiendo de una cohorte de 38 pacientes con imágenes preoperatorias que fueron sometidos a corrección abierta, la mayoría de las diferencias mencionadas anteriormente siguen siendo ciertas (tabla IV). Con la exclusión de los pacientes sometidos a REVA, la pérdida de sangre estimada fue estadísticamente similar entre los candidatos y los no candidatos, pero el porcentaje de pacientes dados de alta domiciliaria permaneció significativamente elevado en el grupo de candidatos. Las complicaciones postoperatorias mayores y menores fueron similares en los dos grupos, incluidos los porcentajes de episodios cardíacos postoperatorios, infección, insuficiencia renal, y fracaso renal.
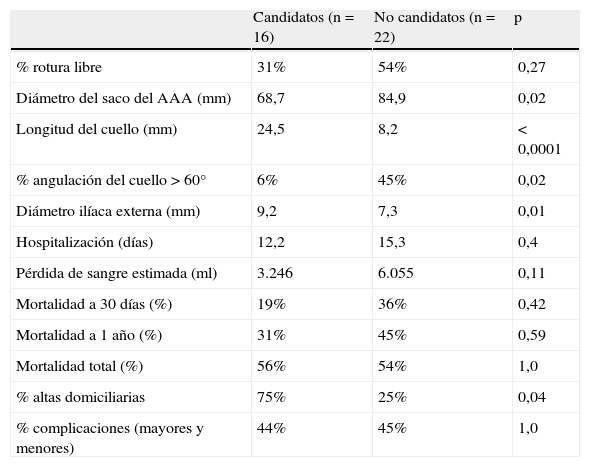
Comparación de la demografía, morfología del aneurisma, y resultados de toda la cohorte de 38 pacientes tratados con corrección abierta de AAAr que dispusieron de imágenes de tomografía axial computarizada preoperatorias para su revisión
| Candidatos (n=16) | No candidatos (n=22) | p | |
| % rotura libre | 31% | 54% | 0,27 |
| Diámetro del saco del AAA (mm) | 68,7 | 84,9 | 0,02 |
| Longitud del cuello (mm) | 24,5 | 8,2 | < 0,0001 |
| % angulación del cuello>60° | 6% | 45% | 0,02 |
| Diámetro ilíaca externa (mm) | 9,2 | 7,3 | 0,01 |
| Hospitalización (días) | 12,2 | 15,3 | 0,4 |
| Pérdida de sangre estimada (ml) | 3.246 | 6.055 | 0,11 |
| Mortalidad a 30 días (%) | 19% | 36% | 0,42 |
| Mortalidad a 1 año (%) | 31% | 45% | 0,59 |
| Mortalidad total (%) | 56% | 54% | 1,0 |
| % altas domiciliarias | 75% | 25% | 0,04 |
| % complicaciones (mayores y menores) | 44% | 45% | 1,0 |
AAA: aneurismas aórticos abdominales.
Los candidatos son aquellos pacientes cuya anatomía hubiese sido adecuada para REVA.
Esta tabla excluye los 5 pacientes que fueron sometidos a REVA para tratar la AAAr.
En este estudio de un único centro destacamos que la idoneidad anatómica de la REVA para AAAr es del 49%. Esto sugiere que aproximadamente la mitad de los pacientes que se presentan con AAAr no son buenos candidatos para la REVA con los dispositivos autorizados en la actualidad y destaca la necesidad de refinar los protocolos, dispositivos y técnicas para optimizar el cuidado de estos pacientes. Estos resultados confirman los hallazgos de varios estudios retrospectivos llevados a cabo en Europa13,14.
También se demostraron varias diferencias en términos de demografía, morfología de los AAA, y resultados peri y postoperatorios al separar a los pacientes con AAAr en grupos, sobre la base de si serían candidatos a la REVA. Esto sugiere que los pacientes con AAAr que son candidatos endovasculares son casos de cirugía abierta potencialmente menos desafiantes que los que no son candidatos a la REVA. Las posibles explicaciones de estos hallazgos tienen relación con los pacientes con AAA de menor diámetro, cuellos más largos, y anatomía ilíaca mayor. La presencia de estos factores morfológicos particulares facilitaría intuitivamente la corrección abierta.
Dados estos factores morfológicos particulares en el grupo de candidatos, es probable que la pérdida de sangre sea ligeramente menor y existiría una menor necesidad de control suprarrenal o supracelíaco. Incluso tras excluir aquellos que fueron sometidos a REVA en nuestra serie, el porcentaje de pacientes dados de alta tras la corrección abierta permaneció significativamente elevado en el grupo de candidatos. Este hallazgo relacionado con el curso postoperatorio corrobora aún más la hipótesis de que los candidatos a la REVA, incluso si son sometidos a corrección abierta, pueden tener un curso más benigno. Esto deberá ser considerado en futuros estudios que comparen el tratamiento endovascular de AAAr con los controles históricos puesto que la comparación con los casos que hubiesen sido candidatos a la REVA puede ser más exacta. Existen muchos trabajos en la literatura que sugieren que, incluso en los casos de REVA programada, los aneurismas de menor tamaño tienen mejores resultados en cuanto a las tasas de ausencia de rotura, intervención secundaria, y retracción del saco6,13,14.
La mortalidad por AAAr sigue siendo extraordinariamente alta, con tasas descritas de aproximadamente el 80-90% en los aneurismas no tratados, y es necesario adoptar estrategias para el futuro que permitan mejorar este proceso mórbido15. Tradicionalmente, la corrección quirúrgica abierta ha sido la única opción para el tratamiento eficaz de AAAr. Sin embargo, la corrección abierta provoca una mortalidad sustancialmente elevada, que oscila entre el 40 y el 70%, y morbilidad, principalmente por hemorragia, lesiones debidas a la intervención, y clampaje aórtico que provoca lesiones isquémicas16. La elevada mortalidad asociada a la corrección abierta de AAAr, junto con el entusiasmo por la REVA, llevaron evidentemente a la ‘‘endoexhuberancia'’ del tratamiento de AAAr.
Además, existen menos efectos adversos fisiológicos con la REVA, en particular en los sistemas cardíaco, respiratorio, y renal, así como una reducción de la respuesta inflamatoria17-20. Así pues, gracias a la mejoría progresiva de los resultados utilizando esta técnica, junto con las mejoras tecnológicas de los dispositivos endovasculares, el uso de la REVA para el tratamiento de AAAr se ha extendido de forma considerable. Se ha teorizado que la disminución del estrés hemodinámico y metabólico observada con la REVA programada se traducirá en mejoras de los resultados en los pacientes con AAAr sometidos a diho procedimiento21.
La viabilidad de la REVA para AAAr se ha establecido en varios estudios7-10. En un metaanálisis realizado por Harkin et al6 de 33 estudios no aleatorizados, los autores acordaron que es posible realizar la REVA para AAAr en pacientes seleccionados, con una tendencia hacia la reducción de la pérdida de sangre, duración del ingreso en cuidados intensivos, complicaciones iniciales y mortalidad. La limitación de la mayoría de los estudios actuales existentes en la literatura es que comparan la tasa de mortalidad de la REVA para AAAr con la de los controles históricos sometidos a corrección abierta. Solamente existe un estudio comparativo aleatorizado sobre la REVA frente a la corrección abierta para el tratamiento de AAAr11. En este estudio, los autores observaron que no existieron diferencias significativas en cuanto a las tasas de mortalidad o de complicaciones postoperatorias en los grupos abierto y endovascular, lo que difiere de su propia serie seleccionada inicialmente y de la experiencia previa de otros autores con la reparación endovascular.
Los resultados favorables en la literatura de la REVAr pueden ser debidos, por tanto, al hecho de que las comparaciones de las tasas de mortalidad y complicaciones se realicen a partir de un grupo muy seleccionado frente a los controles históricos de todas los AAAr del mismo centro, muchas de las cuales no hubiesen sido candidatas a la REVA y probablemente hubiesen obtenido peores resultados. Estas comparaciones pueden no ser tan válidas, y serán necesarios más datos e informes de centros con un mayor volumen para determinar si, realemente, la REVA será el nuevo estándar de tratamiento de AAAr.
Las razones por las que algunos pacientes no son candidatos a la REVA pueden ser las mismas por las que presentan un aumento significativo del riesgo de corrección quirúrgica abierta. Esto se manifiesta en los hallazgos previos de una morfología aneurismática más desafiante en los aneurismas rotos así como en el hecho de que la REVA no supuso ninguna ventaja en la corrección programada para los pacientes de alto riesgo22. Esta teoría también se ve apoyada por los resultados de un estudio realizado por Lee et al23, en el que los autores compararon la morfología de los AAA de los pacientes con rotura o síntomáticos con la de aquellos sometidos a corrección programada. Este estudio mostró que la idoneidad anatómica de la REVA para los pacientes con rotura/síntomas de AAA fue significativamente menor que la de aquellos AAA asintomáticos debido a la anatomía desfavorable del cuello proximal. Esta hipótesis se ve corroborada por nuestros resultados actuales.
Se han estudiado otros factores además de la anatomía para evaluar la aplicabilidad de la REVA a AAAr. En un metaanálisis reciente se observó que el efecto beneficioso de la REVA en la mortalidad en comparación con la cirugía abierta estuvo directamente relacionado con el estado hemodinámico del paciente en el momento de su presentación24. Esto parece indicar que el sesgo de la selección de los pacientes sometidos a REVA, de forma típica solamente cuando son hemodinámicamente estables, favorecería los resultados tras una REVA en comparación con la corrección abierta en el mismo centro. Las razones logísticas, como la disponibilidad del equipamiento y el personal endovascular, a menudo se citan como las razones por las que se realiza una cirugía abierta en pacientes hemodinámicamente inestables. El desarrollo de protocolos de emergencia para la rápida evaluación y triaje de los pacientes con AAAr puede aumentar el uso de la REVA y en última instancia mejorar los resultados de los pacientes. Esto se ha descrito en varias series que han implementado un enfoque multidisciplinar para AAAr, incluyendo a cirujanos vasculares, médicos de urgencias, anestesistas, radiólogos, personal de quirófano, y técnicos25,26. Una vez se estableció este protocolo estandarizado, se logró una mejoría significativa en la mortalidad.
Existen varias limitaciones al estudio actual. Éste fue un estudio retrospectivo que se basó en la exactitud del registro y la obtención de los datos. Además, la idoneidad de los pacientes para la REVAr en esta cohorte se basó en los criterios actuales (2008) de idoneidad para las técnicas endovasculares. Ciertamente, a lo largo de los años hemos mejorado nuestras técnicas endovasculares, de forma que en muchas ocasiones somos capaces de tratar a pacientes sin una anatomía ideal debido a la experiencia acumulada con la REVA programada. Así pues, el conocimiento adquirido, así como las mejoras en los dispositivos, se aplicaron de forma retrospectiva a pacientes con AAAr que se presentaron en un período de 10 años. Es posible que la idoneidad de la REVA para esta experiencia de AAAr, de una década de duración, esté ligeramente sobreestimada debido a los avances en la experiencia de los cirujanos y la mejora de los dispositivos.
ConclusionesA pesar de que existe un entusiasmo significativo por el uso de la REVA en caso de rotura de aneurisma, alentado en parte por los resultados favorables obtenidos a partir de estudios iniciales de tamaño reducido, hay que tener precaución antes de adoptar ampliamente esta técnica. En este estudio, solamente la mitad de los pacientes fueron candidatos adecuados para la REVA con los dispositivos estándar existentes en la actualidad. La modificación de los sistemas de implantes recubiertos que permitan su aplicación en aneurismas con cuellos cortos y abordajes ilíacos difíciles debe mejorar la aplicabilidad de la REVA en los casos futuros de AAAr. Las diferencias en la demografía, morfología aneurismática, y resultados, entre candidatos y no candidatos sometidos a corrección abierta, sugieren la existencia de riesgos diferentes entre los pacientes con rotura de aneurisma. Los protocolos y los informes futuros de la REVA en casos de AAAr deben ajustarse a estos resultados.