Las enfermedades alérgicas suponen, en su conjunto, uno de los principales problemas de salud a los que se enfrentan los sistemas sanitarios. En la Unión Europea, la prevalencia acumulada alcanza a un tercio de la población infantil, y se considera una de las principales epidemias frente a la que urgen medidas eficaces de prevención, diagnóstico y tratamiento.
Puntos clave
A pesar de tener una base patogénica común, estas enfermedades, originadas por un mecanismo de hipersensibilidad tipo I frente a distintos alérgenos, tiene una expresión clínica muy diversa, que va desde la sensibilización asintomática hasta reacciones alérgicas mortales, pasando por un amplio espectro de síntomas respiratorios, digestivos y cutáneos, entre otros.
Ante esta realidad clínica y epidemiológica, desde una perspectiva comunitaria y de eficiencia en la utilización de recursos sanitarios, la atención primaria (AP) debe tener a su alcance herramientas para realizar un diagnóstico alérgico inicial adecuado e instaurar de manera individualizada las medidas preventivas y terapéuticas oportunas.
Diagnóstico de la alergiaMúltiples estudios epidemiológicos, y muy especialmente el estudio internacional de asma y enfermedades alérgicas (ISAAC)1–3, han puesto de manifiesto las enormes variaciones en la prevalencia entre países y regiones, así como la correlación que hay entre las distintas manifestaciones clínicas de la atopia entre sí (asma, rinitis, dermatitis atópica), de forma que la presencia de una manifestación alérgica aumenta el riesgo de presentar otras. España se sitúa entre los países con prevalencia media, donde destacan las amplias diferencias regionales. En el caso del asma, y según los resultados obtenidos en la fase III del citado estudio, se ha observado que la prevalencia entre los adolescentes de 13–14 años se mantiene estable respecto a los datos obtenidos en 1996, pero se ha producido un aumento de la prevalencia entre los niños de 6–7 años4.
Los estudios de cohortes realizados en las últimas décadas han aumentado el conocimiento sobre la epidemiología de las enfermedades atópicas, en general, y del asma, en particular. Así, el concepto de marcha atópica5, describe un patrón cronológico, que clínicamente comienza con dermatitis atópica, que se mantiene o no en el tiempo, y que en edades posteriores se sustituye por asma y/o rinitis alérgica. Inmunológicamente, la marcha atópica se inicia en los primeros meses de vida con sensibilización a alimentos transitoria o persistente, que evoluciona a partir de los 2 años hacia sensibilización a alérgenos inhalantes6–8.
La elevada prevalencia de enfermedades atópicas, el conocimiento de la relación entre sensibilización alimentaria y clínica respiratoria posterior y el valor pronóstico que tiene la demostración de anticuerpos inmunoglobulina (Ig) E específicos frente a diferentes alérgenos (aún en ausencia de clínica) aconsejan, en niños con síntomas, una estrategia de búsqueda activa de sensibilización IgE mediada, dejando atrás definitivamente la actitud expectante del pasado, especialmente en el grupo de edad de los menores de 4–5 años.
La sección Pediátrica de la Academia Europea de Alergia e Inmunología Clínica publicó en 2003 un documento9,10 donde se establecen recomendaciones basadas en la mejor evidencia actualmente disponible, que puede servir de referencia a los pediatras, especialmente del primer nivel asistencial, sobre por qué, a quién, cuándo y cómo realizar estudios de alergia en niños. Aconsejan que todos los niños con posibles síntomas alérgicos, persistentes o recurrentes, así como los que necesiten tratamiento preventivo continuo, sean estudiados desde el punto de vista alergológico, independientemente de su edad.
La prueba diagnóstica ideal para utilizarse en AP debe ser muy sensible y específica, fácil de realizar e interpretar, poco invasiva para el paciente, segura y de bajo coste. Las pruebas in vivo (prick test) constituyen una exploración de primera línea, y sus fundamentos se han publicado recientemente en Anales de Pediatría Continuada11.
La determinación in vitro de IgE específica es el método de referencia, ya que permite cuantificar los valores de anticuerpos. Tanto el prick test como la cuantificación de IgE específica no siempre están disponibles en AP12 o tienen un coste elevado. En este sentido, resultan de interés los métodos diagnósticos que se describen a continuación, disponibles en los últimos años en España, especialmente diseñados para el entorno de la AP.
ImmunoCap™ Phadiatop® e ImmunoCap™ Phadiatop® InfantEl Phadiatop® (Phadia AB, Upssala, Sweden) es una técnica in vitro, cualitativa, de cribado inicial, que permite detectar la presencia en una muestra de sangre venosa de anticuerpos IgE frente a una mezcla de alérgenos13–15. Ante un resultado positivo, en un segundo paso y con la misma muestra de sangre, se cuantifican las IgE específicas alérgeno por alérgeno. Si el resultado inicial es negativo, no son necesarias más determinaciones, porque la probabilidad de alergia es muy baja. si los datos clínicos son discordantes con un resultado negativo, sería necesario cuantificar posteriormente las IgE específicas.
Ambas pruebas se diferencian por el contenido de alérgenos: Phadiatop® contiene una mezcla de los alérgenos inhalantes implicados más frecuentemente en la enfermedad alérgica en mayores de 5 años: ácaros, pólenes de árboles, arbustos, gramíneas y malezas, perro y gato. Phadiatop® Infant contiene además alérgenos alimentarios (leche de vaca, clara de huevo, cacahuete, soja, trigo, almendra y pescado/marisco) y está especialmente indicado en los menores de 5 años con dermatitis atópica, asma o rinitis persistente. Esta mezcla de alérgenos es la causa del 98% de sensibilizaciones alérgica en menores de 5 años.
Este método debe sustituir a la determinación de IgE total como prueba de cribado por su baja especificidad, ya que no resulta un marcador fiable de sensibilización, como ha demostrado el estudio APIA. Este trabajo multicéntrico, realizado en España en AP, es el más amplio de los realizados para evaluar la utilidad de Phadiatop® Infant.
En la tabla 1 se detallan los resultados respecto a las características de este método diagnóstico, obtenidos en los estudios más relevantes sobre este método.
Características y resultados de los principales estudios realizados para evaluar la utilidad de Phadiatop® Infant en la detección de la sensibilización IgE mediada en niños
| Fiocchi et al13 | Ballardini et al14 | Estudio APIA18 | |
|---|---|---|---|
| N.° de pacientes | 147 | 239 | 467 |
| Edad (años) | 0-4 | 2 | 0-5 |
| Sensibilidad, % | 92 (IC del 95%, 82–97) | 96 | 84,2 (IC del 95%, 78,1-88,8) |
| Especificidad, % | 82 (IC del 95%, 72–90) | 98 | 93,8 (IC del 95%, 90,4-96) |
| VPP, % | 89 (IC del 95%, 69–97) | 89 | 89,2 (IC del 95%, 83,6-93,1) |
| VPN, % | 99 (IC del 95%, 84–98) | 93 | 90,6 (IC del 95%, 86,8-93,4) |
IC: intervalo de confianza; VPN: valor predictivo negativo; VPP: valor predictivo positivo.
El Phadiatop® Infant resulta especialmente útil en niños menores de 5 años con dermatitis atópica, sibilancias recurrentes y asma, dado que aporta información sobre sensibilización a alimentos, con el valor predictivo y las implicaciones pronósticas de ésta. Por encima de esta edad, la prueba recomendada sería el Phadiatop®.
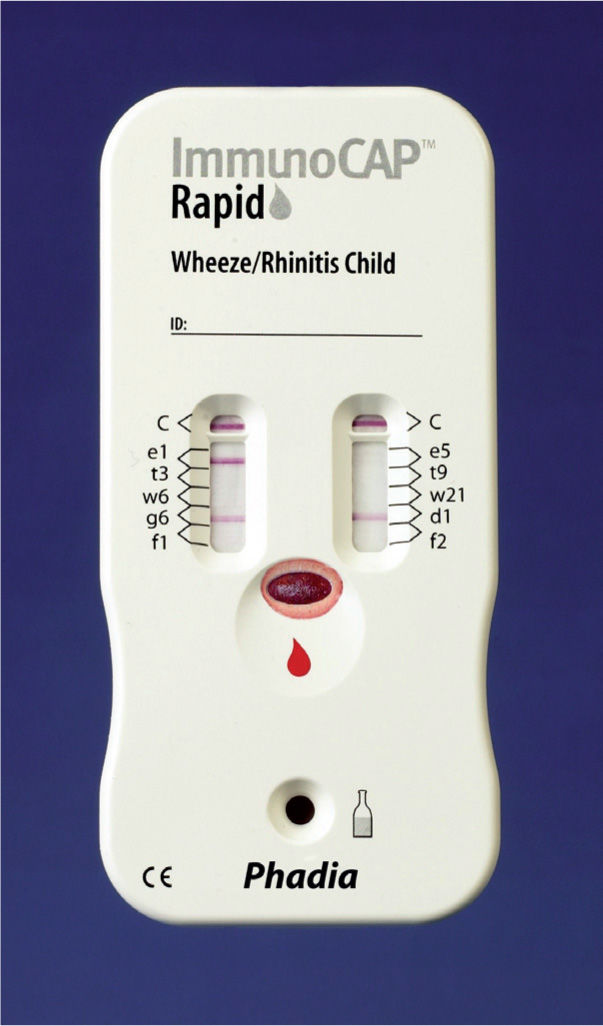
ImmunoCap™ RapidEs un nuevo método diagnóstico, basado en la tecnología Pharmacia CAP System (Phadia AB, Upssala, Suecia), disponible en España desde 2005, que permite detectar IgE específicas de forma individualizada a partir de una muestra de 110 pl de sangre capilar, y cuyos resultados se obtienen en 20min.
En la actualidad, está disponible el “perfil sibilancias-rinitis niños”, compuesto por alérgenos de gato, perro, abedul, olivo, artemisia, parietaria, hierba timotea, ácaros, huevo y leche.
El “perfil eccema”, disponible próximamente, incluye más alérgenos alimentarios: bacalao, avellana, gamba, soja, cacahuete, huevo y leche, además de ácaro, gato y perro. El dispositivo del ensayo consta de 2 orificios, uno para la muestra de sangre y el otro para la solución de desarrollo, y de 2 ventanas rectangulares, en cada una de las cuales se dispone una tira de membrana nitrocelulosa donde se encuentran, formando líneas paralelas, 5 alérgenos por tira. Cada ventana del test cuenta con una zona de control (fig. 1).
Dispositivo para realizar InmunoCap™ Rapid. Se observan 5 líneas coloreadas: de arriba abajo, corresponden a las 2 líneas de control (C) que aseguran la correcta realización de la prueba. En la ventana izquierda, las líneas de color más intenso corresponde al gato (e1), seguida de la hierba timotea (g6). En la ventana derecha, la línea coloreada corresponde al ácaro (d1).
Es una prueba de flujo lateral16, de tipo cualitativa (colorimétrica), que ofrece un resultado positivo o negativo para cada uno de los alérgenos incluidos de manera individualizada en cada dispositivo. Además, permite la evaluación semicuantitativa: a mayor intensidad de color, mayor cantidad de IgE específica.
La muestra de sangre se introduce en un pocillo al que se añade a los 5min solución de desarrollo. Si en este plasma está presente IgE específica frente a alguno de los alérgenos incluidos en el test, se produce una unión en la línea correspondiente. El resultado se considera negativo si no hay ningún viraje de color, y positivo si aparece una línea coloreada de rosa pálido a rojo intenso en el área correspondiente a los distintos alérgenos.
En el estudio IReNE, realizado en AP en España en 2006, se ha evaluado la utilidad del ImmunoCap™ Rapid (ICR) para identificar la alergia en niños de 1–14 años con sibilancias recurrentes. En la tabla 2 se detallan los resultados obtenidos.
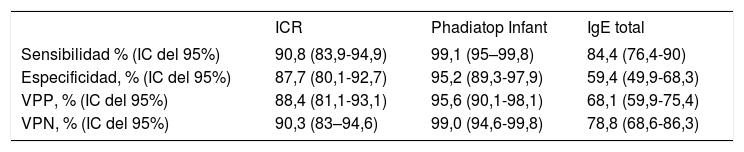
Características y resultados del estudio IReNE19, en el que se detallan los resultados de las pruebas con InmunoCAP Rapid (ICR), Phadiatop Infant e IgE total para el diagnóstico de la atopia en una muestra de 215 niños de 1–14 años con sibilancias recurrentes
| ICR | Phadiatop Infant | IgE total | |
|---|---|---|---|
| Sensibilidad % (IC del 95%) | 90,8 (83,9-94,9) | 99,1 (95–99,8) | 84,4 (76,4-90) |
| Especificidad, % (IC del 95%) | 87,7 (80,1-92,7) | 95,2 (89,3-97,9) | 59,4 (49,9-68,3) |
| VPP, % (IC del 95%) | 88,4 (81,1-93,1) | 95,6 (90,1-98,1) | 68,1 (59,9-75,4) |
| VPN, % (IC del 95%) | 90,3 (83–94,6) | 99,0 (94,6-99,8) | 78,8 (68,6-86,3) |
IC: intervalo de confianza; ICR: InmunoCAP Rapid; VPN: valor predictivo negativo; VPP: valor predictivo positivo.
El ICR está diseñado expresamente para su utilización en AP. Es un método sencillo, rápido, poco invasivo y de fácil lectura. Si los futuros estudios que se realicen confirman los buenos valores de sensibilidad y especificidad de la prueba, puede convertirse en la herramienta de elección como primer paso para el estudio de las enfermedades alérgicas en AP17 incluidos menores de 5 años, puesto que también permite la detección de sensibilización a alimentos.
ConclusiónEl pediatra de AP dispone de nuevas técnicas para el diagnóstico de la alergia en niños con síntomas compatibles. La disponibilidad generalizada y el conocimiento de éstas permitirán llegar a un diagnóstico correcto y posibilitará un tratamiento integral de la mayor parte de estas enfermedades en el entorno de la comunidad. Esta estrategia racionalizará las derivaciones en el ámbito hospitalario, que solo recibiría los pacientes en los que hayan dudas diagnósticas o en los que por la mala evolución o la complejidad de su tratamiento requieran ser evaluados y controlados en servicios especializados, como aconsejan las guías de práctica clínica.