La sedación es un componente esencial en el manejo de los pacientes ingresados en las Unidades de Cuidados Críticos. La mayoría de los pacientes ingresados en estas unidades recibe sedación en algún momento de su estancia debido a su grave estado físico, al alto nivel de invasividad, a los cuidados de enfermería y a muchos otros factores, como el aislamiento, la deprivación de sueño, la incapacidad de comunicarse, etc. La complejidad creciente de los pacientes, con sedaciones muy prolongadas, ofrece con frecuencia problemas en el manejo con los sedantes habituales.
En pediatría se utilizan fundamentalmente las benzodiacepinas y el propofol en periodos cortos, generalmente asociados a opioides. Sin embargo, estos agentes tienen características farmacológicas que los alejan del sedante ideal y efectos adversos como tolerancia, síndrome de abstinencia y acumulación, con el consiguiente retraso en el despertar.
Una alternativa posible a los sedantes convencionales es la sedación por vía inhalatoria, que tiene lugar mediante la acción de anestésicos inhalatorios, utilizados de igual modo que en la anestesia en las intervenciones quirúrgicas, si bien a una dosis inferior. La mayor ventaja de esta vía de administración es el mínimo metabolismo y la escasa acumulación de los agentes halogenados, lo que proporciona una gran precisión en el control de la sedación, con una rápida y predecible recuperación. Actualmente, disponemos del dispositivo AnaConDa® (Anaesthetic Conserving Device), dispositivo diseñado para la administración de los agentes inhalatorios isoflurano y sevoflurano con ventiladores estándar de cuidados críticos.
Puntos clave
- •
En pacientes seleccionados, la sedación inhalatoria en Cuidados Críticos puede constituir una buena alternativa a la sedación intravenosa habitual. Algunas de las indicaciones más claras serían el estatus asmático y el estatus epiléptico.
- •
El mínimo metabolismo y la acumulación de los agentes halogenados proporcionan una gran precisión en el control de la sedación con una rápida y predecible recuperación.
- •
La MAC-awake para el sevofluorano en niños (concentración alveolar mínima que produce pérdida de consciencia pero permite respuesta adecuada a órdenes verbales) se encuentra entre 0,6-1% y disminuye con la edad, y con el uso concomitante de otros sedantes u opiáceos.
- •
El dispositivo AnaConDa® permite utilizar sedantes inhalatorios fuera de quirófano con respiradores convencionales.
El primer gas utilizado fue el halotano, que fue sustituido por el isoflurano, gas de bajo coste pero con eliminación más lenta, lo que lo hace menos manejable. El desflurano, muy irritante en la inducción con mascarilla, no ha tenido mucho impacto en anestesia pediátrica. Los más modernos, sevoflurano y desflurano, llevan utilizándose 15 años, así que sus propiedades farmacodinámicas son bien conocidas. Debido a su perfil de seguridad cardiovascular, el sevoflurano ha ido desplazando al resto de los gases y se ha convertido en el gas de elección en niños, ya que es bien tolerado para la inducción y útil como agente de mantenimiento1. Su perfil de seguridad ha justificado su uso con un amplio rango terapéutico limitado en un extremo por el riesgo de despertar y, en el otro, por sus efectos deletéreos cardiovasculares2.
El sevoflurano tiene escasa solubilidad en sangre por lo que el inicio de acción y la recuperación son rápidos. Tiene efecto hipnótico-sedante, broncodilatador y escasamente analgésico. Interfiere poco en la hemodinámica, sobre todo a bajas concentraciones.
Algunas de las ventajas de la sedación inhalatoria frente a la sedación por vía intravenosa son3:
- –
No produce depresión respiratoria.
- –
No disminuye la motilidad intestinal.
- –
Permite extubación planificada.
- –
Permite ventanas de sedación.
- –
Fácil monitorización y dosificación.
- –
Escasa acumulación.
- –
Metabolismo hepático inferior al 5%, sin metabolitos activos.
- –
Independiente de función renal y hepática.
- –
No necesita vía venosa.
- –
Efecto broncodilatador de algunos gases anestésicos, como sevo e isoflurano.
El uso de sedantes inhalatorios fuera de quirófano no se ha extendido hasta el momento por la necesidad de utilizar para ello máquinas de anestesia con vaporizador, de difícil transporte, que además no tienen todas las modalidades de ventilación, existiendo además el problema de la contaminación ambiental de gas si no se administra con los sistemas de seguridad apropiados4.
La utilización de sedación inhalatoria en Cuidados Críticos constituye una alternativa a los sedantes habituales en pacientes seleccionados. Aunque se conoce su seguridad en el corto plazo, son necesarios más estudios para conocer los efectos a medio y largo plazo de la sedación prolongada con gases halogenados5-7.
Indicaciones- 1.
Pacientes ingresados en la Unidad de Cuidados Críticos, que precisen sedación y que estén en ventilación mecánica a través de tubo endotraqueal o traqueostomía. Estaría especialmente indicado en:
- 2.
Pacientes sedados que han desarrollado una creciente tolerancia a los agentes intravenosos utilizados en su sedación12.
- 3.
Cuando se precisa la interrupción de la administración de medicamentos («drug Holiday»). En estos casos, la sustitución de la sedación por vía intravenosa por sedación inhalatoria a menudo produce una recuperación del estado del receptor en el plazo de 48h, de manera que después los medicamentos por vía intravenosa recuperan su efectividad y se pueden aplicar en dosis más bajas.
- 1.
El sevoflurano está contraindicado en pacientes con antecedentes o sospecha de hipertermia maligna y en aquellos con antecedentes de hipersensibilidad al sevoflurano.
- 2.
El sevoflurano puede producir elevación en los niveles plasmáticos de flúor inorgánico con el uso prolongado. Sin embargo, niveles muy superiores a los normales no han demostrado provocar daño renal. No obstante, no se recomienda un uso superior a 48h sin control de la función renal.
- 3.
El sevoflurano debe utilizarse con precaución en pacientes con enfermedad de Duchenne, ya que en los pequeños puede producir hipercaliemia y depresión miocárdica en adolescentes.
- 4.
Fuga aérea significativa (p. ej., fístula broncopleural).
AnaConDa® (Anaesthetic Conserving Device, Sedana Medical, Sundbyberg, Suecia) es un dispositivo de pequeño tamaño, de fácil colocación, adaptable a todo tipo de ventilador, y que permite la reutilización del gas, con el consiguiente ahorro de anestésico inhalatorio.
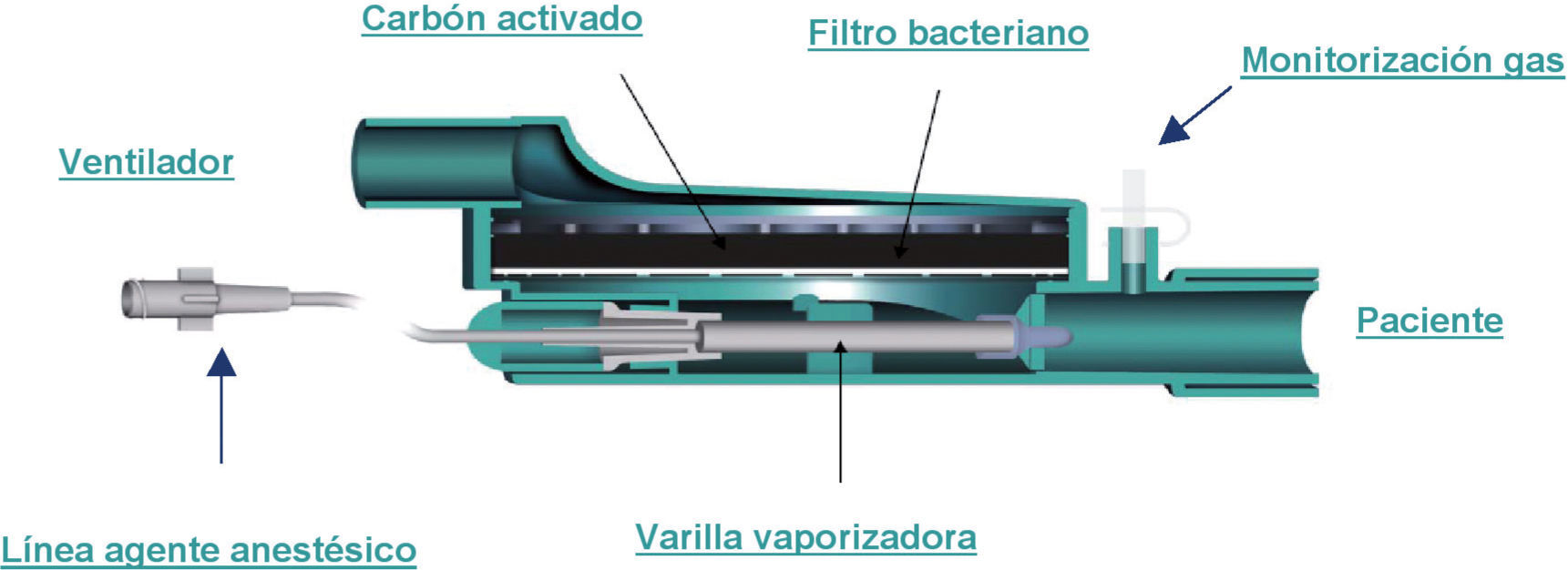
Es básicamente un filtro intercambiador de calor y humedad modificado que, intercalado en el circuito de ventilación del paciente, permite administrar agente halogenado (isoflurano o sevoflurano) por medio de una cámara de vaporización conectada a una jeringa con anestésico líquido (figs. 1 y 2).
Funcionamiento del dispositivo AnaConDa®. El anestésico difunde sobre la superficie de la varilla y se vaporiza instantáneamente, siendo arrastrado por el flujo de gas inspiratorio y entregado a los pulmones. Durante la espiración, el 90% del anestésico volátil se condensa en la superficie de las fibras de carbón activado y se libera de nuevo al paciente en la próxima inspiración. Por consiguiente, solo el 10% del agente anestésico atraviesa el filtro y se elimina finalmente al exterior a través de la salida espiratoria del ventilador.
Se monitorizará al paciente mediante un analizador de gases, que mide la concentración de gas al final de la espiración (ET sevo). Esta medición se llevará a cabo, bien en la línea del dispositivo AnaConDa® destinada a tal efecto o, en el caso de pacientes pequeños en los que el dispositivo se coloque en el asa inspiratoria, se medirá la concentración de gas en la pieza en Y. Para medir el grado de sedación puede apoyarse también en la monitorización del índice biespectral, que se mantendrá entre 40-50 con relajante muscular y 60-65 sin relajante muscular.
La concentración alveolar mínima (CAM-MAC) es la medida de la profundidad anestésica: concentración alveolar mínima que hace que un paciente no se mueva ante un estímulo doloroso.
La MAC del sevofluorano en niños es la siguiente:
- –
1-6 meses: 3,1%.
- –
6-12 meses: 2,7%.
- –
1-12 años: 2,55%.
Para la dosificación en Cuidados Críticos, se utilizará la MAC-awake, que es la concentración alveolar mínima que produce pérdida de consciencia pero permite respuesta a órdenes verbales adecuadamente. Esta concentración para el sevofluorano se encuentra entre 0,6-1%, y disminuye con la edad, y con el uso concomitante de otros sedantes u opiáceos13.
Existen tablas proporcionadas por el fabricante con el ritmo de infusión inicial recomendado para pacientes adultos, que se ajustará posteriormente para la ET sevo deseada. En niños, este ritmo de infusión inicial para una ET sevo 0,7-1% oscila entre 2-7ml/h.
En pocos minutos, el analizador de gases mostrará los valores de ET sevo que se vayan obteniendo. En unos 10-20min los valores se estabilizarán. Hay que tener en cuenta que cuando modifiquemos en el respirador el volumen minuto (la frecuencia respiratoria, el volumen total o ambos), a veces se precisa un reajuste de la velocidad de infusión para mantener constante la concentración de gas administrada.
Como regla general, si un paciente sedado por vía intravenosa va a recibir un anestésico volátil, los requerimientos de opiáceos disminuirán a menos de la mitad, por lo que puede ser útil suspender su infusión temporalmente hasta que baje la concentración en sangre y reiniciar a dosis inferior.
Por otra parte, dosis bajas de opiáceos permitirán una reducción de la ET sevo y, por su acción en el tronco cerebral, facilitan la tolerancia al tubo endotraqueal y suprimen el reflejo tusígeno y la excitación que se produce cuando se interrumpe la administración del anestésico volátil o se administra en concentraciones demasiado bajas.
Por su perfil farmacocinético, el remifentanilo puede ser un fármaco muy útil para asociar a los anestésicos volátiles, ya que tampoco se acumula, incluso en pacientes con insuficiencia hepática y/o renal.
Montaje del dispositivoEl dispositivo AnaConDa® está diseñado para ser colocado entre la pieza en Y del circuito de ventilación del paciente y el tubo endotraqueal. Para conducir el anestésico líquido al evaporador, el dispositivo incorpora una línea de infusión que está conectada a una jeringa de 50ml llena de líquido anestésico; por medio de una bomba de jeringa estándar, se controla la velocidad de infusión. Antes de colocar la jeringa en la bomba, se rellena de agente anestésico líquido por medio de un adaptador especial que conecta la botella de anestésico con la jeringa, evitando así las fugas y la contaminación ambiental. La jeringa y la línea de infusión deben ser las suministradas por el fabricante ya que los anestésicos volátiles pueden disolver los materiales plásticos habitualmente utilizados en las jeringas estándar (fig. 3).
Cuando se rellena la jeringa, se debe tener cuidado para evitar la formación de burbujas en su interior, ya que debido a su alta presión de vapor, los anestésicos volátiles se evaporan en estas burbujas y las hacen crecer si la jeringa se expone a altas temperaturas; las burbujas crecientes pueden bombear el líquido anestésico en el dispositivo AnaConDa® y dar lugar a sobredosis. Las fuentes de calor, por lo tanto, deben tenerse siempre lejos de la jeringa y en el caso de que las burbujas se detecten en el dispositivo, debe desconectarse del paciente e investigar la posible causa.
Durante el uso de dispositivo AnaConDa®, si es necesario aspirar secreciones, lo óptimo es que el paciente tenga conectado un sistema de aspiración cerrada, evitando la desconexión del circuito. En caso de que no lleve aspiración cerrada, para evitar la polución ambiental, se debe parar la jeringa de infusión, desconectar el circuito, aspirar las secreciones y reconectar el circuito, volviendo a poner en marcha luego la jeringa de infusión.
Si el paciente precisa sedación para las aspiraciones, puede administrarse previamente un bolo con la bomba de jeringa de 0,3 a 0,5ml antes de la desconexión.
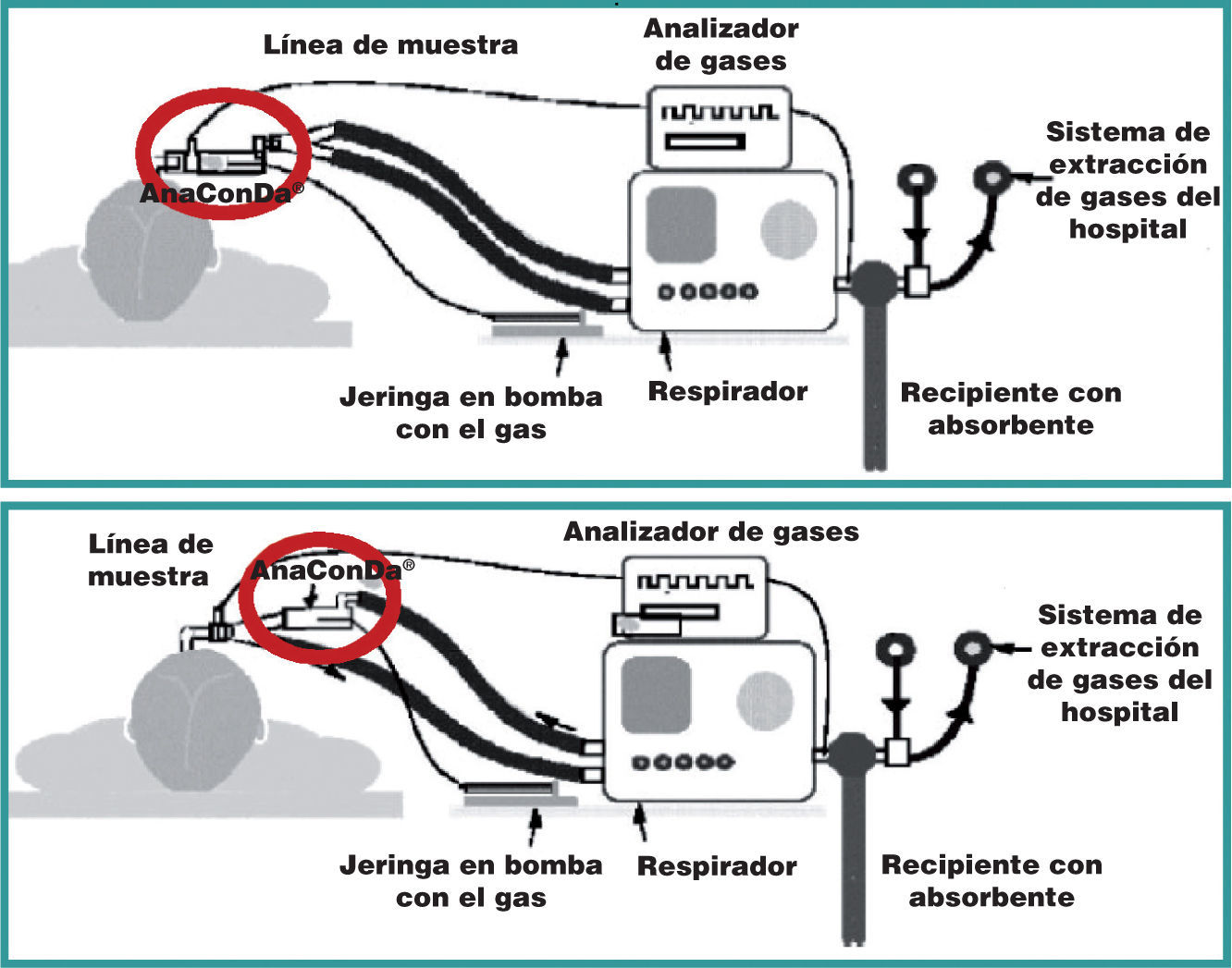
El dispositivo genera un aumento del espacio muerto de aproximadamente 100ml, por lo que no se debe utilizar en pacientes con peso inferior a 30kg o volumen tidal inferior a 350ml. En estos pacientes, se puede interponer el dispositivo entre el respirador y el asa inspiratoria. En este caso, no se producirá el efecto de recirculación y «ahorro» de anestésico inhalatorio que se produce con su uso normal, aunque en estos pacientes el gasto de anestésico no es muy importante (fig. 4).
Colocación del dispositivo AnaConDa®. En esta figura se ilustra la diferente colocación del vaporizador en función del volumen tidal del paciente para evitar el excesivo aumento del espacio muerto: después de la pieza en Y si el volumen tidal es mayor de 350 ml y en la rama inspiratoria si es menor de 350ml.
Para evitar la contaminación ambiental, se conectará la salida del gas del respirador, bien al sistema de extracción de gases del hospital, o bien a un recipiente con material absorbente14.