La rabia es una zoonosis viral que, en ciertas partes del mundo, es enzoótica tanto en animales salvajes como domésticos. Es una enfermedad producida por un virus de la familia Rhabdoviridae y del género Lyssavirus, que se transmite de los animales al hombre. Los huéspedes son los animales carnívoros y numerosas especies de quirópteros (murciélagos)1.
Todos los genotipos de Lyssavirus producen un cuadro de encefalomielitis que conduce inexorablemente a la muerte. Recientemente, se ha publicado algún caso transmitido por murciélagos que ha evolucionado de forma favorable2. La clínica de la rabia se desarrolla en 5 etapas: a) incubación; b) prodrómica; c) manifestaciones neurológicas agudas; d) coma, y e) muerte. El período de incubación es de 4–6 semanas, pero varía entre 5 días a 1 año3,4.
El método diagnóstico definitivo es la biopsia cerebral y la demostración del antígeno del virus rábico o de inclusiones específicas (cuerpos de Negri). Se puede intentar detectar el virus en la saliva, el líquido cefalorraquídeo, la herida y la biopsia de piel y orina por medio de la técnica de reacción encadena de la polimerasa (pcR)5. La técnica diagnóstica estándar es la detección del antígeno del virus de la rabia en el cerebro, por medio de la técnica de anticuerpos fluorescentes o por enzimoinmunoanálisis.
IncidenciaEs muy elevada en Asia, África y América del Sur. Solamente en la India mueren anualmente más de 30.000 personas, la mayoría niños. Se estima que el 13% de los viajeros que visitan el sudeste Asiático tienen contacto con animales6–8. En España, los últimos casos de rabia tuvieron lugar en la década de los años sesenta9.
Mecanismo de transmisiónEl virus está presente en la saliva de los animales infectados. La transmisión se realiza habitualmente por mordeduras de animales. El perro es el más frecuente y los niños son los que tienen más contacto con estos animales. La rabia se puede transmitir también por aerosoles, como puede ocurrir en cuevas donde habitan millones de murciélagos, y mediante trasplante de órganos (se han descrito casos por trasplante de córnea). En los países más desarrollados, que tienen un buen control sanitario de los perros, los murciélagos se han convertido en el reservorio principal10,11.
Vacunas antirrábicasTipos de vacunasLas vacunas disponibles pueden ser de 2 tipos: cultivadas en tejido nervioso y en cultivos celulares.
Las vacunas antiguas o de primera generación se preparaban a partir de tejido nervioso de animales. Fueron las vacunas utilizadas inicialmente por Pasteur, pero tenían reacciones adversas graves debidas a la respuesta inmunitaria desencadenada por los antígenos neuronales. La organización Mundial de la Salud (OMS) ha recomendado el cese de su fabricación. Las vacunas modernas o de segunda generación están preparadas en cultivos celulares de células diploides humanas (HDCV), células Vero (PVRV), células de embrión de pollo (PCECV), riñón de hámster (PHKCV), embrión de pato (PDEV) o de células diploides de mono Rhesus (RVA). La ventaja de estas vacunas es que están libres de proteínas heterólogas, inducen buena respuesta inmunitaria y presentan una eficacia muy buena. El principal inconveniente es su elevado precio. Todas las vacunas de cultivos celulares tienen una eficacia parecida y están libres de desencadenar reacciones alérgicas importantes. En España están disponibles las vacunas HDCV y PCECV.
Vacunación por vía intradérmica. El coste de las pautas intramusculares es elevado, prohibitivo para países en desarrollo. La oMs ha recomendado la utilización de la vía intradérmica en estos países. Tienen la ventaja que requieren menos cantidad de vacuna y resultan más económicos en el 60-80%12. Las vacunas que pueden usarse por esta vía son HDCV, PVRV, PCECV y PDEV. La vía intradérmica no está autorizada en España.
InmunogenicidadLa vacunación induce rápidamente una respuesta humoral elevada. La vacuna tiene una elevada inmunogenicidad y, después de la tercera dosis, en el 99% de los vacunados provoca la producción de anticuerpos por encima del nivel considerado protector. La vacuna induce también una respuesta de memoria inmunológica que se caracteriza por el incremento rápido del título de anticuerpos después de una dosis booster.
EficaciaEs difícil determinar la eficacia de la vacuna antirrábica, por la dificultad a la hora de realizar ensayos clínicos placebo/paciente, y por el desconocimiento del riesgo de tener la enfermedad después del contacto. Si se valora en función de la profilaxis postexposición, la eficacia de la vacuna sola o asociada a inmunoglobulina es muy elevada, cercana al 100%.
Seguridad e interaccionesLas reacciones secundarias a las vacunas de segunda generación son escasas. se han descrito reacciones locales moderadas (dolor, eritema e induración) y reacciones sistémicas (cefaleas y malestar general). se ha observado algún caso de síndrome de Guillain-Barré, pero su asociación con la vacuna no se ha confirmado. Las manifestaciones adversas más significativas se deben a reacciones alérgicas en forma de urticaria, artritis o angioedema.
Profilaxis frente a la rabiaProfilaxis preexposición12–16Está indicada en personas que están expuestas al virus rábico en el laboratorio, o que tienen contacto con mamíferos, incluidos los murciélagos. Igualmente, está indicada en viajeros con destino a países endémicos de rabia, especialmente si visitan áreas alejadas de centros urbanos y no hay garantía de realizar una profilaxis postexposición adecuada.
Pauta de vacunación preexposiciónEn nuestro medio, consiste en administrar por vía intramuscular 3 dosis de 1ml de vacuna HDCV o PCECV los días 0, 7 y 21. No es necesaria gammaglobulina antirrábica.
En personas que están en situación de riesgo profesional, se aconseja analizar una muestra de suero cada 6 meses, y si el título de anticuerpos está por debajo de 0,5 u/ml está indicada una dosis booster de 1ml por vía intramuscular.
Para reducir el coste de la vacuna, puede entrar en consideración la vacunación por vía intradérmica en países autorizados a la dosis de 0,1ml los días 0, 7 y 21. Tiene el inconveniente que presenta más dificultades técnicas en su administración, y se necesita personal muy bien formado. Además, su administración concomitante con cloroquina reduce la respuesta inmunitaria, circunstancia a tener en cuenta en viajeros internacionales que tengan que recibir profilaxis del paludismo.
Profilaxis postexposición12–17Se utiliza para prevenir la enfermedad en individuos expuestos, habitualmente después de ser mordidos por un animal sospechoso de tener rabia. La actitud a tomar va a depender del animal agresor y del tipo de exposición (tablas 1 y 2).
Profilaxis postexposición a la rabia. Centers Disease and Control Prevention de Estados Unidos, 1999
| Tipo de animal | Evaluación y disponibilidad del animal | Profilaxis postexposición recomendada |
|---|---|---|
| Perros, gatos y hurones | Sanos y disponibles para observación durante 10 días | Los pacientes no deben comenzar profilaxis hasta que el animal no desarrolle signos de rabiaa |
| Rabioso o sospechoso | Vacunación inmediata más IGRH | |
| Desconocido (p. ej., escapado) | Consultar a las autoridades sanitarias | |
| Murciélagos, mapaches, zorros, marmotas y otros carnívoros | Considerar como rabioso hasta que se demuestre que es negativo por los tests de laboratoriob | Vacunación inmediata más IGRH |
| Ganado, roedores y logomorfos (conejos y liebres) | Considerar de forma individual | Consultar a las autoridades sanitarias. Mordeduras de ardillas, hámster, cobayas, jerbos, ratas, ratones, otros pequeños roedores, conejos y liebres casi nunca requieren profilaxis antirrábica postexposición |
IGRH inmunoglobulina antirrábica humana.
Guía para el tratamiento postexposición frente a la rabia
| Categoría | Tipo de contacto con animal salvaje o doméstico sospechoso o con rabia confirmada o sin posible observación | Profilaxis recomendada |
|---|---|---|
| I. Sin exposición | Tocar o alimentar animales Lameduras sobre piel intacta | Ninguna (si se tienen datos fiables sobre las circunstancias de la exposición) |
| II. Exposición menor | Mordisco de piel descubierta Arañazos o erosiones leves sin hemorragia |
|
| III. Exposición grave | Mordeduras o arañazos transdérmicos únicos o múltiples, lameduras en piel lesionada Contaminación de membrana mucosa con saliva (lamedura) Exposición a murciélagos |
|
La profilaxis postexposición correcta implica: limpieza cuidadosa de la herida, administración de inmunoglobulina antirrábica (cuando está indicada) y vacunación.
La limpieza de la herida debe realizarse de inmediato con jabón y agua abundante a chorro, como mínimo durante 15min. Si no se dispone de jabón, se utilizará sólo agua. Desinfección con amonio cuaternario, alcohol de 70º o solución acuosa de povidona yodada al 10% y debe asociarse la vacunación antitetánica y tratamiento antibiótico (amoxicilina-ácido clavulánico).
La inmunoterapia pasiva se utiliza en el caso de que el individuo esté encuadrado en la categoría III, o en la II si es un inmunodeprimido (tabla 2). Se dispone de inmunoglobulina antirrábica humana (IGRH), de inmunoglobulina antirrábica equina purificada (IGRE) o de fragmentos de IGRE: F(ab’)2. Actualmente, en los países desarrollados se usa la IGRH, pero debido a su precio elevado se sigue utilizando el antisuero equino en países en vías de desarrollo. Cuando está indicada la aplicación de IGRH, se administrará el día 0, a la dosis de 20 U/kg de peso, y si se utiliza IGRE o F(ab’)2, a 40 U/kg. Actualmente, se aconseja que la dosis total se administre alrededor o dentro de la herida. Si no es posible poner la dosis total a nivel local por circunstancias anatómicas, la cantidad sobrante se inyectará en otra zona por vía intramuscular, pero siempre alejada del lugar de administración de la vacuna. Deben evitarse las suturas en la zona de las lesiones, o retrasarlas lo máximo posible durante varias horas, para que la inmunoglobulina se difunda bien en los tejidos18. Si la superficie lesionada es muy amplia y no es suficiente, la inmunoglobulina calculada se diluirá en suero fisiológico para aplicar en todas las lesiones.
Según el criterio de la OMS, se procederá a la vacunación y a la administración de inmunoglobulina específica en las circunstancias que se indican en la tabla 2.
Pauta de vacunación postexposición1. Individuos no vacunados previamente
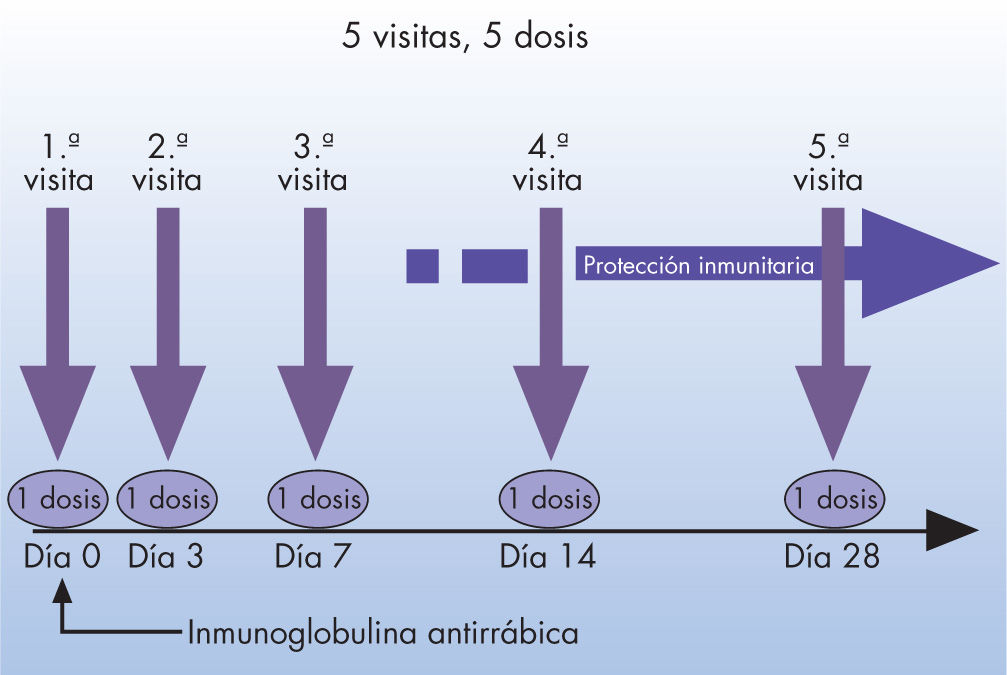
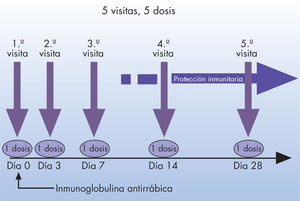
La pauta vacunal recomendada por la oMS es de 5 visitas-5 dosis (régimen Essen). Consiste en administrar por vía intramuscular 5 dosis de 1ml de vacuna los días 0, 3, 7, 14 y 28 (fig. 1).
La protección se alcanza después de la tercera dosis, a partir del día 14 del inicio de la vacunación. En nuestro medio, las vacunas que se administran son HDCV y PCECV.
La vacunación intramuscular en adultos siempre debe realizarse en la región deltoidea y en los niños en la zona anterolateral del muslo. Nunca se utilizará la región glútea.
Vacunación intradérmicaLa oMS recomienda 2 pautas de vacunación intradérmica, siempre que las autoridades competentes del país hayan autorizado la vacunación por esta vía.
1.a pauta: (8-0-4-0-1-1). Se realiza con vacunas HDCV y PCECV:
- —
Día 0: se inyecta por vía intradérmica 0,1ml en 8 lugares distintos y simétricamente situados. Una dosis en cada región deltoidea, en lateral de ambos muslos, región supraescapular y cuadrante inferior del abdomen.
- —
Día 7: 0,1ml vía en 4 lugares. Una dosis en ambas zonas deltoideas y lateral de muslos.
- —
Días 28 y 90: 0,1ml en un lugar, preferible en región deltoidea.
2.a pauta: (2-2-2-0-2). Se realiza con vacunas PVRV o PCECV.
- —
Se inyecta 0,1ml en 2 regiones distintas los días 0, 3, 7 y 28.
2. Individuos vacunados previamente
La vacuna induce memoria inmunológica y se produce una respuesta anamnésica si se administra una dosis booster a un individuo previamente vacunado. Cuando un individuo ya vacunado que ha recibido una pauta completa de vacunación preexposición o postexposición presenta una nueva exposición al virus de la rabia (p. ej., mordedura de un animal sospechoso), debe recibir 2 dosis de recuerdo de vacuna, una el día de la exposición y la segunda a los 3 días. Está indicado el tratamiento local de la herida y no es necesaria la administración de IGRH.
ContraindicacionesNo hay ningún tipo de contraindicación para la profilaxis postexposición para vacunar contra la rabia, ni durante el embarazo ni la lactancia. La mortalidad elevada de la enfermedad hace aconsejable proceder a la inmunización en todos los casos.
Condiciones de conservación, transporte y almacenamientoLa vacuna debe mantenerse entre +2 y +8ºC, sin congelar y protegida de la luz.
Presentaciones comercialesEn España, se han comercializado 2 vacunas: a) la vacuna antirrábica inactivada cultivada en células diploides humanas (HDCV), con el nombre de Vacuna Antirrábica Merieux® (Laboratorios Sanofi Pasteur MSD, SA), que utiliza la cepa Wistar PM/W138-1503-3M, y b) la vacuna antirrábica preparada en cultivos celulares de células embrionadas de pollo purificadas (PCECV) con el nombre de Rabipur® (Laboratorios Chiron Behring GmbH & Co), que utiliza la cepa Flury LEP. Estas vacunas están disponibles en los centros sanitarios de las diferentes comunidades autónomas.