El síndrome de Marfan es un trastorno sistémico del tejido conectivo con una alta variabilidad en su presentación clínica. Las manifestaciones más importantes afectan al sistema ocular, como miopía rápidamente progresiva en la infancia, subluxación o luxación de cristalinos (ectopia lentis) y un riesgo aumentado de desprendiento de retina, glaucoma y catarata precozc1. En el sistema esquelético suele asociar un excesivo crecimiento de los huesos largos, hiperextensibilidad de los mismos, pectus excavatum, pectus carinatum, escoliosis y cara alargada con paladar ojival y posible micrognatia o retrognatia2. En el sistema cardiovascular puede producir la dilatación de la aorta, disección de aorta ascendente, prolapso de la válvula mitral y prolapso de la válvula tricúspide3. La herencia es autosómica dominante y aunque en el 75 % de los casos uno de los progenitores está afecto, en un 25 % de los casos la mutación se produce de novo. El gen FBN1 (fibrilina 1), localizado en el cromosoma 15q21.1, es el único gen relacionado con esta patología, sin embargo se han detectado formas Marfan-like asociadas a los genes TGFBR1 y TGFBR2. En algunos estudios han determinado que también podría estar implicado el gen de la fibrilina 2 (FBN2)4. La proteína fibrilina 1 es una proteína de la matriz extracelular que contribuye en la estructura microfibrilar presente en los tejidos elásticos y no elásticos.
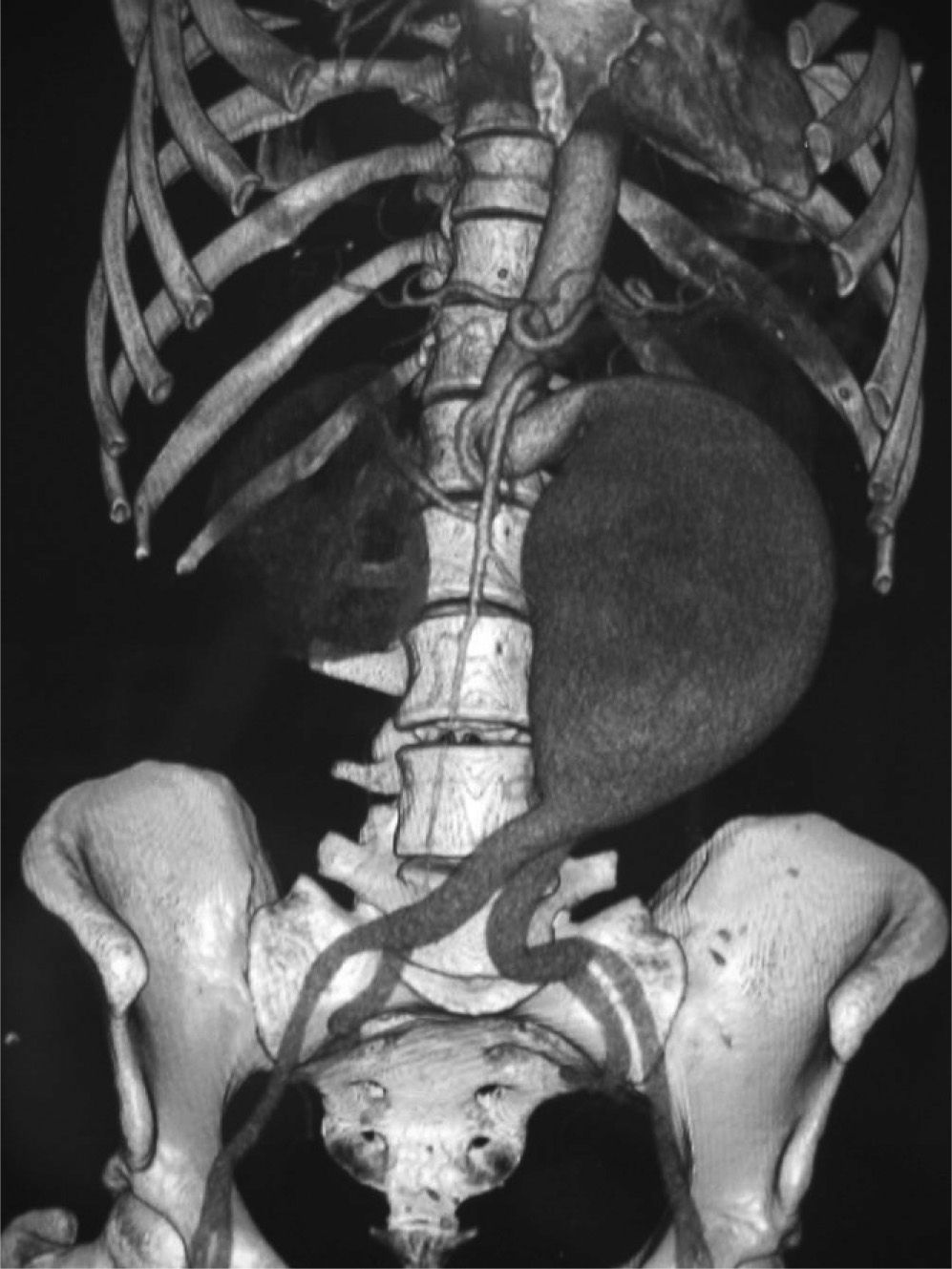
Presentamos el caso de una mujer de 39 años que mostraba un cuadro de abdominalgia inespecífica de 14 días de evolución junto con hiperlatido abdominal. Entre sus antecedentes personales destacaba la presencia de poliquistosis renal, miomas uterinos, esguinces de repetición y ulcus péptico a los 7 años de edad. Sin embargo, el aspecto de mayor relevancia es la luxación congénita de cristalino bilateral que padece la paciente, al igual que su hermana gemela. El único antecedente quirúrgico fue por blefaritis. Durante el estudio diagnóstico en el Servicio de Urgencias se detectó mediante tomografía computarizada la presencia de un aneurisma de aorta abdominal cuyo diámetro máximo fue de 8,6 cm y 15,3 cm de longitud. Presentaba elongación y una angulación del cuello aneurismático superior a 90 grados pero sin afectación del sector iliaco ni signos de complicación (fig. 1). No se detectó afectación de aorta torácica. Se objetivaron también quistes renales. Dados dichos hallazgos, se iniciaron tanto estudio inmunológico como genético, siendo ambos compatibles con síndrome de Marfan. En el estudio molecular del gen FBN1 se puso de manifiesto la presencia de la mutación c.7699+5g>A en heterocigosis. Este hallazgo apoya el diagnóstico de síndrome de Marfan.
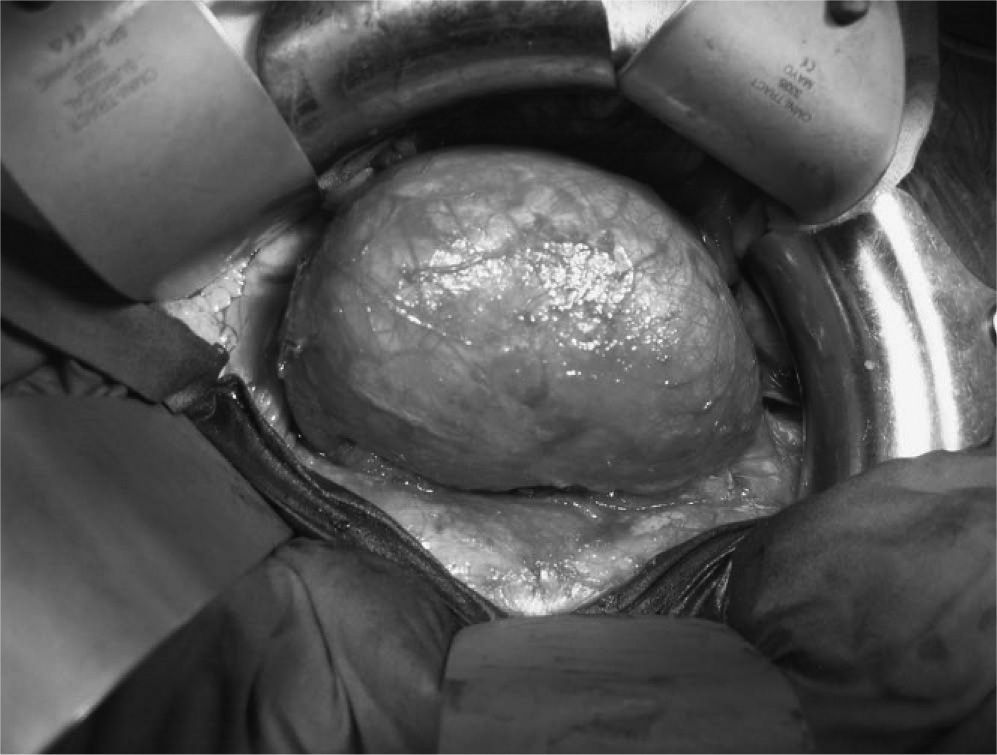
Se planeó la reparación quirúrgica convencional de forma reglada bajo anestesia general. Se realizó el abordaje trans peritoneal mediante laparotomía media. El diámetro máximo del aneurisma fue de 9 cm aproximadamente, con elongación significativa del cuello aneurismático (fig. 2). A continuación se procedió a la apertura aneurismática e injerto terminoterminal con prótesis de dacron del n.° 16. La paciente fue revisada a los 3, 6 y 12 meses, sin hallazgos clínicos significativos. La tomografía computarizada al año objetivaba permeabilidad del injerto sin signos de estenosis ni pseudoaneurisma anastomótico. Se inició el estudio genético de familiares directos.
El aneurisma de aorta en el síndrome de Marfan puede ser extenso y múltiple por la necrosis quística de la media de la pared aórtica 5. Característicamente suelen tener escaso trombo mural a diferencia de los ateroscleróticos. Suelen asociar disección aórtica y afectar a la aorta ascendente, la cual soporta mayores cambios de presión. Por ello, los aneurismas verdaderos de aorta abdominal resultan raros en estos pacientes, teniendo lugar en pacientes más jóvenes (40 años de media en algunas series)3. Un importante porcentaje tiende a la rotura (6,5-33 % según las series)6, incluso con diámetros por debajo del límite quirúrgico (50 mm). Los casos de aneurisma roto asociados a síndrome de Marfan alcanzan una mortalidad quirúrgica del 50 %, que aumenta con la insuficiencia cardiaca que pueden desarrollar estos pacientes en el postoperatorio. La rotura de los aneurismas de diámetro pequeño o la disección en este síndrome se pueden deber a la fragilidad de la pared aórtica, ya que es característica la necrosis quística de la capa media, que puede llegar a afectar al 100 % de los casos en algunas series. Varios aspectos característicos en las pruebas de imagen, como la escasa calcificación y la ausencia de trombo mural, pueden orientar el diagnóstico etiológico de un aneurisma de aorta abdominal, sobre todo si afecta a pacientes jóvenes7. No deberíamos olvidar un estudio programado de la comorbilidad cardiológica, ausente en nuestra paciente, y de sus posibles complicaciones asociadas. En cuanto al tratamiento, dada la tendencia a la rotura incluso con diámetros inferiores a 5 cm y la esperanza de vida de estos pacientes, no parece indicado el tratamiento conservador a pesar de no alcanzar rango quirúrgico. Actualmente no se ha establecido un consenso para el tratamiento mediante reparación endovascular en estos pacientes, por lo que se sigue considerando la reparación convencional con resección e injerto protésico como el tratamiento de elección8. En conclusión, el aneurisma de aorta abdominal en el síndrome de Marfan suele aparecer en rangos de edad más precoces, presentando escaso trombo mural y una especial tendencia a la disección y a la rotura incluso con diámetros inferiores a 5 cm. En la actualidad, el tratamiento de elección es la reparación quirúrgica convencional.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.