El diagnóstico y seguimiento de los pacientes con aneurisma de aorta abdominal (AAA) se realizan mediante medición seriada del diámetro aórtico máximo con ultrasonografía o tomografía computerizada, pero la expansión aórtica es mayoritariamente discontinua, e impredecible en un paciente concreto. Un modelo predictivo fiable de crecimiento y/o rotura aórticos podría ayudar a individualizar el manejo. Nuestro objetivo ha sido definir un modelo predictivo de crecimiento aneurismático a corto plazo a partir de variables clínicas, serológicas y anatómicas.
MétodosSe reclutaron 148 pacientes con AAA aterosclerótico infrarrenal asintomático consecutivos. Se recogieron: datos clínicos (edad, sexo, factores de riesgo cardiovascular, comorbilidad, medicación), diámetro basal de los AAA, crecimiento aórtico prospectivo a un año, y concentraciones basales circulantes de MMP-2, MMP-9, cistatina C, alfa1-antitripsina, mieloperoxidasa, MCP-1, homocisteína, dímero D, PAP y proteína C reactiva. Se elaboraron modelos predictivos del crecimiento prospectivo a un año de los AAA, crecimiento valorado como variable continua (mm/año) y dicotómica (estabilidad, si la tasa de crecimiento era ≤2mm/año; expansión, si era >2mm/año), utilizando regresión lineal y logística, simple y múltiple.
ResultadosCada incremento en las concentraciones de dímero D en 1ng/mL se asoció al aumento medio de 0,0062mm/año en el crecimiento prospectivo de los AAA. La insuficiencia renal crónica aumentó el crecimiento medio en 2,95mm/año. Mayores concentraciones de PAP y la coexistencia de IRC aumentaban el riesgo de expansión aórtica (OR 1,01 y 14523,62; IC 95% 1,00-1,02 y 0-7,39E+40, respectivamente).
ConclusionesLas concentraciones plasmáticas de dímero D y PAP constituyen prometedores biomarcadores predictivos de la expansión prospectiva de los AAA a corto plazo. La insuficiencia renal crónica es un importante factor clínico pronóstico de expansion aórtica. La clasificación del crecimiento de los AAA de forma dicotómica, estabilidad versus expansión, puede ser útil para la elaboración de modelos de decisión y su aplicación clínica.
Abdominal aortic aneurysms (AAA) are currently followed-up by measuring their diameter with serial ultrasound or computed tomography scanning, but evidence shows that AAA growth is mostly discontinuous and unpredictable in a given patient. A reliable predictive model of AAA growth and/or rupture risk could help individualize management. The aim of this study was to define a predictive model of short-term AAA growth with clinical, serological and anatomical data.
MethodsA total of 148 consecutive asymptomatic infrarenal atherosclerotic AAA patients were included. The following details were recorded: clinical data (age, gender, cardiovascular risk factors, comorbidity, medication), baseline aortic diameter, prospective 1-year AAA growth, and the concentration of MMP-2, MMP-9, cystatin C, alpha1-antitrypsin, myeloperoxidase, MCP-1, homocysteine, D-dimer, PAP and C-reactive protein in peripheral blood at the time of baseline assessment. Predictive models were constructed for 1-year AAA growth assessed as a continuous variable (mm/year) as well as a dichotomic variable (defined as stability, if AAA growth rate was ≤2mm/year, versus expansion, if AAA growth rate was >2mm/year), using simple and multiple linear and logistic regression.
ResultsEvery increase by 1ng/mL in the plasma concentration of D-dimer was related to a mean 1-year increase of 0.0062mm in the AAA growth. Likewise, CRF increased the 1-year prospective AAA growth by a mean of 2.95mm. When AAA growth was assessed as a dichotomic variable, both the increase in the peripheral concentrations of PAP and the presence of chronic renal failure (CRF) increased the risk of AAA expansion (odds ratio [OR]: 1.01 and 14,523.62; 95% confidence interval [CI]: 1.00-1.02 and 0-7.39E+40 respectively).
ConclusionsD-dimer and PAP seem to be promising biomarkers of short-term AAA activity. CRF is an important independent prognostic factor of AAA expansion. The dichotomic classification of AAA growth can be useful in the development of management models and their clinical application.
Actualmente, el diagnóstico y el seguimiento de los pacientes con aneurisma de aorta abdominal (AAA) se realizan mediante la medición seriada del diámetro máximo del AAA con ultrasonografía o tomografía computerizada. Aunque se han identificado algunas variables clínicas que influyen sobre el ritmo de crecimiento aneurismático (la diabetes mellitus, por ejemplo, lo ralentiza y el tabaquismo activo lo acelera1–6), se ha demostrado que la expansión aórtica es en su mayoría discontinua, con periodos de crecimiento y de quiescencia alternándose en patrones erráticos, y que la evolución del AAA a corto y medio plazo en un paciente concreto es impredecible7.
La fisiopatología del AAA es compleja, con participación de procesos inflamatorios de bajo grado, proteolisis, trombogénesis y fibrinólisis, apoptosis y neoangiogénesis, además del estrés biomecánico sobre la pared arterial8,9, que interaccionan de formas aún no del todo conocidas. En los ultimos años se han publicado varios trabajos enfocados en la búsqueda de biomarcadores en sangre periférica de pacientes con AAA, que puedan reflejar diferentes procesos fisiopatológicos del AAA, y que se han asociado con el diámetro y/o el crecimiento de los AAA8,10. Algunos de estos biomarcadores parecen prometedores pero aún se encuentran en fase de experimentación, pendientes de su validación y ulterior aplicación clínica. El hallazgo de un marcador circulante válido o la definición de un modelo predictivo de crecimiento del AAA, probablemente combinando datos anatómicos y biológicos, podría ayudar en el manejo individualizado de los pacientes, estimando el riesgo de expansión y rotura en cada caso concreto, e indicando con mayor precisión la necesidad de una exclusión invasiva del AAA, mejorando los protocolos de seguimiento y el coste-efectividad global del manejo de estos enfermos. Incluso podría servir para monitorizar la respuesta al tratamiento endovascular o a un futuro tratamiento farmacológico de la patología.
Dentro de una línea de investigación más amplia, el objetivo de este trabajo ha sido diseñar, mediante la evaluación de variables clínicas, anatómicas y serológicas en un grupo piloto de pacientes con AAA, un modelo predictivo del diámetro basal de los AAA y otro del crecimiento aneurismático prospectivo a un año.
Material y métodosPacientesSe diseñó un estudio observacional de cohortes prospectivo con un grupo de pacientes con AAA.
Se reclutaron, durante 2 años y de forma consecutiva, pacientes con AAA infrarrenal asintomático diagnosticados y/o seguidos en nuestro centro. Se excluyeron pacientes con: AAA sintomático o inflamatorio; múltiples aneurismas sincrónicos (de aorta torácica, femoral, poplíteo); AAA de otra localización (yuxtarrenal, suprarrenal o toracoabdominal); procesos inflamatorios o infecciosos activos, intervenciones quirúrgicas o traumatismo mayor en los 60 días previos; en tratamiento con medicación antiinflamatoria o inmunosupresora; o rechazo del paciente a ser incluido en el estudio.
El estudio fue aprobado por el Comité de Ética del Hospital de Galdakao-Usansolo y se obtuvo el consentimiento informado de cada paciente.
Variables clínicasSe registraron, de cada paciente, los: datos demográficos (edad, sexo); factores de riesgo cardiovascular (tabaquismo activo, hipertensión arterial, diabetes mellitus, hipercolesterolemia); comorbilidad (cardiopatía, enfermedad pulmonar obstructiva crónica, insuficiencia renal crónica [IRC], enfermedad cerebrovascular e isquemia crónica de extremidades inferiores [IC-EEII]); y medicación, especialmente la toma de estatinas.
Se definió un paciente como: hipertenso cuando ya estaba diagnosticado como tal y tomaba medicación específica o cuando se registró su tensión arterial basal >140/90 de forma repetida; diabético cuando ya había sido diagnosticado y estaba siendo tratado (dieta, antidiabéticos orales, insulina) y seguido, o cuando se encontró una glucemia basal >126mg/dL y/o HbA1c ≥6,5%; e hipercolesterolémico cuando los niveles plasmáticos de colesterol total del paciente eran >200mg/dL y/o LDL >100mg/dL y/o ya estaba diagnosticado y tomaba medicación específica o seguía una dieta supervisada.
La cardiopatía registrada incluía la cardiopatía isquémica (antecedentes de angina, infarto de miocardio y/o revascularización percutánea o mediante bypass coronario), enfermedad valvular y arritmia. Los pacientes etiquetados como EPOC tenían que haber sido diagnosticados por un neumólogo y recibían tratamiento y/o seguimiento específicos. Se definió IRC cuando la concentración de creatinina sérica era ≥1,5mg/dL y/o la tasa de filtración glomerular era <60mL/min/1,73 m2. La enfermedad cerebrovascular incluía los antecedentes de accidente cerebral isquémico transitorio y/o ictus y/o se encontró una estenosis carotídea >50% asintomática en el estudio ecográfico de troncos supraórticos realizado de rutina. La IC-EEII se diagnosticó cuando el paciente refería síntomas isquémicos y mostraba una exploración arterial patológica e índice tobillo-brazo <0,90.
Variables anatómicasLos pacientes con AAA de 3-3,9cm fueron seguidos de forma anual con evaluación clínica y ecografía abdominal (SONOLINE SL-2 ecographer [SIEMENS], transductor de 35MHz), mientras que los pacientes con AAA ≥4cm fueron seguidos con periodicidad semestral y mediante TC abdominopélvica con contraste. Los AAA ≥5cm fueron reparados de forma electiva salvo negativa del paciente o riesgo quirúrgico inasumible. En cada prueba de imagen de control, ecográfica o tomográfica, se midió el diámetro máximo exterior de la pared del AAA, perpendicular al eje aórtico, y en los planos transversal, anteroposterior y lateral, registrando la medida máxima.
Se recogió el diámetro máximo del AAA en el momento del reclutamiento del paciente y su crecimiento en el año siguiente cuando estaba disponible (crecimiento prospectivo del AAA a un año=diámetro máximo del AAA un año después del reclutamiento - diámetro máximo del AAA en el momento del reclutamiento). Se valoró el crecimiento prospectivo a un año como variable continua (mm/año) y como variable dicotómica (estabilidad, si la tasa de crecimiento del AAA era ≤2mm/año, versus expansión, si la tasa de crecimiento del AAA era >2mm/año).
Variables serológicasSe obtuvieron 50mL de sangre periférica de cada paciente en el momento del reclutamiento, después de 12 horas de ayuno. Se seleccionaron varios prometedores potenciales biomarcadores del comportamiento de los AAA, cubriendo el estudio de diferentes procesos fisiopatológicos (proteolisis, oxidación-reducción, quimiotaxis, metabolismo proteico, fibrinólisis, inflamación). Así, se cuantificaron las concentraciones circulantes de: metaloproteasa-2 (MMP-2) (ng/mL) (kit ELISA de human MMP-2 Quantikine, Vitro S.A.), metaloproteasa-9 (MMP-9) (ng/mL) (kit ELISA de human MMP-9/NGAL Complex Quantikine, Vitro S.A.), cistatina C (mg/L) (kit de N-latex Cystatin C, Siemens), alfa1-antitripsina (mg/dL) (N- Anti-A1 antitrypsin, Siemens S.L.), mieloperoxidasa (MPO) (ng/mL) (kit de MPO HumanElisa, Deltaclon S.L.), proteína quimiotáctica de monocitos-1 (MCP-1) (pg/mL) (kit ELISA de MCP-1, Grifols S.A.), homocisteína (mcmol/L) (N-latex HCY, Siemens S.L.), dímero D (ng/mL) (kit ELISA de TECHNOZYM® D-Dimer, Technoclone), complejos plasmina-antiplasmina (PAP) (ng/mL) (kit ELISA de PAP Complex, Technoclone) y proteína C reactiva (PCR) (mg/L) (método immunoturbidimétrico).
Análisis estadísticoSe realizó un análisis estadístico descriptivo, utilizando el número y el porcentaje de pacientes para las variables cualitativas y la media con la desviación estándar (DS) o la mediana con el rango intercuartílico para las variables cuantitativas, según su distribución, normal o no (distribución valorada con el test de Kolmogorov-Smirnov). Se elaboraron modelos predictivos para el diámetro máximo basal de los AAA y para el crecimiento prospectivo a un año, utilizando la regresión lineal y logística, simple y múltiple, y la estrategia de modelización por eliminación (backward). Se incluyeron en los modelos multivariantes todas las variables que obtuvieron valores p<0,2 en los análisis univariantes y se ajustaron de forma sistemática por la edad, el sexo y el tabaquismo activo. Sobre la base de estudios publicados previamente se estimó un tamaño muestral de 50 pacientes para un valor de error α de 0,05 y un poder estadístico β de 90%. Se realizaron los análisis mediante el paquete estadístico SPSS 15.0 (www.spss.com), aceptando como significativo un error p<0,10 en los análisis multivariantes.
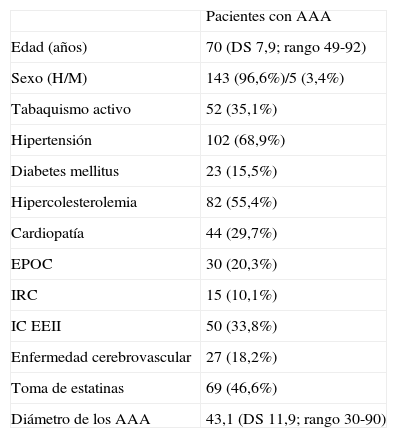
ResultadosSe incluyeron en el estudio 148 pacientes con AAA, 143 (96,6%) de los cuales eran hombres, con una edad media de 70 años (DS 7,9; rango 49-92). Se detallan los datos clínicos de los pacientes en la tabla 1.
Datos clínicos de los pacientes con AAA de la serie (n=148), (factores de riesgo cardiovascular, comorbilidad, medicación, diámetro aórtico)
| Pacientes con AAA | |
| Edad (años) | 70 (DS 7,9; rango 49-92) |
| Sexo (H/M) | 143 (96,6%)/5 (3,4%) |
| Tabaquismo activo | 52 (35,1%) |
| Hipertensión | 102 (68,9%) |
| Diabetes mellitus | 23 (15,5%) |
| Hipercolesterolemia | 82 (55,4%) |
| Cardiopatía | 44 (29,7%) |
| EPOC | 30 (20,3%) |
| IRC | 15 (10,1%) |
| IC EEII | 50 (33,8%) |
| Enfermedad cerebrovascular | 27 (18,2%) |
| Toma de estatinas | 69 (46,6%) |
| Diámetro de los AAA | 43,1 (DS 11,9; rango 30-90) |
H/M=hombre/mujer; EPOC: enfermedad pulmonar obstructiva crónica; IC EEII: isquemia crónica de extremidades inferiores; IRC: insuficiencia renal crónica.
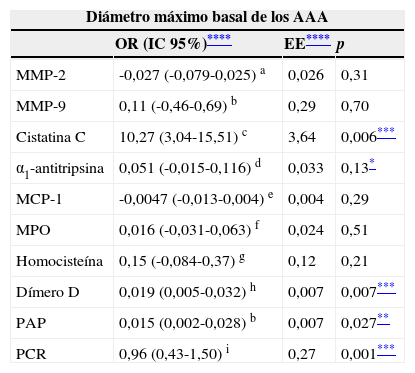
El diámetro medio basal de los AAA era 43,1mm (DS 11,9; rango 30-90). En el análisis univariante se encontró una asociación significativa entre los niveles periféricos de cistatina C, dímero D, PAP y PCR y el diámetro máximo basal de los AAA (tabla 2a). También se halló una asociación directa con el tabaquismo activo e inversa con la coexistencia de IC-EEII. Se detectó una fuerte tendencia a asociar mayor edad de los pacientes con mayor tamaño de sus AAA (tabla 2b). El modelo multivariante confirmó el impacto independiente de las concentraciones de dímero D, PAP y PCR, así como el tabaquismo activo, incrementando el diámetro basal de los AAA, y de la IC-EEII, que se asociaba a diámetros más pequeños de los AAA (tabla 2c). Este modelo explica el 39% del tamaño de los AAA.
Asociación entre las concentraciones periféricas de los diferentes potenciales biomarcadores y el diámetro máximo basal de los AAA–análisis univariante
| Diámetro máximo basal de los AAA | |||
|---|---|---|---|
| OR (IC 95%)**** | EE**** | p | |
| MMP-2 | -0,027 (-0,079-0,025) a | 0,026 | 0,31 |
| MMP-9 | 0,11 (-0,46-0,69) b | 0,29 | 0,70 |
| Cistatina C | 10,27 (3,04-15,51) c | 3,64 | 0,006*** |
| α1-antitripsina | 0,051 (-0,015-0,116) d | 0,033 | 0,13* |
| MCP-1 | -0,0047 (-0,013-0,004) e | 0,004 | 0,29 |
| MPO | 0,016 (-0,031-0,063) f | 0,024 | 0,51 |
| Homocisteína | 0,15 (-0,084-0,37) g | 0,12 | 0,21 |
| Dímero D | 0,019 (0,005-0,032) h | 0,007 | 0,007*** |
| PAP | 0,015 (0,002-0,028) b | 0,007 | 0,027** |
| PCR | 0,96 (0,43-1,50) i | 0,27 | 0,001*** |
EE: error estándar; IC: intervalo de confianza;a n:77; b n: 73; c n:88; d n:139; e n:78; f n:75; g n:135; h n:68; i n:131.
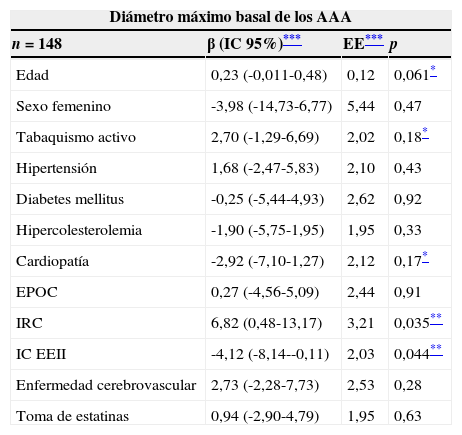
Asociación entre las variables clínicas y el diámetro máximo basal de los AAA–análisis univariante
| Diámetro máximo basal de los AAA | |||
|---|---|---|---|
| n=148 | β (IC 95%)*** | EE*** | p |
| Edad | 0,23 (-0,011-0,48) | 0,12 | 0,061* |
| Sexo femenino | -3,98 (-14,73-6,77) | 5,44 | 0,47 |
| Tabaquismo activo | 2,70 (-1,29-6,69) | 2,02 | 0,18* |
| Hipertensión | 1,68 (-2,47-5,83) | 2,10 | 0,43 |
| Diabetes mellitus | -0,25 (-5,44-4,93) | 2,62 | 0,92 |
| Hipercolesterolemia | -1,90 (-5,75-1,95) | 1,95 | 0,33 |
| Cardiopatía | -2,92 (-7,10-1,27) | 2,12 | 0,17* |
| EPOC | 0,27 (-4,56-5,09) | 2,44 | 0,91 |
| IRC | 6,82 (0,48-13,17) | 3,21 | 0,035** |
| IC EEII | -4,12 (-8,14--0,11) | 2,03 | 0,044** |
| Enfermedad cerebrovascular | 2,73 (-2,28-7,73) | 2,53 | 0,28 |
| Toma de estatinas | 0,94 (-2,90-4,79) | 1,95 | 0,63 |
EE: error estándar; EPOC: enfermedad pulmonar obstructiva crónica; IC: intervalo de confianza; IC EEII: isquemia crónica de extremidades inferiores; IRC: insuficiencia renal crónica.
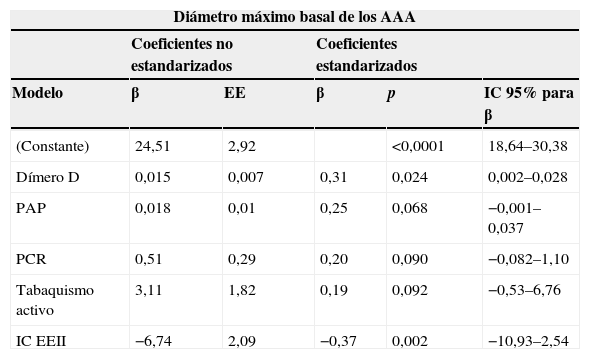
Modelo multivariante para el diámetro máximo basal de los AAA
| Diámetro máximo basal de los AAA | |||||
|---|---|---|---|---|---|
| Coeficientes no estandarizados | Coeficientes estandarizados | ||||
| Modelo | β | EE | β | p | IC 95% para β |
| (Constante) | 24,51 | 2,92 | <0,0001 | 18,64–30,38 | |
| Dímero D | 0,015 | 0,007 | 0,31 | 0,024 | 0,002–0,028 |
| PAP | 0,018 | 0,01 | 0,25 | 0,068 | −0,001–0,037 |
| PCR | 0,51 | 0,29 | 0,20 | 0,090 | −0,082–1,10 |
| Tabaquismo activo | 3,11 | 1,82 | 0,19 | 0,092 | −0,53–6,76 |
| IC EEII | −6,74 | 2,09 | −0,37 | 0,002 | −10,93–2,54 |
| R | R2 | R2 ajustada | EE de la estimación |
|---|---|---|---|
| 0,66 | 0,43 | 0,39 | 6,66 |
EE: error estándar; IC: intervalo de confianza; IC EEII: isquemia crónica de extremidades inferiores.
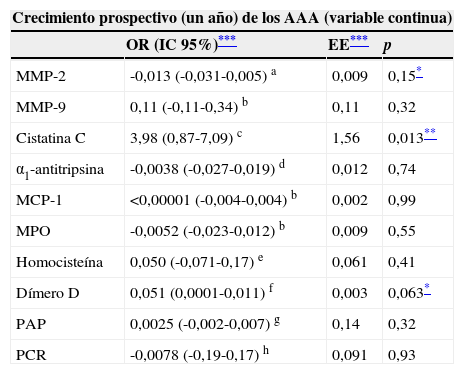
Se pudieron recoger datos del crecimiento prospectivo de 96 AAA. La tasa de crecimiento prospectivo medio a un año fue de 2,7mm (DS 3,2; rango 0-16). Se mantuvieron estables 57 AAA (59,4%) y 39 (40,6%) experimentaron expansión (>2mm/año). En el análisis univariante se encontró una asociación entre las concentraciones circulantes de cistatina C y dímero D con el crecimiento aórtico prospectivo valorado como variable continua (tabla 3a). También se encontró una asociación similar para la IRC (tabla 3b). El modelo multivariante confirmó el impacto independiente de los niveles de dímero D y la IRC sobre mayores tasas de crecimiento aneurismático (tabla 3c). Cuando se analizó el crecimiento del AAA como una variable dicotómica, los niveles periféricos de cistatina C se asociaban de forma significativa con la expansión aórtica, con una tendencia estadística en la misma línea para las concentraciones de PAP, en el análisis univariante (tabla 4a). De nuevo la IRC surgía como el único factor clínico asociado de forma significativa con el crecimiento aórtico (tabla 4b). El modelo multivariante confirmó el impacto independiente de los niveles de PAP y la IRC sobre la expansión de los AAA (tabla 4c).
Asociación entre las concentraciones periféricas de los diferentes potenciales biomarcadores y las tasas de crecimiento prospectivo de los AAA a un año (valorado como una variable continua)–análisis univariante
| Crecimiento prospectivo (un año) de los AAA (variable continua) | |||
|---|---|---|---|
| OR (IC 95%)*** | EE*** | p | |
| MMP-2 | -0,013 (-0,031-0,005) a | 0,009 | 0,15* |
| MMP-9 | 0,11 (-0,11-0,34) b | 0,11 | 0,32 |
| Cistatina C | 3,98 (0,87-7,09) c | 1,56 | 0,013** |
| α1-antitripsina | -0,0038 (-0,027-0,019) d | 0,012 | 0,74 |
| MCP-1 | <0,00001 (-0,004-0,004) b | 0,002 | 0,99 |
| MPO | -0,0052 (-0,023-0,012) b | 0,009 | 0,55 |
| Homocisteína | 0,050 (-0,071-0,17) e | 0,061 | 0,41 |
| Dímero D | 0,051 (0,0001-0,011) f | 0,003 | 0,063* |
| PAP | 0,0025 (-0,002-0,007) g | 0,14 | 0,32 |
| PCR | -0,0078 (-0,19-0,17) h | 0,091 | 0,93 |
EE: error estándar; IC: intervalo de confianza; a n:61; b n: 58; c n:70; d n:86; e n:89; f n:53; g n:56; h n:85.
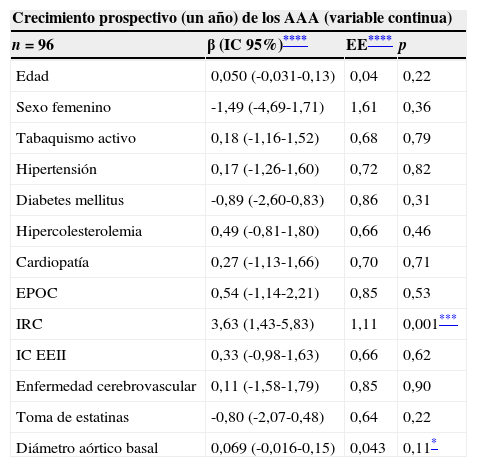
Asociación entre las variables clínicas y el diámetro aórtico basal y las tasas de crecimiento prospectivo de los AAA a un año (valorado como una variable continua)–análisis univariante
| Crecimiento prospectivo (un año) de los AAA (variable continua) | |||
|---|---|---|---|
| n=96 | β (IC 95%)**** | EE**** | p |
| Edad | 0,050 (-0,031-0,13) | 0,04 | 0,22 |
| Sexo femenino | -1,49 (-4,69-1,71) | 1,61 | 0,36 |
| Tabaquismo activo | 0,18 (-1,16-1,52) | 0,68 | 0,79 |
| Hipertensión | 0,17 (-1,26-1,60) | 0,72 | 0,82 |
| Diabetes mellitus | -0,89 (-2,60-0,83) | 0,86 | 0,31 |
| Hipercolesterolemia | 0,49 (-0,81-1,80) | 0,66 | 0,46 |
| Cardiopatía | 0,27 (-1,13-1,66) | 0,70 | 0,71 |
| EPOC | 0,54 (-1,14-2,21) | 0,85 | 0,53 |
| IRC | 3,63 (1,43-5,83) | 1,11 | 0,001*** |
| IC EEII | 0,33 (-0,98-1,63) | 0,66 | 0,62 |
| Enfermedad cerebrovascular | 0,11 (-1,58-1,79) | 0,85 | 0,90 |
| Toma de estatinas | -0,80 (-2,07-0,48) | 0,64 | 0,22 |
| Diámetro aórtico basal | 0,069 (-0,016-0,15) | 0,043 | 0,11* |
EE: error estándar; IC: intervalo de confianza; EPOC: enfermedad pulmonar obstructiva crónica; IRC: insuficiencia renal crónica; IC EEII: isquemia crónica de extremidades inferiores.
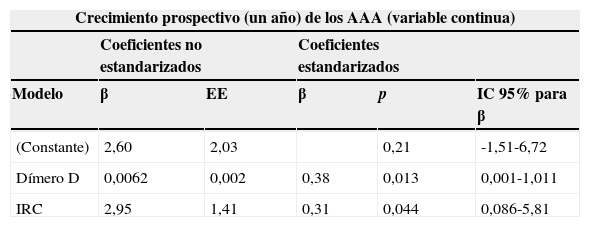
Modelo multivariante para el crecimiento prospectivo de los AAA a un año (valorado como una variable continua)
| Crecimiento prospectivo (un año) de los AAA (variable continua) | |||||
|---|---|---|---|---|---|
| Coeficientes no estandarizados | Coeficientes estandarizados | ||||
| Modelo | β | EE | β | p | IC 95% para β |
| (Constante) | 2,60 | 2,03 | 0,21 | -1,51-6,72 | |
| Dímero D | 0,0062 | 0,002 | 0,38 | 0,013 | 0,001-1,011 |
| IRC | 2,95 | 1,41 | 0,31 | 0,044 | 0,086-5,81 |
| R | R2 | R2 ajustada | EE de la estimación |
|---|---|---|---|
| 0,51 | 0,26 | 0,20 | 2,33 |
EE: error estándar; IC: intervalo de confianza; IRC: insuficiencia renal crónica.
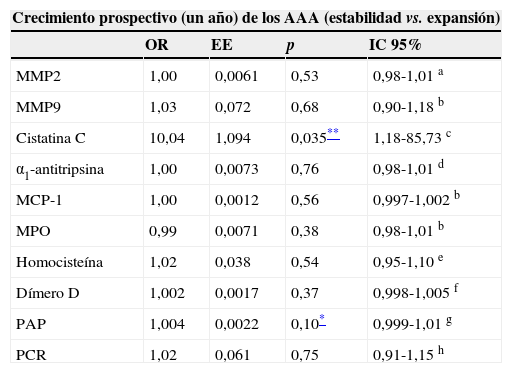
Asociación entre las concentraciones periféricas de los diferentes potenciales biomarcadores y las tasas de crecimiento prospectivo de los AAA a un año (valorado como una variable dicotómica)–análisis univariante
| Crecimiento prospectivo (un año) de los AAA (estabilidad vs. expansión) | ||||
|---|---|---|---|---|
| OR | EE | p | IC 95% | |
| MMP2 | 1,00 | 0,0061 | 0,53 | 0,98-1,01 a |
| MMP9 | 1,03 | 0,072 | 0,68 | 0,90-1,18 b |
| Cistatina C | 10,04 | 1,094 | 0,035** | 1,18-85,73 c |
| α1-antitripsina | 1,00 | 0,0073 | 0,76 | 0,98-1,01 d |
| MCP-1 | 1,00 | 0,0012 | 0,56 | 0,997-1,002 b |
| MPO | 0,99 | 0,0071 | 0,38 | 0,98-1,01 b |
| Homocisteína | 1,02 | 0,038 | 0,54 | 0,95-1,10 e |
| Dímero D | 1,002 | 0,0017 | 0,37 | 0,998-1,005 f |
| PAP | 1,004 | 0,0022 | 0,10* | 0,999-1,01 g |
| PCR | 1,02 | 0,061 | 0,75 | 0,91-1,15 h |
EE: error estándar; IC: intervalo de confianza; a n:61; b n: 58; c n:70; d n:86; e n:89; f n:53; g n:56; h n:85.
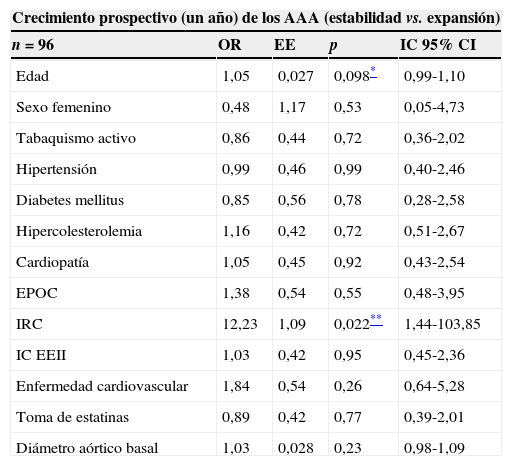
Asociación entre las variables clínicas y el diámetro aórtico basal y las tasas de crecimiento prospectivo de los AAA a un año (valorado como una variable dicotómica)–análisis univariante
| Crecimiento prospectivo (un año) de los AAA (estabilidad vs. expansión) | ||||
|---|---|---|---|---|
| n=96 | OR | EE | p | IC 95% CI |
| Edad | 1,05 | 0,027 | 0,098* | 0,99-1,10 |
| Sexo femenino | 0,48 | 1,17 | 0,53 | 0,05-4,73 |
| Tabaquismo activo | 0,86 | 0,44 | 0,72 | 0,36-2,02 |
| Hipertensión | 0,99 | 0,46 | 0,99 | 0,40-2,46 |
| Diabetes mellitus | 0,85 | 0,56 | 0,78 | 0,28-2,58 |
| Hipercolesterolemia | 1,16 | 0,42 | 0,72 | 0,51-2,67 |
| Cardiopatía | 1,05 | 0,45 | 0,92 | 0,43-2,54 |
| EPOC | 1,38 | 0,54 | 0,55 | 0,48-3,95 |
| IRC | 12,23 | 1,09 | 0,022** | 1,44-103,85 |
| IC EEII | 1,03 | 0,42 | 0,95 | 0,45-2,36 |
| Enfermedad cardiovascular | 1,84 | 0,54 | 0,26 | 0,64-5,28 |
| Toma de estatinas | 0,89 | 0,42 | 0,77 | 0,39-2,01 |
| Diámetro aórtico basal | 1,03 | 0,028 | 0,23 | 0,98-1,09 |
EE: error estándar; IC: intervalo de confianza; EPOC: enfermedad pulmonar obstructiva crónica; IRC: insuficiencia renal crónica; IC EEII: isquemia crónica de extremidades inferiores.
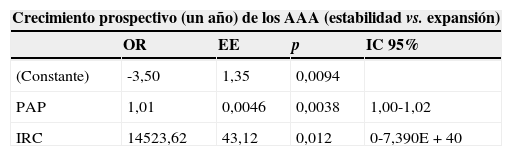
Modelo multivariante para el crecimiento prospectivo de los AAA a un año (valorado como una variable dicotómica)
| Crecimiento prospectivo (un año) de los AAA (estabilidad vs. expansión) | ||||
|---|---|---|---|---|
| OR | EE | p | IC 95% | |
| (Constante) | -3,50 | 1,35 | 0,0094 | |
| PAP | 1,01 | 0,0046 | 0,0038 | 1,00-1,02 |
| IRC | 14523,62 | 43,12 | 0,012 | 0-7,390E+40 |
| Chi cuadrado | p |
|---|---|
| 15,03 | 0,0005 |
EE: error estándar; IC: intervalo de confianza; IRC: insuficiencia renal crónica.
Varios trabajos han correlacionado positivamente las concentraciones de dímero D y PAP con el diámetro de los AAA y con el volumen de trombo mural, incluido un metaanálisis publicado en 200911–15. En el presente trabajo se confirma esta asociación, evidenciando una vez más el papel de la cascada de coagulación-fibrinólisis en la fisiopatología de los AAA. También se ha demostrado repetidamente la presencia de inflamación de bajo grado en el proceso de degeneración aneurismática, con afectación sistémica y manifestación en sangre periférica cuantificable en los niveles, habitualmente elevados, de PCR. Así, varios autores han descrito asociaciones entre las concentraciones plasmáticas de PCR y el diámetro de los AAA asintomáticos en sus respectivas series con indices de correlación r entre 0,48 y 0,7116–19, resultados con los que concuerdan nuestros hallazgos. Sin embargo, la PCR no consigue demostrar una asociación consistente con las tasas de expansion aórtica16,20,21.
El tabaquismo es un factor de riesgo claramente asociado a la aparición y la progresión de los AAA3,5,6,20, y que se asocia a una mayor liberación de elastasa por los neutrófilos circulantes22. Se asocia también de forma significativa con el diámetro basal de los AAA. En nuestro centro se realiza un cribado sistemático de AAA en los pacientes con IC-EEII ya que se demostró que presentan un riesgo aumentado de desarrollar dilatación aórtica, con una prevalencia descrita en nuestra área sanitaria del 13%, la mayoría con AAA <4cm23. Así, un tercio de los pacientes de la presente serie sufrían de IC-EEII, y se estableció una asociación inversa significativa entre la IC-EEII y el diámetro basal de los AAA.
La búsqueda de una asociación entre un biomarcador circulante o una característica clínica o anatómica y el diámetro de los AAA obedece al interés en demostrar una relación de aquel con el espectro de la enfermedad y su fisiopatología. Pero no se debe olvidar que la expansión aórtica es mayoritariamente discontinua, por lo que AAA con igual diámetro pueden presentar niveles de actividad muy diferentes, según se encuentren en un periodo de crecimiento o latencia, lo que repercutirá en los niveles del biomarcador en cuestión. Por ello, las asociaciones de nuestro modelo predictivo, y las descritas en otros artículos previos, son difíciles de interpretar y será el análisis con el crecimiento el que ofrezca datos más relevantes y concluyentes.
Los niveles circulantes de DD y PAP se han asociado de forma independiente con el crecimiento prospectivo a corto plazo de los AAA en nuestro modelo multivariante, resultados que coinciden con un trabajo reciente de Golledge, en el que describe una asociación independiente de las concentraciones plasmáticas de dímero D con la expansión aneurismática media en un seguimiento prospectivo de 5,5 años en una cohorte australiana (β=0,29; p<0,001)11. Lindholt correlacionó los niveles circulantes de PAP con las tasas de crecimiento aneurismático anual (r=0,39; IC 95% 0,16-0,56; p<0,001) y con la probabilidad de alcanzar un tamaño quirúrgico, incluso después de ajustar el modelo por el diámetro aórtico basal, la edad y el tabaquismo24. Las concentraciones de dímero D y de PAP parecen cumplir los criterios de Hill en su asociación con la fisiopatología de los AAA: asociación estadística, consistencia en diferentes estudios y poblaciones, secuencia temporal, efecto dosis-respuesta, especificidad y un mecanismo biológico plausible. Es posible que los niveles plasmáticos de DD y/o PAP incluyan otros ori¿genes diferentes al AAA, pero la asociacio¿n de estas concentraciones circulantes con la historia natural de los AAA pequen¿os ha sido la más consistente descrita hasta el momento.
Las concentraciones circulantes de cistatina C se asocian con el crecimiento prospectivo a corto plazo de los AAA en el análisis univariante, valorado el crecimiento tanto como variable continua como dicotómica, pero la asociación pierde su significación estadística cuando se introduce en un modelo multivariante. En contraste, la IRC emerge como el factor predictivo independiente más importante de expansión aórtica. Esto podría explicarse teniendo en cuenta que la cistatina C es un marcador de la función renal y no solo del proceso inflamatorio vascular. Lindholt describió una asociación independiente de los niveles de cistatina C con las tasas de expansión aneurismática anual (r=-0,24; IC 95% -0,75- -0,05) y sugirió, como possible explicación a sus hallazgos, que la correlación se podía deber a una posible inhibición extracellular de proteasas20. Adicionalmente, la sensibilidad y especificidad de la concentración sérica de cistatina C para la predicción de la expansión aórtica hasta un tamaño quirúrgico (≥5cm) era, en este estudio, de 61 y 57% respectivamente, inferior al valor predictivo del diámetro aórtico aislado (sensibilidad y especifidad de 81 y 81% respectivmente), lo que resta aplicabilidad clínica al hallazgo. En nuestra serie, la cistatina C parece reflejar la disfunción renal de forma más precisa que la actividad inflamatoria aórtica y parece ligar su valor pronóstico para la evolución de los AAA y su eventual aplicabilidad a su reflejo de la IRC. Esto podría ayudar a explicar las diferencias de nuestros hallazgos con los de Lindholt.
El tabaquismo activo se ha asociado repetidamente con crecimiento aneurismático más acelerado, y la diabetes mellitus con mayor estabilidad de los AAA1,11,20,25. Estas asociaciones no se han observado en nuestros modelos. Es posible que se deba a que su impacto se produce en la evolución a medio y largo plazo, sin que sea evidente en periodos cortos de observación. La IRC, por contra, surge repetidamente como un importante factor de riesgo para la progresión de los AAA en varios estudios realizados en nuestro centro a lo largo de la última década2. A la luz de nuestros resultados, consideramos que la IRC es un importante y subestimado factor clínico de riesgo de progresión de los AAA. La prevalencia de la IRC entre los pacientes con AAA es bajo, de alrededor del 10%, pero marca un grupo de alto riesgo, tanto en un mayor riesgo de progresión y rotura del AAA como en un riesgo quirúrgico incrementado.
Se considera, en la práctica clínica actual, que el diámetro máximo del AAA es el factor predictivo de riesgo de rotura más fiable26, y las decisiones terapéuticas se basan fundamentalmente en él. Las tasas de crecimiento aneurismático anuales aumentan con el diámetro aórtico2,27, pero no dejan de ser el resultado de estimaciones lineales prácticas de la expansion aórtica media en cohortes de gran tamaño, mientras que el crecimiento de los AAA es mayoritariamente discontinuo7. Una aproximación al crecimiento aórtico por simple regresión lineal sobrestima la tasa de crecimiento en hasta un 29%27,28. El diámetro de los AAA tiene influencia sobre la evolución a medio y largo plazo pero no necesariamente sobre su comprotamiento a corto plazo, como se pone de manifiesto en este trabajo.
Limitaciones del estudioSe diseñó el estudio como un proyecto piloto, encaminado a definir modelos predictivos iniciales e identificar las variables más prometedoras, que se pondrían a prueba en futuras cohortes a gran escala. Por tanto, el tamaño muestral es limitado y los resultados deben interpretarse con precaución. Además, el modelo predictivo ajustado que hemos obtenido para el crecimiento prospectivo de los AAA, valorado como variable continua, solo obtiene un coeficiente R2 de 26%. Por lo tanto, existe una importante variabilidad en la expansión prospectiva de los AAA que no explica el modelo propuesto. Dada la irregularidad previamente descrita para el comportamiento de los AAA7, será inevitable asumir cierto grado de azar en cualquier modelo predictivo que se pueda definir, pero es evidente que faltan en nuestro modelo otras variables que lo completen y afinen. Además, los factores predictivos que sugerimos deben ser validados en otras series de mayor tamaño.
Los protocolos de seguimiento utilizados en esta cohorte, con control ecográfico de los AAA más pequeños, y tomográfico para aquellos más cercanos a tamaños quirúrgicos, reflejan la práctica clínica habitual. Aunque las mediciones ecográficas conllevan un riesgo de variabilidad de unos ±2mm respecto del CT29, no resultaría ético, desde el punto clínico, dada la radiación acumulada a la que se sometería a los pacientes, ni económico, practicar un CT a todos los pacientes con AAA <4cm en cada control. Además, se garantizaba a los pacientes que el hecho de verse incluidos en el estudio no modificaría su atención sanitaria habitual. Por todo ello, se unieron las mediciones ecográficas y tomográficas en los análisis. Teniendo en cuenta el potencial margen de error de las mediciones ecográficas, se realizaron los análisis adicionales sobre el crecimiento prospectivo de los AAA valorado como una variable dicotómica, considerando expansión con un aumento del diámetro de los AAA >2mm/año, según se describe en la metodología.
Los resultados obtenidos permiten concluir que las concentraciones plasmáticas de dímero D, PAP y PCR y el tabaquismo activo se asocian de forma directa e independiente con el diámetro de los AAA, mientras que la IC-EEII lo hace de forma inversa. Las concentraciones plasmáticas de dímero D y PAP constituyen prometedores biomarcadores predictivos de la expansión prospectiva de los AAA, asociándose de forma independiente con la tasa de crecimiento y la progresión neta, respectivamente, en el año siguiente a su cuantificación. La IRC parece ser un importante factor clínico pronóstico de expansión aórtica. Nuestros hallazgos deben ser validados en series de mayor tamaño y queda por definir un valor de corte en las concentraciones periféricas de las proteínas propuestas como biomarcadores. Consideramos útil la clasificación del crecimiento de los AAA como una variable dicotómica, estabilidad versus progresión, con mayor facilidad para su traslado a la práctica clínica en modelos de decisión.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciaciónBecas de investigación del Departamento de Sanidad del Gobierno Vasco (N.° Exp. 2008111019), SAF 2010-21852 y la Unión Europea (HEALTH F2-2008-200647).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Los autores agradecen a los Dres. S. García and U. Aguirre su revisión de la metodología y los análisis estadísticos de este trabajo, y a los Dres. N. de la Fuente, B. Viviens, M. Izagirre y E. Bravo por su ayuda en el reclutamiento de pacientes y la recogida de datos clínicos.
Este trabajo describe una parte de la Tesis Doctoral de la Dra. M. Vega de Ceniga, que ganó el Premio Abbott a la Mejor Tesis Doctoral del año 2013, otorgado por la SEACV.