El objetivo de este estudio es evaluar la seguridad de la endarterectomía carotídea (EAC) en pacientes sintomáticos y asintomáticos en nuestro servicio.
Pacientes y métodosEste estudio retrospectivo incluye un total de 266 procedimientos realizados en pacientes tanto sintomáticos como asintomáticos, con carácter programado. La seguridad se evaluó en términos de tasa de ictus/muerte e infarto agudo de miocardio (IAM) perioperatorio.
ResultadosEntre enero de 2005 y diciembre de 2012 se realizaron 266 EAC en 238 pacientes. La tasa de ictus/muerte global a los 30 días de la cirugía fue del 3%, siendo la de pacientes sintomáticos de un 4,5% y la de asintomáticos un 2,8%. Se observó un mayor riesgo de sangrado en pacientes tratados previamente con clopidogrel (OR: 3,85; IC: 1,05-11).
ConclusionesAtendiendo a los criterios de calidad necesarios para realizar una EAC podemos concluir que, en nuestro servicio, este procedimiento es seguro y garantiza sus ventajas terapéuticas.
The aim of this study is to assess the safety of carotid endarterectomy (CEA) in symptomatic and asymptomatic patients in our department.
Patients and methodsThis retrospective study included a total of 266 programmed procedures performed in both symptomatic and asymptomatic patients. Safety was evaluated in terms of perioperative rate of stroke/death and acute myocardial infarction (AMI).
ResultsBetween January 2005 and December 2012, 266 CEAs were performed in 238 patients. The overall rate of stoke/death at 30 days after surgery was 3%, 4,5% in symptomatic patients and 2,8% in the asymptomatic cohort. An increased risk of bleeding was observed in patients previosly treated with clopidogrel (OR: 3,85 CI 1,5-11).
ConclusionsConsidering the quality criteria required to perform a carotid endarterectomy we can conclude that in our department, this procedure is safe and ensures its therapeutic benefits.
El beneficio de la endarterectomía carotídea (EAC) para el tratamiento de estenosis sintomáticas moderadas o graves ha quedado demostrado en diversos estudios aleatorizados, desde el North American Symptomatic Carotid Endarterectomy Trial (NASCET) y el European Carotid Surgery Trial (ECST) hasta el más reciente Carotid Revascularization Endarterectomy Versus Stenting Trial (CREST), quedando el tratamiento endovascular reservado para pacientes con alto riesgo quirúrgico, o con características anatómicas de la lesión que dificultan la cirugía abierta1–9.
En los pacientes sintomáticos la indicación de la cirugía está más consensuada. Sin embargo, las estenosis asintomáticas constituyen una indicación más restringida, a pesar de que implican un riesgo de infarto cerebral. Existen estudios, como el ACAS10, el ACST11 y el ACST-112 que han demostrado los beneficios de la cirugía en términos de reducción del riesgo de accidente isquémico transitorio (AIT), de ictus no discapacitante y también de ictus fatal cuando la estenosis es de al menos un 70%1,8,9,13.
La EAC no está exenta de complicaciones, ya que estos pacientes pueden experimentar un ictus, infarto de miocardio (IM) o muerte durante el período perioperatorio, entre otras complicaciones. En uno de los ensayos del CREST publicado en el 20102 concluyen que la EAC es una técnica efectiva y segura y, aunque tiene mayor tasa de IM que el tratamiento endovascular, el riesgo de ictus es superior en este último y, además, ejerce mayor efecto sobre la calidad de vida del paciente. Por ello, se puede realizar siempre que se asegure una baja tasa de morbimortalidad (<6% en pacientes sintomáticos y <3% en asintomáticos) y en pacientes con una esperanza de vida >5 años en quienes se prevé que modifique su longevidad y calidad de vida con respecto al manejo conservador1,8,9,13.
Probablemente la EAC es la intervención quirúrgica que más se ha sometido al análisis de su seguridad y eficacia en el marco de ensayos clínicos aleatorizados. Es por ello, y debido al elevado volumen de cirugías de este tipo realizadas en nuestro servicio, por lo que hemos querido valorar sus resultados.
ObjetivoEvaluar la seguridad de la EAC realizada en nuestro servicio mediante la valoración de la tasa de ictus/muerte y de IM perioperatorio (en los primeros 30 días tras la intervención).
Pacientes y métodosRealizamos un estudio retrospectivo, observacional, que incluyó a todos los pacientes tratados mediante EAC entre enero de 2005 y diciembre de 2012 en el Servicio de Angiología y Cirugía Vascular de un hospital de tercer nivel, con una población adscrita de hasta 338.961 habitantes mayores de 14 años, centro de referencia provincial para esta especialidad. Se revisaron 266 cirugías, en pacientes tanto sintomáticos como asintomáticos, con carácter programado. Los datos se obtuvieron mediante la revisión de historias clínicas y se diseñó una base de datos específica del estudio.
De cada paciente se recogieron las siguientes variables:
- -
Demográficas: sexo y edad.
- -
Antecedentes personales: tabaquismo, hipertensión arterial, diabetes mellitus, dislipidemia, cardiopatía isquémica (CI), AIT o ictus, síndrome de isquemia crónica (SIC) o insuficiencia renal.
- -
Relacionadas con el diagnóstico: motivo de diagnóstico, prueba de imagen, TAC craneal preoperatorio, porcentaje de estenosis, cirugía bilateral (cuánto tiempo transcurrió hasta que se intervino la carótida contralateral), antiagregación o anticoagulación previa a la cirugía y estenosis sintomática o asintomática.
- -
Relacionadas con la cirugía: uso de shunt, cierre directo o con parche, necesidad de transfusión posterior, riesgo quirúrgico según la clasificación American Society of Anesthesiologists (ASA) y complicaciones y estancia postoperatoria.
- -
Seguimiento: fecha de última revisión, ecodoppler y exploración.
Consideramos sintomáticos a aquellos pacientes con un AIT o ictus no discapacitante, definido este como un déficit neurológico focal, de instauración aguda y de menos de 24 h de duración, que no conduce a una discapacidad para las actividades de la vida diaria. Estos fueron principalmente remitidos por el Servicio de Neurología, donde ingresaban tras un evento neurológico y se les realizaba una TC craneal, un ecocardiograma para descartar un origen embolígeno, y un ecodoppler de troncos supraórticos para determinar la presencia de aterotrombosis carotídea que justificara la clínica. Se solicitó en la mayoría de los casos una arteriografía para la confirmación de la estenosis. En estos casos el paciente fue intervenido en las primeras 2 semanas tras el evento.
Por su parte los asintomáticos o fueron diagnosticados a través del programa de screening instaurado desde 2005 en la consulta externa y que consiste en realizar un ecodoppler de troncos supraaórticos a todos los pacientes con SIC o enfermedad aneurismática, o fueron identificados en el estudio de un cuadro neurológico de la carótida contralateral o en territorio no carotídeo.
Una vez diagnosticada la estenosis se instauró el mejor tratamiento médico, basado en antiagregantes y estatinas, que disminuyen la progresión de la enfermedad, así como la tasa de ictus, IM y muerte2,8,9. En aquellos pacientes candidatos a revascularización, se completó el estudio mediante una prueba de imagen (arteriografía, angio-TC o angio-RMN), así como una TC craneal y una valoración neurológica. En los pacientes con antecedentes de CI o clínica compatible con ella, se realizó un SPECT-MIBI, según lo acordado con los servicios de Cardiología y Anestesiología.
La cirugía se realiza bajo anestesia general (excepto en pacientes de muy alto riesgo), con monitorización mediante pulsioximetría, electrocardiograma y tensión arterial (TA) invasiva y la monitorización cerebral para la identificación de isquemia cerebral se realiza a través del Bispectral Index (BIS) y el Near Infrared Reflectance Spectroscopy (NIRS). El shunt se utiliza selectivamente, en casos de oclusión de la ACI contralateral o una presión retrógrada de la ACI inferior a 50mmHg, mientras que el cierre de forma directa o mediante parche (en cuyo caso era siempre sintético de dacron) se deja a elección del cirujano. En todos los casos se administra heparina intravenosa previamente al pinzamiento y se revierte con protamina (1/1)14. Las primeras 24 h permanecen en el Servicio de Anestesiología y Reanimación para un control estricto de la TA y vigilancia de sangrado u otras complicaciones. Tras el alta, se realiza control ecográfico al mes, 6, 12 meses y luego anualmente.
Para el análisis estadístico se utilizó la versión 15.0 del SPSS y el nivel de significación se estableció para una α = 0,05. Para las variables cuantitativas se analizaron los índices de centralización y dispersión: media aritmética y desviación típica. Para las cualitativas se analizó la frecuencia absoluta y las frecuencias relativas. Una vez comprobada la normalidad de las variables con el test de Kolmogorov-Smirnoff, se aplicó el chi cuadrado y la corrección de Fisher en caso de que fuera necesario. Para comparar las diferencias medias se utilizó la t de Student si las variables seguían una distribución normal; si no, la U de Mann Whitney.
ResultadosSe realizaron 266 EAC en 238 pacientes. La tabla 1 resume las características demográficas de los pacientes y sus diferencias entre la población sintomática y asintomática. Hasta un 10% de los pacientes tenían 80 años o más (de los cuales el 53,8% eran asintomáticos y el 46,2% sintomáticos). El 64,6% fueron clasificados como un riesgo III según la clasificación ASA y un 19,4% como un ASA IV. El 66,2% de las carótidas intervenidas fueron asintomáticas, de las cuales el 19,3% fueron derivadas desde Neurología, al identificarse en el estudio de pacientes sintomáticos de la ACI contralateral o por un ictus en territorio no carotídeo; el 74,3% fueron diagnosticadas gracias al programa de screening; de estas últimas, el 72,7% fue identificada desde la primera ecografía, mientras que el 27,3% restante progresó a pesar del mejor tratamiento médico en una media de 34 meses. El 6,4% restante fue diagnosticado por otros motivos, como en el estudio de síncopes o mareos, soplo cervical u otras causas. De las sintomáticas, el 43,3% se manifestó como un AIT y el 56,7% como un ictus. El 55,3% del total de pacientes presentaban una estenosis entre un 90 y un 99%, el 40,2% entre un 70 y un 89% y el 4,1% entre el 50 y el 69%; se intervino un caso de estenosis <50%. Un total de 17 pacientes presentaban una carótida única y en 51 casos se realizó un procedimiento bilateral.
Diferencias en las características demográficas de pacientes sintomáticos y asintomáticos
| Sintomáticas | Asintomática | ||||
|---|---|---|---|---|---|
| Caract demográficas | n | % | n | % | p |
| Edad en años | 68 (59,6-77,6) | 00 | 69,2 (61,1-73,3) | 0,5 | |
| Sexo | |||||
| Hombre | 60 | 75,9 | 133 | 84,2 | 0,1 |
| Mujer | 19 | 24,1 | 25 | 15,8 | |
| FRCV | |||||
| Tabaquismo | 28 | 35,4 | 52 | 32,9 | 0,7 |
| Hipertensión | 58 | 73,4 | 125 | 79,1 | 0,3 |
| Diabetes | 36 | 45,6 | 91 | 57,6 | 0,08 |
| Dislipidemia | 44 | 55,7 | 110 | 69,6 | 0,03 |
| AIT | 9 | 11,4 | 12 | 7,6 | 0,3 |
| ACV | 15 | 19,0 | 20 | 12,7 | 0,2 |
| IAM | 31 | 39,2 | 49 | 31,0 | 0,2 |
| SIC MMII | 18 | 22,8 | 69 | 43,7 | 0,02 |
| IRC | 11 | 13,9 | 25 | 15,8 | 0,7 |
| ASA | |||||
| I | 1 | 1,3 | 0 | 0 | |
| II | 12 | 15,2 | 25 | 15,8 | 0,5 |
| III | 50 | 63,3 | 103 | 65,2 | |
| IV | 16 | 20,3 | 30 | 19,0 | |
ACV: accidente cerebrovascular; AIT: accidente isquémico transitorio; ASA: American Society of Anesthesiologist; FRCV: factores de riesgo cardiovascular; IAM: infarto agudo de miocardio; IRC: insuficiencia renal crónica; SIC MMII: síndrome de isquemia crónica de miembros inferiores.
En cuanto al procedimiento, el 20,3% de las intervenciones se realizó con el paciente doblemente antiagregado (de las cuales hasta el 77,5% presentaban antecedentes de IM), el 9% se encontraban anticoagulados y el resto tomaban un solo antiagregante (el 42,3% AAS y el 29,2% clopidogrel). Los antiagregantes no se suspendieron, mientras que la anticoagulación se suspendió la noche previa a la cirugía. Se utilizó shunt en el 47,7% de los casos y se realizó cierre con parche en el 74,4%. Durante el postoperatorio inmediato presentaron sangrado (definido como aquel que requiriera transfusión o reintervención) 18 pacientes (6,8%), de los cuales 13 se reintervinieron para hemostasia y evacuación del hematoma; de los que sufrieron esta complicación, el 78,6% tomaban clopidogrel. Se observó una relación estadísticamente significativa entre el tratamiento previo con clopidogrel en monoterapia y el riesgo de sangrado posquirúrgico (OR: 3,85; IC: 1,05-11); sin embargo, no fue así en el caso de la doble antiagregación. Tampoco se asoció de forma significativa el sangrado al riesgo de ictus ni muerte perioperatoria. Con respecto a la afectación de pares craneales, hubo 16 casos (6%) de paresia del ramo bucal del nervio facial, 10 de hipogloso (3,8%) y 2 de disfonía por lesión del recurrente (0,8%), recuperándose todos ellos de forma completa. En ningún caso se infectó la herida quirúrgica.
La estancia media postoperatoria fue de 3,6 (±2,8) días, excluyéndose a aquellos pacientes que fallecieron antes de ser dados de alta, y a los que se les realizó algún procedimiento de revascularización de miembros inferiores en el mismo ingreso y que tuvieron, por tanto, una estancia más larga no justificada por la EAC.
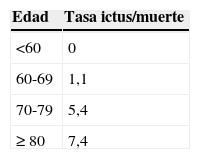
La tasa de ictus/muerte global a los 30 días tras la cirugía fue del 3,3% (9 casos), siendo la de pacientes sintomáticos de 4,5% y la de asintomáticos de 2,8%; no obstante, el ser sintomático no se asoció de forma significativa al riesgo de ictus/muerte (p=0,2). El 40% (2 pacientes) de los fallecidos pertenecían a la cohorte de octogenarios. En las tablas 2 y 3 se resumen la tasa de ictus/muerte y la clasificación ASA según los rangos de edad, respectivamente. Se observa un aumento progresivo del riesgo de ictus y muerte a medida que aumenta la edad del paciente, alcanzando una tasa del 7,4% en los pacientes ≥80 años. Sin embargo, se trata de una tendencia, ya que no se observó una relación estadísticamente sgnificativa (p=0,1) entre la edad y el riesgo de ictus o muerte. Por otro lado, la mayoría de pacientes con un ASA IV correspondieron al grupo de los 70-79 años, seguido del grupo de los 60-69 años. Por tanto, deducimos que en nuestra serie influye más la edad que la comorbilidad en la tasa de ictus/muerte. Hubo un total de 5 muertes, en 2 de las cuales no se llegó a conocer la causa ya que sucedieron en el domicilio tras el alta; otro paciente sufrió una parada cardiorrespiratoria 2 días tras la cirugía, falleciendo por probable causa cardiológica (era portador de un DAI). Otro paciente sufrió un ictus intraoperatorio, falleciendo ese mismo día; otro fue intervenido de urgencia durante el postoperatorio inmediato, realizándose resección de un aneurisma de aorta abdominal y bypass aortobifemoral y aortorrenal izquierdo por una isquemia aguda de miembro inferior derecho, con mala evolución postoperatoria, falleciendo el día después de la cirugía abdominal. Hubo un total de 3 casos documentados de IAM y 5 casos de ictus, de los cuales 2 fueron AIT y 3 ictus, todos ellos recuperados ad integrum excepto el paciente descrito previamente.
El seguimiento se realizó mediante ecodoppler al mes, 6, 12 meses y después anualmente. Se diagnosticaron 12 casos de reestenosis, lo que supone un 4,5%, pero solo una (0,38%) fue hemodinámicamente significativa (considerando significativa una estenosis ≥70%), y solo esta se reintervino. Todas fueron asintomáticas por lo que, excepto esta última, fueron manejadas de forma conservadora, ya que actualmente nuestro criterio es reintervenir únicamente aquellas que producen clínica o las estenosis preoclusivas; al resto se les realiza un control ecográfico para vigilar su posible progresión. De las 12 reestenosis, 7 fueron cerradas mediante parche (lo que supone el 3,5% de todas las que se cerraron con parche) y 5 por cierre directo (suponiendo esto el 7,4% de las cerradas de forma directa); sin embargo, no se observó diferencia estadísticamente significativa entre la tasa de reestenosis y las 2 formas de cierre de la arteriotomía (p=0,08). En cuanto al momento del diagnóstico, solo 3 se identificaron en los primeros 6 meses tras la cirugía, otros 3 en el primer año, y los 6 restantes pasado este tiempo, predominando, por tanto, la progresión de la enfermedad como causa principal de reestenosis.
DiscusiónLos beneficios de la EAC en casos seleccionados de pacientes con estenosis de alto grado sintomática o asintomática han quedado demostrados en distintos estudios americanos y europeos, constituyendo el método más eficaz para disminuir la probabilidad de un ACV a corto y largo plazo. Sin embargo, se ha visto que este beneficio disminuye a medida que aumenta el riesgo quirúrgico y la edad del paciente, siendo una de las decisiones más controvertidas los casos de pacientes octogenarios1–9. Aunque distintos estudios15-20 han demostrado que este grupo de pacientes puede ser tratado mediante una EAC de forma segura, en nuestro servicio observamos un aumento progresivo de la tasa de ictus/muerte a medida que aumenta la edad del paciente, alcanzando un 7,4% en paciente octogenarios. Este resultado nos ha hecho replantear la indicación de esta cirugía en esta cohorte de pacientes, de forma que creemos que estaría indicada en casos muy seleccionados, cumpliendo estrictamente la recomendación de las guías de presentar una esperanza de vida superior a los 5 años.
En cuanto a la antiagregación previa a la cirugía, se observó que aquellos pacientes que tomaban clopidogrel previamente presentaban mayor riesgo de sangrado posquirúrgico de forma significativa. Según los resultados del estudio CAPRIE21, que demostraron la superioridad del clopidogrel frente a la aspirina en la prevención de eventos isquémicos, creemos que los pacientes con aterotrombosis a cualquier nivel deberían tomar preferentemente este medicamento, pero previamente a la cirugía carotídea debería ser sustituido por la aspirina, y ser reintroducido en el postoperatorio inmediato.
Nuestra tasa de reestenosis se sitúa en un 4,5%, pero solo el 3,3% fue hemodinámicamente significativa. Además de determinar el porcentaje de reestenosis, es importante conocer en qué momento aparecen, ya que generalmente las estenosis graves aparecen desde los primeros controles ecográficos, suponiendo por ello que son secundarias a problemas perioperatorios o a hiperplasia miointimal, más que debidas a la progresión de la enfermedad. Sin embargo, en nuestro estudio, se observó que esta última fue la causa más frecuente de reestenosis. No existe consenso sobre la historia natural y el manejo de estas lesiones, pero muchos investigadores consideran que las reestenosis carotídeas constituyen un proceso benigno, la mayoría de las veces asintomático y que, por tanto, debe ser manejado de forma conservadora. Solo las estenosis críticas pueden progresar rápidamente a la oclusión y son, por ello, junto a las que han producido clínica, las únicas indicaciones de reintervención en nuestro centro1,22–25. Las estenosis no críticas son vigiladas ecográficamente.
La tasa de ictus/muerte tanto en pacientes sintomáticos como en asintomáticos en nuestro centro cumple los criterios de calidad para realizar este procedimiento (morbimortalidad<3% para pacientes asintomáticos y<6% para sintomáticos)1,8,9,13. Teniendo en cuenta que hubo 3 IM postoperatorios documentados (de los cuales 2 tenían antecedentes previos de CI), y que 3 de los fallecimientos sospechamos que fueran por enfermedad cardiológica, debemos seleccionar de forma más estricta a los pacientes candidatos a EAC y realizarles un estudio cardiológico más exhaustivo.
ConclusiónSegún los criterios de calidad necesarios para realizar una EAC podemos afirmar que, en nuestro servicio, este procedimiento es seguro y garantiza sus ventajas terapéuticas. A pesar de los buenos resultados, debemos ser más estrictos en la selección de pacientes octogenarios y cardiópatas. Además, a raíz de los resultados obtenidos en el estudio, creemos conveniente sustituir el clopidogrel por la aspirina temporalmente de manera previa a la EAC, para reevaluar si, así, conseguimos disminuir la tasa de sangrado postoperatorio.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.