La claudicación intermitente (CI) es frecuente entre la población occidental, incluida la española; sin embargo, sus características no son bien conocidas.
El objetivo del estudio es conocer el perfil de los pacientes españoles con CI.
Material y métodosEstudio prospectivo, observacional, transversal, multicéntrico y no aleatorizado sobre 1.641 claudicantes, divididos en 2 grupos: a) angiología y cirugía vascular (ACV) (n=920), y b) atención primaria (MAP) (n=721). Los pacientes fueron sometidos a un cuaderno de recogida de datos (CRD), analítica, índice tobillo/brazo (ITB), cuestionario Walking Impairment Questionaire (WIQ) y cuestionario europeo de calidad de vida (EQ-5D).
ResultadosFueron varones el 75,3%, de 68,3±9,4 años, destacando sobremanera el elevado número de factores de riesgo cardiovascular y enfermedades asociadas (fundamentalmente cardiacas), más frecuente en el grupo ACV. El ITB de la serie 0,66±0,19, inferior en grupo ACV (p=0,001). Los porcentajes WIQ fueron: daños motores (48,57±20,12), distancia (35,09±25,73), velocidad (36,18±22,83) y escaleras (41,76±27,62), peores en lo relativo a los daños motores (p<0,001) y distancia (p=0,007) en el grupo ACV. La puntuación EQ-5D fue 0,57±0,21, sin diferencias entre grupos.
ConclusionesLos pacientes españoles con CI presentan 3 características: alto riesgo cardiovascular, limitada capacidad para el ejercicio e importante reducción de la calidad de vida. Existen diferencias entre grupos, dado que los ACV tratan pacientes con enfermedad más avanzada.
Intermittent claudication (IC) is a very prevalent condition in Western countries including the population of Spain. However, little is known about the medical profile and quality of life (QoL) of the IC in Spain.
AimTo determine the clinical characteristics and QoL in a large sample of Spanish patients with IC.
Material and methodsAn observational, prospective, cross sectional and multicentre study was performed between October 2010 and January 2011, with 625 investigators recruiting 1,641 consecutive patients with claudication. The sample was divided into two groups: a) patients evaluated by vascular surgeons (VS) (n=920), and b) patients evaluated by general practitioners (GP) (n=721). Demographical and clinical characteristics, analytical findings (glucose levels and lipid metabolism) and the Ankle-Brachial Index (ABI) were recorded. Each patient included in the study also filled in two questionnaires: the Walking impairment Questionnaire (WIQ) and the European Quality of Life-5 Dimensions (EQ-5D).
ResultsThe population mean age was 68.3±9.4 years; in 75.3% of the cases the patients were males. The presence of risk cardiovascular factors (49.5% of diabetes; 76.9% of hypertension and 65.3% of dyslipemia) and comorbid conditions (in particular, cardiovascular diseases) were high. The mean ABI of the series was 0.66±0.19. Patients in the VS group had more severe IC than patients from GP Group (ABI=0.63 vs ABI=0.71, P<.001). WIQ scores obtained were: a) walking distance=35.09±25.73; b) walking speed=36.18±22.83, and c) stair-climbing capacity=41.76±27.62. We only found significant statistical differences in walking distance between the VS Group and GP Group. The global EQ-5D score was 0,57±0,21. No significant differences were observed between the VS and GP groups.
ConclusionsSpanish patients with IC showed three characteristics: high cardiovascular risk, limited ability to tolerate exercise, and reduction in the quality of their life. There are differences between groups; compared to general practitioners, vascular surgeons treated patients with more advanced disease.
La enfermedad arterial periférica (EAP) de las extremidades inferiores es el producto de una progresiva disminución de flujo arterial, que según el grado de afectación se expresa por diferentes manifestaciones clínicas que van desde el dolor al caminar (claudicación intermitente) hasta la gangrena de la extremidad.
Según el estudio Framingham, 6/10.000 hombres y 3/10.000 mujeres entre 30-44 años y 61/10.000 hombres y 54/10.000 mujeres entre 65-74 años presentan EAP1. El estudio TASC con los estudios disponibles estableció una prevalencia de EAP asintomática entre 0,9-22%, de claudicación intermitente (CI) entre 0,4-14,4% y de isquemia crítica en 1/500 pacientes2. La prevalencia se correlaciona con la edad, en ambos sexos; si bien en menores de 70 años es más frecuente en hombres, mientras que por encima es similar en ambos sexos3. En España, el estudio ESTIME cifró la prevalencia de EAP (asintomática y sintomática) en 8,03%4.
En los claudicantes es muy frecuente la arteriosclerosis en otros territorios arteriales5. Muchos claudicantes no suelen alcanzar estadios críticos con necesidad de cirugía, debido a que antes fallecen por infarto de miocardio o ictus6,7. A pesar de las diferencias entre la evolución local y general de la CI8, esta se acompaña siempre de incapacidad física y alteración de la calidad de vida relacionada con su salud (CVRS).El objetivo del presente estudio es conocer las características (perfil) de los claudicantes españoles en función de 2 grupos de investigadores: angiólogos y cirujanos vasculares (ACV) o médicos de atención primaria (MAP).
Material y métodoEstudio prospectivo, transversal, observacional, no aleatorizado y multicéntrico. Se identificaron especialistas en angiología y cirugía vascular y de atención primaria para participar en el estudio. Cada médico debía incluir 3 o 4 pacientes consecutivos, entre mayo y diciembre de 2011.
Población del estudio VITALLa población muestral fue de 2.127 pacientes con CI. Los pacientes participantes debían cumplir todos los criterios de inclusión y ninguno de exclusión. Finalmente algunos fueron retirados del estudio, después de haber sido incluidos. Todos firmaron un consentimiento informado.
Los criterios de inclusión fueron: CI de miembros inferiores (grado ii de Fontaine) superior al año de evolución, ambos sexos, entre 45-85 años, y de todas las razas. Los criterios de exclusión fueron: no consentimiento para participar en el estudio, pacientes hospitalizados o con enfermedad terminal o grave, enfermedades sistémicas que disminuyan totalmente la movilidad (por ejemplo, EPOC avanzada, insuficiencia cardiaca grave, artritis o artrosis avanzada, etc.), cirugía reciente por enfermedad arterial periférica de las extremidades inferiores (menos de 6 meses), enfermedad psiquiátrica mayor, adicción al alcohol o drogas, isquemia arterial aguda o crítica, pacientes incapaces de contestar a los cuestionarios, o incapaces de comprender las instrucciones del estudio. Finalmente los criterios de retirada fueron: cuestionario clínico incompleto (menos del 80% de los ítems), y que el paciente no autocumplimentara alguno de los cuestionarios.
Instrumentos de medidaEl investigador cumplimentó un cuaderno de recogida de datos (CRD) que incluía un cuestionario de datos demográficos y clínicos (edad, sexo, peso, etc.), una analítica y un índice tobillo/brazo (ITB). Conjuntamente los pacientes autocumplimentaron un cuestionario para el deterioro de la marcha y otro de calidad de vida. Se respetó la confidencialidad dado que los cuestionarios fueron anónimos.
Walking Impairment QuestionaireEl Walking Impairment Questionaire (WIQ) es un instrumento específico para documentar el déficit físico de los claudicantes y no de CVRS9–11. Ha mostrado ser una alternativa válida a la prueba de esfuerzo12.
Aborda aspectos referentes al último mes; está compuesto por tres dominios: a) distancia (que se consigue caminar); b) velocidad (que consigue tener), y c) escaleras (cantidad que consigue subir). En la distancia el cuestionario inquiere al paciente sobre el grado de dificultad de caminar distancias específicas, expresado en una escala Likert de 0 a 4, (en la que 0 representa incapacidad y 4 ninguna dificultad para andar la distancia especificada). En la velocidad se incluyen 4 ítems referentes a la dificultad de caminar a una determinada velocidad, y se valora de la misma forma que la distancia. Finalmente, la capacidad de subir escaleras contiene 3 preguntas sobre la dificultad de subir uno, 2 o 3 tramos de escalera valoradas de la misma manera que las 2 dimensiones anteriores. La puntuación de cada dominio se sitúa entre 0 (incapacidad) y 100% (total capacidad). Se cumplimenta en unos 5 min, y es válido tanto autoadministrado como mediante entrevista13. Existe una versión en español14,15.
Cuestionario europeo de calidad de vida o EuroQolEl Cuestionario europeo de calidad de vida o EuroQol (EQ-5D) es un cuestionario genérico de CVRS utilizado por su sencillez y fácil aplicación16,17. Consta de 3 partes: a) descripción del estado de salud en 5 dimensiones: movilidad, cuidado personal, actividades cotidianas, dolor/malestar y ansiedad/depresión, con 3 posibles respuestas cada una; las puntuaciones obtenidas se resumen en un índice global entre 0 (peor estado de salud posible) y 1 (perfecto estado de salud); b) en la segunda el individuo puntúa su estado de salud en una escala visual analógica (EVA) de 0 (peor posible) a 100 (mejor posible), y c) pensada para obtener valores individuales de preferencia, que no ha sido utilizada en el presente estudio.
El EQ-5D ha sido testado y validado en claudicantes18,19. Existe una versión española20, y otra validada en atención primaria21.
Estudio estadísticoLos datos se documentaron de forma anónima. Estos se tabularon con el programa SPSS v19.0 (IBM, Chicago, Illinois, Estados Unidos), para realizar los cruces necesarios.
Los resultados de variables continuas se presentan como media±desviación estándar (DE), mientras que las variables categóricas se describen con frecuencias y porcentajes. Previo al análisis estadístico, se evaluó la normalidad de las distribuciones de las variables continuas para determinar el test más adecuado. Para llevar a cabo comparaciones entre variables cualitativas se utilizó la prueba ji al cuadrado o el test de Fisher. En el caso de variables continuas evaluadas en función de variables cualitativas se utilizó el t-test para muestras independientes o la prueba de la U de Mann-Whitney cuando se compararon 2 categorías y la prueba de ANOVA o prueba de Kruskal-Wallis en el caso de comparar más de 2 categorías. Todos los análisis con p ≤ 0,05 se consideran estadísticamente significativos.
ResultadosLa población investigada fue 2.127 pacientes, de los cuales se validaron 1.641 (77,2%). El motivo principal de exclusión fueron los cuestionarios (WIQ o EQ-5D) incompletos (483 pacientes). Participaron 356 médicos especialistas en ACV y 269 MAP. El número de pacientes (y de investigadores) se repartió homogéneamente por todo el territorio nacional, en virtud de su nivel de población (fig. 1). Dado que participaron 2 tipos de investigadores, la muestra se dividió en 2 grupos: a) ACV (920 pacientes), y b) MAP (721).
- 1.
Características sociodemográficas. El perfil de la serie fueron hombres en el 75,3%, de 68,3±9,4 años, con un IMC de 27,9±3,6 (sobrepeso 56%), casados (69,5%) y convivencia en familia/pareja (73,2%), que viven en ciudades < 200.000 habitantes (69,6%), jubilados (67,1%), fumadores o ex fumadores (76,3%), sedentarios (73,2%) y con antecedente familiar de enfermedad cardiovascular (59,7%). Existen diferencias significativas en ACV respecto a MAP, en lo referente a: más hombres, menor peso e IMC, residir en zonas más pobladas, más fumadores, y menos sedentarismo en el grupo ACV. En el resto de características no se observaron diferencias (tabla 1).
Tabla 1.Características sociodemográficas de la muestra*
ACV (n=920) MAP (n=721) Total (n=1.641) p Sexo Hombre 717 (77,9) 518 (71,8) 1235 (75,3) Mujer 203(22,1) 203 (28,2) 406 (24,7) 0,005 Edad (años) 68,2 ± 9,8 68,6 ± 8,9 68,3 ± 9,4 0,542 Altura (cm) 167,6 ±7,7 167,8 ± 7,5 167,7 ± 7,6 0,791 Peso (kg) 77,5 ± 10,8 79,3 ±11,2 78,3 ± 11,0 0,016 IMC 27,6 ±3,6 28,2 ± 3,7 27,9 ± 3,6 0,008 IMC categorizado Infrapeso 6 (0,7) 3 (0,4) 9 (0,6) Normal 185 (20,7) 111 (15,6) 296 (18,5) Sobrepeso 500 (56,0) 405 (57,0) 905 (56,4) Obeso 202 (22,6) 192 (27,0) 394 (24,6) 0,003 NS/NC 27 (2,9) 10 (1,4) 37 (2,3) Estado civil Soltero 69 (8,3) 41 (6,0) 110 (7,3) Casado 583 (69,8) 469 (69,1) 1052 (69,5) Viudo 183 (21,9) 169 (24,9) 352 (23,2) 0,135 NS/NC 85 (9,2) 42 (5,8) 127 (7,7) Convivencia Solo 197 (21,6) 150 (21,1) 347 (21,4) Pareja/familia 666 (73,2) 522 (73,3) 1188 (73,2) Otras 47 (5,2) 40 (5,6) 87 (5,4) 0,897 NS/NC 10 (1,1) 9 (1,2) 19 (1,2) Lugar de residencia Menor de 50.000 hab. 297 (32,4) 312 (43,5) 609 (37,3) 50.000-200.000 hab. 279 (30,5) 248 (34,5) 527 (32,3) 200.000-500.000 hab. 191 (20,9) 99 (13,8) 290 (17,7) 500.000-1 millónhab. 52 (5,7) 33 (4,6) 85 (5,2) Más de 1 millón de hab. 97 (10,6) 26 (3,6) 123 (7,5) 0,001 NoS/C 4 (0,4) 3 (0,4) 7 (0,4) Situación laboral Activo 176 (19,2) 153 (21,3) 329 (20,1) Paro 33 (3,6) 21 (2,9) 54 (3,3) Baja 51 (5,5) 26 (3,6) 77 (4,7) Invalidez 47 (5,1) 31 (4,3) 78 (4,8) Jubilado 612 (66,6) 487 (67,8) 1.099 (67,1) 0,259 NS/NC 1 (0,1) 3 (0,4) 4 (0,2) Fumador No 193(21,5) 174 (26,7) 367 (23,7) Sí 357(39,7) 234 (35,9) 591 (38,1) Ex fumador 349 (38,8) 244 (37,4) 593 (38,2) 0,050 NS/NC 21 (2,3) 69 (9,6) 90 (5,5) Sedentarismo No 229 (30,3) 124 (22,1) 353 (26,8) Sí 528 (69,7) 438 (77,9) 966 (73,2) 0,001 NS/NC 163 (17,1) 159 (22,1) 322 (19,6) Historia familiar ECV No 351 (39,3) 272 (41,7) 623 (40,3) Sí 541 (60,7) 380 (58,3) 921 (59,7) 0,349 NS/C 28 (3,0) 69 (9,6) 97 (5,9) ACV: angiólogos y cirujanos vasculares; ECV: enfermedad cardiovascular; IMC: índice de masa corporal; MAP: médicos de atención primaria.
- 2.
Características clínicas:
- a)
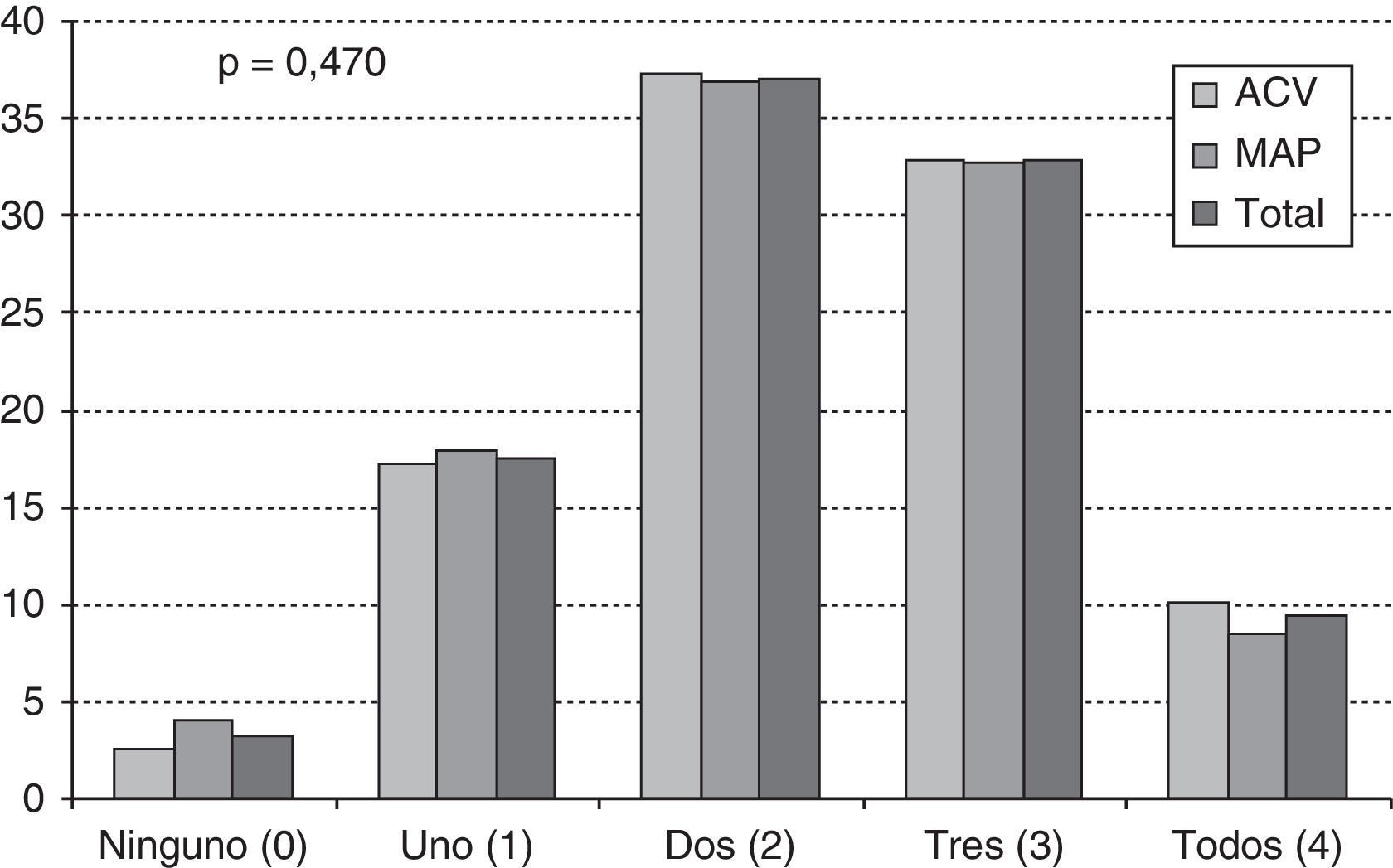
Enfermedad cardiovascular. La presencia de factores de riesgo (FRCV) se resume en 49,5% diabéticos, 76,9% hipertensos y 65,3% con dislipidemia; en el grupo ACV existe significativamente un mayor número de diabéticos (tabla 2). Casi en 10% de pacientes presentaron los 4 FRCV analizados (incluido el hábito de fumar tabaco ya referido con anterioridad) y solo el 3,2% no presentaba ningún FRCV, sin diferencias entre el tipo de investigador (fig. 2).
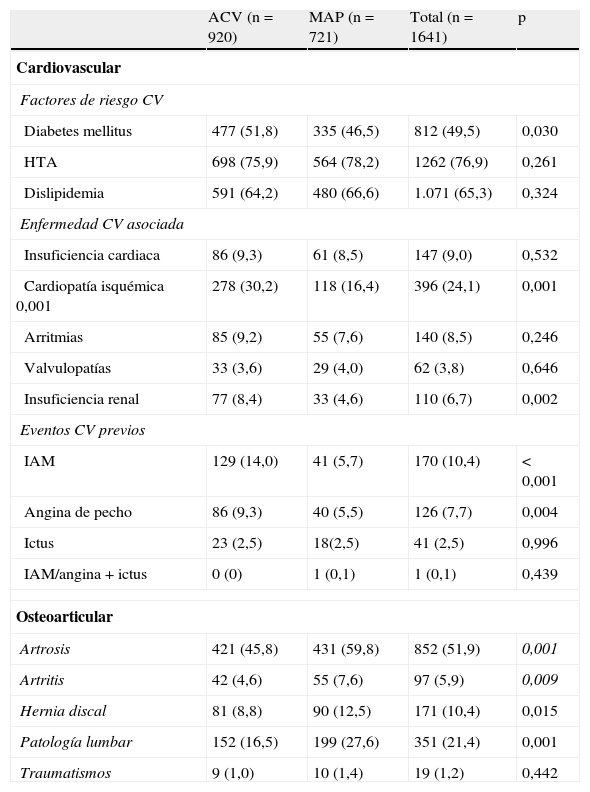
Tabla 2.Características clínicas. Enfermedad asociada*
ACV (n=920) MAP (n=721) Total (n=1641) p Cardiovascular Factores de riesgo CV Diabetes mellitus 477 (51,8) 335 (46,5) 812 (49,5) 0,030 HTA 698 (75,9) 564 (78,2) 1262 (76,9) 0,261 Dislipidemia 591 (64,2) 480 (66,6) 1.071 (65,3) 0,324 Enfermedad CV asociada Insuficiencia cardiaca 86 (9,3) 61 (8,5) 147 (9,0) 0,532 Cardiopatía isquémica 0,001 278 (30,2) 118 (16,4) 396 (24,1) 0,001 Arritmias 85 (9,2) 55 (7,6) 140 (8,5) 0,246 Valvulopatías 33 (3,6) 29 (4,0) 62 (3,8) 0,646 Insuficiencia renal 77 (8,4) 33 (4,6) 110 (6,7) 0,002 Eventos CV previos IAM 129 (14,0) 41 (5,7) 170 (10,4) < 0,001 Angina de pecho 86 (9,3) 40 (5,5) 126 (7,7) 0,004 Ictus 23 (2,5) 18(2,5) 41 (2,5) 0,996 IAM/angina + ictus 0 (0) 1 (0,1) 1 (0,1) 0,439 Osteoarticular Artrosis 421 (45,8) 431 (59,8) 852 (51,9) 0,001 Artritis 42 (4,6) 55 (7,6) 97 (5,9) 0,009 Hernia discal 81 (8,8) 90 (12,5) 171 (10,4) 0,015 Patología lumbar 152 (16,5) 199 (27,6) 351 (21,4) 0,001 Traumatismos 9 (1,0) 10 (1,4) 19 (1,2) 0,442 ACV: angiólogos y cirujanos vasculares; CV: cardiovasculares; HTA: hipertensión arterial; IAM: infarto agudo de miocardio; MAP: médicos de atención primaria.
La enfermedad cardiovascular asociada mayoritaria es la cardiopatía isquémica (24,1%), superior en el grupo ACV (30,2 vs 16,4%; p<0,001). La presencia de insuficiencia renal crónica (6,7%) también fue superior en el grupo ACV (8,4 vs 4,6%; p<0,002). El resto (insuficiencia cardiaca, arritmias y valvulopatías) fueron menos frecuentes y similares en ambos grupos (tabla 2).
Se constató antecedente de IAM o angina de pecho en el 10,4 y 7,7% de la muestra respectivamente, ambas superiores de forma significativa en el grupo ACV. El antecedente de ictus fue del 2,5%, similar en ambos grupos. La asociación IAM/angina+ictus solo se registró en un paciente (tabla 2).
- b)
Enfermedad osteoarticular asociada. La artrosis no invalidante asociada a CI fue del 51,9% (superior en el grupo MAP; p=0,001). La enfermedad lumbar es la segunda entidad osteoarticular (21,4%) asociada, igualmente más frecuente en el grupo MAP (p=0,001). En general, estas enfermedades fueron más frecuentes en el grupo MAP (tabla 2).
- c)
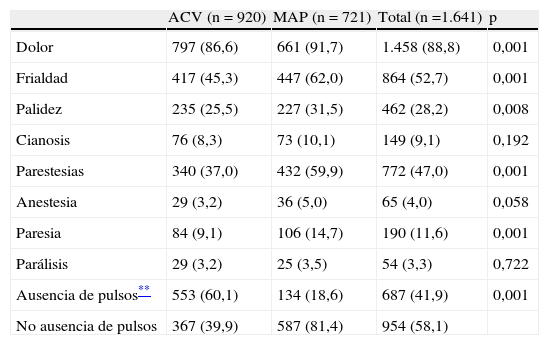
Síntomas y signos de EAP. El síntoma más frecuente fue el dolor (88,8%). La ausencia de pulsos (en algún nivel) se detectó en el 41,9% de los pacientes, superior en el grupo ACV (60,1%) respecto al MAP (18,6%) (p=0,001).
- d)
Otros síntomas y signos. Véase tabla 3.
Tabla 3.Presencia de síntomas y signos de enfermedad arterial periférica*
ACV (n = 920) MAP (n = 721) Total (n =1.641) p Dolor 797 (86,6) 661 (91,7) 1.458 (88,8) 0,001 Frialdad 417 (45,3) 447 (62,0) 864 (52,7) 0,001 Palidez 235 (25,5) 227 (31,5) 462 (28,2) 0,008 Cianosis 76 (8,3) 73 (10,1) 149 (9,1) 0,192 Parestesias 340 (37,0) 432 (59,9) 772 (47,0) 0,001 Anestesia 29 (3,2) 36 (5,0) 65 (4,0) 0,058 Paresia 84 (9,1) 106 (14,7) 190 (11,6) 0,001 Parálisis 29 (3,2) 25 (3,5) 54 (3,3) 0,722 Ausencia de pulsos** 553 (60,1) 134 (18,6) 687 (41,9) 0,001 No ausencia de pulsos 367 (39,9) 587 (81,4) 954 (58,1) ACV: angiólogos y cirujanos vasculares; MAP: médicos de atención primaria.
- a)
- 3.
Presión arterial y analítica. Los niveles medios de glucemia, colesterol y lipidograma, de la serie total y por grupos, pueden observarse en la tabla 4.
Tabla 4.Determinaciones implementadas*
ACV MAP Total p Presión arterial (mm Hg) N = 765 N = 682 N = 1.447 Sistólica 143,4 ± 17,7 141,76 ± 16,4 142,6 ± 17,1 0,042 Diastolica 81,5 ± 10,6 81,2 ± 10,1 81,4 ± 10,3 0,611 Glucemia (mg/dl) N = 822 N = 686 N = 1508 0,001 130,1 ±45,1 122,2 ± 37,8 126,5 ± 42,1 Perfíl lipídico (mg/dl) N = 710 N = 609 N = 1.319 Colesterol total 208,4 ± 47,1 213,5 ± 42,8 210,8 ± 45,3 0,006 HDL 51,9 ± 27,8 50,0 ± 20,7 51,0 ± 24,8 0,313 LDL 128,2 ± 39,7 132,7 ± 38,7 130,3 ± 39,3 0,015 Triglicéridos 158,9 ± 77,4 154,7 ± 60,0 156,9 ± 69,7 0,962 ITB N = 736 N = 284 N = 1.020 Índice 0,63 ± 0,19 0,71 ± 0,19 0,66 ± 0,19 0,001 Normal vs patológico > 0,90 44 (6,0) 54 (19,0) 98 (9,6) < 0,90 692 (94,0) 230 (81,0) 922 (90,4) 0,001 Categorizado > 0,90 44 (6,0) 54 (19,0) 98 (9,6) 0,90-0,50 556 (75,5) 199 (70,1) 755 (74,0) < 0,50 136 (18,5) 31 (10,9) 167 (16,4) 0,001 WIQ N = 920 N =721 N =1.641 Daños motores (%) 47,12 ± 20,40 50,42 ± 19,63 48,57 ± 20,12 0,001 Distancia recorrida 1595,75 ± 1.253,96 1704,92 ± 1.137,58 1.643,71 ± 1.205,07 Distancia (%) 34,07 ± 26,77 36,40 ± 24,28 35,09 ± 25,73 0,007 Velocidad al caminar 16,30 ± 10,59 17,08 ± 10,39 16,64 ± 10,50 Velocidad (%) 35,43 ± 23,01 37,13 ± 22,58 36,18 ± 22,83 0,112 Subir escaleras 118,54 ± 82,19 122,46 ± 76,05 120,26 ± 79,55 Subir escaleras (%) 41,16 ± 28,54 42,52 ± 26,41 41,76 ± 27,62 0,207 EQ-5D N = 920 N = 721 N = 1641 Global (0-1) 0,58 ± 0,21 0,57 ± 0,20 0,57 ± 0,21 0,429 Estado de salud hoy (%) 55,04 ± 21,30 53,79 ± 19,71 54,49 ± 20,63 0,063 ACV: angiólogos y cirujanos vasculares; HDL: lipoproteínas de alta densidad; ITB: índice tobillo/brazo; LDL: lipoproteínas de baja densidad; MAP: médicos de atención primaria.
Nota:
WIQ: Walking Impairment Questionaire=0% peor-100% mejor posible.
EQ-5D=EuroQol=0 peor-1 mejor posible.
Cifras ideales:
PAS/PAD=140/90 o 130/80 (alto riesgo); glucemia<110 (Hb A1C=7%); dislipidemia: colesterol total=200 y LDL=100.
- 4.
Índice tobillo/brazo (ITB). Se realizó en 1.020 pacientes (62,2% de la muestra). Practicado más frecuentemente en el grupo ACV (736 pacientes, 80,0%) respecto a los MAP (284 pacientes, 39,4%). El ITB de la serie fue 0,66±0,19, inferior en el grupo ACV respecto al MAP (0,63 vs 0,71; p=0,001). Un ITB<0,50 se detectó en 167 pacientes (16,4%), más veces detectados en el grupo ACV (p=0,001) (tabla 4).
- 5.
Deterioro de la marcha (WIQ). Los pacientes valoraron los dominios como: a) distancia 35,09±25,73 (%), b) velocidad 36,18±22,83 (%), y c) escaleras 41,76±27,62 (%). Dicho de otra manera, presentaron una merma del 64,9% (distancia), 63,8% (velocidad), y del 58,2% (escaleras). Salvo en la distancia recorrida, peor en el grupo ACV, no se apreciaron diferencias entre grupos. Los daños motores fueron valorados de forma estadísticamente significativa, como más graves en el grupo ACV (tabla 4).
- 6.
Calidad de vida (EQ-5D). Los pacientes valoraron su CVRS global del 0,57±0,21 y su estado de salud «a día de hoy» del 54,49±20,63. Dicho de otra manera, presentan una merma de la calidad de vida ideal entre el 43-45%. No se apreciaron diferencias entre grupos (tabla 4).
Existe mucha documentación sobre el impacto y las consecuencias de la EAP, que hacen de la misma un problema de salud pública. La CI es el síntoma más frecuente de EAP, y como situación crónica ocasiona perjuicios en la CVRS de miles de españoles durante buena parte de su vida22.
Una de las consecuencias prácticas de los estudios epidemiológicos es que permiten calcular y caracterizar la demanda asistencial de un determinado país, región o lugar, basándose en su población y características. Cuando faltan datos, las autoridades sanitarias parecen ignorar la realidad. Afortunadamente, en la última década existen al menos 44 estudios epidemiológicos sobre la EAP exclusivamente españoles23, si bien se ocupan de la CI de un modo muy diferente al aquí tratado. Según diferentes series extranjeras24–27 (tabla 5) podemos decir que los claudicantes españoles son bastante similares. Lo más destacable es su elevada carga de riesgo y enfermedades cardiovasculares asociados. Otros aspecto que llama la atención es la constatación (incluso por los ACV) de síntomas (por ejemplo, cianosis, anestesia, paresia o parálisis) no propios de esta fase de la EAP, pero detectados en un pequeño número de pacientes; lógicamente estos síntomas deben tener relación con otras enfermedades asociadas (diabetes mellitus u osteoarticulares).
Factores de riesgo de enfermedad cardiovascular en una población de claudicantes
| Murabito et al. (2005)*N=5.124 | Lovell et al. (2009)N=501 | Stansby et al. (2011)N=473 | Serie actual (2012)N=1.641 | |
| Edad (media ± DE) | 69 ± 10 | 64,4 | 68 | 68,3 ± 9,4 |
| Hombres (%) | 57 | 46,4 | 75,3 | |
| Fumadores activos (%) | 37 | 18 | 39 | 38,1 |
| Ex fumadores (%) | 38 | 49 | 38,2 | |
| Nunca fumadores (%) | 25 | – | 23,7 | |
| Diabetes mellitus (%) | 25 | 12 | 20 | 49,5 |
| Hipertensión arterial (%) | 62 | 43 | 76,9 | |
| Hipercolesterolemia (%) | 33 | 37 | 65,3 (2) | |
| IMC > 30 (%) | 26 | – | 24,6 | |
| Sedentarismo | – | – | 73,2 | |
| Enfermedad cardiovascular (%) | 49 | – | 30 + 7(1) | 44,6 |
| Historia familiar EAP (%) | – | 36 | 59,7 |
(1) Enfermedad coronaria+ictus; (2) Dislipidemia.
EAP: enfermedad arterial periférica; IM: índice de masa corporal (> 30=obesidad).
Un aspecto poco tratado es la enfermedad osteoarticular (no totalmente incapacitante para deambular) asociada con CI, pues como refieren Breek et al.28 esta comorbilidad de la espalda, cadera o rodilla es muy frecuente en estos enfermos. En nuestra serie, la mitad se asoció con artrosis, y ello indudablemente debe repercutir en la marcha y la CVRS.
El ITB medio de nuestra serie (0,66±0,19) es concordante con lo publicado11,12,29–31, que está en un rango de 0,44 y 0,72 (mediana=0,60). Aunque los MAP entrenados pueden realizar esta técnica con fiabilidad como muestra un estudio francés32 y otro alemán33, los MAP españoles raramente realizan esta medición en la práctica clínica34; en concreto, solo la mitad respecto de los ACV (80 vs 39,4%), hecho que incide negativamente en el diagnóstico precoz y seguimiento de la EAP.
El deterioro de la marcha de nuestros pacientes fue concordante con la literatura médica11–15,35,36. Los daños motores se mantienen en un rango (de porcentajes) entre 39,6 y 63,3 (nuestra serie=48,6), la distancia entre 22,6 y 55,0 (serie=35,1), la velocidad entre 23,9 y 48,3 (serie=36,2) y la dimensión «escaleras» entre 23,8 y 65,0 (serie=41,8).
La CVRS de la serie también es concordante con lo publicado (rango entre 0,52 y 0,70; mediana=0,64). El estado de salud que refieren los pacientes, en nuestra serie fue inferior (54,5%) a lo publicado (mediana, 62%)12,13,31,37,38. Conjuntamente resaltar que la merma de CVRS de los CI es tan elevada como aquella que presentan los pacientes con enfermedades crónicas consideradas más graves (EPOC o insuficiencia cardiaca)39–41.
Los cuestionarios WIQ y EQ-5D han sido creados para que los pacientes con CI valoren su deterioro al ejercicio y CVRS, respectivamente. Chetter et al.18 propusieron que todos los países europeos deberían medir la CVRS de sus pacientes vasculares, hecho que en nuestro país no es frecuente. Está probado que la presencia de EAP se asocia con una disminución global de la actividad física y cómo ello repercute en la CVRS29,42. Conjuntamente, las fases de la enfermedad (estadios) se correlacionan con la CVRS, en el sentido de que disminuye esta según avanza la enfermedad30,31,43,44. Por su parte, la CI supone un deterioro de la CVRS, respecto de controles o individuos sin CI45,46. Ese deterioro afecta fundamentalmente a la función física, más que a otros dominios (psicológico o social).
Finalmente, referir cómo el grupo MAP fue diferente al ACV (menos FRCV y enfermedades cardiovasculares, pero más osteoarticulares), quizás por ello la CVRS fue similar en ambos grupos. El mayor ITB y menor frecuencia de enfermedades cardiovasculares asociadas y otros factores de riesgo (por ejemplo, diabetes mellitus) hacen del grupo MAP menos grave respecto al ACV.
¿Valor de esta investigación? Se trata de un estudio a gran escala (1.641 claudicantes), en todo el territorio nacional, y que incluye los niveles asistenciales que intervienen en el proceso diagnóstico y terapéutico de estos pacientes.
Conjuntamente somos conscientes de limitaciones, como la no determinación del ITB en todos los casos; ello no fue un criterio de exclusión, al ser conscientes de que muchos MAP no la realizarían; y no claudicometría, obviada dado que los MAP carecen de infraestructura para ello.
En conclusión, la presente muestra informa que los claudicantes españoles presentan un elevado número de factores de riesgo cardiovascular y enfermedades asociadas, un deterioro de su marcha y una disminución de su calidad de vida.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciaciónProyecto financiado, a través de la Fundación SEACV, por el Grupo Ferrer.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Al promotor del estudio: Sociedad Española de Angiología y Cirugía Vascular (SEACV).
A la secretaría técnica y estadística: Grupo Saned.