La asistencia circulatoria mecánica permite aportar oxígeno a los tejidos en pacientes con enfermedades cardiacas y/o respiratorias reversibles refractarios a tratamientos convencionales.
ObjetivoMostrar los resultados iniciales de asistencia circulatoria mecánica en niños con cardiopatía en nuestra institución.
MétodoEstudio de cohorte descriptivo retrospectivo entre marzo de 2006 y marzo de 2012. Datos demográficos (edad, sexo, peso, diagnóstico cardiológico), de la cirugía (técnica, tiempo de bomba y de pinzamiento aórtico) y de la asistencia circulatoria mecánica (tipo, indicación, duración, complicaciones y evolución).
ResultadosFueron asistidos 33 pacientes (1.3% del total de cirugías), con oxigenación por membrana extracorpórea en 32 casos y un caso con dispositivo de asistencia ventricular. Mediana de edad 7.4 meses (un día-18años) y peso 6kg (2.3-75). Las malformaciones cardiacas que se asistieron con mayor frecuencia son las trasposiciones de grandes arterias asociadas a otras anomalías y las trasposiciones corregidas (inversión ventricular-doble discordancia). El motivo de ingreso más frecuente fue disfunción biventricular poscardiotomía. En 28 pacientes la asistencia circulatoria mecánica fue postoperatoria y en 4 preoperatoria. Un paciente presentó miocarditis. Mediana de asistencia 3 días (1-10). Complicaciones más frecuentes: infección el 21% y sangrado el 21%. Decanulación electiva en un 94% de los casos. Supervivencia con alta hospitalaria: 52%.
ConclusionesLa asistencia circulatoria mecánica en nuestra institución es una herramienta segura con procedimiento estandarizado. Se utiliza en un reducido número de casos, con supervivencia similar a informes internacionales. Es un procedimiento complejo, plenamente justificado que permitió la recuperación en más de la mitad de los pacientes que de otro modo hubieran fallecido.
Mechanical circulatory support provides oxygen to the tissues in patients with cardiac and/or respiratory reversible disease refractory to conventional treatments.
ObjectiveThe aim of this study is to show our initial results of mechanical circulatory support in children with heart disease.
MethodRetrospective cohort between March 2006 and March 2012. Demographic data (age, sex, weight, cardiac diagnosis), surgery (technique, pump, aortic cross clamping time) and mechanical circulatory support (type of assistance, indication, duration, complications and outcome) were collected.
ResultsThirty-three patients were supported (1.3% of all surgeries), extracorporeal membrane oxygenation 32 cases and one ventricular assist device. The median age 7.4 months (one day-18 years) and weight 6kg (2.3-75). The most frequent cardiac malformations supported were the transpositions of the great arteries associated with other anomalies and the corrected transpositions (ventricular inversion or double discordance). The most common reason for admission was post-cardiotomy biventricular dysfunction. Twenty-eight patients were supported in the postoperative period, 4 in the preoperative period and in one with myocarditis. Median days of support were 3 days (1-10). The most common complications were infection (21%), bleeding (21%). Elective decannulation was achieved in 94% of cases. Hospital discharge survival: 52%.
ConclusionsThe mechanical circulatory support in our institution is a safe and standard procedure. We have been using it in a small number of cases with a similar survival to that reported internationally. This complex procedure is widely justified because it allows for the recovery of more than half of the patients who otherwise would have died.
La asistencia circulatoria mecánica (ACM) es una forma de soporte vital, que permite aportar oxígeno a los tejidos en pacientes con insuficiencia cardiaca y/o respiratoria refractarios a los tratamientos convencionales1. La oxigenación con membrana extracorpórea (ECMO) y la asistencia ventricular (VAD) son formas de ACM que se usan en niños con enfermedad cardiaca y/o respiratoria2. La ECMO es una adaptación del sistema de circulación extracorpórea utilizada durante la cirugía cardiovascular, que permite brindar soporte cardiopulmonar durante un periodo más prolongado (días o semanas), mediante la canulación venosa, el paso de la sangre por un oxigenador y la canulación arterial que entrega sangre oxigenada a la aorta. La VAD solo contribuye con sostén hemodinámico por lo que requiere adecuada función pulmonar y puede ser de tipo izquierdo, derecho o biventricular. La VAD izquierda es la más utilizada y requiere canulación en aurícula izquierda para obtener el retorno venoso de sangre oxigenada que luego es entregada a la aorta. Existen otros tipos de dispositivos como el balón de contrapulsación, pero su utilización es limitada en lactantes y niños debido al pequeño calibre de los vasos femorales y la elevada frecuencia cardiaca en niños3.
El uso más frecuente de la ACM en cirugía de cardiopatías congénitas es en el postoperatorio, sin embargo puede ser útil en la estabilización preoperatoria. Además puede ser de utilidad en otras cardiopatías no quirúrgicas para dar sostén hemodinámico hasta su recuperación. En cualquiera de estos escenarios el objetivo es optimizar la condición del paciente tratando de prevenir el fallo multiorgánico. Es un tratamiento invasivo y complejo, que requiere personal altamente entrenado durante todo el procedimiento, y se aplica en pacientes en los que ha fallado el tratamiento convencional y en los que la insuficiencia cardiaca y/o respiratoria sea potencialmente reversible.
De acuerdo al registro de la Extracorporeal Life Support Organization (ELSO), que recoge datos de más de 100 centros de cirugía cardiaca en el mundo, la supervivencia de los pacientes con ECMO postoperatoria es del 38% en neonatos, del 43% en niños y del 33% en adultos4. Desde el año 2006, el Hospital Garrahan cuenta con un programa de soporte mecánico para el perioperatorio de cirugía cardiovascular, que incluye ECMO, VAD así como otras formas de asistencia circulatoria prolongada5. El objetivo de este trabajo es mostrar los resultados de la experiencia en ACM con ECMO y VAD en pacientes con cardiopatía en nuestra institución.
MétodoSe trata de un estudio de cohorte descriptivo retrospectivo con base en el análisis de las historias clínicas. Se incluyeron todos los pacientes que requirieron asistencia circulatoria mecánica (ECMO o VAD) en la Unidad de Cuidados Intensivos Cardiacos (UCI35) del Hospital de Pediatría «Dr. Juan P. Garrahan» entre marzo de 2006 y marzo de 2012. Por tratarse de un estudio descriptivo no se solicitó el consentimiento informado; el protocolo fue aprobado por el Comité de Ética e Investigación del hospital.
Se recolectaron datos demográficos (edad, sexo, peso, diagnóstico cardiológico), de la cirugía (técnica, tiempo de circulación extracorpórea y tiempo de pinzamiento aórtico) y datos de la ACM (tipo de asistencia, indicación, duración, complicaciones y evolución). Los pacientes que requirieron ACM en el postoperatorio fueron estratificados en 6 categorías según la escala Risk Adjustment for Congenital Heart Surgery (RACHS-1). Esta escala permite el ajuste por el riesgo de mortalidad hospitalaria en relación con la complejidad de la cirugía. El aumento de la categoría se asocia con mayor complejidad de los procedimientos quirúrgicos y un mayor riesgo de mortalidad6.
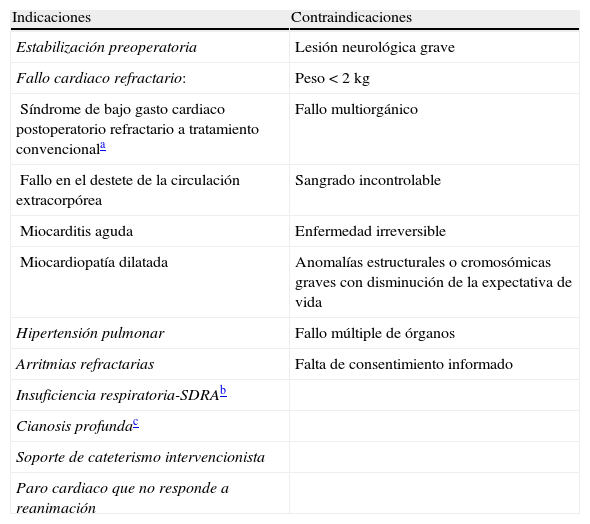
En las tablas 1 y 2 se detallan las indicaciones y contraindicaciones, consideraciones técnicas y objetivos del soporte. Los indicadores para decidir el inicio de la ACM incluyen bajo gasto cardiaco persistente con un rápido empeoramiento de la circulación, mala perfusión tisular, oligoanuria, acidosis láctica en aumento y saturación venosa central<50%, a pesar del máximo soporte inotrópico7.
Indicaciones y contraindicaciones de asistencia circulatoria mecánica
| Indicaciones | Contraindicaciones |
| Estabilización preoperatoria | Lesión neurológica grave |
| Fallo cardiaco refractario: | Peso<2kg |
| Síndrome de bajo gasto cardiaco postoperatorio refractario a tratamiento convencionala | Fallo multiorgánico |
| Fallo en el destete de la circulación extracorpórea | Sangrado incontrolable |
| Miocarditis aguda | Enfermedad irreversible |
| Miocardiopatía dilatada | Anomalías estructurales o cromosómicas graves con disminución de la expectativa de vida |
| Hipertensión pulmonar | Fallo múltiple de órganos |
| Arritmias refractarias | Falta de consentimiento informado |
| Insuficiencia respiratoria-SDRAb | |
| Cianosis profundac | |
| Soporte de cateterismo intervencionista | |
| Paro cardiaco que no responde a reanimación |
SDRA: síndrome de distrés respiratorio agudo.
Optimización de la precarga, medio interno y hemoglobina normal, ventilación mecánica, optimización del ritmo cardiaco y apoyo inotrópico (adrenalina<0.2mcg/kg/min, milrinona<0.75mcg/kg/min, levosimendán 0.1-0.3mcg/kg, 7min) (Moreno et al.5).
Hipoxemia con PaO2<20mm Hg con acidosis metabólica (Wessel et al.13) y/o saturación arterial de oxígeno<60-65% asociado a cardiopatía congénita con cortocircuito intracardiaco y shock cardiogénico, trombosis aguda del shunt sistémico pulmonar, insuficiencia respiratoria aguda exacerbada por enfermedad cardiaca subyacente (Wessel et al.13).
Consideraciones técnicas
| Ecocardiograma transesofágico para descartar defecto residual |
| Sitio de canulación |
| Posquirúrgico inmediato: transtorácico con descompresión de aurícula izquierda |
| Estabilización preoperatoria: cuello (yugular interna y carótida) |
| Técnica: veno- arterial |
| Bomba Biomedicus®. Circuito revestido con superficie no trombogénica. Oxigenador de fibra hueca |
| Flujo 150-200ml/kg/min |
| Infusión de inotrópicos a bajas dosis: dopamina 5mcg/kg/min y vasodilatadores: nitroprusiato de sodio 2-4mcg/kg/min |
| Objetivos |
| SvcO2>70% |
| Disminución de ácido láctico a valores normales |
| Normalización de la función de los órganos |
| TCA: 180-200 |
| El destete electivo se procede luego de 72-96h de soporte completo y en ausencia de patología respiratoria. Se inicia sostén inotrópico con dopamina 8-10mcg/kg/min o adrenalina 0.05mcg/kg/min más milrinona 0.5 mcg/kg/min. Tras 2h de infusión se procede en forma gradual, evaluando función cardiaca con ecocardiograma y parámetros de oxigenación tisular |
SvcO2: saturación venosa central de oxígeno; TCA: tiempo de coagulación activado.
La decisión de interrumpir el soporte e iniciar el destete electivo fue tomada cuando se evidenció suficiente estabilidad cardiorrespiratoria para realizar con éxito el mismo. Asimismo se procedió a suspenderlo cuando se determinó que la disfunción en uno o más órganos era irreversible o irrecuperable8.
Las variables continuas fueron reportadas como media y desviación estándar (DE) o mediana y rango según su distribución. Las medias se compararon con el test t de Student o con la prueba de Mann-Whitney según distribución. Las variables nominales se expresaron como porcentaje y se analizaron con Chi 2 o test exacto de Fisher.
ResultadosDurante el periodo del estudio se realizaron 2,500 cirugías cardiovasculares (un 86% con circulación extracorpórea), con una mortalidad del 5%. Se proporcionó soporte circulatorio a 33 pacientes, que representan el 1.3% del total de cirugías cardiovasculares realizadas en el periodo analizado. La modalidad más utilizada fue la ECMO en 32 casos y solo un paciente utilizó VAD izquierda. En todos los casos se requirió el consentimiento informado de los padres para efectuar el procedimiento.
La mediana de edad fue de 7.4 meses (un día-18 años) y de peso 6kg (2.3- 75); el 42% eran de sexo masculino. Las malformaciones cardiacas que se asistieron con mayor frecuencia fueron las trasposiciones de grandes arterias asociadas a otras anomalías y las trasposiciones corregidas (inversión ventricular o doble discordancia) (tabla 3).
Diagnósticos en orden de frecuencia
| Diagnóstico | n | % | Vivos |
| Trasposición de grandes arterias asociadas a otras anomalías y trasposiciones corregidas (L-TGA o doble discordancia o inversión ventricular)a | 8 | 24.2 | 3 |
| Tetralogía de Fallot | 6 | 18.2 | 3 |
| Ventrículo únicob | 5 | 15.2 | 3 |
| Trasposición de grandes arterias simples | 4 | 12.1 | 2 |
| IAA con CIV | 3 | 9 | 2 |
| ATRV | 2 | 6 | 0 |
| CIV múltiple | 1 | 3 | 1 |
| Anomalía de Ebstein | 1 | 3 | 1 |
| Estenosis supravalvular aórtica y estenosis supravalvular pulmonar | 1 | 3 | 1 |
| Reemplazo valvular mitral | 1 | 3 | 0 |
| Miocarditis | 1 | 3 | 1 |
| Total | 33 | 100 | 17 |
ATRV: anomalía total de retorno venoso pulmonar; CIV: comunicación interventricular; IAA: interrupción de arco aórtico; TGA: trasposición de grandes arterias.
Vivos. TGA complejas asociadas a: estenosis pulmonar con cirugía de Nikaidoh (1), ATRV (1), Rastelli con reemplazo de homoinjerto y de raíz aórtica (1). Fallecidos. TGA complejas: asociadas a CIV múltiple (1), IAA (1), L-TGA con cirugía de Senning-Rastelli (1), L-TGA con doble switch (1), D-TGA con cerclaje e insuficiencia aórtica (1).
Analizados los pacientes postoperatorios por RACHS-1, ningún paciente de categoría i requirió ACM, en categoría ii: el 0.65%, en categoría iii: un 0.95%, en categoría iv: un 3.74% y en v/vi: un 4.6% de los pacientes la requirieron.
La mediana del tiempo de circulación extracorpórea fue de 197min (83-701) y de pinzamiento aórtico de 97min (39-194).
En todos los pacientes posquirúrgicos se descartó defecto de la reparación quirúrgica (defecto residual) utilizando ecocardiografía transesofágica o ecocardiograma transtorácico.
Las indicaciones de ingreso a ECMO se describen en la tabla 4; el motivo de ingreso más frecuente fue la disfunción biventricular poscardiotomía.
En 28 pacientes (85%) la ACM se realizó luego de la cirugía, 16 desde el quirófano y 12 en la UCI dentro de las 72h posquirúrgicas. Por presentar cianosis grave 4 pacientes fueron asistidos antes de la cirugía (2 trasposiciones de grandes arterias, un ventrículo único con anastomosis sistémica pulmonar ocluida y un Fallot en crisis de cianosis refractaria a tratamiento médico). En estos casos se procedió a 24h de estabilización y luego se realizó la reparación quirúrgica, sin requerir ninguno de ellos ECMO en el postoperatorio, con una supervivencia del 100%.
Un paciente con diagnóstico de miocarditis requirió ser asistido en ECMO por fallo miocárdico durante 10 días hasta su recuperación.
La mediana de asistencia de toda la serie fue 3 días (1-10).
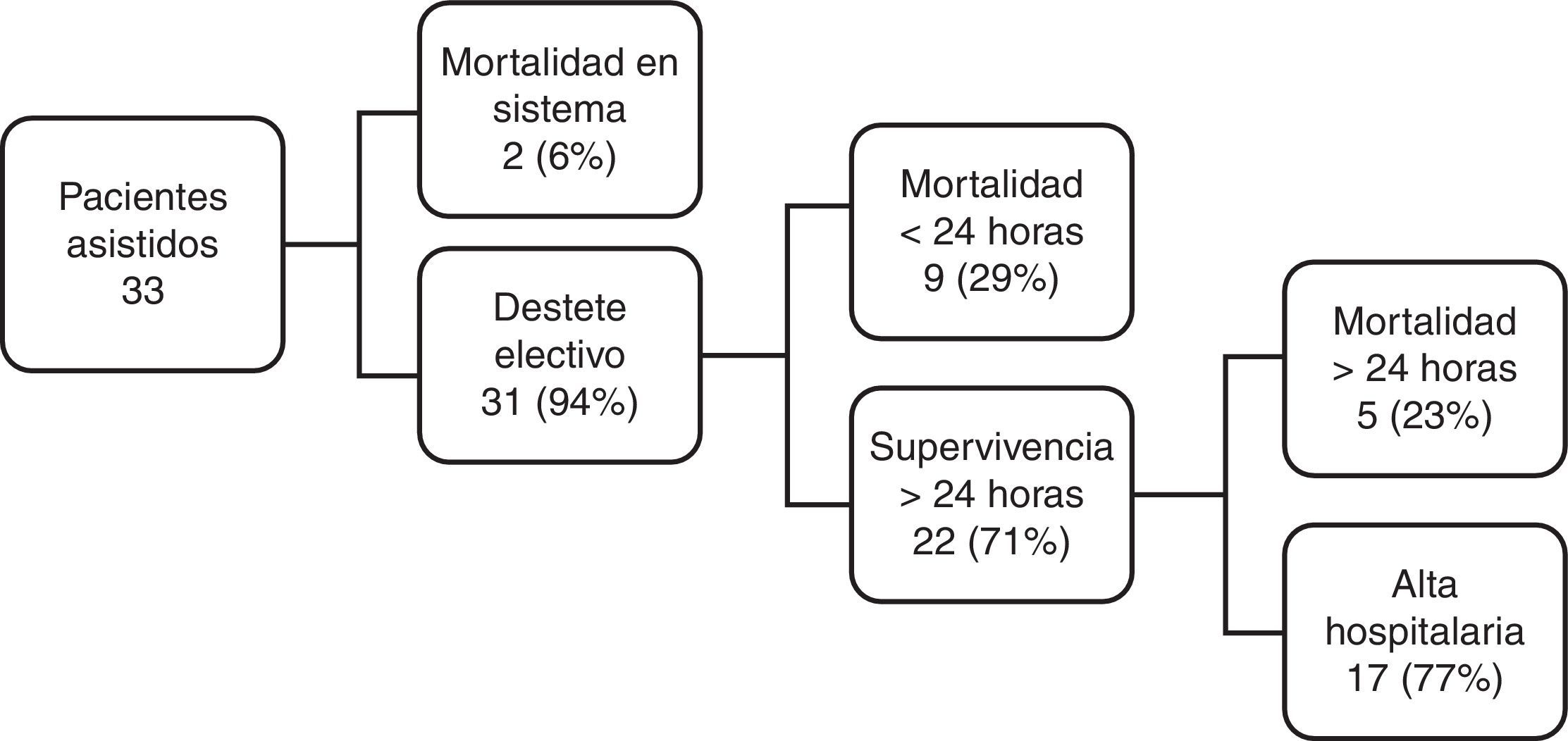
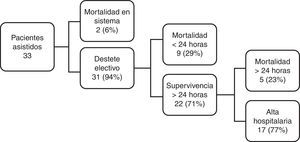
De los 33 asistidos 2 fallecieron en ECMO (uno por sangrado, otro por hemólisis), los restantes 31 (94%) fueron destetados electivamente del soporte. De estos fallecieron 9 dentro de las 24h de la decanulación y 5 en el postoperatorio alejado (3 sepsis, una insuficiencia cardiaca y una muerte cerebral). La supervivencia fue del 52%, es decir 17 pacientes fueron dados de alta hospitalaria (fig. 1).
Las complicaciones en orden de frecuencia fueron: infección sistémica en 7 casos (21%), sangrado que requirió reexploración quirúrgica 7 (21%), disfunción del circuito 3 (9%) (disfunción de las cánulas, uno; bajo flujo, uno; insuficiente retorno venoso, uno), y hemólisis con hemoglobina libre>60mg/dl en 2 (6%). Se realizó hemofiltración durante la ECMO en el 81.48% de los pacientes.
Un paciente asistido en VAD presentó como complicación quirúrgica insuficiencia valvular aórtica con dificultad para mantener un flujo anterógrado suficiente, por lo que fue necesario realizar cirugía de reemplazo de válvula aórtica con prótesis mecánica.
DiscusiónEl síndrome de bajo gasto cardiaco se encuentra presente en el postoperatorio de cirugía de cardiopatías congénitas afectando en un 25% a neonatos y niños9. A pesar del correcto tratamiento médico (asistencia ventilatoria, adecuada precarga, mejoramiento de la contractilidad y disminución de la poscarga) algunos pacientes requieren ACM para el manejo del fallo cardiorrespiratorio refractario, en espera de la recuperación de la disfunción temporal del miocardio. En este informe de nuestros primeros 6 años de experiencia, solo el 1.3% de los pacientes operados requirió ACM y la supervivencia fue similar a la informada por otros centros.
La decisión y el momento oportuno para iniciar el soporte de la circulación es fundamental cuando el tratamiento médico es insuficiente para evitar el daño irreversible de los órganos y no debería iniciarse si es demasiado tarde cuando el fallo multiorgánico se ha instalado. Asimismo, hay comunicaciones de pacientes asistidos en ECMO en forma precoz o aun como prevención del bajo gasto10.
Si bien algunos centros informan experiencia de ECMO luego de reanimación cardiopulmonar con resultados aceptables11, la intervención temprana parecería ser la clave para mejores resultados así como la realización de protocolos y el entrenamiento de un grupo de profesionales en la implementación de esta técnica.
En nuestra serie la principal causa de ingreso a ECMO fue en el 61% (n=20) por disfunción biventricular poscardiotomía sea desde el quirófano o dentro de las 48h Postoperatorias, y un solo paciente fue asistido después de reanimación cardiovascular.
La utilización del hemofiltro se incorporó como una práctica de rutina. Se realizó incluso en pacientes con diuresis conservada y fue de utilidad para obtener balance negativo y disminuir el exceso de líquidos con el fin de obtener una mejor función pulmonar para el momento del destete.
La probabilidad de recuperación de la función ventricular es posible dentro de las primeras de 72-96h de adecuado soporte en ECMO. Mantener a un paciente en ECMO más allá de este tiempo sin evidencia de mejoría de la función cardiaca estaría solo justificado como un puente al trasplante12,13.
Al igual que lo publicado o informado en la ELSO1, el sangrado fue la complicación más frecuente en nuestra serie, además de la infección sistémica. Es importante destacar que la mayoría de las complicaciones ocurrieron en los primeros pacientes de la serie. En este sentido es fundamental la conformación de un grupo de trabajo entrenado y familiarizado con el procedimiento.
La ECMO es una técnica invasiva y de costo elevado, por lo que su uso debe quedar restringido a los pacientes con una enfermedad de base potencialmente reversible en los que se haya optimizado previamente el soporte respiratorio y hemodinámico.
La supervivencia global en nuestra serie fue del 52%; si bien es un resultado alentador, podría explicarse por la menor frecuencia de ventrículos únicos que en otras series. Asimismo es importante resaltar que la ACM es una técnica agresiva con mortalidad elevada que se realiza como técnica de rescate en los pacientes en los que han fallado las demás medidas de soporte.
ConclusionesLa ACM en nuestra institución es un procedimiento estandarizado, que se utiliza en un reducido número de casos, con una supervivencia similar a la reportada internacionalmente. Es un procedimiento complejo que permitió la recuperación en un 52% de los pacientes que de otro modo hubieran fallecido.
FinanciaciónNo se recibió patrocinio de ningún tipo para llevar a cabo este estudio.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.
Al Dr. José Suárez por la revisión del manuscrito, sus consejos y apoyo para el desarrollo del programa de Asistencia Circulatoria Mecánica del Hospital de Pediatría Dr. Juan P. Garrahan.