La fibrilación auricular (FA), con una incidencia aproximada del 30%, es la arritmia más frecuente tras cirugía cardiaca. Se han asociado a la FA factores como la inflamación, la presencia de fibrosis cardiaca, el estrés y la apoptosis de cardiomiocitos.
ObjetivosConsideramos que el remodelado auricular es un proceso preexistente en los pacientes con FA posquirúrgica. Analizamos los factores relacionados con la incidencia de FA en el postoperatorio de cirugía cardiaca.
MétodosIncluimos a pacientes consecutivos, estables hemodinámicamente y en ritmo sinusal, sometidos a cirugía cardiaca programada con circulación extracorpórea. Se valora la caída en FA posquirúrgica.
ResultadosSe incluyeron un total de 100 pacientes sometidos a cirugía de revascularización coronaria (59) o sustitución valvular aórtica (41) por estenosis aórtica grave. La FA postoperatoria se produjo en 29 pacientes con predominio de la cirugía valvular respecto a la cirugía coronaria. Los factores predictivos de la aparición de FA postoperatoria en el análisis multivariable fueron el sexo masculino, la ausencia de terapia crónica con betabloqueadores, la perfusión de fibrinógeno intraoperatorio, valores bajos de colesterol HDL y valores elevados de troponina T ultrasensible en el preoperatorio.
ConclusionesEl colesterol HDL y la troponina T ultrasensible pueden ser biomarcadores útiles para predecir la aparición de FA postoperatoria. La identificación precoz de estos pacientes nos permite adoptar medidas preventivas para minimizar sus efectos negativos.
Atrial fibrillation (AF) has an incidence rate of approximately 30% and is the most frequent arrhythmia following heart surgery. Factors such as inflammation, the presence of heart fibrosis, stress and cardiomyocyte apoptosis, have all been associated with AF.
ObjectivesWe believe that atrial remodelling is a pre-existent process in patients with post-surgical AF. We have analyzed the factors related to the incidence of atrial fibrillation in the period after heart surgery.
MethodsWe included consecutive, hemodynamically stable patients with a sinusal rhythm who were subjected to programmed heart surgery with extracorporeal circulation. An assessment was made of the fall in atrial fibrillation after surgery using prolonged electrocardiographic monitoring.
ResultsA total of 100 patients were included in the study and were subjected to either coronary revascularisation surgery (59) or aortic valve substitution due to severe aortic stenosis (41). Postoperative AF occurred in 29 patients who received predominantly more valve surgery than coronary surgery. The following factors were predictive of postoperative AF in the multivariate analysis: Male sex; beta-blocker therapy for chronic disease; the use of intraoperative; fibrinogen perfusion; low HDL cholesterol values; and high sensitive troponin T values, in the preoperative period.
ConclusionsHDL cholesterol and high sensitive troponin T can be useful biomarkers to predict the occurrence of AF after surgery. The early identification of these patients who develop of FA allows us to take preventive measures to minimize the negative effects.
La complicación arrítmica más frecuente después de cirugía cardiaca es la fibrilación auricular (FA). La FA después de cirugía de revascularización coronaria ocurre en aproximadamente el 30% de los pacientes, mientras que después de cirugía valvular aparece en el 40% de los casos. La incidencia de FA aumenta al 50% en la cirugía combinada1.
La FA postoperatoria afecta de manera negativa a la morbimortalidad quirúrgica y tiene como consecuencia el aumento del tiempo de estancia hospitalaria, mayor uso de recursos e incremento en el costo sanitario2,3.
Son varios los factores que se asocian a la aparición de FA después de cirugía cardiaca4. Estos factores pueden ser preoperatorios, como sexo, edad avanzada5,6, la hipertensión arterial, la diabetes, la insuficiencia cardiaca, y el volumen auricular, o perioperatorios como el tipo de cirugía cardiaca, el tiempo de circulación extracorpórea (CEC) o el uso de balón de contrapulsación intraaórtico. Entre los mecanismos que facilitan el desarrollo de esta arritmia, encontramos la inflamación, la presencia de fibrosis cardiaca, el estrés y la apoptosis de cardiomiocitos7.
Este estudio, además de determinar la incidencia de FA en el postoperatorio de cirugía cardiaca, pretende identificar los factores preoperatorios y perioperatorios que influyen en el desarrollo de la misma. Se miden determinados biomarcadores con un potencial uso para predecir la aparición de FA tras cirugía cardiaca.
MétodosEntre noviembre de 2010 y marzo de 2012 se incluyeron de manera consecutiva 100 pacientes con cardiopatía isquémica o estenosis aórtica grave, estables hemodinámicamente y en ritmo sinusal previo. Los pacientes se sometieron a cirugía programada de revascularización coronaria o de sustitución valvular aórtica mediante CEC.
Fueron excluidos aquellos pacientes con antecedentes de FA en cualquiera de sus presentaciones, otra valvulopatía cardiaca superior a ligera, insuficiencia renal (aclaramiento de creatinina<60ml/h), insuficiencia hepática y enfermedad inflamatoria crónica o neoplásica.
A todos los pacientes se les realizó una historia clínica y exploración física detallada. Se recogieron datos relacionados con el tratamiento crónico previo a la cirugía, especialmente el uso de inhibidores de la enzima convertidora de angiotensina, antagonistas del receptor de angiotensina ii, antagonistas del calcio, betabloqueadores y estatinas.
El estudio preoperatorio incluyó un ecocardiograma transtorácico y una coronariografía. El ecocardiograma determinó el área y gradientes valvulares, la FEVI, el tabique interventricular, los diámetros de aurícula y ventrículo izquierdos, y las ondas E y A.
Se anotaron variables quirúrgicas como tiempo de CEC y de pinzamiento aórtico, tipo de cardioplejía, temperatura mínima alcanzada durante la CEC, tipo de injerto para derivación, uso de balón de contrapulsación intraaórtico y de aminas intraoperatorias.
Se valoró la caída en FA durante el periodo postoperatorio en UCI mediante telemetría continua de 3 derivaciones y posteriormente, registro Holter de 7 días de duración. A los pacientes que presentaron síntomas durante la hospitalización se les realizó un electrocardiograma de 12 derivaciones.
Se realizaron análisis sanguíneos 24 horas antes y 24h después de la cirugía. Se determinaron entre otros, valores de troponina T ultrasensible (TnTus), proteína C reactiva, interleucina 6 y péptido natriurético cerebral.
Consideramos el episodio de FA como sostenido cuando su duración es>2min. La FA se definió por la ausencia de onda p antes del complejo QRS junto con un ritmo ventricular irregular. Se consideró FA clínica al episodio de FA sintomático durante la estancia en planta y registrado en electrocardiograma basal.
Métodos estadísticosLas variables numéricas se presentan como media±desviación estándar, mientras que las variables discretas se resumen mediante frecuencias absolutas y porcentajes.
Se utilizó la prueba de Ji-cuadrado como método para comparar las medias y porcentajes de las distintas variables cualitativas.
Previo al análisis de las variables continuas, se utilizó la prueba de Kolmogorov-Smirnov para identificar el tipo de distribución. En los casos de distribución normal se utilizó la prueba de T de Student, mientras que para las variables que seguían una distribución no normal, se utilizó el estadístico U de Mann Withney.
A su vez, se llevó a cabo un análisis comparativo de medias para múltiples variables. En las que seguían una distribución normal se utilizó el ANOVA de un factor, mientras que en aquellas que seguían una distribución no normal se realizó la prueba H de Kruskal-Wallis.
Se elaboró un modelo de regresión logística multivariable para los factores de riesgo que predecían la FA postoperatoria de nueva aparición. Las asociaciones de valores predictivos independientes con la FA en el modelo final se expresaron mediante la razón de posibilidades con su IC del 95%.
En algunas variables, como el valor de TnTus en el preoperatorio, se determinó un punto de corte mediante la creación de curvas ROC que permitió aumentar la rentabilidad del estudio de regresión.
Los datos obtenidos fueron procesados en el programa informático IBM SPSS Statistics 21.0 (SPSS Inc, Chicago, IL, EE. UU.).
ResultadosDurante el periodo de estudio se intervinieron 100 pacientes, 59 de ellos se sometieron a cirugía de revascularización coronaria y 41 a sustitución valvular aórtica. La relación entre hombres (77) y mujeres (23) fue de 3.3:1; la media de edad fue de 65.14±9.54 años. Las características basales de los pacientes se presentan en la tabla 1.
Características basales de los pacientes incluidos (n=100)
| Variable clínica | %, media±desviación estándar |
|---|---|
| Edad (años) | 65.1±9.5 |
| Edad>60 | 72 |
| Sexo masculino | 77 |
| IMC | 29±4 |
| Tabaquismo | 23 |
| Etilismo | 8 |
| HTA | 70 |
| Dislipidemia | 65 |
| Diabetes | 47 |
| Insulinodependiente | 12 |
| ADO | 38 |
| Cardiopatía isquémica familiar | 29 |
| ACV | 9 |
| EVP | 7 |
| EPOC | 8 |
| NYHA | |
| NYHA I | 33 |
| NYHA II | 50 |
| NYHA III | 17 |
| Euroscore | 4 (2-5) |
| Betabloqueadores | 49 |
| Estatinas | 65 |
| FEVI | 57.7±12.9 |
| DAI | 40.7±5.2 |
| IVAI | 33.9±5 |
| N.ode vasos afectados>2 | 33 |
| TCI>50% | 35 |
ACV: accidente cerebrovascular agudo; ADO: antidiabéticos orales; DAI: diámetro aurícula izquierda; EPOC: enfermedad pulmonar obstructiva crónica; EVP: enfermedad vascular periférica; FEVI: fracción de eyección ventrículo izquierdo; HTA: hipertensión arterial; IMC: índice de masa corporal; IVAI: índice volumen aurícula izquierda; NYHA: New York Heart Association; TCI: tronco coronario izquierdo.
Se produjo FA postoperatoria en un 29% de los casos (29 pacientes), de los cuales, el 69% (20 pacientes) presentó FA clínica. La aparición de FA durante la estancia en UCI fue del 13%. La duración del episodio de fibrilación auricular sostenido más prolongado en cada paciente que sufrió el evento fue de 12.22±13.68h (rango: 1-68h).
Entre los pacientes que presentaron FA, el 65.52% (19 pacientes) precisó terapia antiarrítmica con amiodarona o cardioversión eléctrica (16 y 3 pacientes respectivamente) y en todos los casos se consiguió revertir a ritmo sinusal.
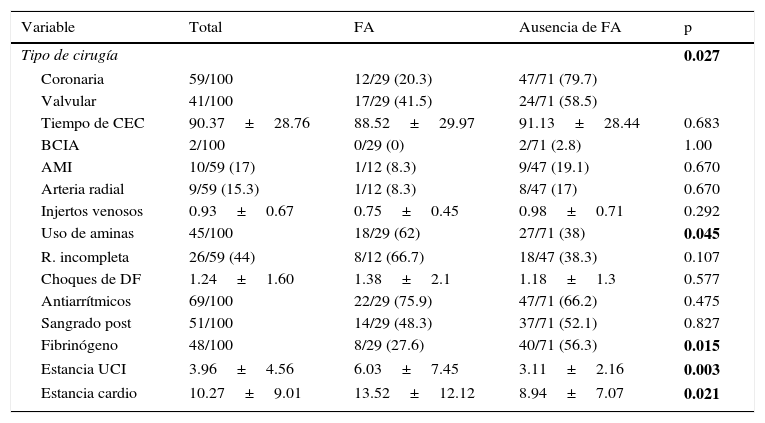
El análisis de Ji-cuadrado objetivó que en los pacientes operados de estenosis aórtica grave aparece con más frecuencia FA sostenida en el postoperatorio (41.5 vs. 20.3%, p=0.027). Dicho análisis encontró significación estadística para la variable edad (p=0.05): Los pacientes>60 años tendrían mayor incidencia de FA posquirúrgica.
Los grados ii y iii de la New York Heart Association se asocian a una mayor incidencia de FA postoperatoria (p=0.032), sin embargo, esta asociación se pierde en el análisis multivariado (tabla 2). La prevalencia de antecedentes como enfermedad pulmonar obstructiva crónica, síndrome de apnea obstructiva del sueño, accidente cerebrovascular, arteriopatía periférica y enfermedad tiroidea en los grupos con o sin aparición de FA postoperatoria fue similar.
Variables perioperatorias en relación con la FA posquirúrgica
| Variable | Total | FA | Ausencia de FA | p |
|---|---|---|---|---|
| Tipo de cirugía | 0.027 | |||
| Coronaria | 59/100 | 12/29 (20.3) | 47/71 (79.7) | |
| Valvular | 41/100 | 17/29 (41.5) | 24/71 (58.5) | |
| Tiempo de CEC | 90.37±28.76 | 88.52±29.97 | 91.13±28.44 | 0.683 |
| BCIA | 2/100 | 0/29 (0) | 2/71 (2.8) | 1.00 |
| AMI | 10/59 (17) | 1/12 (8.3) | 9/47 (19.1) | 0.670 |
| Arteria radial | 9/59 (15.3) | 1/12 (8.3) | 8/47 (17) | 0.670 |
| Injertos venosos | 0.93±0.67 | 0.75±0.45 | 0.98±0.71 | 0.292 |
| Uso de aminas | 45/100 | 18/29 (62) | 27/71 (38) | 0.045 |
| R. incompleta | 26/59 (44) | 8/12 (66.7) | 18/47 (38.3) | 0.107 |
| Choques de DF | 1.24±1.60 | 1.38±2.1 | 1.18±1.3 | 0.577 |
| Antiarrítmicos | 69/100 | 22/29 (75.9) | 47/71 (66.2) | 0.475 |
| Sangrado post | 51/100 | 14/29 (48.3) | 37/71 (52.1) | 0.827 |
| Fibrinógeno | 48/100 | 8/29 (27.6) | 40/71 (56.3) | 0.015 |
| Estancia UCI | 3.96±4.56 | 6.03±7.45 | 3.11±2.16 | 0.003 |
| Estancia cardio | 10.27±9.01 | 13.52±12.12 | 8.94±7.07 | 0.021 |
AMI: uso de 2 arterias mamarias internas; BCIA: balón de contrapulsacion intraaórtico; CEC: circulación extracorpórea; DF: desfibrilación; FA: fibrilación auricular; R. incompleta: revascularización incompleta; UCI: unidad de cuidados intensivos.
En negrita, los valores con significación estadística.
Se encontró significación estadística para el tratamiento crónico con betabloqueadores previo a la cirugía (p=0.028), de manera que dicha terapia reduciría la incidencia de FA posquirúrgica. Sin embargo, en el análisis para el tratamiento crónico con estatinas no se encontró diferencias significativas.
En los pacientes que reciben aminas durante la cirugía aumenta la incidencia de FA postoperatoria (40 vs. 20%, p=0.045).
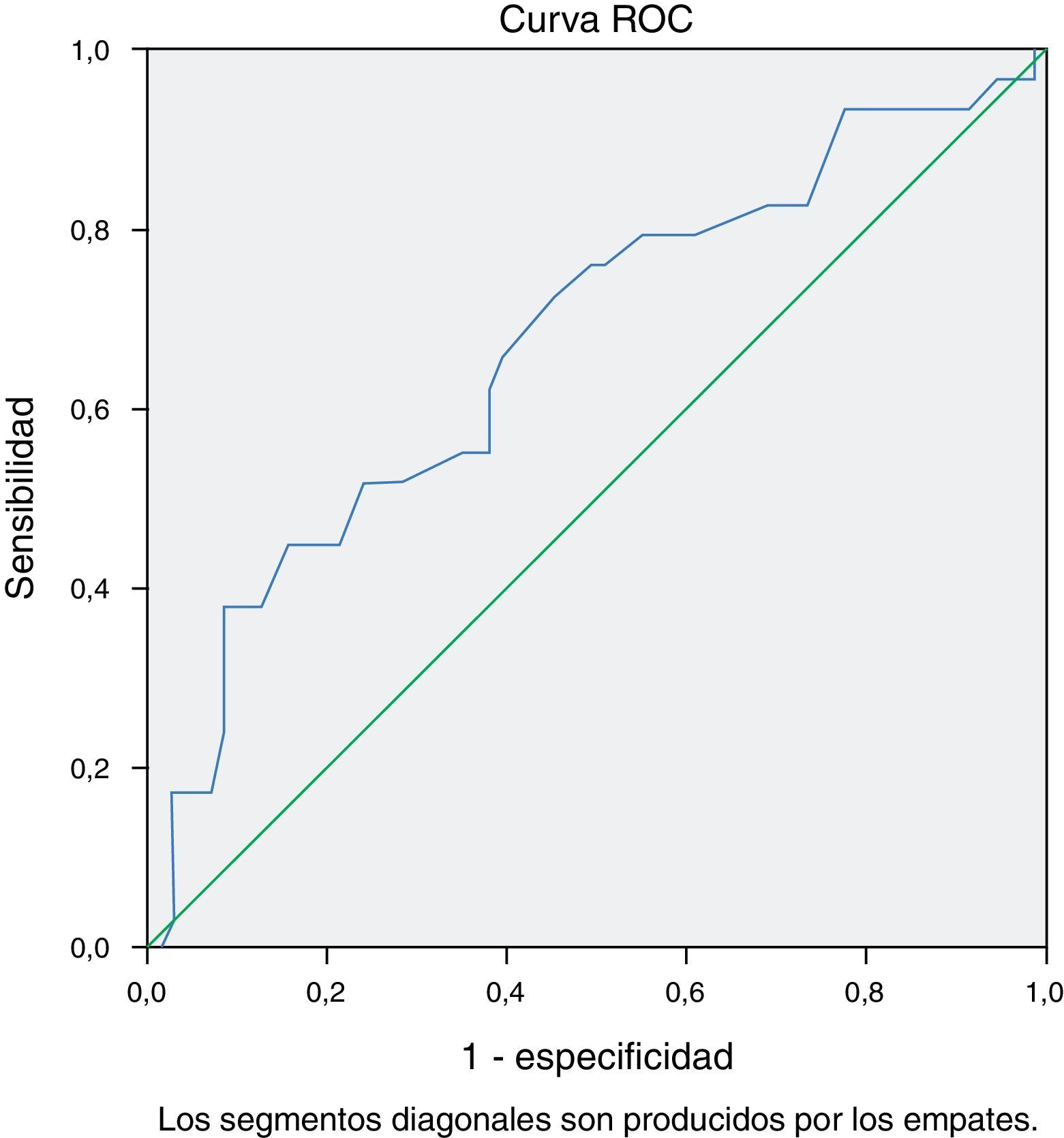
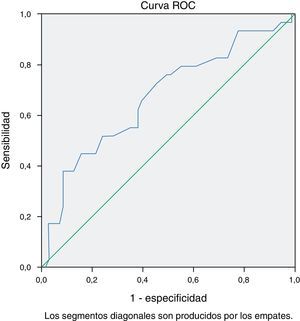
El análisis mediante curva ROC de los valores de TnTus objetivó la asociación con el desarrollo de FA sostenida (fig. 1). El área bajo la curva fue de 0.66 (0.54-0.78) con valor de p=0.015. El mejor punto de corte fue 11.86ng TnTus/l con una sensibilidad de 0.76 y una especificidad de 0.54.
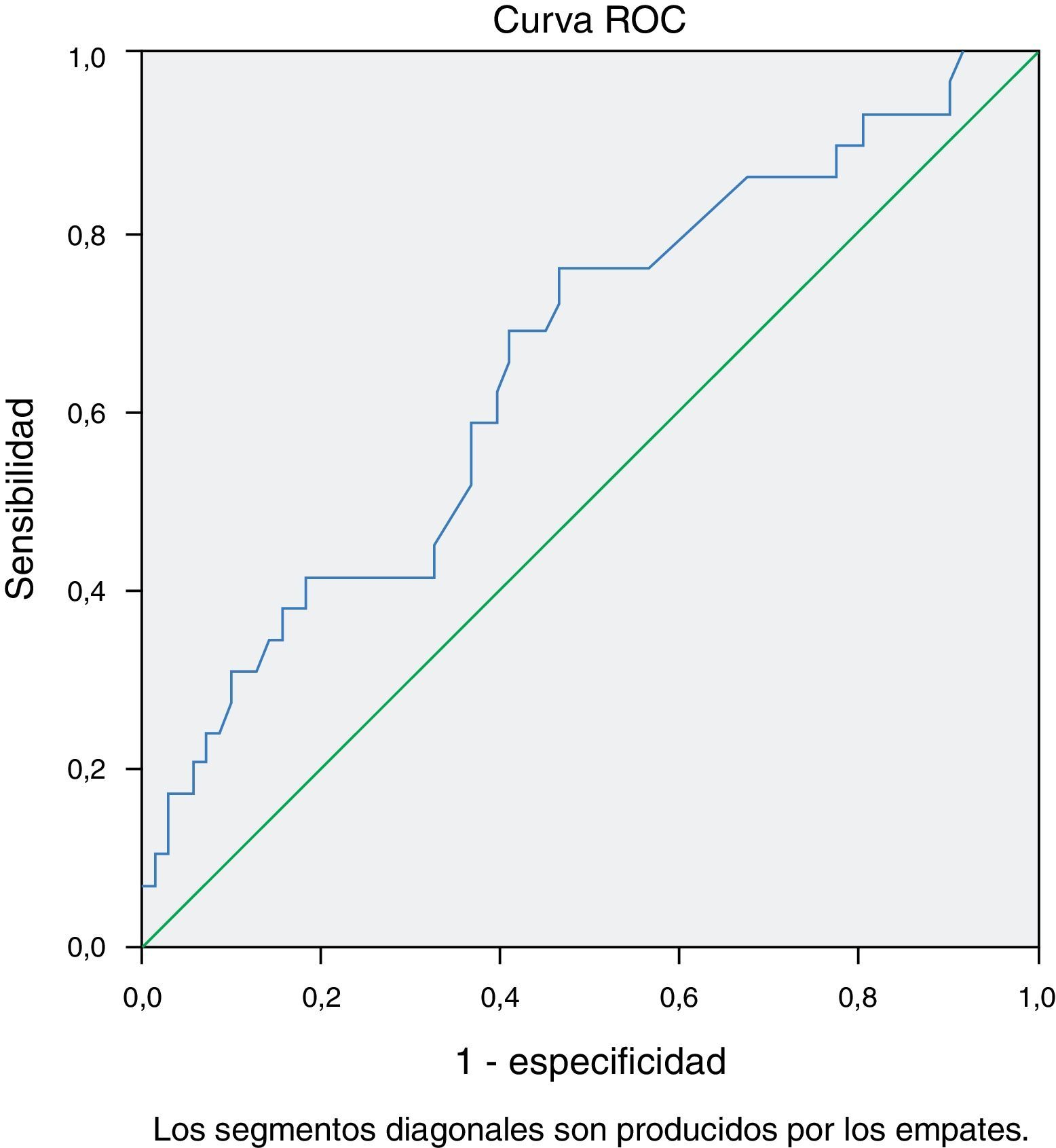
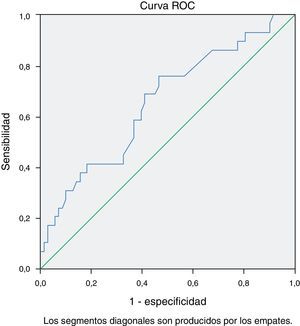
El análisis mediante curva ROC de los valores de colesterol HDL (c-HDL) en el preoperatorio mostró asociación con la aparición de FA postoperatoria (fig. 2). El área bajo la curva fue de 0.67 (0.55-0.79) con valor de p=0.007. El mejor punto de corte fue 38.26mg/dl con una sensibilidad del 76% y una especificidad del 50%.
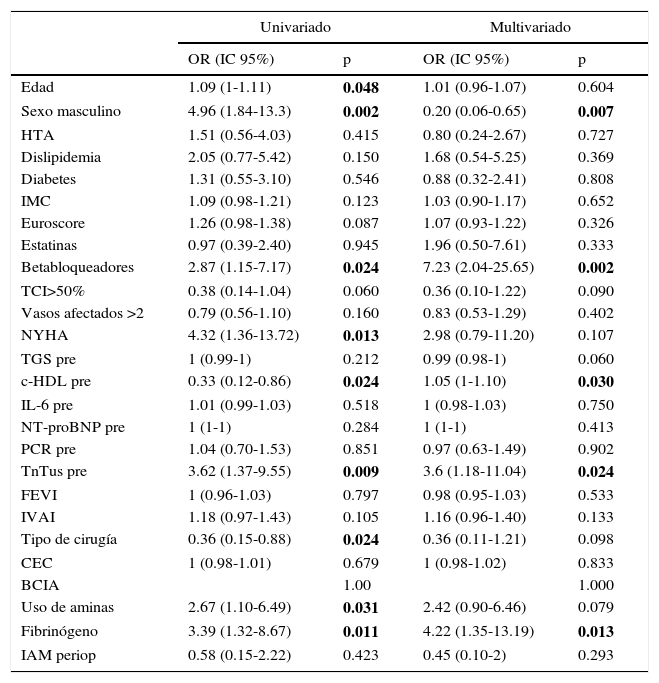
Los factores predictivos de la aparición de FA postoperatoria en el modelo multivariable fueron: el sexo masculino (OR=4.79, p=0.009), el tratamiento con betabloqueadores (OR=7.23, p=0.002), valores preoperatorios elevados de TnTus (OR=0.27, p=0.023), valores reducidos de c-HDL (OR=0.30, p=0.031) y la perfusión de≥2g de fibrinógeno. Sin embargo, variables como la edad, el tipo de cirugía y el uso de aminas durante la cirugía perdieron su significación en el análisis multivariado (tabla 3).
Análisis de regresión logística para los predictores de FA posquirúrgica
| Univariado | Multivariado | |||
|---|---|---|---|---|
| OR (IC 95%) | p | OR (IC 95%) | p | |
| Edad | 1.09 (1-1.11) | 0.048 | 1.01 (0.96-1.07) | 0.604 |
| Sexo masculino | 4.96 (1.84-13.3) | 0.002 | 0.20 (0.06-0.65) | 0.007 |
| HTA | 1.51 (0.56-4.03) | 0.415 | 0.80 (0.24-2.67) | 0.727 |
| Dislipidemia | 2.05 (0.77-5.42) | 0.150 | 1.68 (0.54-5.25) | 0.369 |
| Diabetes | 1.31 (0.55-3.10) | 0.546 | 0.88 (0.32-2.41) | 0.808 |
| IMC | 1.09 (0.98-1.21) | 0.123 | 1.03 (0.90-1.17) | 0.652 |
| Euroscore | 1.26 (0.98-1.38) | 0.087 | 1.07 (0.93-1.22) | 0.326 |
| Estatinas | 0.97 (0.39-2.40) | 0.945 | 1.96 (0.50-7.61) | 0.333 |
| Betabloqueadores | 2.87 (1.15-7.17) | 0.024 | 7.23 (2.04-25.65) | 0.002 |
| TCI>50% | 0.38 (0.14-1.04) | 0.060 | 0.36 (0.10-1.22) | 0.090 |
| Vasos afectados >2 | 0.79 (0.56-1.10) | 0.160 | 0.83 (0.53-1.29) | 0.402 |
| NYHA | 4.32 (1.36-13.72) | 0.013 | 2.98 (0.79-11.20) | 0.107 |
| TGS pre | 1 (0.99-1) | 0.212 | 0.99 (0.98-1) | 0.060 |
| c-HDL pre | 0.33 (0.12-0.86) | 0.024 | 1.05 (1-1.10) | 0.030 |
| IL-6 pre | 1.01 (0.99-1.03) | 0.518 | 1 (0.98-1.03) | 0.750 |
| NT-proBNP pre | 1 (1-1) | 0.284 | 1 (1-1) | 0.413 |
| PCR pre | 1.04 (0.70-1.53) | 0.851 | 0.97 (0.63-1.49) | 0.902 |
| TnTus pre | 3.62 (1.37-9.55) | 0.009 | 3.6 (1.18-11.04) | 0.024 |
| FEVI | 1 (0.96-1.03) | 0.797 | 0.98 (0.95-1.03) | 0.533 |
| IVAI | 1.18 (0.97-1.43) | 0.105 | 1.16 (0.96-1.40) | 0.133 |
| Tipo de cirugía | 0.36 (0.15-0.88) | 0.024 | 0.36 (0.11-1.21) | 0.098 |
| CEC | 1 (0.98-1.01) | 0.679 | 1 (0.98-1.02) | 0.833 |
| BCIA | 1.00 | 1.000 | ||
| Uso de aminas | 2.67 (1.10-6.49) | 0.031 | 2.42 (0.90-6.46) | 0.079 |
| Fibrinógeno | 3.39 (1.32-8.67) | 0.011 | 4.22 (1.35-13.19) | 0.013 |
| IAM periop | 0.58 (0.15-2.22) | 0.423 | 0.45 (0.10-2) | 0.293 |
BCIA: balón de contrapulsacion intraaórtico; CEC: circulación extracorpórea; c-HDL: colesterol HDL; FEVI: fracción de eyección de ventrículo izquierdo; HTA: hipertensión arterial; IAM: infarto agudo de miocardio; IC: intervalo de confianza; IL-6: interleucina 6;IMC: índice de masa corporal; IVAI: índice volumen aurícula izquierda; NT-proBNP: péptido natriurético cerebral; NYHA: New York Heart Association; OR: odds ratio; PCR: proteína C reactiva; TCI: tronco coronario izquierdo; TGS pre: triglicéridos en el preoperatorio; TnTus: troponina T ultrasensible.
En negrita, los valores con significación estadística.
Los pacientes que presentaron FA postoperatoria permanecieron más tiempo ingresados tanto en la unidad de cardiología como en cuidados intensivos (p de 0.003 y 0.021 respectivamente) (tabla 2).
DiscusiónSegún la literatura, la incidencia de FA después de cirugía cardiaca abierta es de casi el 30%. En nuestro estudio identificamos un 29% de FA postoperatoria. Son varios los factores que se han asociado al desarrollo de FA después de cirugía cardiaca. El uso de betabloqueadores de forma crónica antes de la cirugía reduce la incidencia de FA postoperatoria8,9. En nuestro estudio se objetiva una menor incidencia de FA en los pacientes que previamente estaban recibiendo tratamiento con betabloqueadores, de manera que podemos considerarlo un factor protector frente a la aparición del evento, tal como ha sido reportado previamente10.
Sin embargo, a diferencia de estudios como el de Kokkonen et al.6, el factor edad no pudimos asociarlo a una mayor incidencia de FA, lo que puede explicarse por un pequeño tamaño muestral.
Dentro de los mecanismos favorecedores de la FA posquirúrgica se encuentran la inflamación, la fibrosis, el estrés y la apoptosis de cardiomiocitos. Existen marcadores bioquímicos como la proteína C reactiva y la interleucina 6 que miden la inflamación11 y otros como el péptido natriurético cerebral que se relacionan con el estrés de los cardiomiocitos. Nuestro estudio no ha encontrado significación estadística para estos marcadores. Sin embargo, hemos hallado una importante asociación entre los valores de TnTus y el desarrollo de FA en el postoperatorio. La TnTus podría utilizarse como biomarcador de FA después de cirugía cardiaca; valores por encima de 11.86ng/l indicarían una mayor incidencia de FA. Las troponinas son marcadores sensibles y específicos del daño miocárdico y han demostrado ser un factor pronóstico independiente en los síndromes coronarios agudos12. Se ha propuesto que las concentraciones elevadas de troponina T pueden ser debidas a la presencia de daño miocárdico en curso y puede reflejar la pérdida de miocitos viables característica de la insuficiencia cardiaca progresiva13. Autores como Moreno et al.14 observaron que valores elevados en suero de TnTus se asociaron con la gravedad de la miocardiopatía hipertrófica, lo que indica que la TnTus podría ser un biomarcador de la remodelación cardiaca en esta enfermedad como indicador de daño miocárdico subclínico. En la actualidad se están desarrollando métodos de ensayo muy sensibles para las troponinas cardiacas; se considera que estas son marcadores biológicos de la apoptosis de miocitos, procesos de remodelado o del aumento del recambio celular fisiológico que ocurre en diferentes orígenes etiológicos de la lesión cardiaca15,16. El remodelado estructural se ha propuesto como el sustrato arritmogénico que perpetúa la FA17.
Otro factor independiente predictivo de FA postoperatoria es el nivel bajo de c-HDL, valores<38.26mg/dl marcarían un riesgo para el desarrollo de FA. El hallazgo de la asociación entre las cifras bajas de c-HDL y la aparición del evento nos parece de una gran importancia y debería ampliarse en futuros estudios. Sería interesante analizar el efecto del aumento de las cifras de c-HDL (utilizando medidas higiénicas y toma de ácidos grasos monoinsaturados) en la incidencia de FA postoperatoria.
Otras lipoproteínas como el c-LDL no están relacionadas con la aparición de FA postoperatoria, como ocurre en el estudio de Baeza et al.10.
A diferencia de autores como Arribas-Leal et al.18, nosotros no hemos encontrado un efecto protector de las estatinas frente al desarrollo de FA posquirúrgica. Estos autores describen el beneficio del tratamiento con estatinas derivado de la mejora del metabolismo lipídico y la prevención de la aterosclerosis, además de sus acciones antiinflamatorias y antioxidantes y de la reducción de la disfunción endotelial y activación neurohormonal. Deberán realizarse estudios más amplios que permitan aclarar el papel de las estatinas en la protección frente a la FA postoperatoria.
Como factores perioperatorios hemos objetivado la asociación de la perfusión de fibrinógeno con el desarrollo de FA tras la cirugía. Pensamos que este resultado debería ser el inicio de un estudio más amplio que comparase la aparición de FA posquirúrgica entre grupos sometidos o no a tratamiento con fibrinógeno.
A diferencia del estudio de Shirzad et al.19, nuestros resultados no demostraron asociación entre el uso de balón de contrapulsación intraaórtico y el desarrollo de FA después de cirugía cardiaca.
Dentro de las limitaciones de este estudio incluimos, en primer lugar, el escaso tamaño de la muestra poblacional; en segundo lugar, el tratarse de un estudio monocentro, así existen factores como el escaso uso de balón de contrapulsación que nos impiden evaluar su efecto sobre el desarrollo de FA; en tercer lugar, señalar que solo hemos incluido 2 tipos de tratamiento quirúrgico, de manera que desconocemos el resultado de estos marcadores en otros grupos de pacientes; y por último el diseño, que limita la relación de causalidad y solo permite analizar asociaciones.
ConclusionesEl c-HDL y la TnTus pueden ser biomarcadores útiles para predecir la aparición de FA postoperatoria. La identificación precoz de los pacientes que presentarán FA nos permite adoptar medidas preventivas para minimizar sus efectos negativos.
FinanciaciónNo se recibió patrocinio de ningún tipo para llevar a cabo este estudio.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.