El infarto agudo de miocardio representa la primera causa de muerte no trasmisible a nivel mundial. Su diagnóstico es una tarea altamente compleja que se ha intentado modelar mediante métodos automáticos. Se expone una revisión sistemática de estudios de pruebas diagnósticas de los síndromes coronarios agudos mediante sistemas inteligentes.
MétodosRevisión sistemática de la literatura a partir de Medline, Embase, Scopus, IEEE/IET Electronic Library, ISI Web Of Science, Latindex y LILACS de la evaluación diagnóstica de los síndromes coronarios agudos mediante sistemas inteligentes. Fue realizada por 2 revisores de manera independiente y las discrepancias se resolvieron por una tercera persona. Se extrajeron las características operativas de cada herramienta.
ResultadosEn total, 35 artículos cumplieron los criterios de inclusión. En 22 (62.8%) se utilizaron redes neuronales. Cinco comparan varias herramientas de sistemas inteligentes. En 13 se abarcaba todos los síndromes coronarios agudos y en 22 solo los infartos. En 21 los datos de entrada fueron la clínica y el electrocardiograma, en 10 solo el electrocardiograma. La mayoría utilizan como referente estándar el contexto clínico. Se encontraron altos niveles de precisión diagnóstica con un mejor rendimiento en el caso de redes neuronales y máquinas de soporte de vectores en comparación con las herramientas estadísticas de reconocimiento de patrones y árboles de decisiones.
ConclusionesEncontramos una amplia evidencia de que los abordajes a través de las herramientas de sistemas inteligentes alcanzan un alto nivel de precisión por lo que deberían ser consideradas como herramientas para el soporte de las decisiones diagnósticas de los síndromes coronarios agudos.
Acute myocardial infarction is the leading cause of non-communicable deaths worldwide. Its diagnosis is a highly complex task, for which modelling through automated methods has been attempted. A systematic review of the literature was performed on diagnostic tests that applied intelligent systems tools in the diagnosis of acute coronary syndromes.
MethodsA systematic review of the literature is presented using Medline, Embase, Scopus, IEEE/IET Electronic Library, ISI Web of Science, Latindex and LILACS databases for articles that include the diagnostic evaluation of acute coronary syndromes using intelligent systems. The review process was conducted independently by 2 reviewers, and discrepancies were resolved through the participation of a third person. The operational characteristics of the studied tools were extracted.
ResultsA total of 35 references met the inclusion criteria. In 22 (62.8%) cases, neural networks were used. In five studies, the performances of several intelligent systems tools were compared. Thirteen studies sought to perform diagnoses of all acute coronary syndromes, and in 22, only infarctions were studied. In 21 cases, clinical and electrocardiographic aspects were used as input data, and in 10, only electrocardiographic data were used. Most intelligent systems use the clinical context as a reference standard. High rates of diagnostic accuracy were found with better performance using neural networks and support vector machines, compared with statistical tools of pattern recognition and decision trees.
ConclusionsExtensive evidence was found that shows that using intelligent systems tools achieves a greater degree of accuracy than some clinical algorithms or scales and, thus, should be considered appropriate tools for supporting diagnostic decisions of acute coronary syndromes.
La enfermedad cardiovascular es la principal causa de muerte en los países industrializados y se espera que para el año 2020 también lo sea para los países en vía de desarrollo1. Una de sus formas de presentación, los síndromes coronarios agudos (SCA), es la principal causa mortalidad. Este síndrome es una entidad con un alto grado de complejidad que para su diagnóstico requiere considerar los datos de la historia clínica, los antecedentes personales y familiares, en conjunto con varias ayudas diagnósticas sustentadas principalmente en el electrocardiograma (ECG), biomarcadores, las pruebas de estratificación no invasivas y la angiografía coronaria. Por lo general, debe llevarse a cabo en el ambiente de urgencias en el que la rapidez del diagnóstico es esencial y existe además una amplia variedad de diagnósticos diferenciales que incluyen otras condiciones que pueden poner en peligro la vida del paciente.
Los esfuerzos en la atención clínica incluyen de manera cada vez más frecuente el uso de instrumentos de gestión electrónica, dentro de las que se incluyen las herramientas inteligentes, con el objetivo de mejorar los tiempos y la precisión en el diagnóstico para brindar una servicio de mayor calidad constituyendo esto un paradigma en el modelo de atención que incluye un soporte a las decisiones clínicas2. Se entiende como «sistemas inteligentes» aquellos intentos de emular la inteligencia humana, los cuales favorecen el razonamiento y aprendizaje en ambientes inciertos o imprecisos3, término que es sinónimo, hasta cierto punto, de los de inteligencia artificial, inteligencia computacional y reconocimiento de patrones. Está constituido principalmente por: sistemas basados en reglas (o sistemas expertos), redes neuronales artificiales (ANN), computación evolutiva, lógica difusa, máquinas de soporte de vectores (SVM), redes de creencia bayesianas, árboles de decisiones, sistemas de ensamble como Ada-Boost y Bagging, sistemas multiagentes (o agentes racionales colaborativos) entre otros.
Una revisión sistemática llevada a cabo en el 2010, en la que se evaluó el valor de los instrumentos para descartar los SCA, encontró que ninguna de ellas logró cumplir con los requerimientos de seguridad para los clínicos al momento de soportar el diagnóstico4. Dicha revisión incluyó solo herramientas basadas en reglas diseñadas por los médicos y modelos de regresión logística; no se tuvo en cuenta las que estaban basadas en sistemas inteligentes. Ninguna de las guías de práctica clínica actual que abordan el diagnóstico del dolor torácico hace alguna consideración acerca de su uso5–7.
Al tratarse de un problema altamente complejo, el diagnóstico médico ha generado la necesidad de buscar una forma para lograr su estandarización como proceso, se ha convertido en un campo de estudio para la aplicación de los sistemas inteligentes, por lo que su aplicación reviste interés especial en la entidad clínica responsable de la mayor cantidad de muertes en el mundo. Es por ello que en el presente trabajo se lleva a cabo una revisión sistemática de la literatura de los estudios de pruebas diagnósticas que evalúen la aplicación de herramientas de sistemas inteligentes en el diagnóstico de los SCA, las cuales puedan ser aplicadas al paciente que consulta por dolor torácico a urgencias.
MetodologíaEstrategia de búsquedaSe consultaron las siguientes bases de datos; Medline, Embase, Scopus, IEEE/IET Electronic Library e ISI Web Of Science, Latindex y LILACS; la búsqueda incluyó información hasta abril de 2014 y se limitó a estudios publicados en inglés o en español. En el material suplementario se exponen los términos usados en cada base de datos. La condición a estudio fueron los SCA que se encuentran constituidos por el infarto agudo de miocardio con y sin elevación del segmento ST así como por la angina inestable. Se tomó como prueba índice los diferentes aplicativos con el uso de sistemas inteligentes para el apoyo diagnóstico de los SCA.
Al poner en consideración la evolución temporal del diagnóstico de los SCA, principalmente del infarto, se decidió no limitar el referente de diagnóstico a un conjunto predefinido de estudios revisando que fueran apropiados para la época. En todo caso se describen rigurosamente dentro de los resultados los criterios de cada estudio para la definición de los casos.
Criterios de inclusiónSe incluyeron todos los estudios publicados que utilizaron herramientas de sistemas inteligentes para el diagnóstico de los SCA independientemente de la duración del seguimiento o el estatus de la publicación. Solo se incluyeron los artículos en idioma inglés o español.
Criterios de exclusiónNo se consideraron aquellos estudios que evaluaron: solo el ECG mediante procesamiento directo de la señal, estudios de Holter, formas alternas para su toma (p. ej.: ECG ortogonal, magnetocardiogramas) o procesamiento alterno de la señal de este (p. ej.: transformación discreta de ondas), el resultados de la prueba de esfuerzo convencional (ECG de ejercicio), reconocimiento de imágenes de perfusiones miocárdicas, tomografía, resonancia magnética nuclear o angiografía coronaria invasiva, telemetría u otros conceptos de computación ubicua, evaluaciones de factores de riesgo o pronóstico del SCA o intervenciones terapéuticas, se descartaron los que evaluaban el síndrome de muerte súbita, debido a que corresponde a un espectro diferente de los SCA.
Selección de los estudios y extracción de los datosSe hizo una selección de los artículos que cumplieran los criterios de inclusión para esta revisión mediante la lectura del título y el resumen; para los artículos restantes se procedió a la lectura del texto completo. Este proceso fue ejecutado por 2 revisores de manera independiente (MT y AY). Las discrepancias se resolvieron con la participación de una tercera persona (JS). La extracción de los datos fue llevada a cabo por uno de los revisores (JS) mediante un formato establecido previamente que reunió las características de la población, de la herramienta utilizada y la exactitud diagnóstica. Se extrajeron las características operativas de las herramientas estudiadas en términos de sensibilidad, especificidad, valores predictivos o área bajo la curva ROC (receiver-operating characteristic).
Riesgo de sesgosSe utilizó la lista de chequeo del Quality Assessment of Diagnostic Accuracy Studies (QUADAS) 28 para el cual se realizó una definición operativa de cada uno de los ítems que la constituye.
El estudio fue aprobado por el comité de investigaciones y ética de la Fundación Universitaria de Ciencias de la Salud y el Hospital de San José de Bogotá.
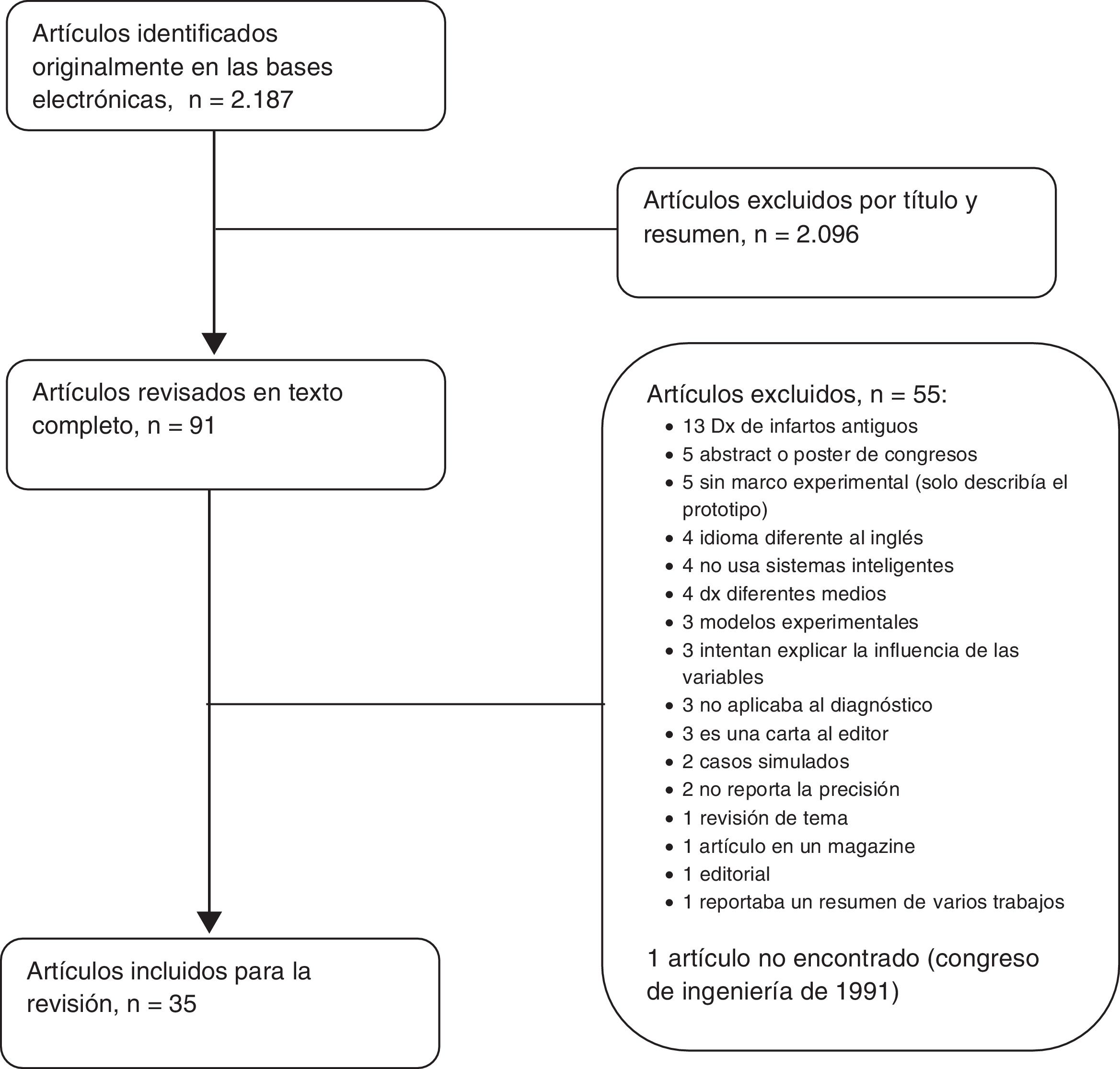
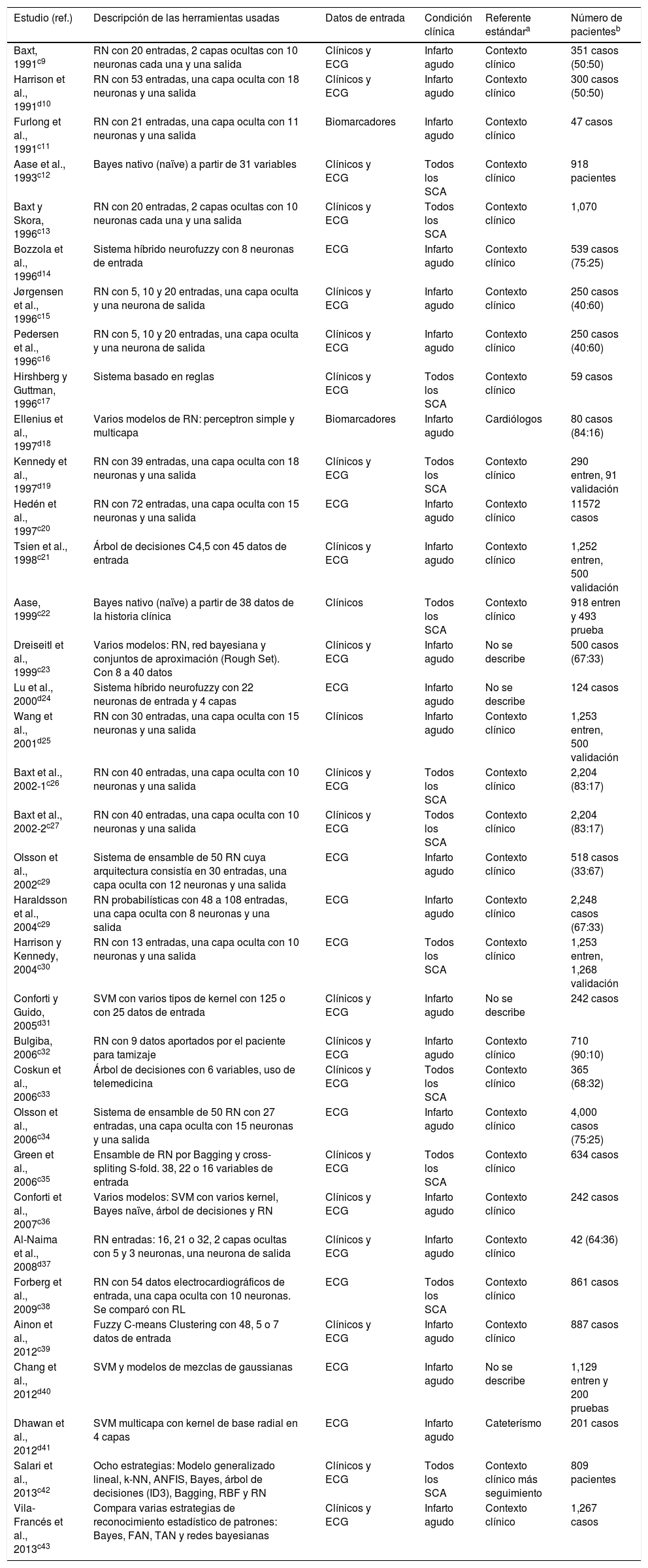
ResultadosSe identificaron 2,187 referencias de la búsqueda en bases de datos. A partir de los títulos y los resúmenes se seleccionaron 91 para revisión del texto completo, de los cuales 35 artículos cumplieron los criterios de inclusión. En la figura 1 se muestra el flujograma de los artículos que fueron tenidos en cuenta durante el proceso de búsqueda (). La primera tabla resume los diseños empleados y la población sobre la que se desarrolló (tabla 1) y en la segunda se muestran los resultados de su desempeño diagnóstico organizando los artículos en estricto orden cronológico (tabla 2).
Estructura y características del entrenamiento de los diferentes sistemas inteligentes
| Estudio (ref.) | Descripción de las herramientas usadas | Datos de entrada | Condición clínica | Referente estándara | Número de pacientesb |
|---|---|---|---|---|---|
| Baxt, 1991c9 | RN con 20 entradas, 2 capas ocultas con 10 neuronas cada una y una salida | Clínicos y ECG | Infarto agudo | Contexto clínico | 351 casos (50:50) |
| Harrison et al., 1991d10 | RN con 53 entradas, una capa oculta con 18 neuronas y una salida | Clínicos y ECG | Infarto agudo | Contexto clínico | 300 casos (50:50) |
| Furlong et al., 1991c11 | RN con 21 entradas, una capa oculta con 11 neuronas y una salida | Biomarcadores | Infarto agudo | Contexto clínico | 47 casos |
| Aase et al., 1993c12 | Bayes nativo (naïve) a partir de 31 variables | Clínicos y ECG | Todos los SCA | Contexto clínico | 918 pacientes |
| Baxt y Skora, 1996c13 | RN con 20 entradas, 2 capas ocultas con 10 neuronas cada una y una salida | Clínicos y ECG | Todos los SCA | Contexto clínico | 1,070 |
| Bozzola et al., 1996d14 | Sistema híbrido neurofuzzy con 8 neuronas de entrada | ECG | Infarto agudo | Contexto clínico | 539 casos (75:25) |
| Jørgensen et al., 1996c15 | RN con 5, 10 y 20 entradas, una capa oculta y una neurona de salida | Clínicos y ECG | Infarto agudo | Contexto clínico | 250 casos (40:60) |
| Pedersen et al., 1996c16 | RN con 5, 10 y 20 entradas, una capa oculta y una neurona de salida | Clínicos y ECG | Infarto agudo | Contexto clínico | 250 casos (40:60) |
| Hirshberg y Guttman, 1996c17 | Sistema basado en reglas | Clínicos y ECG | Todos los SCA | Contexto clínico | 59 casos |
| Ellenius et al., 1997d18 | Varios modelos de RN: perceptron simple y multicapa | Biomarcadores | Infarto agudo | Cardiólogos | 80 casos (84:16) |
| Kennedy et al., 1997d19 | RN con 39 entradas, una capa oculta con 18 neuronas y una salida | Clínicos y ECG | Todos los SCA | Contexto clínico | 290 entren, 91 validación |
| Hedén et al., 1997c20 | RN con 72 entradas, una capa oculta con 15 neuronas y una salida | ECG | Infarto agudo | Contexto clínico | 11572 casos |
| Tsien et al., 1998c21 | Árbol de decisiones C4,5 con 45 datos de entrada | Clínicos y ECG | Infarto agudo | Contexto clínico | 1,252 entren, 500 validación |
| Aase, 1999c22 | Bayes nativo (naïve) a partir de 38 datos de la historia clínica | Clínicos | Todos los SCA | Contexto clínico | 918 entren y 493 prueba |
| Dreiseitl et al., 1999c23 | Varios modelos: RN, red bayesiana y conjuntos de aproximación (Rough Set). Con 8 a 40 datos | Clínicos y ECG | Infarto agudo | No se describe | 500 casos (67:33) |
| Lu et al., 2000d24 | Sistema híbrido neurofuzzy con 22 neuronas de entrada y 4 capas | ECG | Infarto agudo | No se describe | 124 casos |
| Wang et al., 2001d25 | RN con 30 entradas, una capa oculta con 15 neuronas y una salida | Clínicos | Infarto agudo | Contexto clínico | 1,253 entren, 500 validación |
| Baxt et al., 2002-1c26 | RN con 40 entradas, una capa oculta con 10 neuronas y una salida | Clínicos y ECG | Todos los SCA | Contexto clínico | 2,204 (83:17) |
| Baxt et al., 2002-2c27 | RN con 40 entradas, una capa oculta con 10 neuronas y una salida | Clínicos y ECG | Todos los SCA | Contexto clínico | 2,204 (83:17) |
| Olsson et al., 2002c29 | Sistema de ensamble de 50 RN cuya arquitectura consistía en 30 entradas, una capa oculta con 12 neuronas y una salida | ECG | Infarto agudo | Contexto clínico | 518 casos (33:67) |
| Haraldsson et al., 2004c29 | RN probabilísticas con 48 a 108 entradas, una capa oculta con 8 neuronas y una salida | ECG | Infarto agudo | Contexto clínico | 2,248 casos (67:33) |
| Harrison y Kennedy, 2004c30 | RN con 13 entradas, una capa oculta con 10 neuronas y una salida | ECG | Todos los SCA | Contexto clínico | 1,253 entren, 1,268 validación |
| Conforti y Guido, 2005d31 | SVM con varios tipos de kernel con 125 o con 25 datos de entrada | Clínicos y ECG | Infarto agudo | No se describe | 242 casos |
| Bulgiba, 2006c32 | RN con 9 datos aportados por el paciente para tamizaje | Clínicos y ECG | Infarto agudo | Contexto clínico | 710 (90:10) |
| Coskun et al., 2006c33 | Árbol de decisiones con 6 variables, uso de telemedicina | Clínicos y ECG | Todos los SCA | Contexto clínico | 365 (68:32) |
| Olsson et al., 2006c34 | Sistema de ensamble de 50 RN con 27 entradas, una capa oculta con 15 neuronas y una salida | ECG | Infarto agudo | Contexto clínico | 4,000 casos (75:25) |
| Green et al., 2006c35 | Ensamble de RN por Bagging y cross-spliting S-fold. 38, 22 o 16 variables de entrada | Clínicos y ECG | Todos los SCA | Contexto clínico | 634 casos |
| Conforti et al., 2007c36 | Varios modelos: SVM con varios kernel, Bayes naïve, árbol de decisiones y RN | Clínicos y ECG | Infarto agudo | Contexto clínico | 242 casos |
| Al-Naima et al., 2008d37 | RN entradas: 16, 21 o 32, 2 capas ocultas con 5 y 3 neuronas, una neurona de salida | Clínicos y ECG | Infarto agudo | Contexto clínico | 42 (64:36) |
| Forberg et al., 2009c38 | RN con 54 datos electrocardiográficos de entrada, una capa oculta con 10 neuronas. Se comparó con RL | ECG | Todos los SCA | Contexto clínico | 861 casos |
| Ainon et al., 2012c39 | Fuzzy C-means Clustering con 48, 5 o 7 datos de entrada | Clínicos y ECG | Infarto agudo | Contexto clínico | 887 casos |
| Chang et al., 2012d40 | SVM y modelos de mezclas de gaussianas | ECG | Infarto agudo | No se describe | 1,129 entren y 200 pruebas |
| Dhawan et al., 2012d41 | SVM multicapa con kernel de base radial en 4 capas | ECG | Infarto agudo | Cateterísmo | 201 casos |
| Salari et al., 2013c42 | Ocho estrategias: Modelo generalizado lineal, k-NN, ANFIS, Bayes, árbol de decisiones (ID3), Bagging, RBF y RN | Clínicos y ECG | Todos los SCA | Contexto clínico más seguimiento | 809 pacientes |
| Vila-Francés et al., 2013c43 | Compara varias estrategias de reconocimiento estadístico de patrones: Bayes, FAN, TAN y redes bayesianas | Clínicos y ECG | Infarto agudo | Contexto clínico | 1,267 casos |
ANFIS: adaptive neuro fuzzy inference system; ECG: electrocardiograma; FAN: Forest Augmented Network; k-NN: k vecinos cercanos; RBF: función de base radial; RL: regresión logística; RN: red neuronal; SCA: síndromes coronarios agudos; SVM: máquina de soporte de vectores; TAN: Tree Augmented Network.
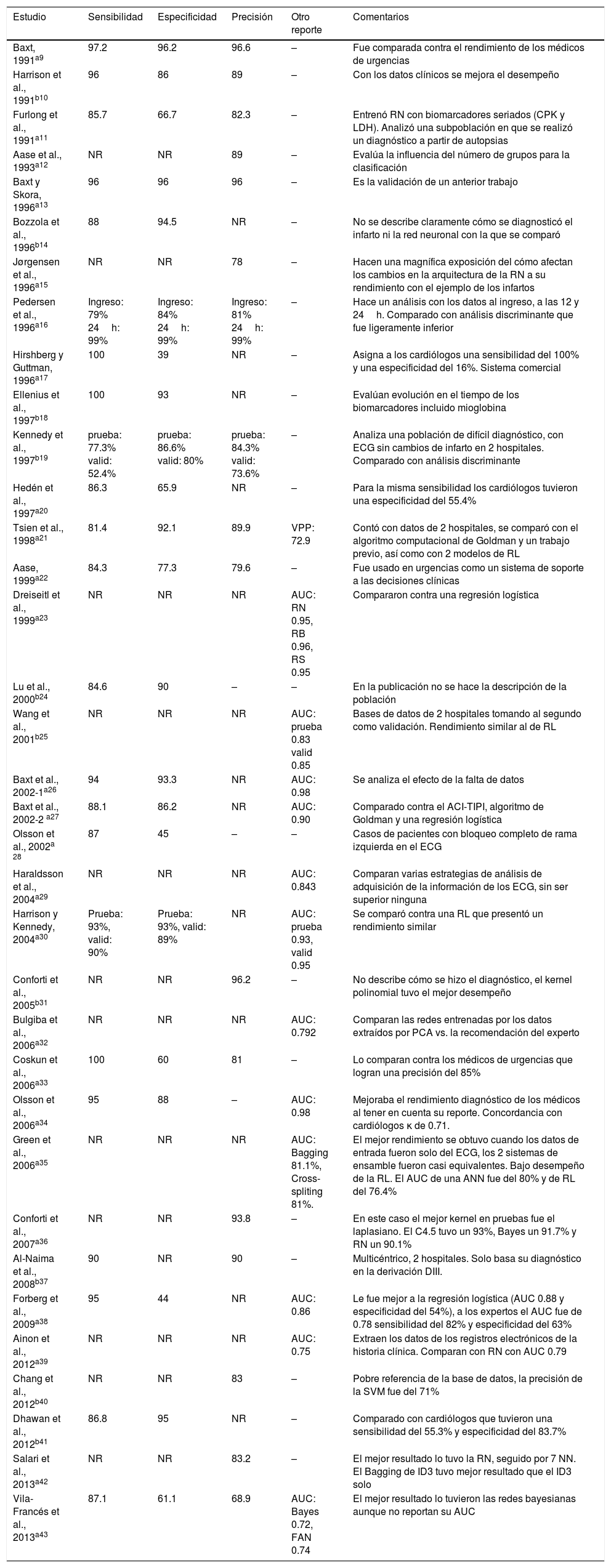
Rendimiento diagnóstico de los sistemas inteligentes
| Estudio | Sensibilidad | Especificidad | Precisión | Otro reporte | Comentarios |
|---|---|---|---|---|---|
| Baxt, 1991a9 | 97.2 | 96.2 | 96.6 | – | Fue comparada contra el rendimiento de los médicos de urgencias |
| Harrison et al., 1991b10 | 96 | 86 | 89 | – | Con los datos clínicos se mejora el desempeño |
| Furlong et al., 1991a11 | 85.7 | 66.7 | 82.3 | – | Entrenó RN con biomarcadores seriados (CPK y LDH). Analizó una subpoblación en que se realizó un diagnóstico a partir de autopsias |
| Aase et al., 1993a12 | NR | NR | 89 | – | Evalúa la influencia del número de grupos para la clasificación |
| Baxt y Skora, 1996a13 | 96 | 96 | 96 | – | Es la validación de un anterior trabajo |
| Bozzola et al., 1996b14 | 88 | 94.5 | NR | – | No se describe claramente cómo se diagnosticó el infarto ni la red neuronal con la que se comparó |
| Jørgensen et al., 1996a15 | NR | NR | 78 | – | Hacen una magnífica exposición del cómo afectan los cambios en la arquitectura de la RN a su rendimiento con el ejemplo de los infartos |
| Pedersen et al., 1996a16 | Ingreso: 79% 24h: 99% | Ingreso: 84% 24h: 99% | Ingreso: 81% 24h: 99% | – | Hace un análisis con los datos al ingreso, a las 12 y 24h. Comparado con análisis discriminante que fue ligeramente inferior |
| Hirshberg y Guttman, 1996a17 | 100 | 39 | NR | – | Asigna a los cardiólogos una sensibilidad del 100% y una especificidad del 16%. Sistema comercial |
| Ellenius et al., 1997b18 | 100 | 93 | NR | – | Evalúan evolución en el tiempo de los biomarcadores incluido mioglobina |
| Kennedy et al., 1997b19 | prueba: 77.3% valid: 52.4% | prueba: 86.6% valid: 80% | prueba: 84.3% valid: 73.6% | – | Analiza una población de difícil diagnóstico, con ECG sin cambios de infarto en 2 hospitales. Comparado con análisis discriminante |
| Hedén et al., 1997a20 | 86.3 | 65.9 | NR | – | Para la misma sensibilidad los cardiólogos tuvieron una especificidad del 55.4% |
| Tsien et al., 1998a21 | 81.4 | 92.1 | 89.9 | VPP: 72.9 | Contó con datos de 2 hospitales, se comparó con el algoritmo computacional de Goldman y un trabajo previo, así como con 2 modelos de RL |
| Aase, 1999a22 | 84.3 | 77.3 | 79.6 | – | Fue usado en urgencias como un sistema de soporte a las decisiones clínicas |
| Dreiseitl et al., 1999a23 | NR | NR | NR | AUC: RN 0.95, RB 0.96, RS 0.95 | Compararon contra una regresión logística |
| Lu et al., 2000b24 | 84.6 | 90 | – | – | En la publicación no se hace la descripción de la población |
| Wang et al., 2001b25 | NR | NR | NR | AUC: prueba 0.83 valid 0.85 | Bases de datos de 2 hospitales tomando al segundo como validación. Rendimiento similar al de RL |
| Baxt et al., 2002-1a26 | 94 | 93.3 | NR | AUC: 0.98 | Se analiza el efecto de la falta de datos |
| Baxt et al., 2002-2 a27 | 88.1 | 86.2 | NR | AUC: 0.90 | Comparado contra el ACI-TIPI, algoritmo de Goldman y una regresión logística |
| Olsson et al., 2002a 28 | 87 | 45 | – | – | Casos de pacientes con bloqueo completo de rama izquierda en el ECG |
| Haraldsson et al., 2004a29 | NR | NR | NR | AUC: 0.843 | Comparan varias estrategias de análisis de adquisición de la información de los ECG, sin ser superior ninguna |
| Harrison y Kennedy, 2004a30 | Prueba: 93%, valid: 90% | Prueba: 93%, valid: 89% | NR | AUC: prueba 0.93, valid 0.95 | Se comparó contra una RL que presentó un rendimiento similar |
| Conforti et al., 2005b31 | NR | NR | 96.2 | – | No describe cómo se hizo el diagnóstico, el kernel polinomial tuvo el mejor desempeño |
| Bulgiba et al., 2006a32 | NR | NR | NR | AUC: 0.792 | Comparan las redes entrenadas por los datos extraídos por PCA vs. la recomendación del experto |
| Coskun et al., 2006a33 | 100 | 60 | 81 | – | Lo comparan contra los médicos de urgencias que logran una precisión del 85% |
| Olsson et al., 2006a34 | 95 | 88 | – | AUC: 0.98 | Mejoraba el rendimiento diagnóstico de los médicos al tener en cuenta su reporte. Concordancia con cardiólogos κ de 0.71. |
| Green et al., 2006a35 | NR | NR | NR | AUC: Bagging 81.1%, Cross-spliting 81%. | El mejor rendimiento se obtuvo cuando los datos de entrada fueron solo del ECG, los 2 sistemas de ensamble fueron casi equivalentes. Bajo desempeño de la RL. El AUC de una ANN fue del 80% y de RL del 76.4% |
| Conforti et al., 2007a36 | NR | NR | 93.8 | – | En este caso el mejor kernel en pruebas fue el laplasiano. El C4.5 tuvo un 93%, Bayes un 91.7% y RN un 90.1% |
| Al-Naima et al., 2008b37 | 90 | NR | 90 | – | Multicéntrico, 2 hospitales. Solo basa su diagnóstico en la derivación DIII. |
| Forberg et al., 2009a38 | 95 | 44 | NR | AUC: 0.86 | Le fue mejor a la regresión logística (AUC 0.88 y especificidad del 54%), a los expertos el AUC fue de 0.78 sensibilidad del 82% y especificidad del 63% |
| Ainon et al., 2012a39 | NR | NR | NR | AUC: 0.75 | Extraen los datos de los registros electrónicos de la historia clínica. Comparan con RN con AUC 0.79 |
| Chang et al., 2012b40 | NR | NR | 83 | – | Pobre referencia de la base de datos, la precisión de la SVM fue del 71% |
| Dhawan et al., 2012b41 | 86.8 | 95 | NR | – | Comparado con cardiólogos que tuvieron una sensibilidad del 55.3% y especificidad del 83.7% |
| Salari et al., 2013a42 | NR | NR | 83.2 | – | El mejor resultado lo tuvo la RN, seguido por 7 NN. El Bagging de ID3 tuvo mejor resultado que el ID3 solo |
| Vila-Francés et al., 2013a43 | 87.1 | 61.1 | 68.9 | AUC: Bayes 0.72, FAN 0.74 | El mejor resultado lo tuvieron las redes bayesianas aunque no reportan su AUC |
ANN: redes neuronales artificiales; AUC: área bajo la curva ROC; CPK: creatinfosfocinasa; ECG: electrocardiograma; FAN: Forest Augmented Network; LDH: lactato deshidrogenasa; PCA: análisis de componentes principales; RL: regresión logística; RN: red neuronal; SVM: máquina de soporte de vectores.
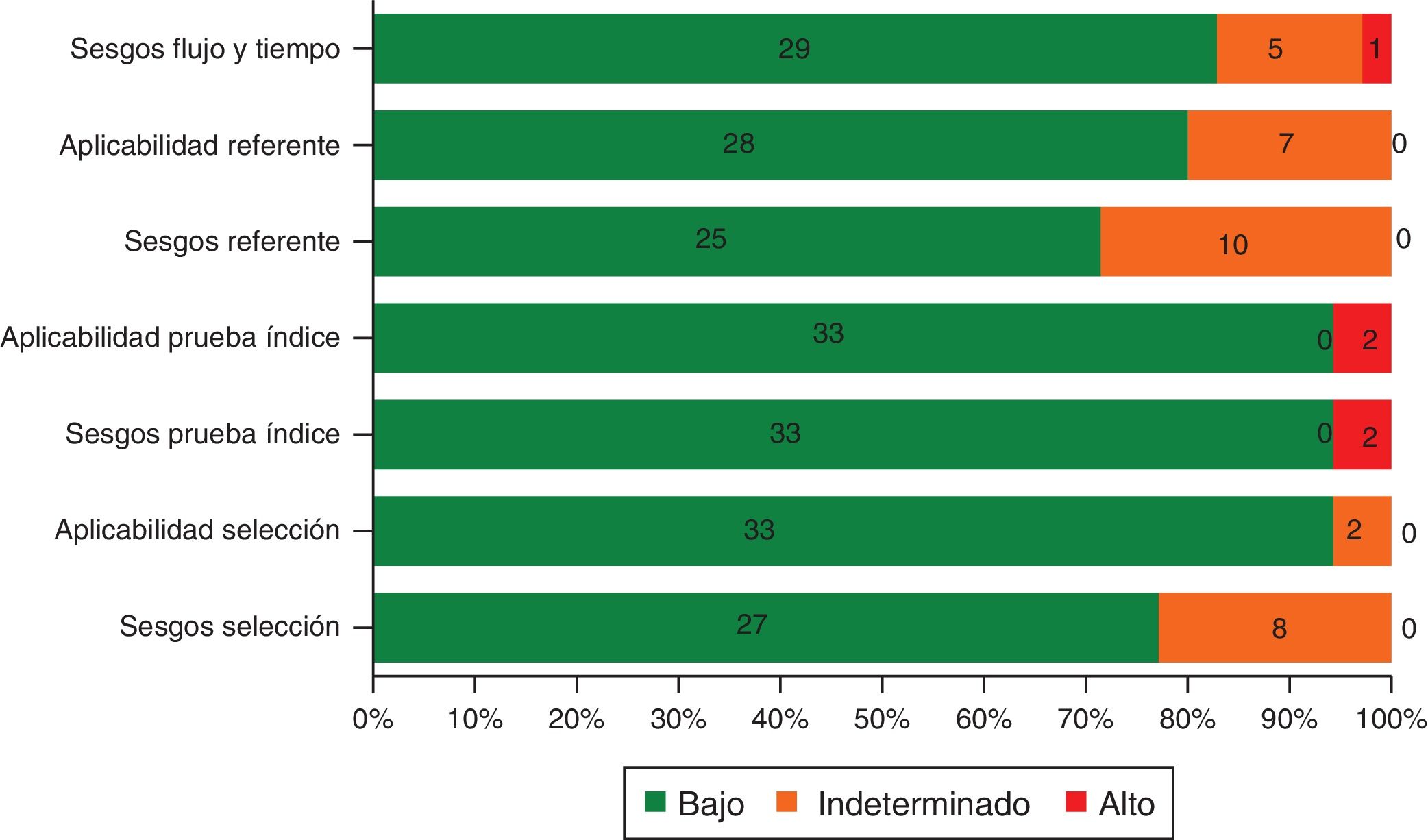
Al realizar el análisis del riesgo de sesgos mediante la herramienta QUADAS 2 (tabla 3), podemos notar que en general se obtuvo un bajo riesgo en la mayor parte de los estudios. El problema más frecuentemente descrito se centró en la descripción de la base de datos usada con lo que no quedan claro algunos aspectos de la selección de los pacientes y del referente para el diagnóstico11,14,22–24,37,39–41,43 (fig. 2). Los casos de riesgo alto incluyen estudios donde se usó solo las derivación DIII37 y V1 a V440 del ECG para el diagnóstico de los infartos, limitando la posibilidad diagnóstica a un subgrupo de infartos (de pared inferior o anterior respectivamente).
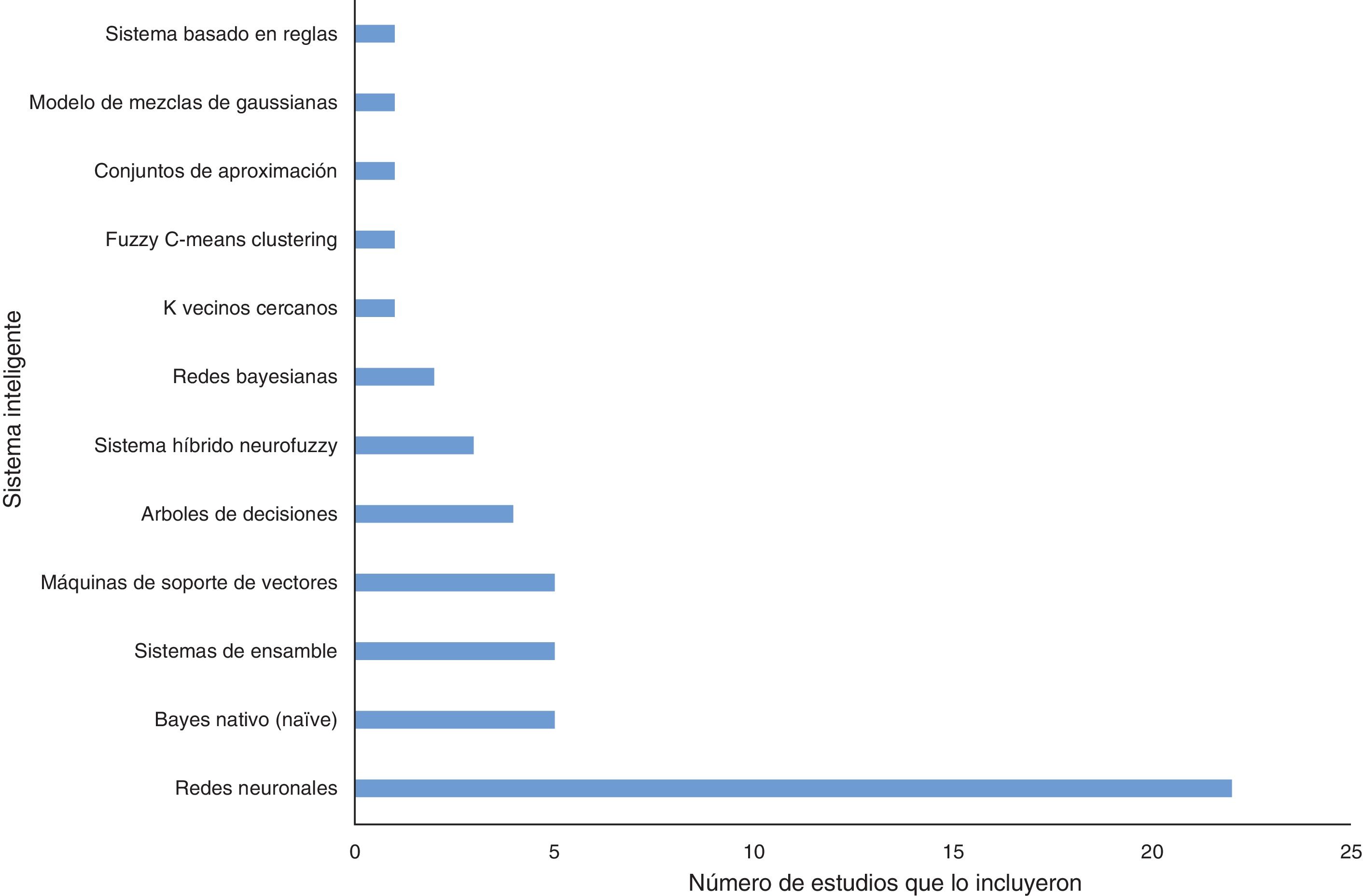
Se encuentra que en 22 (62.8%) de los casos se utilizaron las redes neuronales como la herramienta de sistemas inteligentes (fig. 3), las cuales fueron evaluadas con experimentos amplios que incluían diversas distribuciones en su arquitectura (números de datos de entrada, capas ocultas, neuronas de salida), algoritmos de entrenamiento, tipo de red (perceptron simple, múltiple o red probabilística29) y contextos clínicos. En 5 trabajos se comparan los rendimientos de varias herramientas de sistemas inteligentes (uno comparó 8 estrategias)23,36,40,42,43. En los últimos años fueron publicados con mayor frecuencia estudios que evaluaron SVM31,36,40,41 y sistemas de ensamble28,34,35. En 7 casos se utilizaron estrategias de reconocimiento estadístico de patrones12,22,23,36,40,42,43 y un estudió evaluó un sistema de clustering39.
En 13 trabajos se buscaba realizar el diagnóstico de todos los SCA9,12,13,17,19,22,26,27,30,33,35,38,42 y en 22 solo de los infartos (uno de ellos en casos de bloqueos completos de rama izquierda28). En 21 casos se tuvo en cuenta como datos de entrada aspectos clínicos y electrocardiográficos, en 10 solo datos electrocardiográficos14,20,24,28–30,34,38,40,41, en 2 solo datos clínicos22,25 y en 2 casos solo de biomarcadores de lesión miocárdica11,18. La mayoría de los sistemas inteligentes utilizan como referente estándar el contexto clínico dado por la combinación de aspectos clínicos, ECG, biomarcadores junto a alguna estrategia de estratificación; en un estudio estuvo determinado por el concepto de los cardiólogos18, en otro por angiografía coronaria41 y en uno se tuvo en cuenta los hallazgos de enfermedad en autopsias11. Se desconoce el referente estándar en 4 estudios23,24,31,40. En 7 casos se compararon los resultados con regresión logística21,23,25,27,30,35,38. En 4 casos se comparó con el desempeño de los médicos de urgencias9,33,34,38, en 3 casos con cardiólogos17,18,41 y en 2 casos se compararon con algoritmos computacionales (Goldman y ACI-TIPI)21,27.
En la mayor parte de los casos se alcanzaron altos niveles de precisión para el diagnóstico (tabla 2), encontrando el mejor rendimiento en el caso de varias redes neuronales con precisiones tan altas como el 96 y 98%9,13,26,31.
DiscusiónEl primer intento documentado para desarrollar y aplicar herramientas computacionales para el soporte del diagnóstico de los SCA fue quizá el expuesto por el grupo de Pozen en 198044,45. Aún hoy, luego de 35 años de intensa búsqueda de herramientas de apoyo al diagnóstico de la entidad que da cuenta de la mayor mortalidad en el mundo, no se encuentra una solución definitiva a este tema. Los sistemas inteligentes o de reconocimiento estadístico de patrones se constituyen en una ruta prometedora. Los resultados expuestos demuestran que, por lo general, son mejores que los expuestos para las reglas de predicción clínica que se apoyan en computadores4 o son independientes de ellos46.
En la revisión realizada se encontraron 35 artículos en los que se evaluaron herramientas de sistemas inteligentes en el diagnóstico de los SCA. A través de la experiencia previa, este número no logra abarcar por completo los trabajos que abordan este tema. Debe decirse al respecto que las bases de datos procedentes de ingeniería no tienen estandarizados los términos usados como palabras clave, de manera opuesta a lo que pasa en las que proceden de medicina. Esta situación parece ser más notoria en los artículos presentados en congresos o conferencias. Como es de esperarse, los artículos que proceden de medicina hacen una descripción más completa de la población que es motivo de estudio y del referente para diagnóstico, mientras que en los de ingeniería tiende a descuidarse estos puntos y darse prelación a la descripción detallada de los aspectos metodológicos y de desarrollo del sistema.
Por tratarse de herramientas desarrolladas de manera automática a partir de la base de datos con la que se alimenta, en la que los datos de ingreso están pareados con el diagnóstico, el aspecto de flujo y tiempo por lo general no constituía riesgo de sesgo a pesar de conocerse el diagnóstico del referente de antemano. Se encuentra una amplia variabilidad en sus resultados con un mejor rendimiento aparente en el caso de ANN y SVM en comparación con las herramientas estadísticas de reconocimiento de patrones y árboles de decisiones (tabla 2). Cuando se comparó con los médicos, su resultado siempre fue superior a ellos. En los estudios en los que se podía establecer de antemano un umbral (principalmente en ANN) se dio prelación a una sensibilidad alta sacrificando la especificidad con el fin de favorecer el diagnóstico de los casos positivos.
Desde el planteamiento de la revisión se esperaba una amplia heterogeneidad entre los estudios, por lo que desde el principio se descartó la realización de un metaanálisis. Las poblaciones investigadas eran diversas, los criterios aplicados como referentes variaron con el paso del tiempo, se consideraban en algunos los biomarcadores o ECG, mientras en otros solo correspondía a datos clínicos y, aun usando la misma herramienta, el método de entrenamiento y arquitectura tiene un gran nivel de variación.
Al analizar la escasa penetración de estos sistemas en la práctica médica Richardson46 propone 3 categorías de barreras para el diagnóstico clínico basado en la evidencia: desde el punto de vista de la evidencia disponible, aspectos del diagnóstico y del sistema de salud.Al considerar el primero de estos puntos, la investigación realizada nos aporta una visión general acerca de la evidencia disponible, es claro que existe una buena cantidad de estudios que vienen llevándose a cabo desde hace bastante tiempo, pero que por lo general no son fácilmente disponibles para el profesional de la salud que finalmente tendrá a su cargo la toma de dichas decisiones. Parece ser visto como un experimento aislado, desligado de la práctica.
Una buena parte de los estudios que se encuentran en bases de datos procedentes de la ingeniería presentan limitaciones para el acceso y su consulta por parte del personal de la salud, y a no ser que sea la línea de trabajo habitual de este, no es tenida en cuenta. Vemos además que el enfoque de las publicaciones es amplio, consideran diversos espectros de la enfermedad, que van desde la isquemia inducida en laboratorio41, telemedicina33, triage inicial32 hasta la utilidad como punto definitorio de la conducta posterior22,34. En la mayor parte de ellos no se contemplan otras preguntas diagnósticas como los diagnósticos diferenciales.
Un aspecto fundamental que debe tenerse en cuenta es que existe la posibilidad que los estudios de precisión diagnóstica evalúen solo una parte del desempeño de las herramientas de soporte a las decisiones en el diagnóstico. En lugar de buscar niveles casi perfectos de sensibilidad y especificidad, otro camino podrían ser los estudios en los que se ponga de manifiesto la mejoría en la tasa de aciertos al momento de asignar a los pacientes a cierta área de hospitalización o decidir su alta. Como ejemplo presentamos los trabajos de Jonsbu et al.47 que expone como su herramienta mejora en la práctica la asignación de los pacientes en comparación con la forma tradicional, y el de Wilson et al.48 que incluye el dato de la lectura automática del ECG en la decisión de trombólisis prehospitalaria en pacientes con infarto. Ambos estudios fueron excluidos al no mostrar datos de precisión diagnóstica.
La interpretación de los hallazgos de los ECG presenta sus problemas particulares; es así como en una revisión sistemática se concluyó que tanto los médicos de diferentes especialidades como el software cometen frecuentemente errores en dicha interpretación49. En casi un tercio de los estudios de la revisión, solo se consideró como datos de entrada al sistema la señal electrocardiográfica, sometida o no a algún sistema de procesamiento; sus resultados muestran un desempeño muy bueno para el caso específico de los SCA.
Al considerar las limitaciones de la revisión encontramos que no hay una estandarización de los términos al interior de las bases de datos con lo cual es probable que algunos artículos hayan quedado fuera. A través del tiempo se ha dado una evolución en las definiciones de los SCA lo que hace que el referente no pueda ser aplicable a todos los trabajos de una forma uniforme. Por otro lado, se encuentra una heterogeneidad en la manera como es descrito el rendimiento diagnóstico de las pruebas evaluadas y en la mayor parte de los casos no se puede elaborar tablas de contingencia para ilustrar los falsos y verdaderos positivos/negativos.
Los sistemas inteligentes ya hacen parte de nuestra vida cotidiana. En medicina, el desarrollo más importante se ha centrado en el reconocimiento automático de imágenes especialmente en radiología, big data enfocado hacia farmacovigilancia y modelamiento de epidemias en salud pública. El presente trabajo expone la el extenso camino llevado a cabo en búsqueda de nuevas herramientas que ayuden al diagnóstico de los SCA, sobre todo cuando quien se enfrenta al paciente es personal médico no especializado como ocurre en muchas ocasiones. Aunque aún no se cuente con una aplicación que haga uso de estas herramientas a pie del paciente, es probable que pronto lo veamos en la práctica gracias al avance importante de la tecnología en los últimos años y la investigación creciente en estos temas.
ConclusionesEsta revisión expone cómo las herramientas de sistemas inteligentes tienen alto rendimiento en el diagnóstico de los SCA utilizando diferentes fuentes de entradas como lo son datos clínicos, biomarcadores y ECG así como varias de estas herramientas en donde las redes neuronales son las más utilizadas. Teniendo en cuenta lo descrito se debe considerar a futuro el uso de estas herramientas en la práctica clínica habitual.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónNinguna.
Conflicto de interesesLos investigadores dejamos constancia que no poseemos ningún clonflicto de intereses.