Introducción
La función primordial del ventrículo derecho (VD) es controlar el retorno venoso al corazón y mantener las presiones bajas en el lecho vascular pulmonar. Esta función es posible por su diseño geométrico y morfológico. Sus paredes delgadas, la distensibilidad y sus presiones bajas lo hacen adecuado para la circulación del volumen, que en presencia de sobrecarga de presión aguda produce dilatación.
Su función depende, al igual que en el ventrículo izquierdo (VI), de la frecuencia cardiaca, precarga, poscarga y contractilidad. El VD puede fallar por diversos factores, como sobrecarga de presión, volumen o isquemia, pero un solo mecanismo parece no ser suficiente para propiciar la falla. En este contexto, la estabilidad hemodinámica es efecto de la contracción del VI y el septo interventricular (SIV), contracción auricular, sincronía atrioventricular y el mantenimiento de su perfusión sistólica-diastólica. En consecuencia, el VD debe proporcionar una precarga adecuada al VI y, de acuerdo con su poscarga (resistencia vascular pulmonar [RVP] o la impedancia de la circulación pulmonar), adoptar una función de bomba semejante a la del VI.
Definiciones
Se ha formulado la siguiente definición: "La falla del ventrículo derecho (FVD) puede definirse como un síndrome que refleja la incapacidad del VD para llenarse o expulsar su contenido apropiadamente. La manifestación clínica cardinal es la retención hídrica".
Asimismo, se considera que "la disfunción del ventrículo derecho (DVD) se refiere a anormalidades del llenado o contracción del VD sin referencia a signos y síntomas de insuficiencia cardiaca. Estos pacientes asintomáticos pueden considerarse como una etapa temprana de la FVD".
Falla del vd en el posoperatorio de la cirugía cardiaca
El síndrome de bajo gasto cardiaco (GC) derecho ocurre por FVD. Después de un procedimiento de cirugía cardiaca es una causa importante de morbilidad y mortalidad. La forma refractaria de la FVD puede identificarse luego de una cardiotomía en 0.1%, después de un trasplante cardiaco en 2% a 3% y con el uso de dispositivos de asistencia ventricular izquierda (DAVI) en 20% a 30%. La mortalidad intrahospitalaria puede ser hasta de 70% a 75%.
Fisiopatología
La disfunción miocárdica y la hipertensión pulmonar (HP) después de circulación extracorpórea (CEC) casi siempre son leves y no inducen un bajo GC posoperatorio. Se ha informado FVD en diferentes contextos, por ejemplo tras una cardiotomía posterior a CEC y en presencia de isquemia y disfunción miocárdica; en pacientes que requieren DAVI, ya que el volumen expulsado provoca cambios en la geometría del VD; en el trasplante cardiaco con sustrato isquémico o enfermedad vascular pulmonar e HP. Otros factores relacionados con FVD posoperatoria son protección miocárdica insuficiente durante la operación; tiempo de CEC prolongado; isquemia o infarto al miocardio por embolia coronaria u obstrucción de puentes; pérdida de la sincronía atrioventricular o arritmias; HP inducida por protamina; daño pulmonar por reperfusión con desarrollo de HP secundaria; tromboembolia pulmonar posoperatoria; y depresión miocárdica vinculada con sepsis; de igual modo, la interdependencia ventricular, en un VD previamente dilatado o con HP, y la infusión de volumen pueden ocasionar desplazamiento del septo interventricular hacia el VI, lo que modifica la geometría ventricular y su relación de presión-volumen. La consecuencia puede ser la disminución de la distensibilidad y la contracción del VI, con un bajo GC resultante.
Manifestaciones clínicas
La expresión clínica cardinal es la congestión venosa sistémica e inestabilidad hemodinámica y la regurgitación tricuspídea debido a la dilatación del VD e HP. Otro signo es la hipoxemia de grado variable debido al cortocircuito de la aurícula derecha (AD) a la izquierda a través de un agujero oval permeable o a la desigualdad de la ventilación-perfusión secundaria a un bajo GC.
Importancia clínica de la falla ventricular derecha
En condiciones no quirúrgicas, la FVD puede ser un marcador pronóstico, modifica la calidad de vida y altera la evolución natural o el estado hemodinámico en diferentes afecciones clínicas, como la hipertensión arterial pulmonar idiopática, la tromboembolia pulmonar aguda y crónica, y el infarto agudo del miocardio con extensión al VD. Además, la FVD es un marcador pronóstico o funcional en pacientes con disfunción del VI consecutiva a cardiopatía isquémica o valvular.
En condiciones posoperatorias del corazón (válvulas, anomalías congénitas, arterias coronarias, DAVI o trasplante), se ha sugerido que los datos de la función del VD podrían ayudar a estratificar mejor a los pacientes, incluidos aquéllos con inestabilidad hemodinámica posoperatoria. Su limitación ha sido la definición de la FVD en la validación de índices pronósticos, como el euroSCORE o el Parsonnet. La información disponible procede de trabajos pequeños retrospectivos en casi todos los casos, en los cuales se ha definido la DVD de manera diversa.
En la revascularización miocárdica (RVM) se ha definido la DVD por el cambio en la fracción del área ventricular derecha (RVFAC) <35% o la obstrucción dinámica del tracto de salida del VD (gradiente >25 mmHg), con 41 pacientes obtenidos retrospectivamente de un primer protocolo y con 800 del segundo de manera retrospectiva-prospectiva. En estos estudios se notificó una disminución de la supervivencia a largo plazo y una incidencia elevada para desconectarse de la CEC. En 60 pacientes posoperados con inestabilidad hemodinámica, la DVD se acompañó de una mortalidad alta, con un análisis prospectivo y el marcador fue la RVFAC <35%. En cuanto a la cirugía valvular, en dos estudios retrospectivos se incluyó a 382 individuos sometidos a un procedimiento valvular mitral o mitroaórtico y a 50 pacientes posoperados tras una intervención de cirugía valvular de alto riesgo; la definición de DVD fue clínica o bien se utilizaron la RVFAC <32% y el índice de función miocárdica ventricular derecha >0.50 y se concluyó que la FVD fue el mayor predictor de mortalidad y que se vinculó con una elevada incidencia de insuficiencia circulatoria.
Las series de casos retrospectivos sobre cirugía de defectos congénitos y comunicación interatrial, en los cuales el criterio de DVD fue el remodelado del VD, los resultados mostraron que la edad avanzada y la relajación anormal del VD se relacionaron con remodelado incompleto del VD. En tres estudios prospectivos efectuados en personas con tetralogía de Fallot, que incluyeron a 35, 41 y 17 sujetos, respectivamente, la DVD fue la fisiología restrictiva del VD en los dos primeros y el remodelado del VD en el tercero; las conclusiones fueron la predicción de bajo GC posoperatorio, estancia prolongada en cuidados intensivos, mejor tolerancia al ejercicio y VD más pequeños; la dilatación del VD (volumen final diastólico > 170 ml/m2) se vinculó con remodelado incompleto del VD. En dos trabajos retrospectivos, uno con 31 pacientes, efectuados en individuos con FVD que requirieron DAVI, se utilizó una fracción de expulsión de 11.8% como marcador de DVD y se concluyó que era necesario un DAVI en presencia de fiebre, edema pulmonar y transfusiones sanguíneas intraoperatorias; en un segundo estudio que analizó a 245 sujetos con DAVI y FVD como definición, 23 (9%) de ellos requirió dispositivos de asistencia del VD y los predictores de riesgo fueron género femenino y causas no isquémicas.
En otro protocolo retrospectivo sobre trasplante cardiaco que utilizó la base de datos de la Sociedad Internacional de Transplante de Corazón y Pulmón, el marcador fue FVD con falla circulatoria y se identificó muerte temprana en más de 20% de los casos.
Importancia de la función del vd en pacientes con hipertensión pulmonar
En los modelos de riesgo Parsonnet y euroSCORE se incluyó la HP y se la definió como el factor de riesgo para mortalidad más importante en pacientes posoperados de cirugía cardiaca. Este riesgo no dependió del nivel de presión arterial pulmonar y sí pareció relacionarse con el estado de la función del VD. En la cirugía valvular mitral, la DVD fue predictor de falla circulatoria posoperatoria; en la tromboendarterectomía de la tromboembolia pulmonar crónica, la FVD es un factor de riesgo para mortalidad perioperatoria, aunque ahora se reconoce que el principal predictor de muerte es la HP residual posoperatoria. En sujetos con HP programados para un procedimiento no cardiaco la DVD fue el mejor predictor de supervivencia.
Tratamiento
En la actualidad, el tratamiento dirigido a los pacientes con HP está enfocado principalmente en los mecanismos de vasoconstricción, trombosis y proliferación celular. Sin embargo, es poca la evidencia existente acerca del tratamiento de la DVD y, en casi todos los casos, el conocimiento a este respecto deriva de subanálisis de estudios con los enfoques ya mencionados. De manera adicional, la mayor parte de estos estudios incluye a pacientes con formas crónicas de la HP, por ejemplo la hipertensión arterial pulmonar idiopática y la secundaria a otros padecimientos o la tromboembolia pulmonar aguda y crónica. Por esta razón se considera que son necesarios más estudios acerca del tratamiento de la DVD aguda, sobre todo en el contexto de la terapia intensiva posoperatoria.
Identificación de los pacientes de alto riesgo
Se consideran individuos de gran riesgo aquéllos programados para una intervención de cirugía cardiaca con HP o DVD previa, con tiempos de CEC o tiempo de isquemia prolongados, y personas con desigualdad en el tamaño respecto de quienes reciben un DAVI.
Medidas para reducir el riesgo
Se han sugerido las siguientes: optimizar la protección miocárdica, evitar la hipotensión arterial sistémica, establecer vigilancia y optimizar la precarga, instituir un control adecuado de la oxigenación y la ventilación mecánica (VM) y utilizar vasodilatadores pulmonares de manera selectiva.
Control de la frecuencia y el ritmo cardiaco
Los trastornos del ritmo cardiaco, y en particular las arritmias supraventriculares y el bloqueo auriculoventricular de grado diverso, ocurren con frecuencia en pacientes posoperados de una operación cardiaca, lo cual puede modificar el GC. Es importante mantener el ritmo sinusal y la sincronía auriculoventricular en presencia de DVD. Asimismo, deben aplicarse medidas farmacológicas o eléctricas para establecer un apropiado ritmo cardiaco antes de iniciar vasopresores o instituir apoyo mecánico.
Precarga del ventrículo derecho
La reanimación hídrica debe ser conservadora y el uso de diuréticos está indicado para evitar la sobrecarga de volumen central. El equilibrio de líquidos es de suma importancia, ya que puede relacionarse con el riesgo de hipovolemia o la sobrecarga de volumen. La hipovolemia puede desencadenar hipotensión sistémica debido al GC bajo relacionado con un inadecuado llenado ventricular durante la diástole y la sobrecarga de volumen puede afectar la función cardiaca debido al principio de interdependencia ventricular. La reanimación con líquidos, ante un VD dilatado, puede incrementar su volumen e interferir con el llenado del VI. Por esta razón, es preferible la administración en bolo de soluciones cristaloides de 250 a 500 ml, seguido de una cuidadosa reevaluación. Se ha sugerido establecer objetivos de perfusión para hacer un uso racional de las cargas con líquidos y evitar efectos adversos. La reanimación con volumen debe iniciar cuando la presión venosa central es < 10 mmHg con seguimiento estrecho del GC. Las cargas con volumen se deben evitar o suspender cuando la presión de la AD se incrementa más de 3 mmHg sin observar cambios en el GC.
Ventilación mecánica
Es común observar disfunción pulmonar después de operaciones que requieren CEC. La disfunción pulmonar puede manifestarse en la forma de daño pulmonar agudo o síndrome de insuficiencia respiratoria aguda (SIRA) en 2% de los casos, y cursar con vasoconstricción pulmonar hipóxica e incremento de la poscarga al VD. El SIRA tiene una mortalidad aproximada de 50% y es de gran importancia identificarla en el periodo posoperatorio con el fin de establecer un manejo ventilatorio adecuado. La sobredistensión pulmonar debe evitarse debido a que puede aumentar en grado significativo la RVP, por colapso de los vasos alveolares, y llevar a la FVD. Durante la evolución del SIRA se requieren con frecuencia incrementos progresivos de las presiones en la vía respiratoria como intento de asegurar un adecuado intercambio de oxígeno, lo que podría resultar en sobredistensión alveolar. Se ha aconsejado instituir medidas de protección pulmonar en aquellos enfermos que cursan con daño pulmonar agudo o SIRA en el periodo posoperatorio. El volumen corriente debe ajustarse de modo sistemático y calculado con base en el peso predicho para género y talla; se recomienda emplear volumen corriente bajo (4-6 ml/kg) para mantener una presión meseta < 30 cm H2O; la frecuencia respiratoria se debe ajustar para mantener el pH arterial entre 7.30 y 7.45. Además, se sugiere utilizar una apropiada combinación de fracción inspiratoria de oxígeno y presión positiva al final de la espiración para alcanzar una adecuada oxigenación (PaO2: 55 a 80 mmHg o saturación por oximetría de pulso de 88% a 95%). Las medidas de protección pulmonar tienen como objetivo limitar la presión en la vía respiratoria y, por lo tanto, reducir la sobredistensión pulmonar, es decir, la presión transpulmonar. En teoría, esto genera una menor poscarga por disminución de la compresión de vasos intraalveolares durante la VM y, en consecuencia, un menor trabajo del VD. Las medidas de protección pulmonar también ofrecen protección cardiaca y contribuyen a mantener una baja impedancia ventricular derecha. Asimismo, deben evitarse la hipoxemia, hipercapnia o acidosis, ya que pueden exacerbar la HP. Se ha aconsejado la implementación de protocolos de retiro de la VM en aquellos pacientes con requerimientos de VM por más de 24 h. Diferentes estudios han demostrado que la aplicación de pruebas de ventilación espontánea como parte del proceso del retiro de la VM disminuye la duración de ésta. Completar una prueba de ventilación espontánea de forma satisfactoria implica una elevada probabilidad de éxito en el retiro. También se ha notificado la institución de protocolos de sedación y analgesia con interrupción diaria en pacientes críticos cuando la condición clínica es óptima para el retiro de la VM.
Vasodilatadores pulmonares para la hipertensión pulmonar o la FVD posoperatorias
Los vasodilatadores pulmonares (VP) se han utilizado en forma inhalada en los procedimientos de cirugía cardiaca. Éstos incluyen milrinona, óxido nítrico (NO), prostaciclina, sildenafilo e iloprost. Se ha demostrado en modelos experimentales que el uso de VP, como la milrinona y la prostaciclina en forma inhalada, reduce la disfunción endotelial arterial pulmonar. Con esta observación, el compromiso pulmonar observado con la CEC y su efecto en la poscarga al VD podrían ser menores. La prostaciclina, milrinona e iloprost demostraron disminuir la HP y requieren menor apoyo vasoactivo que un grupo placebo. El momento de su administración parece tener efecto diferencial entre su uso anterior y posterior a la CEC. La CEC previa redujo más la presión arterial pulmonar (PAP) y la frecuencia de reingreso a CEC respecto del grupo al cual se le administró al final. Estas observaciones fueron reproducibles con prostaciclina y NO inhalados en comparación con VP intravenosos de uso habitual y milrinona. Además, el tiempo de estancia en cuidados intensivos y en el hospital fue menor. La evidencia retrospectiva sugiere que los VP (NO) podrían reducir la FVD refractaria después de dispositivos de asistencia del VD, trasplante o cirugía de cardiopatías congénitas. La equivalencia de ambos (prostaciclina inhalada y óxido nítrico) son de similar eficacia al mejorar la hemodinámica pulmonar; la diferencia podría encontrarse en las vías de administración, tipo de fármaco, costo, posibilidad de causar hipotensión sistémica y desigualdad en la relación ventilación-perfusión pulmonar.
Apoyo vasopresor e inotrópico
Este apoyo puede ser necesario si sobreviene inestabilidad hemodinámica por FVD aguda posoperatoria. El objetivo debe ser evitar la hipotensión arterial y con ello el desarrollo de isquemia del VD. En pacientes con DVD leve a moderada, después de una operación cardiaca sin hipotensión grave, se han utilizado dobutamina y milrinona; ambos podrían disminuir el GC y la PAP. El mismo efecto se ha observado en sujetos con HP (PAP media > 25 mmHg), en quienes si bien decreció la presión capilar pulmonar, también lo hizo la resistencia vascular sistémica. El levosimendán, un sensibilizador de calcio, se ha prescrito en el síndrome de bajo GC y falla cardiaca, pero la experiencia en la FVD es aún escasa.
Tratamientos alternos o adyuvantes de la FVD
Los niveles ideales de hemoglobina en pacientes con FVD no se han establecido; sin embargo, cuando se agrega además oxigenación tisular comprometida, es probable que los niveles sugeridos actualmente en el paciente crítico sin enfermedad cardiopulmonar previa sean insuficientes.
La administración de fármacos bloqueadores β e inhibidores de la enzima convertidora de angiotensina mejora la hemodinámica de pacientes con falla biventricular, aunque en el paciente con FVD pura se sugiere no emplearlos de manera sistemática y existe poca evidencia que sustente su empleo al igual que el de la digoxina.
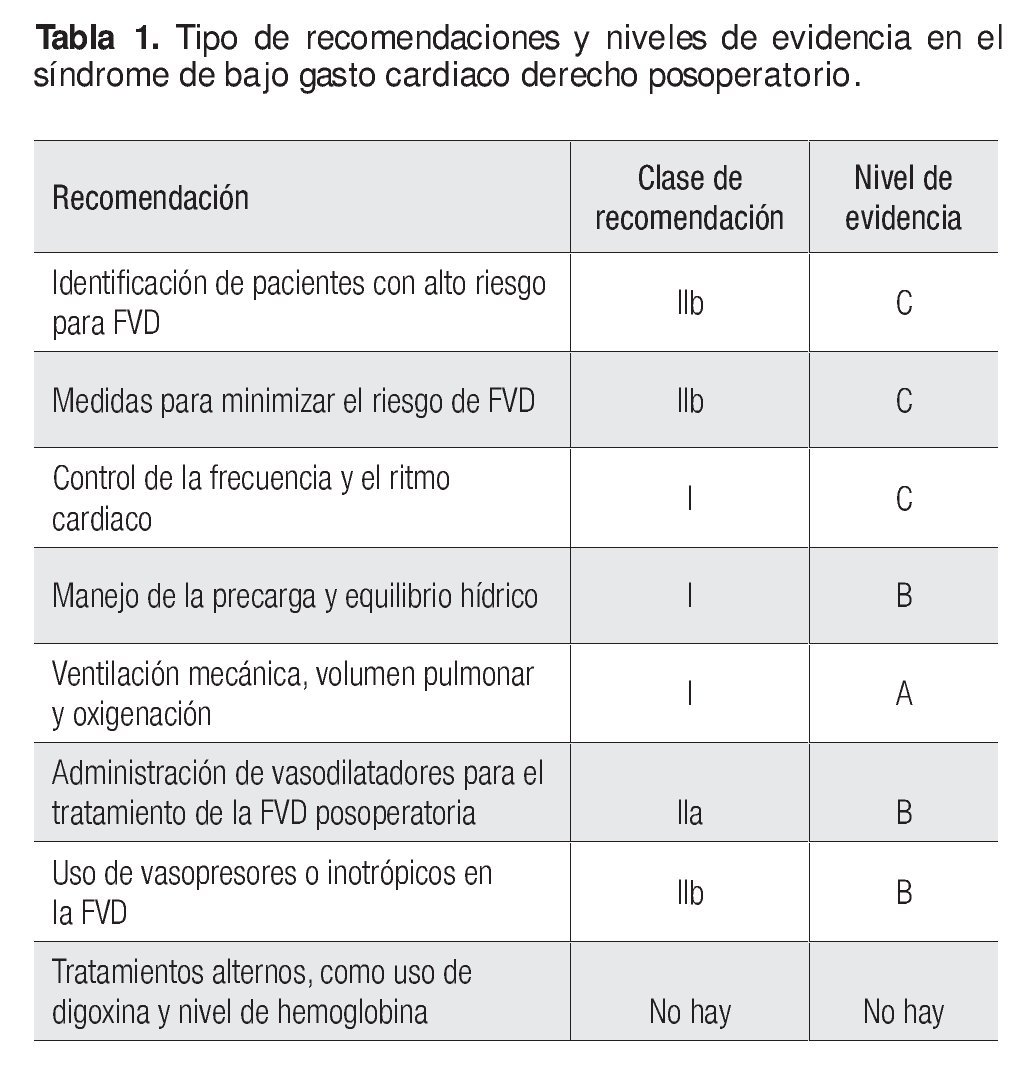
En la Tabla 1 se resumen las recomendaciones y sus niveles de evidencia en el control y tratamiento del síndrome de bajo gasto cardiaco derecho posoperatorio.
Bibliografía
Ardehali A, Hughes K, Sadeghi A, et al. Inhaled nitric oxide for pulmonary hypertension after heart transplantation. Transplantation 2001;72:638-641.
Argenziano M, Choudhri AF, Moazami N, et al. Randomized, double-blind trial of inhaled nitric oxide in LVAD recipients with pulmonary hypertension. Ann Thorac Surg 1998;65:340-345.
Aubin MC, Laurendeau S, Mommerot A, et al. Differential effects of inhaled and intravenous sildenafil in the prevention of the pulmonary endothelial dysfunction due to cardiopulmonary bypass. J Cadiovasc Pharmacol 2008;51:11-17.
Barnard D, Alpert JS. Right ventricular function in health and disease. Curr Probl Cardiol 1987;12:417-449.
Beck JR, Mongero LB, Kroslowitz RM, et al. Inhaled nitric oxide improves hemodynamics in patients with acute pulmonary hyper-tension after high-risk cardiac surgery. Perfusion 1999;14:37-42.
Berstein AD, Pasonnet V. Bedside estimation of risk as an aid for decision-making in cardiac surgery. Ann Thorac Surg 2000;69:823-828.
Bogaard HJ, Abe K, Vonk Noordegraaf A, et al. The right ventricle under pressure. Cellular and Molecular Mechanisms of right-heart failure in pulmonary hypertension. Chest 2009;135:794-804.
Brook AD, Ahrens TS, Schaiff R, et al. Effect of a nursing-implemented sedation protocol on the duration of mechanical ventilation. Crit Care Med 1999;27:2609-2615.
Chen JM, Levin HR, Rose EA, et al. Experience with right ventricular assist devices for perioperative right-sided circulatory failure. Ann Thorac Surg 1996;61:305-310.
Clark SC. Lung injury after cardiopulmonary bypass. Perfusion 2006;21:225-228.
Cullen S, Shore D, Redington A, et al. Characterization of right ventricular diastolic performance after complete repair tetralogy of Fallot. Restrictive physiology predicts slow post-operative recovery. Circulation 1995;91:1782-1789.
Davlouros PA, Niwa K, Webb G, et al. The right ventricle in congenital heart disease. Heart 2006;92:127-138.
Denault AY, Chaput M, Couture P, et al. Dynamic right ventricular outflow tract obstruction in cardiac surgery. J Thorac Cardiovasc Surg 2006;132:43-49.
Doyle AR, Dhir AK, Moors AH, et al. Treatment of perioperative low cardiac output syndrome. Ann Thorac Surg 1995;59:S3-S11.
Ely EW, Baker AM, Dunagan DP, et al. Effect on the duration of mechanical ventilation of identifying patients capable of breathing spontaneously. N Engl J Med 1996;335:1864-1869.
Esteban A, Alia I, Gordo F, et al.: Extubation outcome after spontaneous breathing trials with T-tube or pressure support ventilation. Am J Respir Crit Care Med 1997;156:459-465.
Esteban A, Alia I, Tobin MJ, et al.: Effect of spontaneous breathing trial duration on outcome of attempts to discontinue mechanical ventilation. Am J Respir Crit Care Med 1999;159:512-518.
Fattouch K, Sbraga F, Sampognaro R, et al. Treatment of pulmonary hypertension in patients undergoing cardiac surgery with cardiopulmonary bypass: a randomized, prospective, doubled-blind study. J Cardiovasc Med 2006;7:119-123.
Feneck RO, Sherry KM, Withington PS, et al. Comparison of the hemodinamic effect of milrinone and dobutamine in patients after cardiac surgery. J Cardiothorac Vasc Anesth 2001;15:306-315.
Ferlinz J. Right ventricular function in adult cardiovascular disease. Prog Cardiovasc Dis 1982;25:225-267.
Follath F, Cleland JG, Just H, et al. Efficacy and safety of intravenous Levosimendan compared with dobutamina in severe low-output heart failure (the LIDO study): a randomized double blind trial. Lancet 2002;360:196-202.
Gatzoulis MA, Clark AL, Cullen S, et al. Right ventricular diastolic function 15 to 35 years after repair of tetralogy of Fallot. Restrictive physiology predicts superior exercise performance. Circulation 1995;91:1775-1781.
Ghio S, Gavazzi A, Campana C, et al. Independent and additive prognostic value of right ventricular systolic function and pulmonary artery pressure in patients with chronic heart failure. J Am Coll Cardiol 2001;37:183-188.
Guarracino F, Cariello C, Danella A, et al. Right ventricular failure: pPhysiology and assessment. Minerva Anestesiol 2005;71:307-312.
Hache M, Denault AY, BelisleS, et al. Inhaled epoprostenol (prostacyclin) and pulmonary hypertension before cardiac surgery. J Thorac Cardiovasc Surg 2003;125:642-649.
Haddad F, Ashley E, Michelakis E. New insights for the diagnosis and management of right ventricular failure, from molecular imaging to targeted right ventricular therapy. Curr Opin Cardiol 2010;25:131-140.
Haddad F, Couture P, Tousignant C, et al. The right ventricle in cardiac surgery, a perioperative perspective: II. Pathophysiology, clinical importance, and management. Anesth Analg 2009;108:422-433.
Haddad F, Denault AY, Couture P, et al. Right ventricular myocardial performance index predicts peri-operative mortality or circula-tory failure in high risk valvular surgery. J Am Soc Echocardiogr 2007;20:1065-1072.
Hill NS, Roberts KR, Preston IR. Postoperative pulmonary hypertension: etiology and treatment of a dangerous complication. Respir Care 2009;54:958-968.
Hoeper MM, Mayer E, Simonneau G, et al. Chronic thromboembolic pulmonary hypertension. Circulation 2006;113:2011-2020.
Hosenpud JD, Bennett LE, Keck BM, et al. The registry of the International Society for Heart and Lung Transplantation: Seventeenth official report-2000. J Heart Lung Transplant 2000;19:909-931.
Jurnois D, Baufreton C, Mauriat P, et al. Inhaled nitric oxide as a therapy for pulmonary hypertension after operations for congenital heart defects. J Thorac Cardiovasc Surg 1994;107:1129-1135.
Jurnois D, Pouard P, Mauriat P, et al. Effects of inhaled nitric oxide administration on early postoperative mortality in patients operated for correction of atrio-ventricular canal defects. J Thorac Cardiovasc Surg 1994;107:1129-1135.
Kaul TK, Fields BL. Posoperative acute refractory right ventricular failure: IIncidence, pathogenesis, management and prognosis. Cardiovasc Surg 2000;8:1-9.
Kerbaul F, Gariboldi V, Giorgi R, et al. Effects of Levosimendan on acute pulmonary embolism-induced right ventricular failure. Crit Care Med 2007;35:1948-1954.
Kieler-Jensen N, Lundin S, Ricksten SE, et al. Vasodilatar therapy after heart transplantation: effects of inhaled nitric oxide and intravenous prostacyclin, prostaglandin E1, and sodium nitroprusside. J Heart Lung Transplant 1995;14:436-443.
Kormos RL, Gasior TA, Kaway A, et al. Transplant candidate´s clinical status rather than right ventricular function defines need for univentricular versus biventricular support. J Thorac Cardiovasc Surg 1996;111:773-782.
Kress JP, Pohlman AS, O`Connor, et al. Daily interruption of sedative infusions in critically ill patients undergoing mechanical ventilation. N Engl J Med 2000;342;1471-1477.
Lahm T, McCaslin Ch, Wozniak T, et al. Medical and surgical treatment of acute right ventricular failure. J Am Coll Cardiol 2010;56;1435-1446.
Lamarche Y, Malo O, Thorin E, et al. Inhaled but not intravenous milrinone prevents pulmonary endotelial dysfunction after cardiopulmonary bypass. J Thorac Cardiovasc Surg 2005;130:83-92.
Lamarche Y, Perrault LP, Maltais S, et al. Preliminary experience with inhaled milrinone in cardiac surgery. Eur J Cardiothorac Surg 2007;31:1081-1087.
Leather HA, Ver EK, Segers P, et al. Effects of levosimendan on acute pulmonary embolism-induced right ventricular failure. Crit Care Med 2003;31:2339-2343.
Levine S, Nguyen T, Taylor N, et al. Rapid disuse atrophy of diaphragm fibers in mechanically ventilated humans. N Engl J Med 2008;358;1327-1335.
MacLaren R, Plamondon JM, Ramsay KB, et al. A prospective evaluation of empiric versus protocol-based sedation and analgesia. Pharmacotherapy 2000;20:662-672.
Maslow AD, Regan MM, Panzica P, et al. Precardiopulmonary bypass right ventricular function is associated with poor outcome after coronary artery bypass grafting in patients with severe left ventricular systolic dysfunction. Anesth Analg 2002;95:1507-1518.
Missant C, Rex S, Segers P, et al. Levosimendan improves right ventriculovascular coupling in a porcine model of right ventricular dysfunction. Crit Care Med 2007;35:707-715.
Moazami N, Pasque MK, Moon MR, et al. Mechanical support for isolated right ventricular failure in patients after cardiotomy. J Heart Lung Transplant 2004;23:1371-1375.
Morelli A, Teboul JL, Maggiore SM, et al. Effects of levosimendan on right ventricular afterload in patients with acute respiratory distress syndrome: a pilot study. Crit Care Med 2006;34:2287-2293.
Nashef SA, Roques F, Hammill BG, et al. Validation of European System for Cardiac Operative Risk Evaluation (euroSCORE) in North American cardiac surgery. Eur J Cardiothoracic Surg 2002;22:101-105.
Ochiai Y, McCarthy PM, Smedira NG, et al. Predictors of severe right ventricular failure after implantable left ventricular assist device insertion: analysis of 245 patients. Circulation 2002;106:I198-I202.
Oz MC, Ardehali A. Collective review: perioperative uses of inhaled nitric oxide in adults. Heart Surg Forum 2004;7:E584-E589.
Pinzani A, de GG, Pinzani V, et al. Pre and postoperative right cardiac insufficiency in patients with mitral or mitral-aortic valve diseases. Arch Mal Coeur Vaiss 1993;86: 27-34.
Rastan AJ, Bittner HB, Gummert JF, et al. On-pump beating heart versus off-pump coronary artery bypass surgery evidence of pump-induced myocardial injury. Eur J Cardiothorac Surg 2005;27:1057-1064.
Reichert CL, Visser CA, van den Brinck RB, et al. Value of biventricular function in hypotensive patients after cardiac surgery as assessed by esophageal echocardiography. J Cardiothorac Vasc Anesth 1992; 6:429-432.
Santamore W, Dell´Italia LJ. Ventricular iInterdependence: Ssignificant left ventricular contributions to right ventricular systolic function. Prog Cardiovasc Dis 1998:40:4:289-308.
Stobierska-Dzierzek B, Award H, Michler RE. The evolving management of acute right-sided heart failure in cardiac transplant recipients. J Am Coll Cardiol 2001;38:923-931.
Taylor DO, Edwards LB, Boucek MM, et al. Registry of the International Society for Heart and Lung Transplantation: Twenty-fourth official adult heart transplant report-2007. J Heart Lung Transplant 2007;26:769-781.
The Acute Respiratory Distress Syndrome Network. Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. N Engl J Med 2000;342:1301-1308.
Theodoraki K, Panagiota R, Thanopoulos A, et al. Inhaled iloprost controls pulmonary hypertension after cardiopulmonary bypass. Can J Anesth 2002;49:963-967.
Therrien J, Provost Y, Merchant N, et al. Optimal timing for pulmonary valve replacement in adults after tetralogy of Fallot repair. Am J Cardiol 2005;95:779-782.
Tscholl D, Langer F, Wendler O, et al. Pulmonary thromboendarterectomy-risk factor for early survival and hemodynamic improvement. Eur J Cardiothorac Surg 2001;19:771-776.
Vlahakes GJ. Right ventricular failure following cardiac surgery. Coron Artery Dis 2005:16:27-30.
Wang H, Gong M, Zhou B, et al. Comparison of inhaled and intravenous milrinone in patients with pulmonary hypertension undergoing mitral valve surgery. Advan Ther 2009;26:462-468.
Webb G, Gatzoulis MA. Atrial septal defect in the adult recent progress and overview. Circulation 2006;114:1645-1653.
Yeo TC, Dujardin KS, Tei C, et al. Value of Doppler-derived index combined systolic and diastolic time intervals in predicting outcome in primary pulmonary hypertension. Am J Cardiol 1998;81:1157-1161.
Zamanian RT, Haddad F, Doyle RL, et al. Management strategies for patients with pulmonary hypertension in the intensive care unit. Crit Care Med 2007;35:2037-2050.