La muerte súbita cardiaca está caracterizada por un colapso o paro cardiaco súbito secundario a arritmias cardiacas, en personas con o sin enfermedad cardiaca; la sangre deja de fluir al cerebro y todo el organismo y causa la muerte si no es tratada dentro de minutos1–5. Algunos de estos pacientes llegan a tener síntomas poco antes del evento, pero para establecer el diagnóstico definitivo de un episodio de muerte súbita se requiere que los síntomas tengan menos de una hora de duración3. La mayoría de los casos son secundarios a cardiopatía isquémica y ocurren a nivel extrahospitalario5,6,7, en menor porcentaje pueden ser debidos a enfermedad vascular cerebral, rotura de aneurismas aórticos o tromboembolia pulmonar masiva4,8,9.
Incidencia y prevalenciaLa muerte súbita es un problema de salud público a nivel mundial5,8,6. Se reporta en diferentes poblaciones y continúa representando al menos del 20-30% de los decesos de origen cardiaco; en países como EE. UU. es la responsable del 7-18% de los decesos totales5. En México no conocemos la incidencia y prevalencia de la muerte súbita o del paro cardiaco súbito. En Francia la incidencia es de 32.1 casos por millón de habitantes/año10, en China es de 41.3 casos por 100,000 habitantes/año11, en EE. UU. la incidencia varía y va de 70 a 155 casos por 100,000 habitantes/año, lo que puede representar entre 185,000 y 400,000 casos anuales5,12. En la población infantil se ha informado una incidencia de 3.2 casos por 100,000 habitantes/año en Holanda13. El mayor número de casos se presenta en población entre 45 a 75 años de edad, debido principalmente al desarrollo de enfermedad arterial coronaria12,14-16. En algunas poblaciones como las de origen latino, en New York, se ha observado que al menos el 45% de los casos son menores de 65 años de edad6,12. Tiene un franco predominio en la población masculina, pero con una participación cada vez mayor en el sexo femenino donde se ha informado que puede representar el 35% de la mortalidad de origen cardiaco17,18. En México no conocemos la incidencia y prevalencia, pero podemos hacer un cálculo aproximado de las víctimas de muerte súbita; en el 2008 se reportaron 59,579 fallecimientos en adultos por cardiopatía isquémica19, es probable que al menos 30% de estos fueran de forma súbita, lo que representa 17,873 casos/año. Dos trabajos publicados en nuestro país estiman que el número puede ser tan alto como de 70,000casos/año20,21. A nivel mundial, en el 2008 ocurrieron 17.3 millones de muertes por enfermedades cardiovasculares, de las cuales 7.3 millones fueron por cardiopatía isquémica22; es probable que el 30% de estos fallecimientos fueran de forma súbita, lo 2 que representa 2.19 millones de muertes súbita/año. La tabla 1 muestra un resumen de la información estadística aproximada del paro cardiaco súbito a nivel mundial.
Estimación aproximada de muertes súbitas a nivel mundial, causas y supervivencia
| Muertes cardiovasculares en el mundo (2008) | 17.3 millones |
| Muertes de origen cardiaco a nivel mundial (2008) | 7.3 millones |
| Proporción estimada de muertes súbitas (30% de las muertes de origen cardiaco) | 2.19 millones |
| Causas de muerte súbita | |
| A) Cardiopatía isquémica | 60-70% |
| B) Miocardiopatías (dilatada, hipertrófica, infiltrativa, valvular, insuficiencia cardiaca sistólica o diastólica | 20-30% |
| C) Enfermedad arrítmica primaria | 5–10% |
| Arritmia más frecuente detectada | |
| A) Fibrilación ventricular o taquicardia ventricular | 60–80% |
| B) Actividad eléctrica sin pulso y asistolia | 20–40% |
| Casos a nivel extrahospitalario | 70–89% |
| Supervivencia promedio estimada | <5% |
En las víctimas mayores de 35 años de edad, la enfermedad arterial coronaria con o sin infarto de miocardio es la responsable de la mayoría de los casos, según diversos estudios6,7,9-11,14,15,18,23. Se considera que el 30-40% de los casos son portadores de algún otro tipo de cardiopatía como: miocardiopatía dilatada (adquirida o congénita), miocardiopatía hipertrófica (adquirida o congénita), miocardiopatía infiltrativa, valvular o insuficiencia cardiaca6,15. En las víctimas menores de 35 años las principales causas reportadas son: miocardiopatía hipertrófica, anomalías congénitas de las arterias coronarias, displasia arritmogénica del ventrículo derecho o enfermedades arrítmicas primarias como síndrome de QT largo, síndrome de QT corto, síndrome de Brugada, síndrome de repolarización precoz, Wolff-Parkinson-White, taquicardia ventricular (TV) catecolaminérgica o fibrilación ventricular (FV) idiopática13,22,24-27. En la población entre 35 y 45 años de edad se ha detectado una mayor incidencia de miocardiopatía dilatada secundaria a obesidad así como al uso de drogas ilicitas28.
Arritmias responsablesLa FV y la TV son las arritmias responsables del mayor número de casos de paro cardiaco súbito5,29. Otros ritmos responsables son la asistolia y la actividad eléctrica sin pulso6,18.
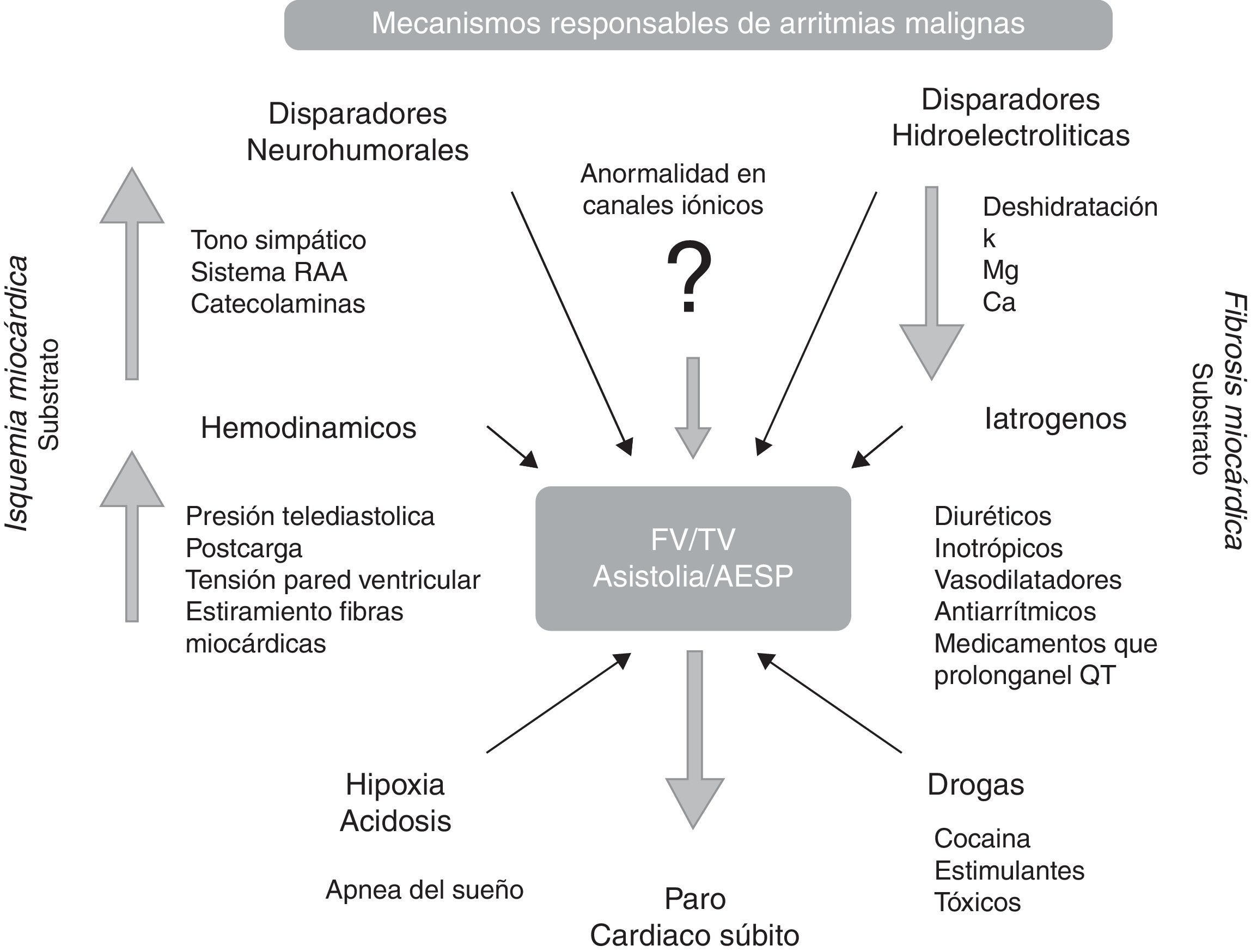
Para que se presente un episodio de FV o TV se requiere la participación de sustratos y disparadores de arritmias como se muestra en la figura 1. Los sustratos más importantes son la isquemia, la fibrosis miocárdica4,8,13,14 y las anomalías genéticas13,30. La isquemia miocárdica favorecerá la dispersión de los períodos refractarios a nivel de las células del miocardio ventricular4,8, la fibrosis miocárdica favorece el desarrollo de circuitos de reentrada ventricular14,15 y las anomalías genéticas en los canales iónicos favorecen alteraciones en la despolarización o repolarización ventricular13. Varios disparadores de arritmias están involucrados, entre los que podemos encontrar: 1) Incremento en la actividad del sistema nervioso autónomo, en la actividad neurohumoral, del sistema renina angiotensina e incremento en el nivel de catecolaminas circulantes; 2) Factores hemodinámicos como aumento de presión telediastólica, de la poscarga, de tensión de la pared ventricular y estiramiento de las fibras de miocardio ventricular; 3) Alteraciones hidroelectrolíticas como hiponatremia, hipocalemia, hipocalcemia, hipomagnesemia y deshidratación; 4) Hipoxia; 5) Acidosis; 6) Factores iatrogénicos secundarios al uso de fármacos como diuréticos, inotrópicos, vasodilatadores, antiarrítmicos o fármacos que prolongan el intervalo QT o que favorecen patrones electrocardiográficos tipo Brugada; 7) Alcohol y drogas como cocaína o LSD y 8) Estimulantes como metilfenidato, exceso de cafeína, exceso de ejercicio, etc.4,8.
TratamientoEl tratamiento del paro cardiaco súbito secundario a FV o TV es la desfibrilación ventricular31, y cuanto más temprano se realice, mayor será la posibilidad de revertir a ritmo sinusal (fig. 2). Al primer minuto, el éxito de la desfibrilación ventricular es superior al 90%, y desciende 7-10% por minuto sin reanimación cardiopulmonar (RCP); con RCP la probabilidad de revertir a ritmo sinusal desciende, de un 3-4% por minuto32. La RCP prolonga la ventana de tiempo para poder realizar desfibrilación exitosa33. Se deberá realizar la cadena básica de supervivencia ante un paciente en paro cardiaco. Dicha cadena implica la detección temprana del paciente y activación del sistema de urgencia médica, RCP temprana, desfibrilación temprana, cuidados avanzados tempranos y cuidados tempranos posreanimación. Al realizar todos los eslabones de la cadena de supervivencia dentro de los primeros 5min del colapso, se mejoran de forma significativa las tasas de supervivencia de estos pacientes31–34 (fig. 3). La colocación de desfibriladores externos automáticos en sitios públicos junto con la realización de maniobras básicas de RCP por el observador de una víctima de paro cardiaco súbito ha demostrado que mejora significativamente la supervivencia, por lo que se recomienda ampliamente la colocación de desfibriladores externos automáticos y el entrenamiento al público en maniobras básicas de RCP en escuelas, aeropuertos, gimnasios, empresas y lugares estratégicos de la comunidad con alta densidad poblacional35. El desfibrilador automático implantable (DAI) es un equipo con alta posibilidad de revertir a ritmo sinusal un episodio de TV o FV ya que puede desfibrilar en menos de 15seg una de estas arritmias36–39. La FV produce una contracción irregular y caótica del miocardio ventricular, con la consecuente incapacidad del corazón para mantener el flujo sanguíneo corporal; de no ser revertida a ritmo sinusal, pasará a asistolia y posteriormente causará la muerte del paciente32,36. En la figura 4 se muestran ejemplos de FV, ritmo agónico y asistolia.
Relación entre el tiempo transcurrido y la posibilidad de revertir a ritmo sinusal con desfibrilación, en casos sin reanimación cardiopulmonar. Adaptada de: Cummins58.
Representación esquemática de varios escenarios de paro cardiaco súbito, RCP, desfibrilación y supervivencia. Observe el escenario en color azul, con aplicación temprana de la cadena básica de supervivencia la posibilidad de supervivencia mejora hasta un 50-60% de las víctimas. RCP: reanimación cardiopulmonar.
La supervivencia del paro cardiaco súbito a nivel extrahospitalario varía ampliamente según el lugar del estudio, pero se estima que es menor al 5%16; en EE. UU. se ha reportado una supervivencia promedio del 4.6%1–3. El mayor determinante de supervivencia es la realización de RCP temprana y desfibrilación precoz35. Cuando se hacen ambos procedimientos dentro de los primeros 5min de ocurrido el paro cardiaco súbito, se puede lograr una supervivencia, evaluada al alta hospitalaria, mayor al 50% y con buena recuperación neurológica40. El DAI ha demostrado su utilidad tanto en prevención primaria de muerte súbita en pacientes con fracción de expulsión menor del 35%38 como en prevención secundaria en sujetos que ya han sobrevivido a un episodio de paro cardiaco súbito39.
Grupos de riesgoLa mayoría de los casos de muerte súbita son pacientes con factores de riesgo para cardiopatía isquémica, sin diagnóstico de enfermedad cardiovascular1–8,29,41; el segundo grupo son los portadores de alguna cardiopatía, pacientes que pueden estar recibiendo atención médica pero que no tienen características de alto riesgo para muerte arritmica6,9-13,16,23; y el tercer grupo son los supervivientes de un paro cardiaco súbito o los que se han detectado con alto riesgo para muerte arrítmica6,25-27,31. En la tabla 2 se describen las características generales de los 3 grupos de riesgo de muerte súbita cardiaca.
Grupos de riesgo para muerte súbita cardiaca
| Características | |
|---|---|
| Grupo 1 | |
| Población general con factores de riesgo para cardiopatía isquémica | Hipertensión arterial sistémicaTabaquismoDiabetes mellitusObesidad, dislipidemia o sedentarismo |
| Grupo 2 | |
| Población con cardiopatía adquirida o congénita | Cardiopatía estructural:Cardiopatía isquémica, cardiopatía hipertrófica, miocardiopatía dilatada, miocardiopatía infiltrativa, insuficiencia cardiaca sistólica o diastólica, displasia arritmogénica del ventrículo derecho. Anomalía congénita en el nacimiento de arterias coronarias. Cardiopatías congénitasEnfermedad arritmogénica primaria asintomáticaSíndrome de Brugada, síndrome de QT largo, síndrome de QT corto, Wolff-Parkinson-White, síndrome de repolarización precoz |
| Grupo 3 | |
| Pacientes recuperados de un episodio de PCS o con antecedentes de TV, FV o síncope (secundario a arritmias ventriculares) | Cardiopatía estructural:Insuficiencia cardiaca sistólica con una fracción de expulsión persistente por debajo del 35%, cardiopatía isquémica, hipertrófica, dilatada o infiltrativaEnfermedad arritmogénica primaria sintomáticaSíndrome de Brugada, síndrome de QT largo, síndrome de QT corto, Wolff-Parkinson-White, síndrome de repolarización precoz, taquicardia ventricular catecolaminérgica o fibrilación ventricular idiopática |
FV: fibrilación ventricular; PCS: paro cardiaco súbito; TV: taquicardia ventricular.
Cualquier paciente en estos grupos se considera de mayor riesgo y deberá ser motivo de una revisión más exhaustiva cuando tenga antecedentes familiares de muerte súbita.
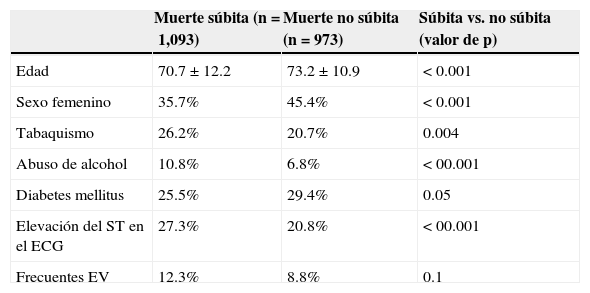
La presencia de isquemia miocárdica sintomática o asintomática es el factor de riesgo más importante para desarrollar muerte súbita en los adultos, desafortunadamente en muchos de estos pacientes será el primer y único síntoma5,8,11,23,41. Se han estudiado pacientes con cardiopatía isquémica crónica y se han detectado algunos predictores de muerte súbita; en un estudio de 30,680 pacientes con diagnóstico de cardiopatía isquémica y seguidos por 3.3 años, se observó que tienen mayor prevalencia de muerte súbita los pacientes del sexo masculino, de menor edad (70 frente a 74 años), fumadores, con elevación del segmento ST y con más extrasístoles ventriculares42 (tabla 3). Otros marcadores de riesgo de muerte súbita son la mayor presencia de isquemia miocárdica residual detectada por tomografía simple con emisión de positrones, en pacientes que ya han sufrido un infarto de miocardio; a mayor isquemia, mayor es la prevalencia de muerte súbita43. A mayor grado de fibrosis miocárdica detectada por resonancia magnética nuclear, mayor la posibilidad de arritmias ventriculares y muerte súbita38. También se ha demostrado que a mayor prevalencia de oclusión total de arterias coronarias relacionadas con el infarto, mayor la probabilidad de arritmias ventriculares y muerte súbita44.
Factores de riesgo en pacientes con cardiopatía isquémica que fallecieron por muerte súbita comparados con los que fallecieron de forma no súbita
| Muerte súbita (n=1,093) | Muerte no súbita (n=973) | Súbita vs. no súbita (valor de p) | |
|---|---|---|---|
| Edad | 70.7±12.2 | 73.2±10.9 | <0.001 |
| Sexo femenino | 35.7% | 45.4% | <0.001 |
| Tabaquismo | 26.2% | 20.7% | 0.004 |
| Abuso de alcohol | 10.8% | 6.8% | <00.001 |
| Diabetes mellitus | 25.5% | 29.4% | 0.05 |
| Elevación del ST en el ECG | 27.3% | 20.8% | <00.001 |
| Frecuentes EV | 12.3% | 8.8% | 0.1 |
ECG: electrocardiograma; EV: eventos vasculares.
Modificada de Every et al.42.
Los pacientes con insuficiencia cardiaca sistólica y fracción de expulsión persistentemente por debajo del 35% tienen alto riesgo de fallecer por muerte súbita o por progresión de la insuficiencia cardiaca45,46. Es importante reconocer a los pacientes con mayor riesgo de paro cardiaco súbito, ya que son los candidatos apropiados para recibir un DAI con lo que se reduce su mortalidad47. La fracción de expulsión como único predictor de paro cardiaco súbito tiene limitaciones y es insuficiente, por lo que es necesario utilizar otros marcadores48. Clasificar a los pacientes con insuficiencia cardiaca sistólica utilizando la escala de Seattle permite dividirlos en 5 categorías; las categorías con mayor riesgo de paro cardiaco súbito son las categorías 1 y 2, intermedio la categoría 3 y bajo las categorías 4 y 549. Las categorías 4 y 5 tienen mayor riesgo de fallecer por progresión de falla de bomba. Esta clasificación nos permite optimizar los recursos y tener una mejor recomendación para utilizar un DAI50 (tabla 4). Los pacientes con insuficiencia cardiaca «diastólica» (fracción de expulsión preservada) tienen también una alta prevalencia de muerte súbita cardiaca51, por lo que es otro grupo que deberá ser clasificado para detectar a aquellos pacientes con alto riesgo de paro cardiaco súbito y puedan ser beneficiados con un DAI para reducir su mortalidad3. Los pacientes con insuficiencia renal son un grupo de alto riesgo de muerte súbita. Según el registro de datos renales de EE. UU. (US Renal Data System), el 22% de todas las muertes en estos pacientes son por muerte súbita cardiaca52. La incidencia se incrementa con la edad, un 2% por año para pacientes entre 20 y 44 años de edad, un 3.7% por año para pacientes entre 45 y 64 años de edad y un 7% por año para aquellos de 65 años o más53. Se ha determinado que el daño renal es un predictor independiente de paro cardiaco súbito y afecta tanto a hombres como a mujeres54.
Escala de Seattle de insuficiencia cardiaca sistólica modificada y nivel de recomendación aproximado para la utilización de desfibrilador automático implantable
| Categoría 1 | Categoría 2 | Categoría 3 | Categoría 4 | Categoría 5 | |
|---|---|---|---|---|---|
| Mortalidad anual calculada | 1.11-3.58% | 3.59-5.26% | 5.26-7.3% | 7.3-11.14% | 11.15-63.48% |
| Edad (años) | 50 | 57 | 61 | 64 | 68 |
| Hombres (%) | 69 | 72 | 77 | 81 | 86 |
| Clase NYHA IIII (%) | 5 | 18 | 27 | 41 | 61 |
| Cardiopatía isquémica (%) | 30 | 42 | 52 | 61 | 75 |
| Fracción de expulsión (%) | 25 | 25 | 24 | 25 | 21 |
| Presión arterial sistólica (mmHg) | 126 | 120 | 120 | 116 | 110 |
| Creatinina (mg/dl) | 1.0 | 1.0 | 1.1 | 1.2 | 1.4 |
| QRS (mseg) | 104 | 107 | 112 | 114 | 120 |
| Caminata a 6min (metros) | 380 | 365 | 359.6 | 310.5 | 280.4 |
| Muerte súbita | Alto | Alto | Intermedio | Bajo | Bajo |
| Muerte por falla de bomba | Bajo | Bajo | Intermedio | Alto | Alto |
| Recomendación para utilizar un desfibrilador automático implantable | Alto | Alto | Intermedio | Bajo | Bajo |
Modificada de Levy et al.49.
Los atletas de alto rendimiento tienen mayor mortalidad cardiovascular24,55,56,. En los grupos menores de 35 años de edad, las principales causas de muerte súbita son: miocardiopatía hipertrófica, anomalías de las arterias coronarias y displasia arritmogénica del ventrículo derecho24. En ausencia de cardiopatía estructural el síndrome de Wolff-Parkinson-White, el síndrome de Brugada, el síndrome de QT largo, el síndrome de QT corto y la TV polimórfica catecolaminérgica son los causantes más frecuentes30. En grupos de atletas mayores de 35 años de edad, la principal causa de muerte súbita es la cardiopatía isquémica, como en la población general11. En la región de Véneto, Italia, se analizaron 1,386,600 jóvenes, de los cuales 112,790 fueron atletas competitivos. Durante el seguimiento de 21 años se presentaron 300 casos de muerte súbita con una incidencia para los atletas de 2.3 por 100,000/ año y para los no atletas de 0.9 por 100,000/año, con un riesgo relativo estimado entre atletas y no atletas de 1.95 para hombres y 2 para mujeres. El estudio histopatológico en estos casos mostró una anomalía subyacente como displasia arritmogénica del ventrículo derecho, anomalía congénita de arterias coronarias o enfermedad coronaria prematura como principales causas del paro cardiaco súbito. El estudio concluyó que el ejercicio como tal no es el causante de aumento de la mortalidad, sino que es un disparador de muerte súbita principalmente en aquellos atletas que tienen una condición cardiovascular que los predispone a mayor mortalidad; de estos hallazgos surge la recomendación de realizar una adecuada revisión médica que incluya electrocardiograma a personas que desean realizar ejercicio de alto rendimiento para valorar su condición cardiovascular57.
ConclusionesLa muerte súbita cardiaca continúa siendo un problema de salud pública a nivel mundial. El mayor número de casos se presenta en la población general, a nivel extrahospitalario y en personas que no se conocían portadores de cardiopatía, donde solo se han encontrado factores de riesgo cardiovascular para cardiopatía isquémica. El control de estos factores de riesgo y la prevención de cardiopatía isquémica son las principales medidas para reducir la incidencia de muerte súbita cardiaca en la población general. En un número importante de casos es el primer y único síntoma de cardiopatía isquémica. También se presenta en pacientes con otras cardiopatías o en los supervivientes de paro cardiaco súbito o con marcadores de alto riesgo de muerte arrítmica. La RCP y la utilización de desfibriladores externos automáticos son medidas que deben ser conocidas por todo el personal de salud y la población general para mejorar la supervivencia de los pacientes con paro cardiaco súbito. Es indispensable identificar a los grupos de alto riesgo de muerte arrítmica ya que se pueden beneficiar del implante de un DAI, dispositivo que ha demostrado que reduce la mortalidad por arritmias ventriculares malignas.
FinanciaciónNinguna.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.