Introducción
La aparición del cardio-desfibrilador implantable (CDI), a inicios de la década del ochenta, dio origen a una época de avances vertiginosos en el tratamiento y prevención de la muerte súbita cardiaca; una de las formas más frecuentes de muerte en la familia humana y de todos los mamíferos en general.
A pesar de las enormes exigencias, que acorde con los dictados de la medicina basada en la evidencia, le fue solicitada a la terapia de cardio-desfibrilación, ésta alcanzó los resultados requeridos con éxito y se convirtió, dentro de las guías actuales, en la terapia de elección para el tratamiento y prevención de la muerte súbita cardiaca (MSC). A pesar de ello, el uso del CDI continúa siendo un tema polémico en la comunidad médica en general.
Entrando en tema...
Clásicamente, el paciente se encuentra perfectamente bien en un momento y agoniza unos instantes más tarde. En esta simple frase se condensan las tres características que definen a la muerte súbita: 1. Fenómeno natural, 2. Inesperado, 3. Rápido.
La pérdida de la conciencia es casi inmediata tras la instauración generalmente de una arritmia ventricular rápida, y menos frecuentemente, de asistolia ventricular o de bradicardia extrema. La detención circulatoria que sigue se acompaña del cese de movimientos respiratorios, aunque a veces pueden persistir, brevemente, movimientos respiratorios jadeantes. Las convulsiones generalizadas y las pupilas dilatadas y fijas son comunes y, en ocasiones, una marcada cianosis.
Se define como muerte clínica el lapso durante el cual la circulación se ha interrumpido pero todavía persiste la vida a nivel celular. El tiempo para el rescate será dramáticamente breve, no más allá de diez minutos, pero con una caída exponencial de las probabilidades de supervivencia con cada minuto transcurrido.
Si el paciente fue rescatado, nos hallaremos frente a una indicación de prevención secundaria. Si el episodio que hemos descrito aún no ha ocurrido, pero tenemos sensible evidencia de que pueda ocurrir en el futuro, nos hallamos frente a una indicación de prevención primaria.
Entre estos dos estrechos márgenes asechan nuestras incertidumbres e indecisiones relativas al uso del CDI. Alguna de las inconsistencias que padecemos podría resumirse en un cierto número de preguntas ante las cuales deberíamos de disponer de una respuesta adecuada para el paciente y satisfactoria para nosotros, los médicos.
¿Cuál es el verdadero impacto de la muerte súbita de causa cardiaca en la población occidental y cuál es el mecanismo más frecuente?
Habida cuenta de la dificultad para establecer el diagnóstico de muerte súbita, que siempre es retrospectivo, y cuya mayoría, ocurre en ámbitos no hospitalarios, la cifra varía de acuerdo a las diversas fuentes bibliográficas, pudiendo estimarse el número entre 7501 y 10002 muertes súbitas cardiacas por millón de habitantes y por año, que se relaciona en 80% de los casos con cardiopatía isquémica, con o sin síntomas.
Téngase en cuenta además, que 50% de todas las muertes cardiacas ocurre de manera súbita.
Con relación al mecanismo subyacente, existen numerosos factores que pueden actuar en distintos escenarios, tales como el sistema nervioso (desbalance del tono autonómico), el tisular (secuelas fibróticas, bloqueos unidireccionales y mecanismos de re-entrada), trastornos celulares (aumento de la excitabilidad o demoras en la repolarización que originan arritmias por aumento del automatismo o mecanismo gatillado), alteraciones subcelulares (activación o desactivación de los canales iónicos como la corriente de Ca++ y de K+ , o mutaciones de los canales de Na+ ).
El resultado de todas estas alteraciones solas o combinadas, favorecen preferentemente el desarrollo de taquiarritmias ventriculares y justifican el amplio predominio que ejercen por sobre las bradiarritmias en la generación de episodios de muerte súbita.3
¿Cuál es la población expuesta a la MSC?
Desde el inicio de la terapia con implante de cardio-desfibrilador los estudios se centraron en subgrupos de alto riesgo; pacientes mayoritariamente coronarios, con antecedentes de infarto de miocardio y con acentuado compromiso de la función ventricular, evidenciado por una baja fracción de eyección ventricular izquierda. Así los estudios de prevención secundaria (AVID,4 CIDS,5 CASH6) y los de prevención primaria (MADIT,7 MADIT II,8 SCD-HeFT9), demostraron las ventajas del CDI sobre las terapias con drogas en poblaciones con severa enfermedad cardiaca.
Sin embargo, la MSC se observa en todos los niveles de una población general, aunque la incidencia difiere en los distintos segmentos estudiados, donde el número de eventos muestra una relación inversa al porcentaje de riesgo, debido al enorme denominador que representa la población general, cuando se la compara con subgrupos de alto riesgo, que son proporcionalmente muy pequeños, pero con una cifra de muertes anuales muy alta.
Desde el clásico esquema de Myerburg y colaboradores10 hasta el registro de Maastrich,11 se ha hecho constar claramente que los pacientes involucrados en los estudios antes mencionados, representan una porción pequeña del total de MSC anuales (alrededor de 24%), mientras que otro 21% agrupa individuos con antecedentes cardiovasculares, pero que permanecen asintomáticos con buena función ventricular; en tanto más de 50% restante lo constituyen sujetos sin antecedentes, con funciones ventriculares normales y asintomáticos, tornando altamente dificultosa la tarea de identificar al individuo en riesgo.
3. ¿Cuándo tiempo debe de transcurrir para poder descartar el riesgo de MSC en un paciente con antecedentes de infarto de miocardio y que rol desempeñan los procedimientos de revascularización (quirúrgicos o mediante cateterismo) para disminuir las probabilidades de MSC?
La respuesta debe involucrar el proceso que toda injuria al músculo cardiaco origina: el remodelado cardiaco.12 A nivel ventricular el remodelado cardiaco se expresa por hipertrofia, necrosis, apoptosis, fibrosis y dilatación; mientras a nivel sistémico, el mecanismo neurohumoral adaptativo del sistema circulatorio, intenta colaborar generando taquicardia, vasoconstricción y retención líquida. La consecuencia final será cambios morfológicos en el corazón que, aunque siendo un proceso fisiológico compensatorio, actuará como factor etiopatogénico de la insuficiencia cardiaca. Debido además a que es un proceso que se retroalimenta permanentemente, sus efectos negativos pueden emerger mucho tiempo después de ocurrido el evento que le dio origen.
Congruente con lo comentado, en el registro de Maastricht11 el tiempo promedio entre el infarto y la MSC fue de 9.75 años, mientras que en la serie de Pascale y colabores13 alcanzó los 12.4 años. Por su parte Wilber y colaboradores14 partiendo del estudio MADIT II, demuestra beneficios significativos del CDI, aún mas allá de 15 años de ocurrido el infarto de miocardio.
Con relación a los procedimientos de revascularización ligados a la presencia de isquemia, sin duda deberán llevarse a cabo toda vez que estén indicados, sin dejar por ello de advertir dos factores importantes: 1. La revascularización actúa sobre grandes vasos y no tiene efecto en regiones periféricas donde el fenómeno isquémico puede persistir (en particular en individuos con diabetes); 2. La presencia de una secuela de infarto, que los procedimientos de revascularización no modifican, sigue brindando el sustrato necesario para el desarrollo de arritmias ventriculares rápidas (en particular la taquicardia monomórfica sostenida), independiente del resultado del tratamiento antiisquémico que se haya aplicado. Prueba de esto último se observa, una vez más, en el registro de Maastricht, en el que 38% de los sujetos que padecieron MSC, habían recibido previamente algún tipo de terapia de revascularización.
En resumen, no existen plazos para descartar el riesgo de MSC relacionado a un evento cardiaco lejano, ni la terapia de revascularización tiene efectos sobre el riesgo que representa la secuela del infarto, en cuanto a sustrato que favorece la aparición de arritmias rápidas, sustentadas en un mecanismo de reentrada.
¿Es la terapia farmacológica una alternativa válida frente al CDI para la prevención de la MSC?
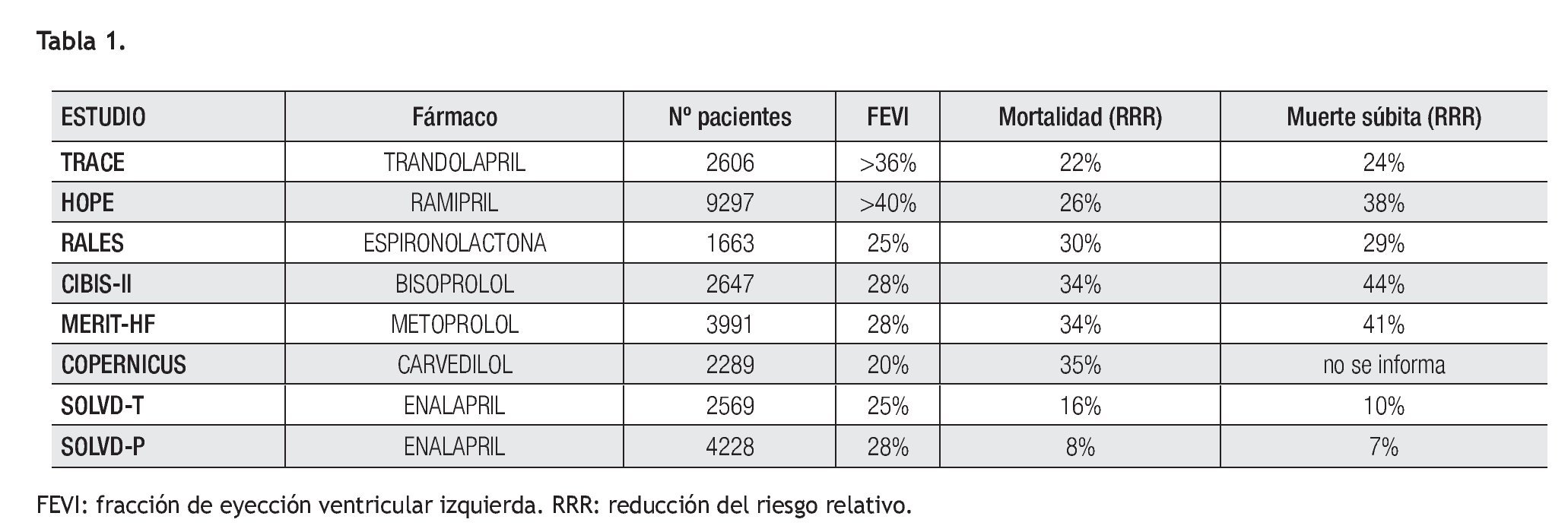
He aquí que el moderno arsenal de drogas que empleamos a diario, particularmente para el control y tratamiento de la hipertensión arterial, la cardiopatía isquémica y la insuficiencia cardiaca, nos ha alertado sobre el impacto favorable que estas drogas producen sobre la mortalidad total y también sobre la MSC.15-18 De tal manera que nos lleva a cuestionarnos acerca de la posibilidad de usarlas como tratamiento alternativo frente al CDI. En la Tabla 1 la mayoría de las drogas que figuran demuestran tener efectos reductores en la incidencia de MSC cuando se compara los resultados con los pacientes de los grupos controles. Sin embargo lo que vemos enunciado son descensos del riesgo relativo, que llevados a valores de riesgo absoluto, sólo significa una leve mejora en el número de muertes con relación a los que no recibieron tratamiento.
Por ejemplo, el efecto de los beta bloqueadores para la prevención de la muerte súbita cardiaca en términos de reducción del riesgo absoluto, varía entre 1.3% y 2.2% de acuerdo a la droga utilizada19. Resultados mejores publican Packer y colaboradores,20 con carvedilol, y a seis meses de seguimiento se advierte una disminución del riesgo absoluto de 4.6%, mientras con igual tiempo de seguimiento y droga, Bristow21 informa disminuciones mayores. Cuando se comparan estos resultados con los obtenidos con el CDI, se observa que éstos logran reducciones del riesgo absoluto en el orden de 7% a 7.9%, tanto en prevención primaria,22 como secundaria a dos años de seguimiento,23 llegando particularmente el estudio MADIT hasta 17%.
En suma, no hay discusión en cuanto al efecto reductor sobre la MSC y la mortalidad de toda causa que aportan las drogas cualitativamente hablando; pero el resultado se busca en términos cuantitativos y debería reflejarse en una reducción importante del riesgo absoluto. En ese aspecto, el CDI ofrece resultados superiores a los que aporta la terapia farmacológica incluyendo antihipertensivos, antialdosterónicos, ácido acetilsalicílico, betabloqueadores, antiarrítmicos y aún estatinas.
A pesar de ello, en la visión actual se impone el concepto de beneficio acumulado, donde la suma de tratamientos (drogas más dispositivos) obtiene un porcentaje mayor de reducción del riesgo absoluto y sustenta el empleo de tratamientos asociados.
Un párrafo aparte merece el empleo de antiarrítmicos, especialmente la amiodarona, droga que clásicamente se ha utilizado para comparar contra el CDI. Los estudios antes mencionados, como el AVID4 en prevención secundaria o el SCD-HeFT9 en prevención primaria en sujetos con insuficiencia cardiaca, han demostrado taxativamente que en pacientes con severo daño miocárdico y baja fracción de eyección, la amiodarona no tiene efecto sobre la mortalidad total, y solamente podría emplearse como alternativa al CDI en individuos con fracción de eyección superior a 35%.
Por consiguiente el tratamiento preventivo de la MSC debe hacerse mediante el empleo del CDI, sin que se pueda considerar otra alternativa en el momento actual. La asociación de fármacos es ventajosa en cuanto contribuye, aunque en menor grado, a la reducción del riesgo absoluto y, en el caso de los betabloqueadores, por su participación además en la disminución de las terapias de choque del CDI.24
¿Se debe indicar el Estudio Electrofisiológico (EEF) para seleccionar al paciente que requiere del CDI?
La prevención de la MSC encuentra en el CDI una herramienta de bien probada eficacia, que sin embargo no puede utilizarse con amplitud, debido a que la identificación del paciente que pueda beneficiarse del CDI, se basa en criterios para predecir el riesgo de muerte arrítmica poco específicos, como son la fracción de eyección ventricular izquierda y la presencia de insuficiencia cardiaca clínicamente manifiesta (clases funcionales II - III - IV).
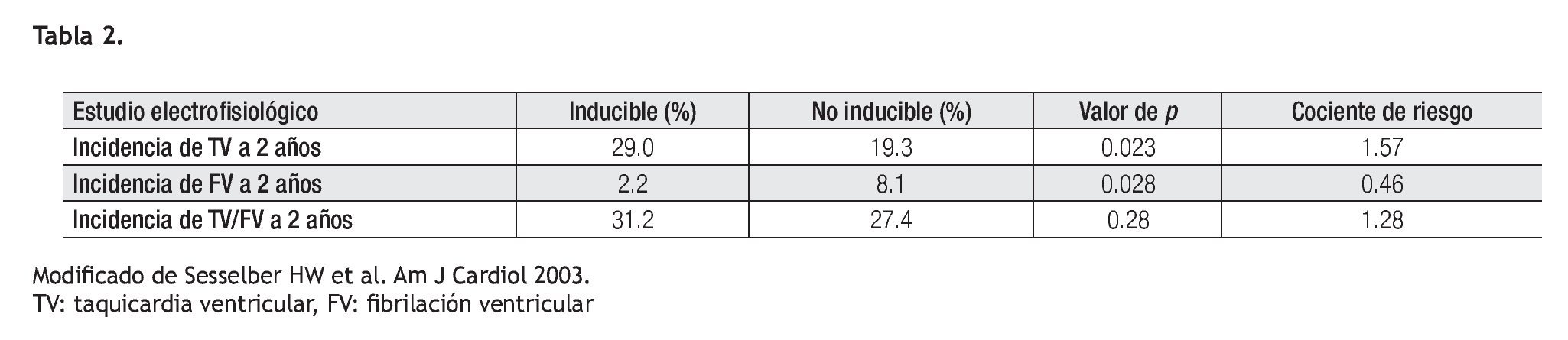
En tal sentido, cabe preguntarse de que manera podría colaborar el EEF en el reconocimiento de sujetos en riesgo. ¿Qué aporta la bibliografía en este campo? En la publicación de Buxton y colaboradores, surgida del estudio MUSTT,25 que utiliza el EEF para discriminar los posibles beneficiarios de tratamiento (drogas o CDI), los resultados demostraron la falta de valor predictivo del procedimiento, y como resultado colateral, la ventaja del CDI para la reducción de mortalidad total y MSC cuando se lo comparó con drogas. Por su parte la publicación de Sesselberg HW,26 con pacientes del estudio MADIT II, encuentra un valor predictivo positivo entre los sujetos que desarrollaron TV en el EEF, pero como contrapartida, en los no inducibles la incidencia de FV fue significativamente mayor, por lo que a dos años de seguimiento la suma de eventos (TV + FV) mostraron una absoluta paridad entre ambos grupos, independiente de cual hubiera sido el resultado del EEF, e invalidando este procedimiento para dictaminar conductas acerca del implante de un CDI (Tabla 2).
Resumiendo, el EEF no es un recurso confiable para la toma de decisiones relativas a la indicación de un CDI como prevención de la MSC y solamente en subgrupos muy particulares podría ser un recurso a emplear para fortalecer la decisión terapéutica.
¿Qué actitud debemos tomar con relación a la población en riesgo que no está incluida en los estudios clínicos que corrientemente utilizamos?
La discusión planteada en la pregunta dos nos indica que más de 75% de las MSCs ocurren en individuos pertenecientes a lo que podría considerarse población sana y por ello prácticamente invisibles a nuestros ojos; o con antecedentes cardiovasculares pero buena condición cardiaca y asintomáticos. Los primeros suelen ser personas jóvenes cuyo riesgo está ligado a enfermedades genéticas,27 los segundos se relacionan con enfermedades degenerativas que también pueden tener componentes genéticos y/o tratarse de sujetos expuestos a una sobrecarga de estrés de gran magnitud.28
En ambos casos los intentos de identificación de individuos con alto riesgo de sufrir una MSC, nos recuerda que la medicina es un arte y no una ciencia exacta, y que la astucia clínica que despleguemos será nuestro principal recurso.
En el interrogatorio debe indagarse acerca de muertes súbitas familiares a temprana edad y en episodios sincopales o casi sincopales del paciente que pudieran haberse atribuido a causas vasovagales benignas. En oportunidades el ECG puede aportar datos de gran valor para identificar patologías que pueden ser asintomáticas hasta ese momento, como ser la onda delta en el WPW, la onda épsilon en la displasia arritmogénica del ventrículo derecho (ARVD), la presencia de intervalos QT largos (LQTS), etc. En particular, deberán tenerse en cuenta aquellas entidades que estadísticamente sean las más frecuentes, dentro de su rareza (miocardiopatía hipertrófica 1:500 habitantes, WPW 1:500, Brugada 1: 1000, LQTS 1: 5000, ARVD 1: 5000).
Para los sujetos con antecedentes cardiovasculares, la detección durante el examen físico de una frecuencia cardiaca elevada en reposo puede ser el único alerta que nos anuncie de cambios en la condición cardiaca.29,30 Se debe también mantener la atención sobre los factores de riesgo (en especial el perfil lipídico), valorar anualmente mediante test ergométrico eventuales alteraciones del ECG o arritmias en el esfuerzo y seguimiento anual mediante ecocardiografía que nos revele cambios morfológicos importante atribuible a remodelado cardiaco, que casi siempre se asocia a incrementos del riesgo de desarrollar insuficiencia cardiaca o MSC. La percepción de extrasístoles aisladas o la referencia del paciente a ocasionales palpitaciones requiere formalmente al menos un monitoreo continuo de 24 horas.
¿Son peligrosos los cardio-desfibriladores automáticos implantables? y ¿cómo afectan la calidad de vida?
El CDI es una terapia extrema cuyo objetivo último es rescatar al paciente de un episodio arrítmico presumiblemente mortal. El choque que recibe el paciente, si se encuentra consciente, es doloroso y desagradable (aunque pueda implicar haberle salvado la vida). Por tanto no es posible esperar del CDI mejoras de la calidad de vida, excepto en el aspecto de brindarle al usuario la reconfortante sensación de estar protegido contra arritmias potencialmente letales.
Diversas publicaciones han hecho conocer que la terapia de choque encierra el riesgo de promover daños al músculo cardiaco, y que ello se debe de tener en cuenta cuando se hace un balance de los beneficios y perjuicios que están ligados al uso de ésta terapia.31 Al respecto tres puntos deben ser considerados: a). Un porcentaje de individuos implantados recibirá a lo largo de su vida choques innecesarios32 (choques inapropiados), debido a la percepción errónea por parte del dispositivo, de señales que interpreta como arritmia ventricular; b). Los choques pueden eventualmente inducir una arritmia donde no la había (choque inapropiado) o acelerar una arritmia ventricular verdadera, generando mayor riesgo para el paciente; c). El choque somete al músculo cardiaco a una corriente de elevado voltaje (~740 voltios) y es capaz de generar daño en el músculo cardiaco. La circunstancia de desencadenar choques múltiples incrementa la magnitud del daño.
Aunque existe relación demostrada entre número de choques y aumento del riesgo de muerte, también lo hay en el tipo de choque: para sujetos que recibieron choques inapropiados la sobrevida al año alcanza 94.9%, mientras que en los que recibieron choques apropiados la cifra desciende a 76.9%; marcando que además del efecto negativo del choque, el grado de compromiso miocárdico (arritmias graves = miocardio más comprometido), tiene un rol en la evolución de esos pacientes.33
Por otro lado debemos saber que un CDI ofrece la posibilidad de tratar arritmias ventriculares malignas mediante dos alternativas: la sobre-estimulación ventricular (a través de un tren de ondas de igual frecuencia, o con aceleración progresiva de los estímulos: rampa), o el choque, liberando energías del orden de hasta 30 Joules o superiores de acuerdo a las marcas y modelos existentes. Un manejo adecuado de la programación34 y la posibilidad de agregar más criterios para discriminar la señal percibida, vale decir, buscar mayor especificidad en el reconocimiento de la arritmia en cuestión (comienzo brusco, estabilidad, ancho del complejo QRS, entre otros), dará como resultado una disminución de las complicaciones indeseables que se asocian al CDI.
Los dispositivos más actualizados pueden intentar además, terapia de sobre-estimulación al tiempo que cargan los capacitores (que acumulan la energía que se aplicará en el choque), en un intento, que estadísticamente se ha probado exitoso,35 de controlar la arritmia y abortar el choque. También cuentan con la capacidad de constatar la persistencia de la arritmia una vez cargada la energía que se dispondrá para el choque pudiéndose, una vez más, abortar el mismo en caso de remisión espontánea del ritmo anómalo.
En resumen, el CDI es un dispositivo de alta complejidad para tratar una entidad con altísimo riesgo de vida, que requiere ser manejado por expertos para lograr el máximo beneficio, al tiempo que se minimiza la probabilidad de generar efectos negativos.
Correspondencia: Raúl Garillo.
Universidad Católica Argentina, Facultad de Medicina. Ciudad Autónoma de Buenos Aires, Perú 635, CABA. Buenos Aires (1068)
Teléfono: +5411 4361 0280.
Correo electrónico:raul.aachen@gmail.com
Recibido el 7 de abril de 2010;
aceptado el 17 de junio de 2010.