Introducción
Abciximab es el fragmento Fab del anticuerpo monoclonal quimérico humano-murino 7E3 que se fija a la glucoproteína IIb/IIIa, vitronectina y receptores Mac-1 humanos. Actúa mediante inhibición de la agregación plaquetaria evitando la unión del factor de von Willebrand y otras moléculas adhesivas al fibrinógeno en la zona de unión del receptor de la GP IIb/IIIa.1
La principal indicación de abciximab es la prevención de eventos cardiovasculares adversos mayores (MACE por sus siglas en Inglés) durante tratamiento de intervención coronaria percutánea en pacientes con síndrome coronario agudo. Sus efectos adversos más relevantes son la hemorragia y la trombocitopenia.2 Berkowitz y colaboradores3 clasifican ésta última complicación en cuatro grupos progresivos según la reducción del recuento plaquetario: a) trombocitopenia <100 x 109/L; b) trombocitopenia grave <50 x 109/L; c) trombocitopenia grave aguda <50 x 109/L dentro de las 24 horas de iniciada la terapia y en d) trombocitopenia profunda aguda <20 x 109/L, dentro de las primeras 24 horas de iniciada la terapia.
Existe una clara asociación entre los inhibidores de la glucoproteína IIb/IIIa (GP IIb/IIIa) y trombocitopenia, definida como una cuenta plaquetaria <100 x 109/L que ocurre en 2.5% a 6% de los pacientes; y una trombocitopenia severa (<50 x 109/L) que ocurre en 0.4% a 1.6% de los casos en diversos ensayos clínicos, mientras que la transfusión de plaquetas es requerida en 0.9 % a 6% de los pacientes.4-6 En el registro de readministración de abciximab reportado por Tcheng y colaboradores,7 la trombocitopenia ocurrió en 4.6% de los pacientes, incluidos 2.4% que desarrollaron trombocitopenia profunda <20 x 109 células/L.
La trombocitopenia asociada al abciximab ocurre típicamente dentro de las 24 horas posteriores a la exposición, a diferencia de la inducida por otros fármacos que requiere mayor tiempo desde que son administrados hasta inducir sensibilización.8 Una hipótesis para explicar la rápida ocurrencia de trombocitopenia después de la exposición inicial al abciximab consiste en la existencia de anticuerpos preformados específicos murinos dentro de la estructura molecular del anticuerpo monoclonal quimérico humano-murino.9
Presentación del caso
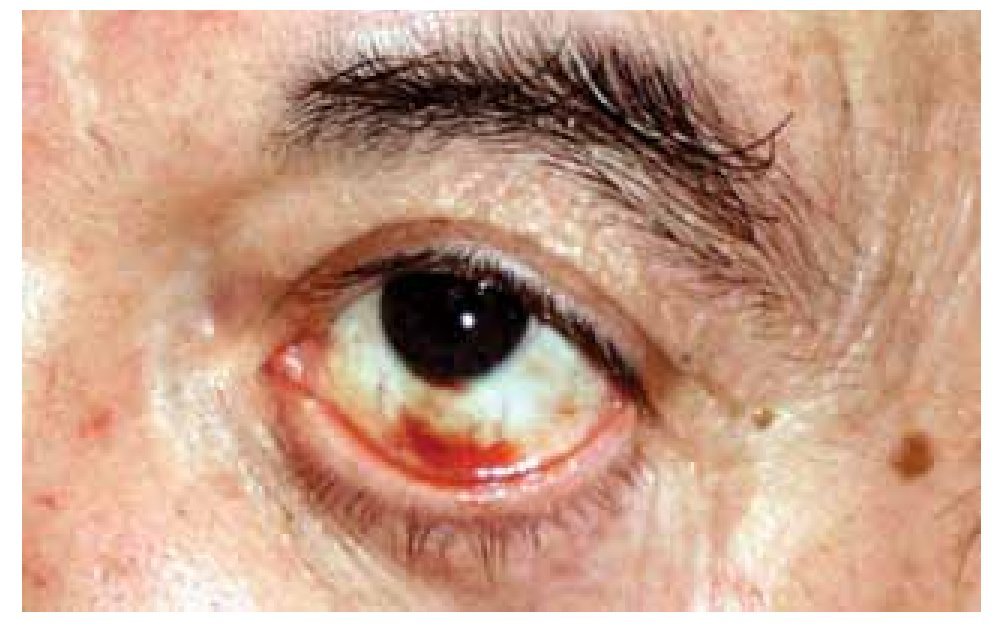
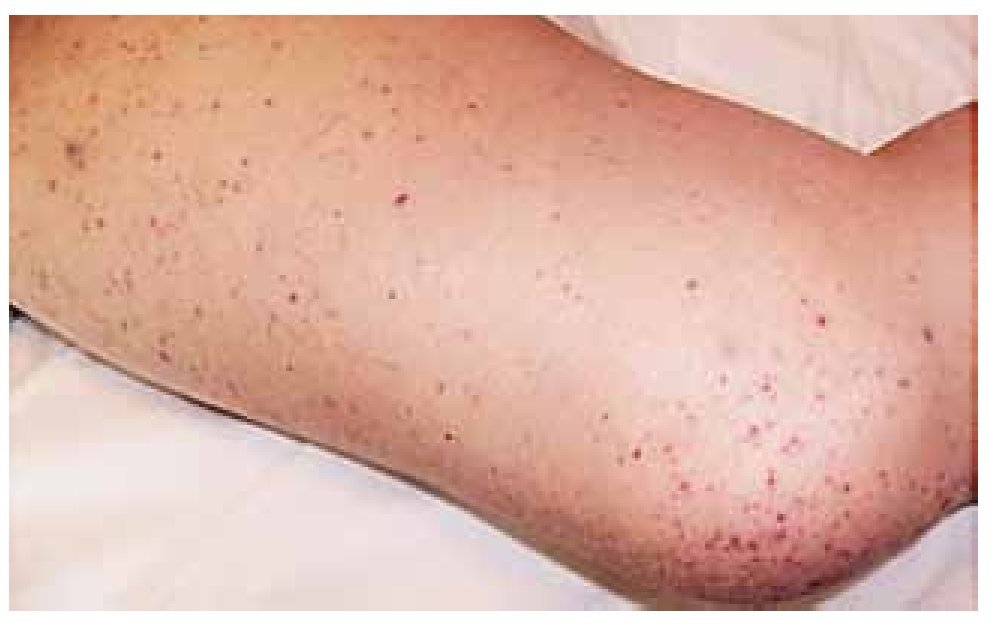
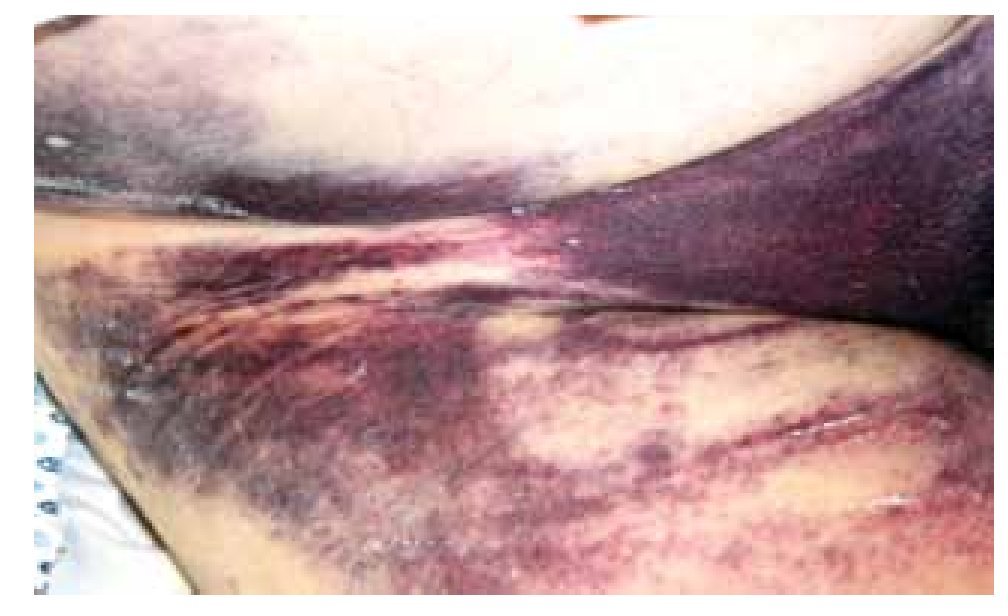
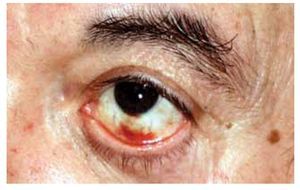
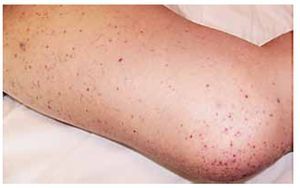
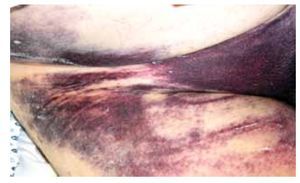
Hombre de 65 años de edad, fumador, con hipertensión arterial y dislipidemia en tratamiento farmacológico que acudió con angina inestable de reciente inicio, progresiva, sin elevación de marcadores de daño miocárdico. Su electrocardiograma mostró cambios de repolarización por isquemia antero-lateral y el ecocardiograma, alteraciones de movilidad anterior y apico-lateral. Se realizó coronariografía con hallazgo de varias lesiones de 70% a 80% de obstrucción del diámetro luminal en los tercios proximal, medio y distal de una arteria descendente anterior (DA) grande. Se realizó angioplastía con colocación de 4-stents medicados de sirolimus con expansión óptima y flujo TIMI 3 más perfusión. Se premedicó al paciente con ácido acetilsalicílico 325 mg, clopidogrel 600 mg y heparina 5000 uI intravenosas. Debido al número de Stents colocados se decidió administrar abciximab (ReoPro®) 25 mg/Kg en bolo seguido de infusión a 10 μg/min (0.125 μg/kg/min) durante tres horas. Inmediatamente después del procedimiento, el paciente tuvo urticaria, agitación psicomotriz, hemorragia sub-conjuntival (Figura 1), gingivorragia y petequias diseminadas (Figura 2) e inició la formación de un hematoma en el sitio de punción (Figura 3). La cuenta plaquetaria previa a la intervención era de 218 x 109/L, y la cifra tres horas posterior al procedimiento de 2 x 109/L. El perfil de coagulación mostró un: tiempo de protrombina 15.6 segundos (control 11.1 segundos); tiempo de tromboplastina parcial 39.7 segundos (35.1 segundos); tiempo de hemorragia 14.5 minutos (método de Ivy, uno a siete minutos); dímeros D 1000 pcg/dL (<500 pcg/dL). El estudio de agregación plaquetaria inducida por heparina (método de test de agregación plaquetaria a bajas concentraciones de heparina y método de activación plaquetaria inducida por heparina) y los anticuerpos antiplaquetarios resultaron negativos. Se suspendió abciximab y antiplaquetarios.
Figura 1. Hemorragia sub-conjuntival.
Figura 2. Púrpura cutánea con petequias de predominio en extremidades inferiores.
Figura 3. Importante hematoma en región del muslo derecho, sitio a través del cual se tuvo el acceso vascular arterial para la intervención coronaria.
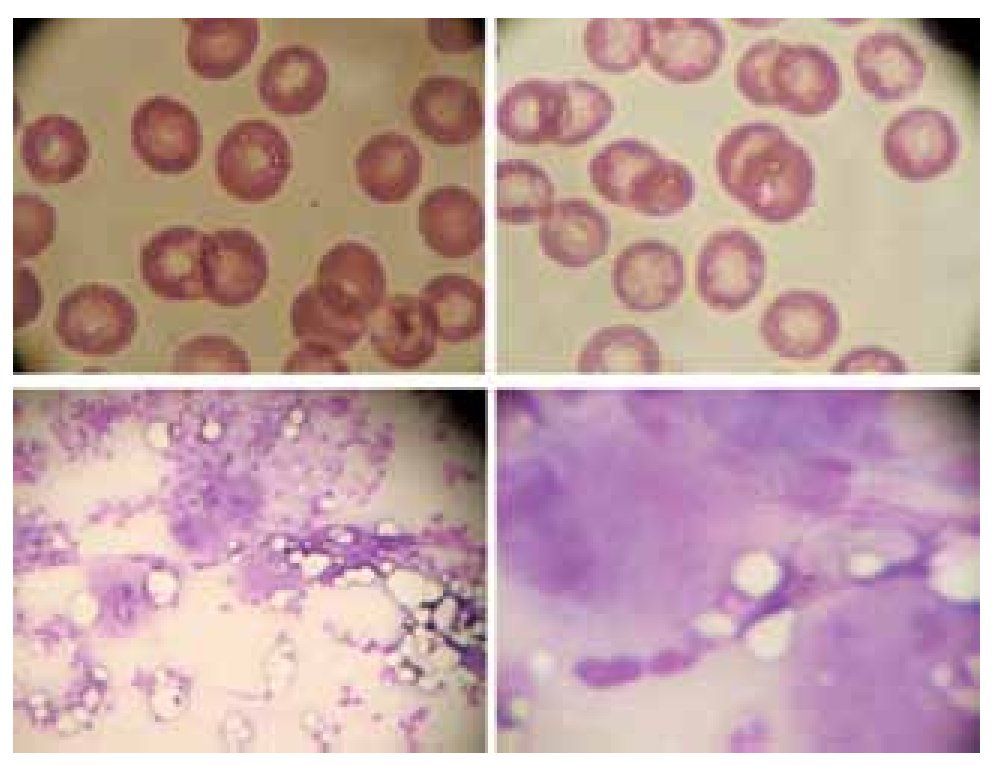
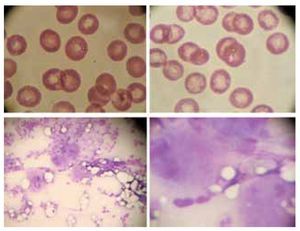
A las 24 horas la cuenta plaquetaria se redujo a 1 x 109/L corroborada en frotis de sangre periférica. Se realizó aspirado de médula ósea que mostró hiperplasia de serie megacariocítica sin satelitismo plaquetario (Figura 4) y se inició tratamiento médico de la trombocitopenia con transfusión de concentrados plaquetarios (indicados por cuenta plaquetaria <2 x 109/L y púrpura mucocutánea atribuida a la trombocitopenia), se obtuvo un control plaquetario posterior a transfusión de 21 x 109/L, corticosteroides sistémicos (metilprednisolona 1 g/día vía intravenosa tres dosis), e inmunoglobulina IV (inmunoglobulina humana normal, octagam® 1 g intravenoso durante cinco días) hasta que se obtuvo cuenta plaquetaria mayor de 10 x 109/L. Los controles a las 72 y 96 horas fueron 19 x 109/L y 58 x 109/L respectivamente.
Figura 4. Las imágenes superiores muestran un frotis de sangre periférica del paciente donde se aprecia la ausencia de plaquetas. Así mismo, las imágenes inferiores del aspirado de medula ósea muestran a la izquierda (10 aumentos) 4 megacariocitos, y en el acercamiento (40 aumentos) se puede apreciar la ausencia de plaquetas en el citosol de las mismas.
El paciente fue dado de alta hospitalaria al sexto día con cuenta plaquetaria de 54 x 109/L y tratamiento con clopidogrel 75 mg/día, enoxaparina subcutánea 40 mg/ día, atorvastatina 80 mg/día, prednisona 50 mg/día.
Un día después de su egreso, tuvo dolor retroesternal intenso súbito y un electrocardiograma realizado a los 30 minutos del inicio que mostró elevación del segmento ST de más de 3 mm anterior extenso. Y la cuenta plaquetaria a su ingreso (séptimo día desde el inicio) fue de 596 x 109/L.
Se realizó coronariografía de emergencia con hallazgo de trombo oclusivo en stent de DA tercio medio con flujo TIMI 0. Se procedió con angioplastía primaria, heparina 5000 U intravenosas y tirofiban en doble bolo e infusión ajustada por peso con permeabilidad del vaso y flujo TIMI 3 sin perfusión. Tuvo elevación enzimática e hipocinesia severa con adelgazamiento de tercio distal del septum anterior en ecocardiograma de control, fue dado de alta a las 72 horas del segundo procedimiento intervencionista con clopidogrel, ácido acetilsalicílico, atorvastatina y metoprolol. Su curso posterior se ha mantenido sin complicaciones a diez meses de seguimiento.
Discusión
Ya desde 1998, berkowitz y colaboradores habían notado que el subgrupo con trombocitopenia por abciximab parecía tener características distintas con respecto a otras causas farmacológicas de esta entidad y que puede ser detectada mediante conteo plaquetario dentro de las primeras 24 horas.3 La determinación realizada de dos a cuatro horas después de iniciada la infusión de abciximab permitiría identificar aquellos pacientes con riesgo para desarrollar trombocitopenia, especialmente las variedades aguda severa y profunda y se propuso un abordaje diagnóstico donde resalta la importancia de: obtener un conteo plaquetario previo a la intervención, una a cuatro horas después de la administración del bolo intravenoso del fármaco y conteos plaquetarios diarios durante la estancia intrahospitalaria y al egreso del paciente. Si la cuenta de plaquetas cae por debajo de 100 x 109/L o menos de 50% de sus valores previos a la infusión, se obliga descartar la posibilidad de pseudotrombocitopenia para lo que se debe obtener un conteo plaquetario en citrato de sodio y otro en heparina, evaluación del frotis para conteo manual y se deben considerar otros agentes causales.
Ya en el año 2000, Llevadot y colaboradores comentaron la observación en estudios clínicos de fenómenos de trombosis arterial y venosa como complicaciones potencialmente devastadoras en la fase de recuperación de la trombocitopenia asociada al uso estos fármacos, pudiendo explicar, en parte, la mayor frecuencia de infarto agudo al miocardio recurrente observado en pacientes con trombocitopenia secundaria a inhibidores de la GP IIb/ IIIa, con clara evidencia de que las cuentas plaquetarias incrementan de manera progresiva y no predecible una vez suspendido el abciximab;10 sin embargo, en este caso se pudo documentar un infarto agudo al miocardio y confirmar claramente un fenómeno de trombocitosis a las 24 horas de su egreso con evidencia angiográfica de trombo oclusivo en stent de DA tercio medio con respuesta a la administración de heparina, tirofiban e intervención percutánea intracoronaria con permeabilidad del vaso tratado sin trombosis ni trombocitopenia recurrentes.
En el caso clínico actual se realizó un abordaje diagnóstico y de tratamiento, con el objetivo de excluir otras causas reconocibles de trombocitopenia aguda profunda y una vez considerada la posibilidad de trombocitopenia severa inducida por fármacos, las cuentas plaquetarias fueron monitorizadas de manera frecuente. Una estrategia consistió en suspender el inhibidor GP IIb/IIIa si la cuenta de plaquetas disminuía de 50 x 109/L. Se indicó la transfusión de plaquetas debido a la manifestación clínica de púrpura mucocutánea y cuenta plaquetaria menor a de 10 x 109/L. No se demostró hemorragia severa ni fue necesario algún procedimiento invasivo de emergencia que son otras indicaciones absolutas para la transfusión de plaquetas.10 Además, se consideró suspender la aspirina y clopidogrel debido al riesgo de hemorragia severa.11 Se administraron corticosteroides sistémicos e inmunoglobulina intravenosa, ya que ambos tratamientos farmacológicos han sido considerados como estándar en el tratamiento de otras trombocitopenias mediadas por mecanismos inmunológicos, por ejemplo la púrpura trombocitopénica idiopática y algunas otras trombocitopenias relacionadas. Aunque la indicación de su uso en pacientes con trombocitopenia severa asociada a inhibidores de la GP IIb/IIIa mediados inmunológicamente son limitados y controvertidos.12 En lo referente al manejo con esteroides e inmunoglobulina intravenosa, los trabajos de Jacob y colaboradores donde fueron aleatorizados en un estudio diseñado a tres brazos terapéuticos 43 pacientes con trombocitopenia sintomática de origen indeterminado de acuerdo al siguiente régimen: a) prednisona oral (1 mg/kg/día); b) gamma-globulina intravenosa (IVIG) 400 mg/kg/día por cinco días; c) los dos regímenes (prednisona oral y gamma-globulina intravenosa), se concluyó que: los pacientes con un esquema combinado (prednisona e IGIV) mostraron respuesta completa significativamente mayor que aquellos que recibieron IVIG sola; los que recibieron prednisona sola mostraron respuesta más favorable que aquellos que recibieron IVIG sola.13 Dicho sustrato teórico sustentó la decisión de utilizar el esteroide sistémico e IVIG en el presente caso clínico con un incremento sostenido en los valores medidos de plaquetas y corroborados mediante visualización en frotis de sangre periférica
En un análisis que incluyó ensayos clínicos prospectivos, aleatorizados y controlados con placebo hasta el año 2000, Dasgupta y colaboradores evidenciaron que el uso intravenoso de abciximab previa a angioplastia, incrementó la incidencia de trombocitopenia leve (cuentas plaquetarias de 50 a 90 x 109/L o 100 x109/L) comparado contra placebo (4.2% vs. 2%; p <0.001, razón de momios 2.13); y en los pacientes que recibieron abciximab más heparina, tuvieron el doble de frecuencia de trombocitopenia severa (cuentas plaquetarias 20 a 50 x 109/L) cuando se compararon con aquellos que habían recibido únicamente heparina (1% vs. 0.4%; p <0.01; razón de momios 2.48).14 Además en dicho análisis se demostró que eptifibatida y tirofiban no incrementaron significativamente el riesgo de trombocitopenia severa cuando se compararon contra placebo y heparina, con una clara una asociación de riesgo. La trombocitopenia aguda profunda (cuentas <20 x 109/L) ocurrió en 0.1% a 0.5% de los pacientes tratados con agentes inhibidores de la glucoproteína IIb/IIIa y su incidencia parece ser ligeramente mayor con abciximab cuando se administró en bolo e infusión.
Como señalan Merilini y colaboradores, a partir del análisis de estudios en pacientes que recibieron tratamiento intravenoso con inhibidores de la glucoproteína IIb/IIIa, se sugirió que el uso de abciximab conlleva más del doble de riesgo para la incidencia de trombocitopenia severa cuando se compara contra tirofiban y al asociarse con heparina. Y lo destacable es que dicha trombocitopenia se encuentra asociada con resultados desfavorables como son: el incremento en la frecuencia de hemorragias, isquemia recurrente, necesidad de revascularización urgente y muerte.15
Conclusión
El mecanismo que causa la trombocitopenia no está por completo caracterizado. Puede ocurrir un reducción acelerada en la cuenta de plaquetas después de la administración de abciximab dentro de una a dos horas de la exposición inicial, o puede haber un declive significativo en el transcurso de días posterior al inicio de la terapia. La readministración del anticuerpo monoclonal, pero no de otras moléculas inhibidoras pequeñas (eptifibatida o tirofiban) se asocia a riesgo significativo de trombocitopenia recurrente.16 En correlación con la literatura mundial, en los pacientes llevados a la sala de hemodinámica y sometidos a intervención coronaria percutánea se sugiere observar la posibilidad de que los inhibidores de la GP IIb/IIIa con o sin asociación a heparinoides produzcan una depleción importante de las cifras plaquetarias, realizar un abordaje estructurado para excluir otras causas reconocidas además de un tratamiento intensivo mediante la suspensión el fármaco, el uso de concentrados plaquetarios el monitoreo hematológico estrecho y considerar el empleo de esteroides sistémicos e IGIv en pacientes refractarios con comportamiento atípico.
La identificación temprana de esta complicación es fundamental en la prevención de la hemorragia mayor con la necesidad implícita de interrumpir el tratamiento anti-plaquetario y el consecuente riesgo de eventos adversos cardiovasculares mayores.
Correspondencia: Enrique Frutos Rangel.
Tarascos 3435. Fracc. Monraz. Guadalajara, Jalisco. 44670.
Teléfono: (33) 38130042, ext: 2621.
Correo electrónico: enrifrut@megared.net.mx
Recibido el 18 de febrero de 2009;
aceptado el 18 de agosto de 2011.