Introducción
La hipertensión arterial (HTA) es un importante factor de riesgo cardiovascular (FRCV) y un poderoso indicador de riesgo para la supervivencia. El impacto de la HTA sobre la salud de la población mundial es elevado, ya que causa un 5,8% de las muertes totales y supone la tercera causa de fallecimiento no esperado tras la malnutrición y el hábito tabáquico. En España la HTA está relacionada con una de cada 4 muertes totales y una de cada 2,5 muertes cardiovasculares1.
Uno de los factores determinantes de dicho impacto es el mal control de la presión arterial (PA), que aproximadamente ocurre en 3 de cada 4 hipertensos2-4. Una reducción insuficiente de la PA en los hipertensos tratados puede ser un factor importante para el exceso de morbimortalidad cardiovascular observada5. Esto hace necesario modificar la actitud conservadora actual del profesional sanitario a la hora de utilizar pautas terapéuticas que mejoren el control de la PA. Las directrices del Joint National Committee (JNC-VI)6 y de la World Health Organization/International Society of Hypertension (WHO/ISH)7 destacan la necesidad de mejorar el grado de control de la PA, implementando actitudes terapéuticas que contemplan las combinaciones de fármacos para incrementar al máximo la eficacia hipotensora.
Este estudio se diseñó sobre la base de que en nuestro país el grado de control de la HTA es bajo y que en atención primaria (AP) es donde se tratan la mayoría de los hipertensos2,4,8. El objetivo principal fue evaluar la efectividad de la combinación lisinopril-hidroclorotiazida (LH) a dosis fijas en el control de la PA de los pacientes hipertensos tratados con monoterapia y mal controlados en las condiciones reales de uso en la práctica clínica. Además, se planteó como objetivo secundario evaluar el efecto de LH sobre los diferentes FRCV.
Material y métodos
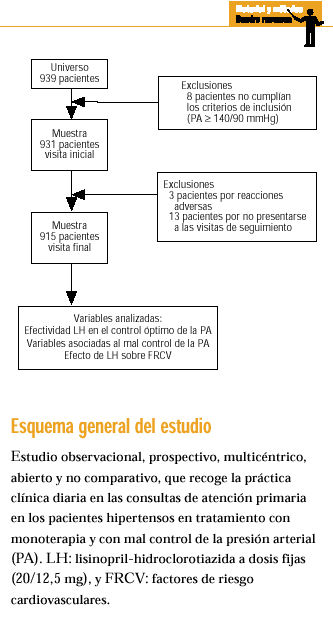
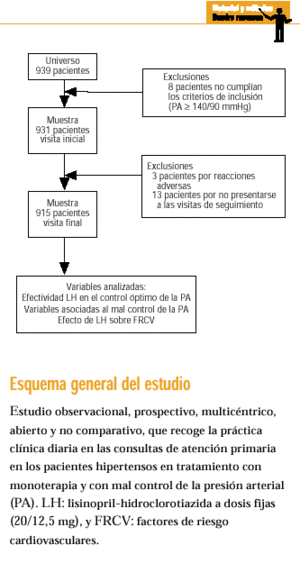
Se diseñó un estudio observacional, naturalista, prospectivo, multicéntrico, abierto y no comparativo. Participaron 199 médicos de AP de las 17 comunidades autónomas españolas y el trabajo de campo se realizó entre noviembre de 1998 y noviembre de 1999. El período de inclusión fue de 6 meses y el tiempo de observancia y seguimiento de los pacientes de otros 6 meses.
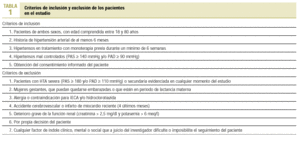
Una vez que el investigador había decidido iniciar tratamiento con dosis fijas diaria de LH (20/12,5 mg) y el paciente cumplía todos los criterios de inclusión y ninguno de exclusión, se le pedía el consentimiento informado y, tras su obtención, se incluía en el estudio (tabla 1).
Se seleccionaron por muestreo consecutivo a medida que acudían a la consulta 931 pacientes hipertensos, 403 varones (43,3%) y 528 mujeres (56,7%) con una edad media de 62,0 ± 10,3 años. Completaron las visitas programadas 915 pacientes (98%) que fueron incluidos en el análisis.
Los pacientes fueron seguidos a lo largo de 6 meses, con una visita inicial de inclusión y 3 de seguimiento, a los meses 1, 3 y 6. Los investigadores cumplimentaron un cuaderno de recogida de datos para cada paciente por entrevista directa, donde se registraron las siguientes variables: edad, sexo, peso, talla, índice de masa corporal (IMC), antecedentes familiares de enfermedad cardiovascular, enfermedades concomitantes, año de diagnóstico de la HTA, tipo de tratamiento antihipertensivo previo, frecuencia cardíaca (FC), PAS y PAD, presión del pulso (PP) y una determinación analítica básica (fórmula, función renal e iones, función hepática, perfil lipídico y glucémico).
Las medidas de la PA las realizaron en los centros de salud médicos y/o enfermeras, utilizando esfigmomanómetros de mercurio y manguitos de tamaño adecuado a la circunferencia del brazo (recomendaciones de la OMS-SIH)7. En todas las visitas se realizaron 2 determinaciones de la PA, en condiciones estandarizadas, tras las cuales se clasificó la PA en estadio 1, 2 o hipertensión sistólica aislada (HSA), siguiendo las recomendaciones del JNC-VI. El diagnóstico de mal control se realizó cuando la media de 2 tomas de PA fue >= 140 mmHg de PAS y/o 90 mmHg de PAD. En los diabéticos se consideró un control adecuado de la PA, cuando la PAS < 130 mmHg y la PAD < 85 mmHg. Se calculó la PP como la diferencia entre la PAS y la PAD. Se consideró a un paciente con hipercolesteremia cuando el colesterol plasmático fue > 200 mg/dl, en presencia de concentración de triglicéridos < 200 mg/dl y obesidad cuando el índice de masa corporal (IMC) era >= 30 kg/m2.
El cálculo del tamaño muestral se realizó estimando un porcentaje de control del 50% en el total de la muestra del estudio, con una precisión de ± 3% para un intervalo de confianza (IC) del 95%. Esto supuso un tamaño muestral de 1.068 pacientes. Se realizó estadística descriptiva mediante el cálculo de medias con su desviación estándar (DE) para las variables continuas y de proporciones para las variables categóricas. Se comparó las medidas iniciales con las finales mediante la t de Student para muestras apareadas en las variables continuas con distribución normal, y con el test de Wilcoxon no paramétrico en las variables no distribuidas normalmente. En el caso de variables categóricas dicotómicas, se utilizó el test de McNemar en muestras apareadas y la ji-cuadrado en el resto de casos. La asociación lineal entre variables cuantitativas continuas se evaluó mediante modelos de regresión lineal. Se estableció un nivel de confianza del 95%.
Resultados
Participaron 199 médicos de AP que finalmente incluyeron 931 pacientes, 403 varones (43,3%) y 528 mujeres (56,7%), de los que 915 (98%) completaron las visitas programadas y fueron incluidos en el análisis. La edad media fue de 62,0 ± 10,3 años y la antigüedad de la HTA de 7,8 ± 6,0 años. El IMC fue de 28,5 ± 4,3 kg/m2. Un 26,8% presentaba HTA en estadio 1 y el 73,2% en estadio 2; un 10,6% tenía HSA. En el tratamiento antihipertensivo previo, los IECA fueron los fármacos más utilizados (43,4%), seguidos de diuréticos (29,0%), antagonistas del calcio (22,8%), bloqueadores beta (3,1%), ARA II (1,0%) y bloqueadores alfa (0,6%). Un 25,4% de los pacientes hipertensos no tenía otros FRCV asociados, el 45,7% tenía uno y el 28,9% más de uno (hipercolesteremia, 30,7%; tabaquismo, 22,7%, y diabetes, 17,7%).
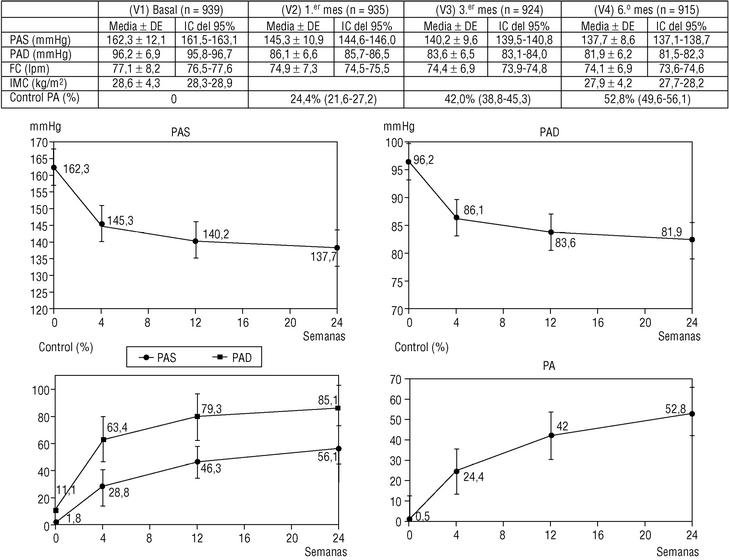
Durante el seguimiento hubo un descenso de la PAS (24,6 ± 3,5 mmHg) y de la PAD (14,3 ± 0,7 mmHg) (p < 0,001). En el análisis multivariado la reducción de la PAS se relacionó con la edad de los pacientes (b = 0,483; p = 0,005) y con el descenso del colesterol total (b = 0,195; p = 0,007), mientras el descenso de la PAD no se relacionó con ninguna de las variables evaluadas.
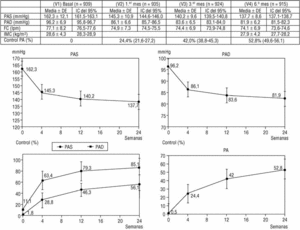
El porcentaje de control de la PA aumentó hasta el 52,8% (p < 0,001) en la última visita (fig. 1). En el análisis de regresión logística multivariado, la edad fue la única variable asociada con el control de la PA (para una diferencia de edad de 10 años, odds ratio [OR], 0,81; IC del 95%, 0,71-0,92%; p = 0,001). Las cifras promedio de los pacientes no controlados al final del seguimiento fueron de 144,3 ± 6,4 mmHg para la PAS y de 84,5 ± 6,3 mmHg para la PAD.
Figura 1. Imagen superior: valores de PAS, PAD, FC, IMC y control global de la PA en las 4 visitas de seguimiento del estudio (medias ± desviación estándar e intervalos de confianza del 95%). Imagen inferior: evolución de los valores medios de PAS, PAD y porcentaje de control de PAS y PAD y control global de PA (PAS < 140 mmHg y PAD < 90 mmHg), a lo largo de las 24 semanas de seguimiento del estudio.
La PP basal fue de 66,1 ± 12,1 mmHg y la final de 55,7 ± 8,3 mmHg. Hubo una reducción en la PP de 10,4 ± 4,3 mmHg (p < 0,001). Inicialmente presentaron mayor PP los sujetos hipertensos de más edad (r = 0,2092; p < 0,001), los que tenían una PAS más alta (r = 0,8408; p < 0,001) y aquellos con valores menores de PAD (r = 0,3481; p < 0,001); no así los diabéticos, ni los dislipémicos. No hubo diferencias entre sexos. El descenso de la PP se relacionó en un modelo de regresión lineal multivariante con la edad (b = 0,441; p = 0,0034), la antigüedad de la HTA
(b = 0,433; p = 0,048) y con el descenso del colesterol total (b = 0,135; p = 0,010).
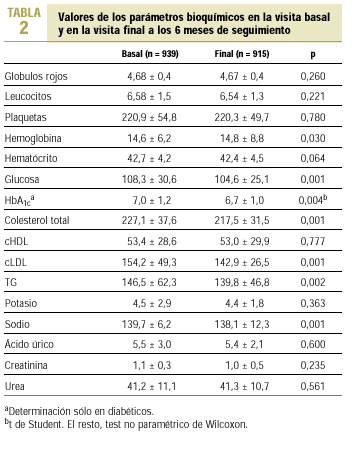
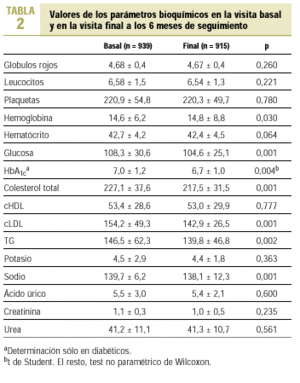
Respecto a los parámetros bioquímicos, a las 24 semanas de tratamiento hubo una disminución del colesterol total (p < 0,001), del cLDL (p < 0,001), de los triglicéridos (p = 0,002), de la glucosa (p < 0,001) y del sodio (p < 0,001), que fueron independientes de la reducción de la PA (excepto el colesterol total, que se relacionó con la PAS tal como se ha comentado previamente). El resto de parámetros no experimentó cambios significativos (tabla 2).
En el subgrupo de diabéticos, 118 mujeres (71,1%) y 48 varones (28,9%), con una edad media de 64,7 ± 9,8 años, hubo una reducción en la PAS de 22,9 ± 3,2 mmHg y en la PAD de 12,6 ± 2,1 mmHg (p < 0,001). El grado de control de la PA aumentó hasta el 9,0% (p < 0,001), y fue mayor el control de la PAD (64,6%) que el de la PAS (9,5%). Hubo una mejoría del perfil glucémico: la glucosa descendió desde 157,1 ± 40,7 a 139,7 ± 31,9 mg/dl (p = 0,001) y la HbA1c de 7,0 ± 1,24 a 6,7 ± 1,0 mg/dl (p = 0,004), y del lipídico: CT de 228,6 ± 36,5 a 217,3 ± 30,8 mg/dl
(p = 0,000) y cLDL de 155,3 ± 32,5 a 145,0 ± 25,5 mg/dl (p = 0,002). La reducción de la PAS y la PAD se relacionó con el descenso de la HbA1c en el grupo de diabéticos con la PA controlada (r = 0,885; p = 0,01, y r = 0,809; p = 0,005, respectivamente).
Se registraron y notificaron sólo 6 casos (0,6%) de efectos adversos (tos, mareo, intolerancia gástrica, insuficiencia renal, dislipemia y cefalea). De estos 6 casos, la tos y la insuficiencia renal tuvieron una relación probable con el fármaco y en el resto de los casos fue dudosa. Sólo la intolerancia gástrica tuvo una intensidad alta. En estos 3 casos el investigador modificó el tratamiento, por lo que fueron retirados del estudio.
Discusión
Este estudio se realizó en una cohorte de hipertensos en tratamiento con monoterapia y sin control adecuado de sus cifras de PA, que acudieron a las consultas de los centros de AP.
La principal limitación del estudio radica en la falta de grupo control, si bien los estudios naturalísticos como éste, con criterios de inclusión y exclusión poco limitantes, reflejan con objetividad los resultados de la práctica clínica diaria, al incluir pacientes representativos de las consultas de AP y no modificar la actuación clínica. En ocasiones, los resultados de los ensayos clínicos, debido a los criterios tan restrictivos de inclusión de pacientes, son difíciles de extrapolar al ámbito de la AP.
Los pacientes incluidos estaban en tratamiento con monoterapia antihertensiva previa durante un período mínimo de 6 semanas, tiempo considerado como aceptable para decidir el cambio de estrategia terapéutica4-7. La mayoría se trataba con IECA, seguidos de diuréticos y antagonistas del calcio, aspecto ya constatado en el ámbito de la AP9.
En consonancia con las recomendaciones más actuales, la mejor actitud a adoptar en los hipertensos en los que el fármaco inicial no es capaz de controlar la PA es la asociación de 2 fármacos hipotensores a dosis bajas con acción sinérgica entre ellos4-7. Estas asociaciones farmacológicas a dosis fijas son una alternativa en este tipo de hipertensos, debido a su mayor eficacia con menos efectos secundarios, por mejorar el cumplimiento terapéutico y por ser más eficientes que el incremento de dosis o la monoterapia secuencial10,11. En nuestro estudio la combinación de LH a dosis fijas controló la PA de un 52,8% de los hipertensos no controlados con monoterapia. Hay otras combinaciones a dosis fijas de antagonistas del calcio y bloqueadores beta o IECA, que incluso controlan la PA en un mayor porcentaje de pacientes, pero que por su mayor complejidad son más utilizados en el entorno hospitalario (unidades de hipertensión y/o consultas de cardiología, etc.) que en las consultas de AP12,13.
Casi el 75% de los hipertensos incluido en el estudio puede considerarse hipertenso de alto riesgo, ya que tenían asociados uno o más FRCV, además de la edad media superior a 60 años, por lo que podemos considerar que el tratamiento con LH proporcionó un grado de control satisfactorio de la PA (52,8%) en esta cohorte de pacientes. Al igual que en poblaciones similares14, sólo la edad se relacionó con el mal control de la PA; a mayor edad peor control de la PA. Aunque hay evidencia de que la coexistencia de otros FRCV limita la respuesta antihipertensiva e impide el adecuado control de la PA15,16, en nuestro estudio la coexistencia de uno o más FRCV no influyó en el control tensional. Esto posiblemente esté en relación con una menor influencia de los FRCV en este grupo de hipertensos con mayor resistencia al control de su PA, ya que no se había conseguido dicho control con el tratamiento previo en monoterapia. Como en estudios previos realizados en poblaciones similares9,11, encontramos una mejoría en los parámetros del perfil glucémico y del lipídico, aunque su significado clínico no sea de gran relevancia.
En el subgrupo de diabéticos, el control de la PA fue sólo del 9,0%, aunque mayor que el citado por otros estudios2. El tratamiento con la combinación LH disminuyó significativamente las cifras de PAS y de PAD (p < 0,001). En diabéticos hipertensos se ha demostrado más efectivo el tratamiento combinado con 2 fármacos que continuar con monoterapia, ya sea incrementando la dosis o cambiando a otros fármacos11. Además, la PAS fue de más difícil control que la PAD. En nuestro estudio el porcentaje de control de la PAD fue del 64,6%, mientras que el de la PAS fue sólo del 9,5%. El descenso de la PAS y la PAD se relacionó con la reducción de la HbA1c en el grupo de pacientes con PA controlada, y no así en el grupo de los diabéticos no controlados. El perfil lipídico y glucémico mejoraron significativamente, posiblemente en relación con los beneficios que producen los IECA en los pacientes diabéticos más allá de la simple reducción de la PA17-19.
Otro aspecto a analizar es el impacto de la combinación LH sobre la PP. En la actualidad no se ha definido la PP normal, aunque diferentes estudios poblacionales han puesto de manifiesto que una PP mayor de 65 mmHg se asocia con una mayor morbimortalidad cardiovascular20,21. En la visita basal tenían una PP de alto riesgo el 49% de los pacientes, que tras 6 meses de tratamiento con LH disminuyó significativamente hasta los 55,7 ± 8,3 mmHg. El descenso medio de 10,4 ± 4,3 mmHg, estuvo en línea con otros trabajos que también utilizaron fármacos en combinación fija22. Como en otros estudios23, el descenso de la PP se correlacionó negativamente con la edad (a mayor edad menor descenso), lo que traduce el aumento paralelo de la PAS que se produce con el envejecimiento por los cambios estructurales de la pared vascular. A diferencia de otras series, no encontramos relación con sexo, diabetes y obesidad, aunque sí con descenso del colesterol total24,25. No hay estudios que analicen la influencia de los diferentes antihipertensivos sobre la PP, aunque la mayoría desciende la PP debido a la disminución de las resistencias periféricas y secundariamente la rigidez arterial. Sin embargo, el amplio descenso de la PP que se ha producido en nuestro estudio, además, puede verse incrementado por el efecto protector sobre la función endotelial y los cambios estructurales vasculares que producen los fármacos que actúan bloqueando el sistema renina-angiotensina26,27.
Uno de los objetivos del tratamiento con combinaciones a dosis fijas es minimizar la incidencia de efectos adversos al administrar menor dosis de cada fármaco. En nuestro estudio la incidencia de efectos adversos fue muy baja (0,6%) en comparación a los datos publicados de los ensayos clínicos con LH28 y asociaciones similares29. Esto se debe en gran medida a la limitación que supone el tipo de diseño del estudio y también al bajo grado de notificación de reacciones adversas espontáneas que se producen en nuestro país en el ámbito de AP30,31.
En conclusión, los resultados de nuestro estudio indican que en el ámbito de la AP la combinación a dosis fijas de lisinopril + hidroclorotiazida controla un 52,8% de los pacientes hipertensos previamente tratados con monoterapia y con mal control de su PA. Además de su importante efecto antihipertensivo, reduce significativamente la PP y produce un impacto favorable sobre los diferentes FRCV, mejorando el perfil lipídico y el glucémico.
Agradecimientos
Queremos agradecer a todos los médicos de AP que participaron en el estudio por su inestimable colaboración al proporcionar los datos necesarios para su realización. AstraZéneca Farmacéutica Spain, S.A., proporcionó la infraestructura necesaria para llevar a cabo el estudio.
Correspondencia: Onofre Vegazo García. C/ Serrano Galvache, 56. Parque Norte. Edificio Roble. 28033 Madrid. España. Correo electrónico: onofre.vegazo@astrazeneca.com
Manuscrito recibido el 20 de febrero de 2002.
Manuscrito aceptado para su publicación el 17 de julio de 2002.