Introducción
En los últimos 20 años se ha observado un importante crecimiento del interés en la evaluación de la calidad de vida relacionada con la salud (CVRS)1-4, coincidiendo sus inicios con la proposición de la Organización Mundial de la Salud (OMS) de un nuevo concepto de salud, desde una perspectiva integral y multidimensional5. La medida de la calidad de vida se ajusta perfectamente a esta nueva visión de la salud, por lo que se ha considerado un indicador válido del resultado terapéutico, lo que ha contribuido a un incremento de los instrumentos elaborados para su valoración.
La medición de la CVRS se lleva a cabo mediante instrumentos denominados cuestionarios, que han sido clasificados en: a) genéricos, aquellos que son aplicables a todo tipo de enfermedades y pacientes y b) específicos, cuando están diseñados y adaptados para un determinado tipo de enfermedad y paciente.
El uso de instrumentos genéricos de evaluación de la CVRS es útil, pero hay una tendencia al desarrollo de medidas específicas para cada enfermedad o trastorno, pues éstas posibilitan una información más precisa de la situación del sujeto en relación con su enfermedad, son más sensibles a cambios clínicamente significativos y contribuyen, cuando es necesario, a la toma de decisiones médicas frente a cambios en el tratamiento.
En el ámbito de la infección por el virus de la inmunodeficiencia humana (VIH) la importancia de la evaluación de la CVRS está ampliamente reconocida y se ha desarrollado un gran número de instrumentos específicos con este fin, como por ejemplo, MOS-HIV, MQOL-HIV, HIV-PARSE, HIV-QOL, HOPES, EORTC QLQ-C30-HIV, FAHI, AIDS-HAQ, MQOL-McGill Quality of Life, HAT-QOL, HIV-QL31. (Para una revisión detallada de estas escalas véase Badia et al3.) Se dispone de la versión en español de los cuestionarios FAHI3, HOPES6, MOS-HIV7-9 y MQOL-HIV7-9; no obstante, sólo los dos últimos están validados para su uso en España.
Entre los cuestionarios de CVRS que se han empleado para la evaluación de la calidad de vida en personas VIH+ se destaca la adaptación del Medical Outcomes Study Survey-Short Form 30 Items (MOS-SF-30), debido a sus buenos indicadores psicométricos1,10,11. Además, a partir de la versión de 30 ítems, han aparecido versiones posteriores hasta llegar a la versión de 35 ítems, que fue denominada MOS-HIV7-9. El objetivo de Wu et al1, autores del MOS-SF-30, fue desarrollar una medida del estado de salud corta, pero exhaustiva, con la que se pudieran valorar los aspectos del estado funcional y el bienestar en personas con infección por el VIH; para ello partían de la premisa de que para que un instrumento fuese factible para estudios clínicos y multicéntricos, éste debía ser breve y autoadministrado; sensible a aspectos clínicos importantes, como síntomas, cambios en el estado clínico, deterioro cognitivo y estados de fatiga, y con capacidad de medir de forma específica las distintas dimensiones de la salud.
En este marco, el objetivo del presente trabajo es estudiar las propiedades psicométricas para la muestra española de una versión de 30 ítems del cuestionario de calidad de vida relacionada con la salud MOS-SF-30. De forma más concreta este estudio pretende, en primer lugar, verificar la consistencia interna de cada subescala y para el total de los ítems. En segundo lugar, trata de contrastar la validez concurrente a través de las relaciones que la escala mantiene con distintas mediciones clínicas e inmunológicas (estadio de la clasificación de los Centers for Disease Control and Prevention --CDC--, carga viral y linfocitos T CD4). Por último, quiere verificar la capacidad de la escala para diferenciar a los sujetos, por una parte, según el estadio de la infección por el VIH en que se encuentren y, por otra, de acuerdo con los valores de carga viral detectable o indetectable.
Material y métodos
Se ha evaluado a 100 sujetos VIH+, entre 3 meses y 14,8 años de infección por el VIH, de ambos sexos, procedentes del servicio de medicina interna-unidad VIH de un hospital universitario urbano. El criterio de inclusión en la muestra fue ser mayor de 18 años de edad y VIH+. Los criterios de exclusión fueron: consumo de drogas en los últimos 6 meses y no aceptación del consentimiento informado.
Medidas e instrumentos
Datos sociodemográficos y clínicos. Mediante un cuestionario autoaplicado, se recogió información sobre la edad, el sexo, la orientación sexual, la situación laboral, el nivel de estudios y el modo de transmisión del VIH. Del historial médico se extrajo el perfil clínico e inmunológico, incluyendo el estadio de la clasificación de los CDC, la carga viral, los linfocitos T CD4 y el tiempo de infección por el VIH en meses.
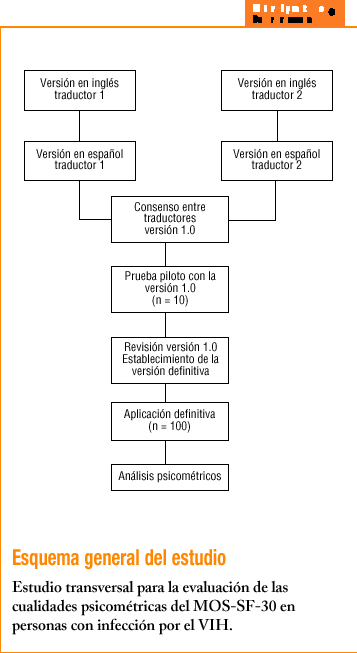
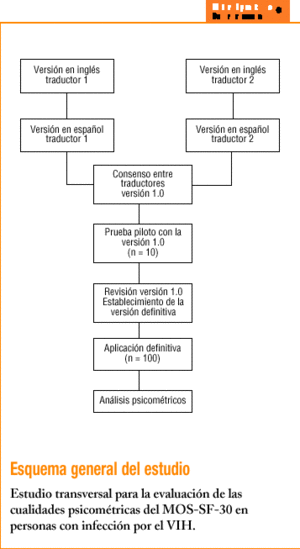
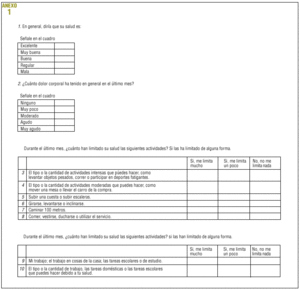
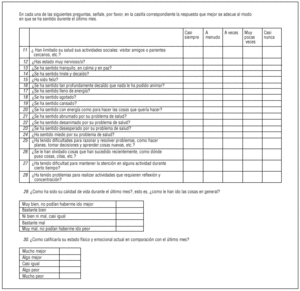
Calidad de vida relacionada con la salud. La CVRS se ha evaluado a través de la versión en español del MOS-SF-30 de Wu et al1, traducida por Remor12. El proceso de traducción incluyó: a) la traducción independiente por dos traductores bilingües inglés-español; b) la comparación y el consenso de las dos versiones en una única versión; c) la prueba piloto con 10 sujetos VIH+ para testar la comprensión de la versión en español (la prueba piloto no se incluyó en el análisis psicométrico), y d) la revisión de la versión traducida y consensuada considerando las modificaciones sugeridas durante la prueba piloto. La versión final en español (anexo en Internet) tiene una presentación ligeramente distinta de la que se expone en el anexo del artículo original de Wu et al1. Para la formulación de la presentación se consideró la opinión de los sujetos encuestados en la prueba piloto. El MOS-SF-30 consiste en 22 ítems con escala ordinal de 5 puntos (0 a 4) y ocho con 3 puntos (0 a 2). Los ítems se subdividen en 11 subescalas que miden salud general percibida, dolor, funcionamiento físico, funcionamiento social, salud mental, energía/fatiga, actividad diaria, malestar respecto a la salud, funcionamiento cognitivo, calidad de vida percibida y transición de salud. La obtención de la puntuación se ha simplificado en detrimento de la propuesta por Wu et al1. Los ítems son sumados, previa inversión de los ítems 13, 15, 17 y 20, y se obtiene una puntuación directa de CVRS global, que varía en un rango de puntuación de 0 a 100, en el que el 0 indica el grado más bajo de calidad de vida y 100, el más alto. De la misma forma, la interpretación de cada subescala se obtiene a través de puntuación directa, indicando una mayor puntuación para una calidad de vida más elevada en cada subescala (excepto para las subescalas de dolor y malestar respecto a la salud, donde mayor puntuación indica menores dolor y malestar).
Procedimento
La evaluación se llevó a cabo entre febrero y abril de 1999. Se seleccionó a 4 pacientes consecutivos por día, tomando como base los criterios de inclusión y exclusión. Este procedimiento se mantuvo hasta completar el total de la muestra. A todos los pacientes se les explicó de una forma breve el objetivo del estudio. La incorporación fue voluntaria, tras firmar un consentimiento informado en el que se aceptaban las condiciones. Los procedimientos seguidos en este trabajo se han publicado con detalle en otro artículo13.
Plan de análisis
Inicialmente se ha llevado a cabo un análisis descriptivo de la muestra a través del análisis de frecuencias, medias y porcentajes con respecto a las variables sociodemográficas, clínicas, inmunológicas y de la CVRS. Para evaluar la fiabilidad de la escala, se ha desarrollado el análisis de consistencia interna (alfa de Cronbach) para cada subescala y para el conjunto de 30 ítems de la versión en español del MOS-SF-30. A continuación, para examinar la validez concurrente, se ha analizado la correlación (Pearson), incluyendo las variables clínicas e inmunológicas y las dimensiones de la CVRS. Finalmente, para examinar la capacidad discriminatoria del cuestionario, se ha realizado el análisis de varianza (ANOVA) de un factor, atendiendo a la clasificación de los CDC (asintomáticos, sintomáticos y sida) e incluyendo, por una parte, las dimensiones que conformaban la evaluación de la calidad de vida relacionada con la salud y, por otra, la puntuación global de la escala. En la misma línea del análisis anterior se compararon los valores de calidad de vida entre sujetos con carga viral indetectable (< 400 copias/µl), controlada (401-30.000 copias/µl) y no controlada (> 30.000 copias/µl), siguiendo el criterio de Phair y Murphy14.
Resultados
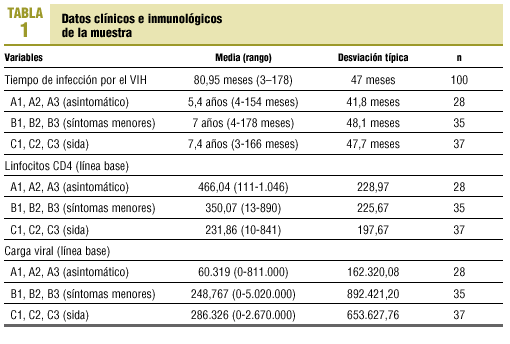
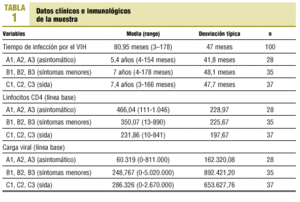
La muestra del estudio está formada por un total de 100 sujetos, con edades comprendidas entre 24 y 69 años con una media ± desviación típica (DT) de 37,3 ± 8,3 años; 59 de ellos eran varones y 41, mujeres. El 50% tenía estudios primarios; el 17%, secundarios, y el 31%, universitarios. El 63%, trabajaba. El modo de infección por el VIH fue mayoritariamente por vía sexual (56%), seguido del uso de drogas lor vía parenteral (29%). La orientación sexual declarada mayoritariamente fue la heterosexual (75%). Las características clínicas e inmunológicas de los sujetos incluidos en la muestra se exponen en la tabla 1.
En relación con el tratamiento anti-VIH, el 91% de los sujetos de la muestra estaba en tratamiento antirretroviral de gran actividad (conocido como TARGA, generalmente combinación de tres o más fármacos inhibidores de la proteasa y de la transcriptasa inversa análogos de los nucleósidos); el 1%, con monoterapia y el 8% se encontraba sin tratamiento en la fecha de la evaluación.
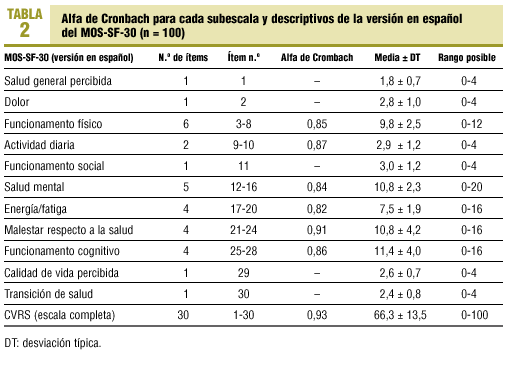
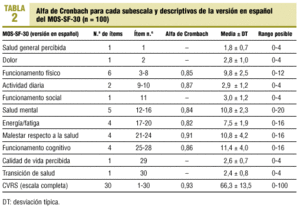
Los datos descriptivos (media, DT y rango posible) para cada subscala del MOS-SF-30 y para la calidad de vida relacionada con la salud global se presentan en la tabla 2.
Validez de contenido del cuestionario original
El cuestionario de calidad de vida relacionada con la salud MOS-SF-30 ha sido publicado por Wu et al1 a partir de un conjunto de ítems desarrollado por el Medical Outcomes Study (MOS)15, y contenidos recogidos a partir de la revisión de la bibliografía, entrevistas y discusión con expertos en el ámbito del sida, y entrevistas con pacientes infectados por el VIH. La versión final de 30 ítems ha sido resultado de sucesivos análisis psicométricos llevados a cabo por los autores de la versión original del cuestionario.
Consistencia interna
La consistencia interna (alfa de Cronbach) de la escala completa y el estadístico para cada subescala con más de un ítem se presenta en la tabla 2.
Validez concurrente
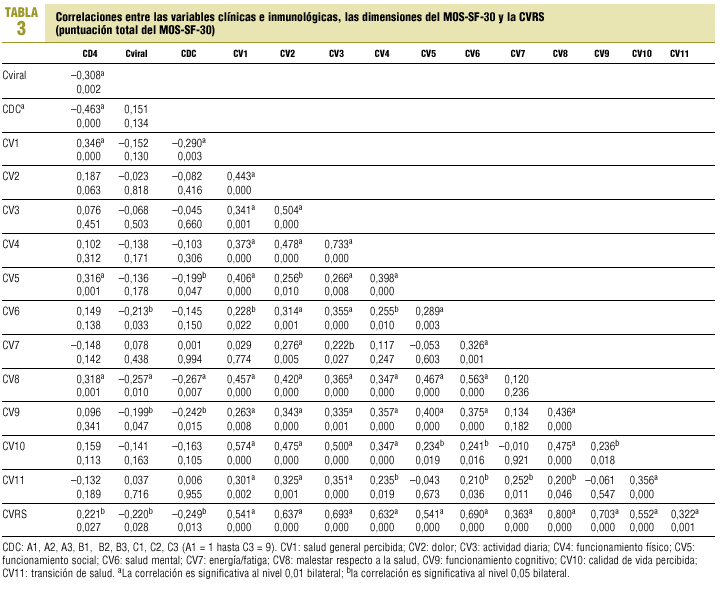
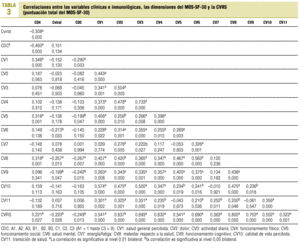
Asociaciones entre las distintas dimensiones MOS-SF-30 y las medidas clínicas e inmunológicas. Para verificar las asociaciones entre las distintas subescalas, la CVRS (puntuación total) y las variables clínicas e inmunológicas se llevó a cabo un análisis de correlación de Pearson (tabla 3).
Capacidad discriminatoria entre los estadios de la enfermedad (estadios de la clasificación de los CDC)
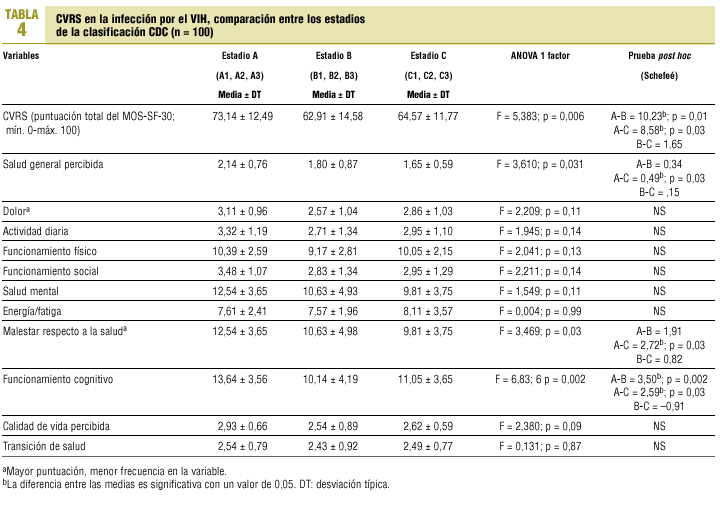
Para verificar la capacidad de discriminación del cuestionario MOS-SF-30 entre los distintos estadios de la enfermedad, se efectuó un ANOVA de un factor (estadios de la clasificación de los CDC), y pruebas post hoc mediante el contraste de Scheffeé para distinguir entre qué estadios se producen específicamente las diferencias.
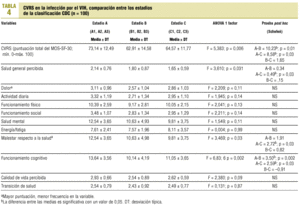
Los datos relativos a la CVRS de los sujetos incluidos en este estudio, considerando las distintas dimensiones evaluadas para lograr la CVRS, se presentan en la tabla 4, donde se exponen en detalle los estadísticos referentes a las comparaciones entre los estadios de la clasificación de los CDC en este aspecto.
La CVRS (sumatorio de todas las dimensiones) presentó diferencias entre los estadios de la clasificación de los CDC; los pacientes que se encontraban en el estadio A (asintomáticos) han sido los que mayor calidad de vida han evidenciado (tabla 4). Las dimensiones de la CVRS que han presentado diferencias en cuanto a los estadios de la clasificación de los CDC en que se encontraban los sujetos fueron: la salud general percibida (mayor salud percibida para las pacientes asintomáticos), malestar respecto a la salud (mayor malestar para los pacientes asintomáticos) y el funcionamiento cognitivo (mejor funcionamento cognitivo para los pacientes asintomáticos). Los estadísticos se presentan en detalle en la tabla 4.
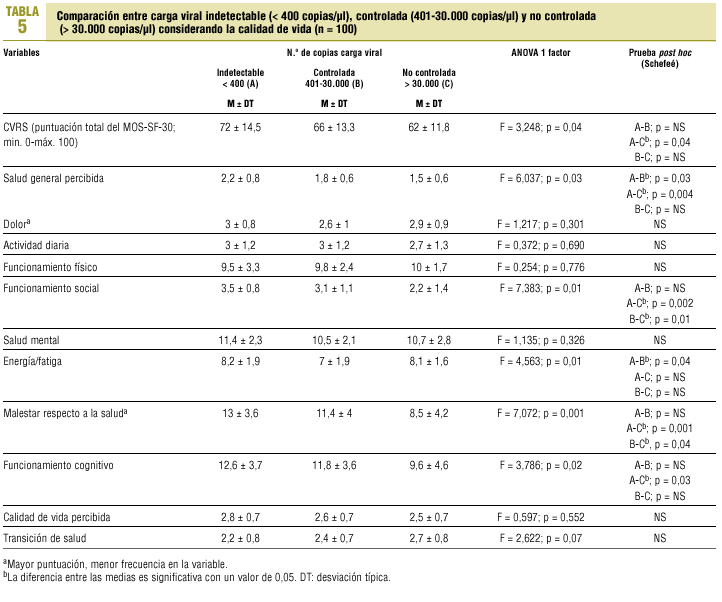
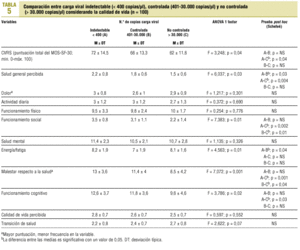
Capacidad discriminatoria entre carga viral indetectable, detectable controlada y no controlada
Para verificar la capacidad discriminante del cuestionario MOS-SF-30 entre los sujetos con una carga viral indetectable (< 400 copias/µl), controlada (401-30.000 copias/µl) y no controlada (> 30.000 copias/µl) se llevó a cabo un análisis de varianza (ANOVA, pruebas post hoc de Scheffeé). Los resultados indican, en general, una calidad de vida mayor para los pacientes con una carga viral indetectable o detectable controlada (tabla 5). No obstante, los resultados sólo son significativos para las subescalas de salud general percibida, funcionamiento social, energía/fatiga, malestar respecto a la salud, funcionamiento cognitivo y para la puntuación total del MOS-SF-30.
Discusión
La finalidad de este estudio ha sido presentar la versión en español del cuestionario MOS-SF-30 y analizar su fiabilidad y validez para la evaluación de la CVRS en personas VIH+. Este instrumento ha sido capaz de diferenciar los valores de la CVRS entre los pacientes VIH+ asintomáticos y aquellos con síntomas o sida. Asimismo ha permitido diferenciar los grados de calidad de vida en los sujetos con carga viral indetectable y detectable.
No obstante, es oportuno anticipar, como posibles limitaciones de este estudio, que en primer lugar todos los sujetos incluidos estaban siendo atendidos de forma adecuada en una unidad hospitalaria de VIH altamente especializada, lo que quizá podría no ser representativo de la población española infectada. Sin embargo, los resultados aquí arrojados proporcionan información útil sobre el desempeño de la versión en español del cuestionario MOS-SF-30 en una muestra de sujetos VIH+, en distintas etapas de la infección por el VIH y en TARGA. En segundo lugar, por tratarse de un estudio de diseño transversal no se presentan medidas sobre el índice de estabilidad (test-retest) y cambio a lo largo del tiempo, que podrían ser también claves importantes para dar seguimiento a futuras investigaciones. En tercer lugar, a pesar de los buenos resultados en cuanto a las características psicométricas del instrumento, su capacidad discriminatoria entre los diferentes estadios de la infección y entre los valores de carga viral es limitada, lo que sugiere cierta precaución a la hora de su aplicación en los ámbitos clínico e individual.
Consideradas las limitaciones, podemos señalar que la versión en español de la escala MOS-SF-30 ha demostrado ser un instrumento útil en la evaluación de la CVRS en la infección por el VIH; en concreto, los ítems del cuestionario se han cumplimentado sin dificultad en un tiempo corto; los datos psicométricos de la escala han sido buenos, siguiendo la misma línea de los informados por la versión original en inglés1,10,11, y la consistencia interna tanto de las subescalas (entre 0,84 y 0,91) como de la escala completa (0,93) también ha sido buena.
La validez concurrente16, proporcionada en términos de correlaciones, entre las puntuaciones del test en cuestión y las del criterio (en nuestro caso las medidas biomédicas) ha sido asimismo adecuada. La puntuación total de la CVRS y las puntuaciones relativas a algunas de las dimensiones del MOS-SF-30 han evidenciado correlaciones relevantes con los estadios de la clasificación de los CDC, linfocitos T CD4 y carga viral, lo que sugiere que la versión en español de la escala MOS-SF-30 es una medida válida para evaluar el estado de salud y la CVRS.
La validez de las medidas de CVRS puede ser establecida si se presume que la CVRS se deteriora a medida que la enfermedad progresa. No obstante, sólo hay una asociación modesta entre los indicadores del estado de salud que pueden ser usados como marcadores del grado de enfermedad. En nuestro caso hemos utilizado medidas biológicas (linfocitos T CD4 y carga viral) y clínicas (clasificación de los CDC) como indicadores de progresión de la infección por el VIH. Otros trabajos con CVRS no han presentado asociación entre dimensiones de la CVRS y los indicadores objetivos de salud o estadios de la clasificación de los CDC10,11; esto no significa necesariamente que estas medidas sean inválidas, ya que la asociación entre las medidas psicológicas y los indicadores objetivos de salud no presentan un patrón lineal.
Por otra parte, algunas de las dimensiones de la CVRS (p. ej., salud general percibida, malestar respecto a la salud y funcionamiento cognitivo) se han mostrado capaces de discriminar entre los sujetos asintomáticos y aquellos con síntomas o sida, y lo mismo se observa con la puntuación global del MOS-SF-30. Teniendo en cuenta que los valores de carga viral también son buenos predictores de progresión a sida o muerte14, se observó que las puntuaciones de las subescalas salud general percibida, funcionamiento social, energía/fatiga, malestar respecto a la salud y funcionamiento cognitivo, así como la puntuación total del MOS-SF-30, han sido significativamente distintas entre los sujetos con una carga viral indetectable y detectable (controlada y no controlada). No obstante, es oportuno señalar que las restantes subescalas son relativamente poco sensibles a los cambios en los indicadores de progresión de la enfermedad para esta muestra.
Por todo ello, este estudio ofrece soporte empírico a la utilidad de la versión en español de la escala MOS-SF-30 para la evaluación de la calidad de vida relacionada con la salud en personas con infección por el VIH. Consideramos que este tipo de instrumentos adquiere una gran importancia a la vista de los avances en la lucha contra el sida, reflejados en la disponibilidad de tratamientos más efectivos y eficaces, que han permitido a las personas afectadas por el VIH prolongar su vida17,18. Poder contar con indicadores globales del impacto de la enfermedad y del tratamiento en la vida del paciente, como es el caso del cuestionario MOS-SF-30 o de los conocidos cuestionarios MOS-HIV y MQOL-HIV, puede ayudar al médico en la toma de decisiones sobre posibles cambios de tratamiento, pasando a priorizar y valorar en mayor medida el bienestar y la percepción del paciente sobre su estado de salud.
Agradecimiento
El autor desea expresar su agradecimiento al Prof. Dr. Jorge López Martínez (UAM) por los comentarios y sugerencias a la primera versión de este manuscrito.
Correspondencia: Eduardo Remor. Departamento de Psicología Biológica y de la Salud. Facultad de Psicología. Universidad Autónoma de Madrid. Ciudad Universitaria de Cantoblanco. 28049 Madrid. España. Correo eletrónico: eduardo.remor@uam.es
Manuscrito recibido el 25 de septiembre de 2002.
Manuscrito aceptado para su publicación el 24 de febrero de 2003.