Introducción
El presente artículo es la versión abreviada de una parte de los aspectos abordados en la guía de práctica clínica (GPC) publicada recientemente sobre la menopausia y la posmenopausia1. Dicha guía ha sido elaborada por la Sociedad Española de Ginecología y Obstetricia (SEGO), la Asociación Española para el Estudio de la Menopausia (AEEM) y la Sociedad Española de Medicina de Familia y Comunitaria (semFYC), con el apoyo metodológico del Centro Cochrane Iberoamericano (CCIb). La versión en formato electrónico de la guía completa puede consultarse en la web de semFYC (http://www.semfyc.es) y en las respectivas webs de las instituciones participantes.
En este artículo, el primero de una serie de tres, se aborda y evalúa la eficacia de las diversas medidas de prevención y tratamiento, ya sea farmacológico o no, dirigidas a mejorar los síntomas asociados con la menopausia. En el segundo artículo se contempla la evaluación del riesgo de fractura y el cribado de la osteoporosis en la mujer posmenopáusica. En el tercer y último artículo de la serie se revisan los riesgos y beneficios del tratamiento hormonal (TH), a partir de los nuevos conocimientos aportados por los diferentes ensayos clínicos aleatorizados (ECA).
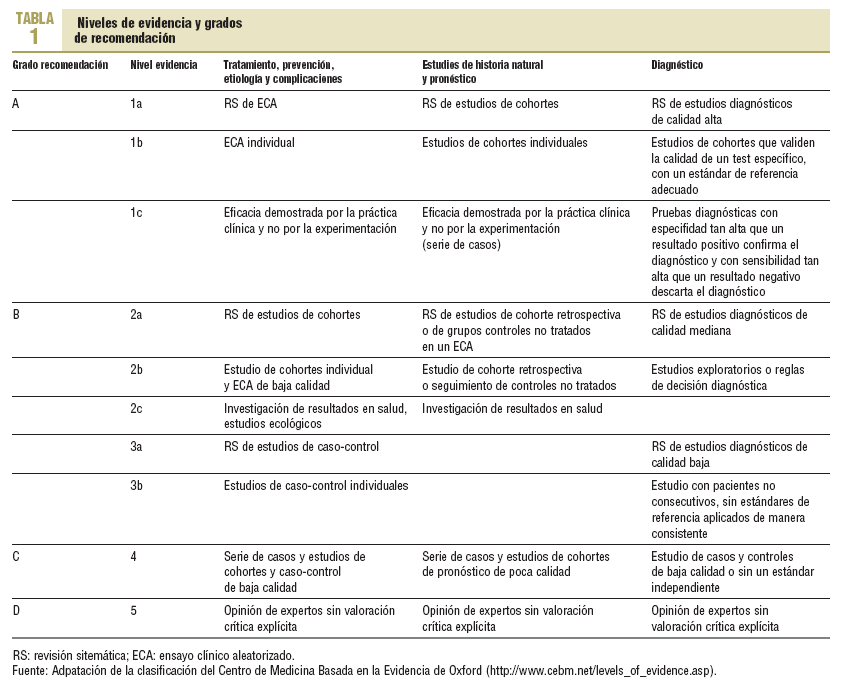
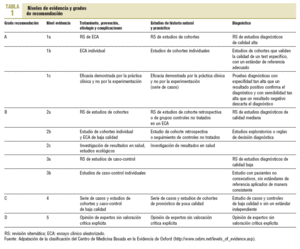
En la elaboración de la GPC se han tenido en cuenta los elementos esenciales contemplados en los criterios del instrumento AGREE (Appraisal of Guidelines, Research and Evaluation for Europe, http://www.agreecollaboration.org), que son los estándares europeos sobre GPC: definición del alcance y los objetivos de la guía, desarrollo y revisión por un equipo multidisciplinario, identificación sistemática de la evidencia científica, formulación explícita de las recomendaciones, claridad en la presentación de la guía y sus recomendaciones, aplicabilidad en el medio, actualización periódica e independencia editorial. Los niveles de evidencia y grados de recomendación se han elaborado a partir de la clasificación del Centro de Medicina Basada en la Evidencia de Oxford (http://www.cebm.net/levels_of_evidence.asp). En la tabla 1 se presenta una adaptación de esta propuesta de trabajo por parte del CCIb (http://www.cochrane.es), para los estudios de intervención.
Síntomas en la menopausia y la posmenopausia
Como consecuencia de los cambios hormonales que ocurren en la menopausia (secundarios a la pérdida definitiva de la actividad folicular del ovario), algunas mujeres presentan síntomas que pueden afectar a su calidad de vida2. Estos síntomas, aunque no son una amenaza grave para la salud y son autolimitados, pueden llegar a interferir con la actividad cotidiana2.
La menopausia y la posmenopausia se han relacionado con diversos síntomas y procesos crónicos. Diversos estudios observacionales muestran de manera consistente una asociación causal entre los síntomas vasomotores y vaginales y la disminución de estrógenos3. Los síntomas urinarios (incontinencia urinaria e infecciones urinarias de repetición) presentan una asociación débil y controvertida3,4.
Síntomas vasomotores
Los síntomas vasomotores (bochornos, sofocos) se presentan como una sensación subjetiva de calor que habitualmente se asocia con una vasodilatación cutánea y sudación seguida de un descenso de la temperatura corporal y una aceleración transitoria de la frecuencia cardíaca. La clínica vasomotora suele comenzar en la perimenopausia y desaparece de forma gradual con los años. Los sofocos y las sudaciones nocturnas pueden provocar alteraciones del sueño que favorecen la aparición de cuadros de fatiga, irritabilidad, disminución de la concentración y falta de memoria. El insomnio, la cefalea y los mareos, aunque pueden estar presentes en mujeres con síntomas vasomotores intensos, no han mostrado una asociación causal con la disminución de estrógenos3.
Síntomas vaginales
Tras la menopausia se produce una pérdida de elasticidad del introito vulvar y una reducción tanto de la actividad de las glándulas vaginales como del grosor del epitelio escamoso vaginal, lo que comporta una disminución de la lubrificación y, en algunas mujeres, sequedad vaginal y dispareunia4. A medida que avanza la posmenopausia, la atrofia vaginal es más importante y los síntomas de sequedad vaginal y dispareunia pueden ser más manifiestos2,3.
Intervenciones para los síntomas vasomotores
Educación sanitaria
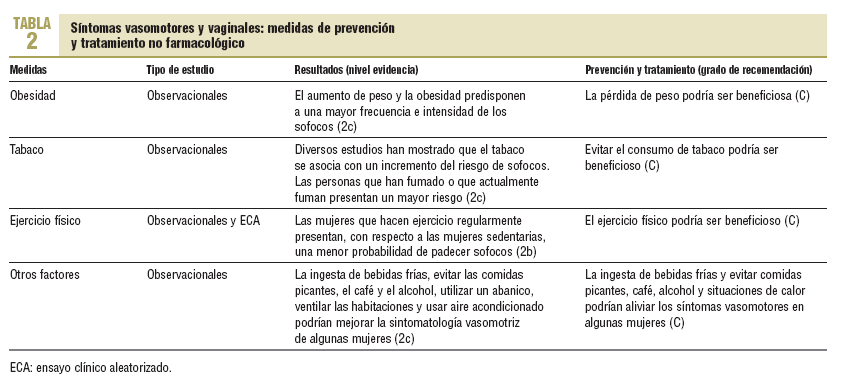
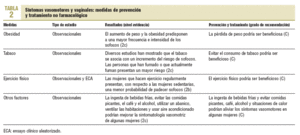
Diversos estudios, la mayoría observacionales, han mostrado una asociación entre determinados factores de riesgo y la frecuencia y/o intensidad de los síntomas vasomotores1,5. El aumento de peso, la obesidad, el tabaco y el sedentarismo podrían aumentar la presencia de sofocos1,6. En la tabla 2 se presentan las diversas recomendaciones sobre las medidas de prevención y la evidencia que las soporta. Otros factores que no son modificables (raza, ooforectomía, menopausia quirúrgica y algunas enfermedades crónicas) también se asocian con un mayor riesgo de síntomas vasomotores1.
Tratamiento hormonal
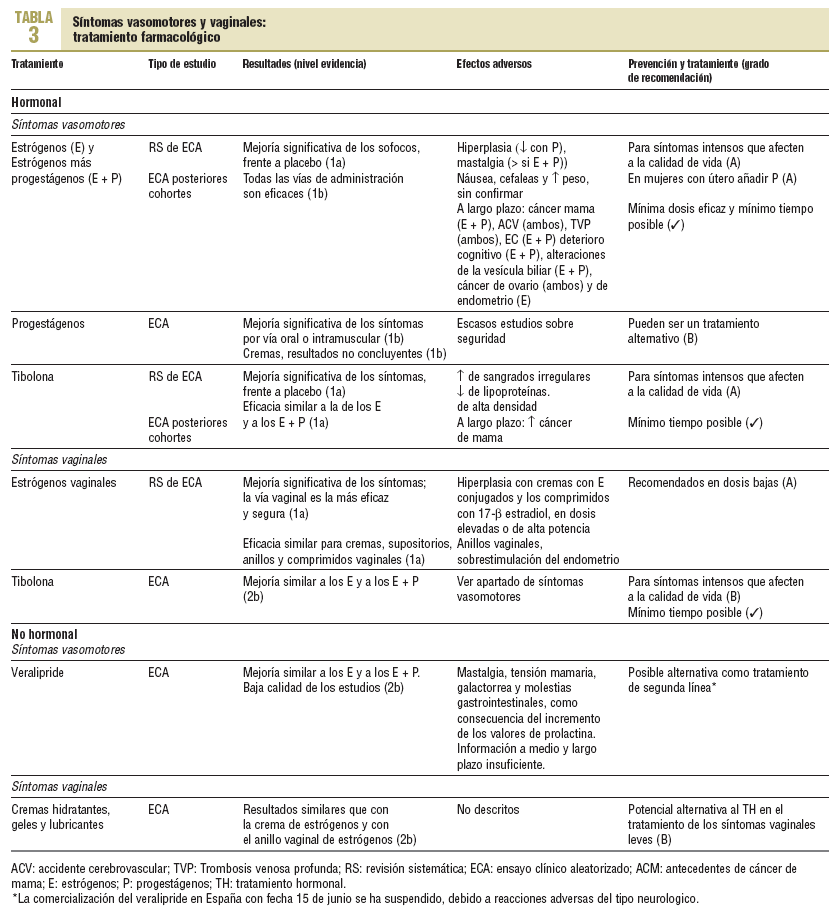
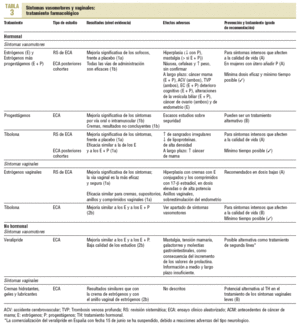
Estrógenos y estrógenos combinados con progestágenos. En una revisión sistemática (RS)7 y en ECA posteriores se ha demostrado que los estrógenos orales, solos o combinados con progestágenos, son superiores al placebo y reducen la frecuencia de los sofocos (tabla 3). Este efecto es superior para los estrógenos combinados con progestágenos (odds ratio [OR] = 0,18; intervalo de confianza [IC] del 95%, 0,13-0,24 frente a OR = 0,37; IC del 95%, 0,26-0,54)7. Diversos ECA también han mostrado la eficacia de los estrógenos administrados por vía transdérmica (gel, parches, implantes) y por vía intranasal1. Asimismo, según una reciente RS8, los estrógenos conjugados y el 17 ß-estradiol en las distintas formas de presentación son superiores de forma similar frente al placebo. La respuesta individual al tratamiento con estrógenos es variable y las mujeres pueden requerir dosis diferentes.
Cuando los estrógenos se administran solos, aumenta el riesgo de hiperplasia endometrial, el cual disminuye al añadir progestágenos. Los efectos adversos a corto plazo son leves, pero a largo plazo el balance es desfavorable (v. apartado Riesgos del TH).
Tibolona. Los resultados de dos RS9,10 y posteriores ECA muestran que la tibolona comparada con el placebo reduce de forma significativa los sofocos y las sudaciones nocturnas (tabla 3) y muestra una eficacia similar a la de los estrógenos. Los diferentes ECA no muestran a corto plazo efectos adversos importantes, aunque a largo plazo se ha observado un aumento del riesgo de cáncer de mama. Las diferentes agencias de evaluación de medicamentos recomiendan utilizar la tibolona únicamente para el tratamiento de los síntomas vasomotores intensos a corto plazo11.
Tratamientos no hormonales
El veralipride, la clonidina, la metildopa, la gabapentina y algunos antidepresivos son fármacos que también han sido evaluados mediante ECA. No obstante, y a pesar de los resultados obtenidos, en la mayoría de estos estudios se incluye a un reducido número de mujeres, el tiempo de seguimiento es corto y su calidad es generalmente baja1. Muchos de estos estudios se han realizado en mujeres con cáncer de mama y se desconoce si sus resultados son generalizables a todas las mujeres posmenopáusicas que presentan síntomas vasomotores. Estos fármacos no están actualmente aprobados en nuestro país en la indicación de tratamiento para los síntomas vasomotores en las mujeres posmenopáusicas. La comercialización del veralípride se ha suspendido recientemente en España.
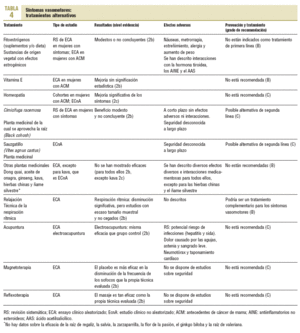
Tratamientos alternativos y/o complementarios
Actualmente hay un mayor interés en las terapias complementarias y alternativas propiciado por los riesgos a largo plazo del TH. A pesar de que la evidencia científica es escasa, su utilización está muy extendida y muchas mujeres las prefieren por ser aparentemente más naturales. En nuestro medio no hay estudios sobre su utilización pero, al igual que en otros países, están disponibles en tiendas de dietética, herbolarios y farmacias, y también se pueden obtener a través de internet.
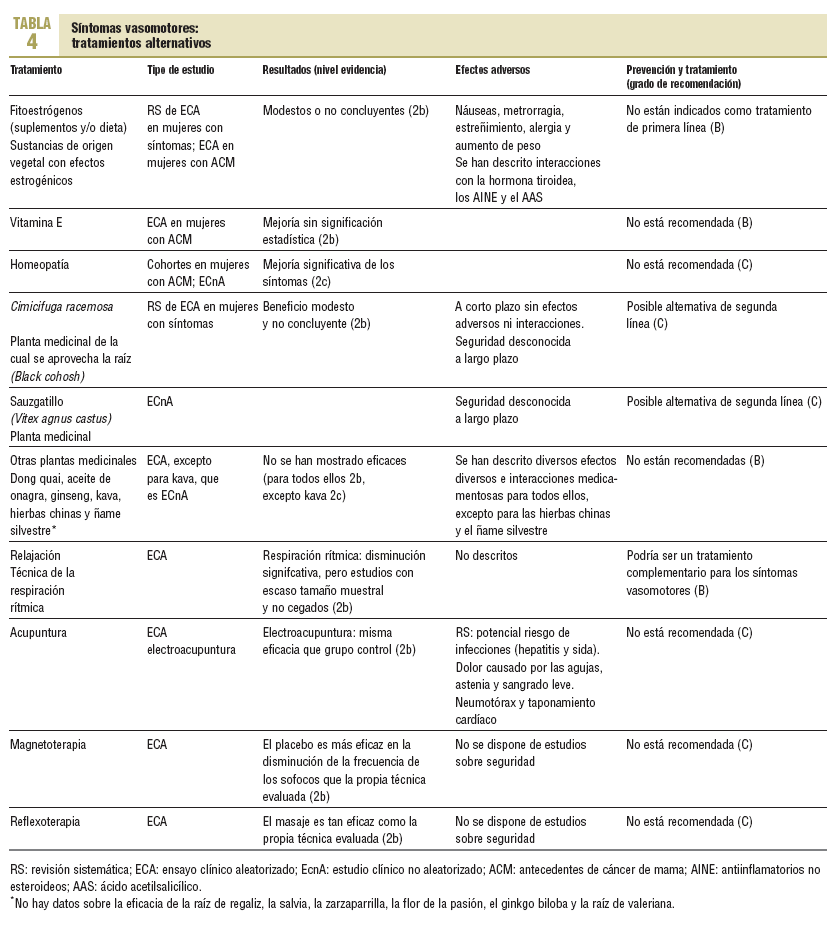
Fitoestrógenos, vitamina E y homeopatía. A pesar de la popularidad de los fitoestrógenos, sobre todo de las isoflavonas derivadas de la soja y el trébol rojo, las RS muestran resultados modestos o no concluyentes12-14. Con respecto a la vitamina E y la homeopatía, los estudios disponibles son escasos, de baja calidad metodológica y con resultados no concluyentes1 (tabla 4).
Hierbas medicinales. Entre las múltiples opciones disponibles, únicamente Cimicifuga racemosa (Black cohosh)14-16 ha mostrado un modesto beneficio, aunque no concluyente. Este tratamiento y el sauzgatillo (Vitex agnus castus) están aprobados por la comisión E del Gobierno alemán que regula la seguridad y la eficacia de las hierbas medicinales para su utilización en el tratamiento de los síntomas vasomotores (http://www.herbalgram.org/default.asp?c=comission_e).
Otras plantas medicinales, como el dong quai (Angelica sinensis), el aceite de onagra o prímula (Oenethera biennis), el ginseng (Panax ginseng), el kava (Piper methysticum), las hierbas chinas y el ñame silvestre (Dioscorea villosa) no han mostrado una mejoría de los síntomas vasomotores. No se dispone de estudios en los que se evalúe la eficacia de la raíz de regaliz, la salvia, la zarzaparrilla, la flor de la pasión, el ginkgo biloba o la raíz de valeriana.
Otras técnicas. La respiración rítmica (respiración lenta, controlada y con el diafragma, en el momento de iniciarse el sofoco), ya sea de manera aislada o como parte de una intervención que incluya otras técnicas de relajación, es la única técnica que ha mostrado una disminución de la sintomatología vasomotora. La acupuntura, la reflexoterapia y la magnetoterapia no han mostrado mejoría de los síntomas vasomotores (tabla 4).
Tratamiento de los síntomas vaginales
La educación sanitaria en los síntomas vaginales tiene un menor papel que en los síntomas vasomotores. El tabaco, el ejercicio físico y la obesidad no han mostrado ninguna asociación concluyente3,6.
Tratamiento hormonal
Dos RS muestran que los estrógenos son eficaces en el tratamiento de los síntomas vaginales, siendo la vía vaginal la más eficaz17,18 (tabla 3). Esta vía de administración permite, además, el control de los síntomas con dosis bajas. La eficacia es similar tanto para las cremas como para los supositorios, los anillos y los comprimidos vaginales18. La tibolona, comparada con el TH, ha mostrado una mejoría similar de los síntomas, pero no se dispone de ECA que la evalúen frente a los estrógenos vaginales.
Tratamientos no hormonales
No se dispone de ECA controlados con placebo que evalúen la eficacia de las cremas hidratantes, los geles o los lubricantes no hormonales para aliviar los síntomas vaginales. Los ECA que han comparado una crema hidratante vaginal no hormonal con una crema con estrógenos o con un anillo vaginal liberador de estrógenos han mostrado una reducción similar de estos síntomas1.
Riesgos del tratamiento hormonal
En la década de los noventa se pusieron en marcha diversos ECA de gran tamaño y a largo plazo, tanto en mujeres sanas (WHI19,20 y WISDOM21) como en mujeres con antecedentes cardiovasculares (HERS)22. Estos estudios mostraron resultados contrarios a los efectos preventivos observados en los estudios observacionales previos, lo que planteó un cambio profundo en la práctica clínica de la menopausia. Entre los efectos adversos a largo plazo se ha observado un incremento significativo de tromboembolia, las enfermedades cardiovasculares, los accidentes cerebrovasculares, el cáncer de mama, la demencia y las alteraciones de la vesícula biliar. Asimismo, el estudio de cohortes Million Women Study mostró un incremento significativo de la incidencia de cáncer de mama, tanto en las mujeres que recibieron estrógenos con o sin progesterona como tibolona.
Ante los resultados desfavorables de estos estudios, la Agencia Española del Medicamento, al igual que otras agencias internacionales, ha resaltado que el balance riesgo-beneficio es desfavorable y su utilización no está justificada en mujeres sin sintomatología11. Esta información incluye a todas las especialidades farmacéuticas que contienen estrógenos con o sin progesterona y a la tibolona.
Aplicación práctica: estrategias terapéuticas
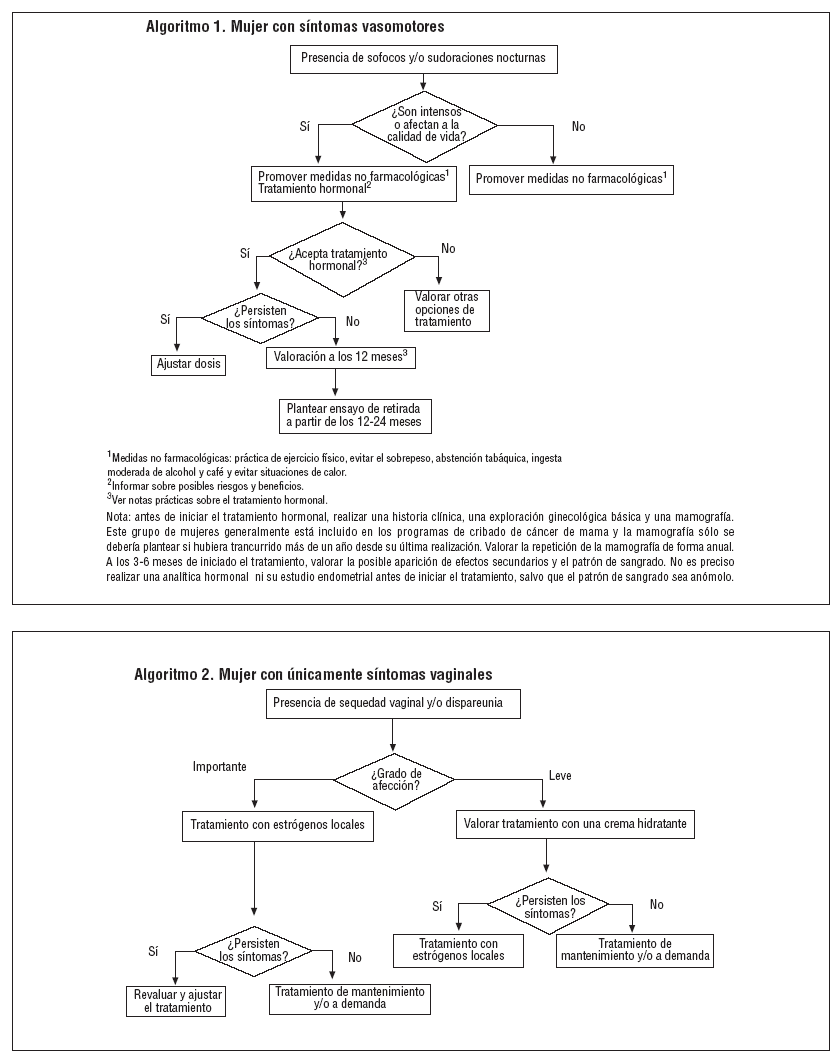
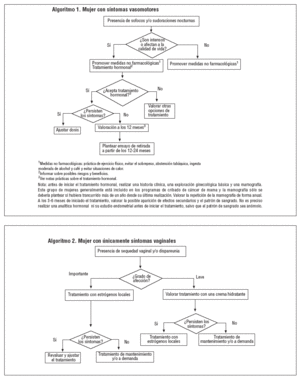
Mujer con síntomas vasomotores (algoritmo 1). Ante una mujer con clínica vasomotora se debe evaluar su repercusión sobre su calidad de vida, así como la presencia de síntomas vaginales. Se debe explicar la naturaleza autolimitada y la benignidad de los síntomas y promover medidas de educación sanitaria, independientemente de la intensidad de éstos. Si los síntomas son percibidos como importantes, se debe valorar con la mujer la posibilidad de iniciar un tratamiento hormonal (estrógenos, con o sin progestágenos o tibolona) tras explicar sus riesgos y beneficios. Si la mujer acepta este tratamiento y no presenta ninguna contraindicación, debería iniciarlo con la dosis más baja disponible y durante el mínimo tiempo posible.
Dependiendo de la intensidad de la sintomatología inicial se debe proponer la retirada del TH de manera progresiva a partir de los 12-24 meses. En la retirada es aconsejable utilizar una dosis menor durante 3-6 meses y posteriormente ir alternando 1, 2 o más días sin tratamiento, de forma progresiva. Puede obtenerse una dosis más baja cortando una parte de los parches, aplicando una menor cantidad de gel o dividiendo los comprimidos.
Si la mujer no acepta el TH, se han de valorar conjuntamente otras opciones menos efectivas de tratamiento (fitoestrógenos, Cimicifuga racemosa) u otras técnicas (entrenamiento de la respiración rítmica).
Mujer con síntomas vaginales únicamente (algoritmo 2). Ante una mujer que presente síntomas vaginales aislados (sequedad vaginal y/o dispareunia) se debe evaluar la repercusión que éstos tienen sobre la calidad y la satisfacción de las relaciones sexuales. Si la mujer presenta también síntomas vasomotores, se debe proceder según el algoritmo 1. Si el grado de afección es importante, se ha de proponer un TH con estrógenos tópicos en cualquiera de sus diferentes presentaciones (comprimidos vaginales, óvulos o cremas). El tratamiento se aplica a diario durante 2-4 semanas y posteriormente se puede pasar a 1 o 2 comprimidos por semana, o continuar de forma diaria en el caso de los óvulos y las cremas. Si los síntomas han mejorado, se debe continuar el tratamiento y ajustar progresivamente la posología hasta encontrar una dosis óptima de mantenimiento. Posteriomente se plantea un tratamiento a demanda, o bien la utilización de una crema hidratante. Ante una recurrencia de los síntomas, se ha de valorar reiniciar el tratamiento. Si los síntomas son leves o la mujer no acepta el tratamiento tópico con estrógenos, valorar el tratamiento con una crema hidratante.