Introducción
La inmunización frente a enfermedades como tos ferina, difteria, polio, sarampión, parotiditis, rubéola y tétanos aparece asociada a la reducción del problema sanitario originado por estas infecciones. Los resultados más importantes se han conseguido en los países desarrollados, alcanzándose grandes niveles de cobertura vacunal, aunque de forma general se ha producido un importante avance en todo el mundo en la lucha contra las enfermedades transmisibles.
En los últimos tiempos, y debido a los avances tecnológicos y científicos, las expectativas frente al desarrollo de nuevas vacunas han ido tomando cuerpo, fijándose como objetivo enfermedades como el sida, la malaria o la tuberculosis1. Esta situación ha permitido no sólo el desarrollo de nuevas vacunas potencialmente más eficaces y seguras2, sino también que su coste de producción sea el menor posible3,4.
El diseño de vacunas frente a infecciones agudas tiene como objetivo conferir inmunidad antes de la replicación del agente infeccioso; son las denominadas vacunas preventivas. Pero aun cuando la infección se hace crónica o latente se puede recurrir a la vacunación para desarrollar una respuesta inmunitaria. Esta circunstancia se da cuando el huésped no ha podido superar la infección debido a la inhibición de las respuestas o a la mala presentación del antígeno. Estaríamos ante las llamadas vacunas terapéuticas5.
Por otro lado, las enfermedades crónicas no han quedado al margen del contexto de desarrollo de nuevas vacunas introduciéndose la diferenciación entre los dos tipos de vacunas anteriormente mencionadas: profilácticas (de carácter preventivo) y terapéuticas (destinadas a frenar el desarrollo de la enfermedad)6. En la actualidad los ensayos clínicos se orientan hacia el desarrollo de vacunas para procesos crónicos como el cáncer, la diabetes mellitus o la demencia tipo Alzheimer5.
En este marco nos planteamos describir la situación de tres de las vacunas que se encuentran actualmente en fase de experimentación, como son la vacuna frente al virus de la inmunodeficiencia humana (VIH), la vacuna contra la malaria y las vacunas antitumorales.
Vacunas frente al VIH
Dos décadas después de la primera evidencia clínica del sida, la pandemia provocada por el VIH continúa en aumento y ha provocado que más de 60 millones de personas en el mundo hayan sido infectadas por el virus. Se estimó que a finales del año 2001 habría 40 millones de personas en el planeta viviendo con el virus7.
Parece lógico pensar que el desarrollo de una vacuna eficaz y segura contra el VIH sería la única forma de frenar una epidemia para la que no existe una terapia curativa. En la XIII Conferencia Internacional sobre el Sida, celebrada en Durban (Sudáfrica), el desafío para conseguir una vacuna frente al sida se convirtió en uno de los temas de mayor relevancia de los que se abordaron en dicha reunión.
Pero el desarrollo de la vacuna se enfrenta a una serie de dificultades derivadas tanto de las características del propio virus (variabilidad genética), como de la patogenia de la enfermedad (persistencia, latencia intracelular); además requieren de un componente de inmunidad humoral (existencia de anticuerpos neutralizantes) y otro de inmunidad celular (respuesta citotóxica o CTL)8. También debemos tener en cuenta que la experimentación con modelos animales está limitada al no disponer un modelo animal ideal9. El objetivo de una vacuna frente al VIH sería generar una respuesta inmune capaz de controlar la replicación del virus, evitando así la destrucción del sistema inmunitario. Habría que atenuar la infección para que las personas infectadas fuesen capaces de convivir con el virus a largo plazo.
En el momento actual, las estrategias de investigación para el desarrollo de la vacuna van desde la utilización de proteínas de la estructura del VIH como inmunógenos (gag, pol, enf), nuevos vectores vivos (poxvirus), virus vivos atenuados, hasta vacunas de ADN en combinación con otros sistemas de expresión10.
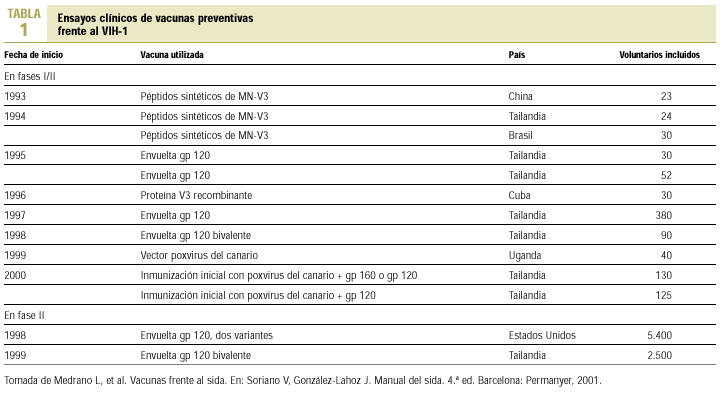
Desde el año 1987, cuando se llevó a cabo el primer ensayo clínico en fase I en Estados Unidos, hasta la actualidad, diferentes ensayos clínicos tanto en fase I como en fase II se han realizado en voluntarios sanos y enfermos de cara a evaluar la inmunogenicidad y seguridad de diferentes preparados vacunales (tabla 1). De los resultados de estos ensayos se desprende que todas las vacunas inducen respuestas específicas de linfocitos T, pero solamente en una se ha observado significativa actividad CTL CD8+ con distinta duración e intensidad en algunos individuos vacunados con vectores vivos. Algo semejante está ocurriendo con las vacunas basadas en ADN desnudo, que han demostrado ser buenos inductores de CTL CD8+ y anticuerpos neutralizantes, aunque utilizando modelos animales11.
Sin embargo, no podemos abstraernos del debate sobre los aspectos éticos de este tipo de intervención. En este contexto, la Organización Mundial de la Salud (OMS) ha elaborado una serie de recomendaciones para la realización de estos ensayos clínicos que podríamos resumir en tres aspectos fundamentales:
La puesta en marcha de ensayos en fases I y II comenzará en países desarrollados que garanticen la seguridad de la vacuna y la respuesta inmune.
Posteriormente se repetirán algunos de estos ensayos en países en vías de desarrollo con características sociosanitarias que podrían afectar a la seguridad y a la respuesta inmune.
Se recomienda realizar ensayos en fase III simultáneamente en países industrializados y en desarrollo, en cohortes con altas incidencia de infección por el VIH.
El desarrollo de una vacuna contra el sida es un proceso complejo que requiere un seguimiento muy concreto para conseguir preparados vacunales seguros y eficaces. Algunos autores hablan de un plazo de 7-10 años para disponer de la vacuna frente al VIH9.
La realización de nuevos ensayos clínicos con los candidatos vacunales de los que se dispone en la actualidad debe seguir su curso para poder certificar su poder inmunógeno y su capacidad protectora.
Vacunas frente al cáncer
La idea de controlar el cáncer mediante la estimulación del sistema inmunológico no es nueva; hace más de un siglo ya se utilizaron extractos bacterianos para estimular la respuesta inmune en tumores específicos. La facilidad del sistema inmune para reconocer las células malignas ha abierto la puerta al desarrollo de vacunas antitumorales con el fin de tratar o prevenir varios tipos de cáncer12. De hecho, el principio fundamental en el que se basa el desarrollo de estas vacunas es la presentación al sistema inmunitario de una serie de antígenos tumorales que éste reconozca como una señal de alerta13.
Las vacunas contra el cáncer se han probado tanto en modelos animales como humanos. En la actualidad se están desarrollando diferentes estudios clínicos con vacunas candidatas para establecer la viabilidad de inmunizar a pacientes con cáncer contra sus propios tumores14,15.
Existen dos tipos de cánceres para los que comienzan a desarrollarse vacunas. En el primero de ellos la aparición del tumor se asocia con la infección viral, como sería el caso del carcinoma hepatocelular primario y la infección por el virus de la hepatitis B, la asociación del sarcoma de Kaposi con la infección por herpesvirus, así como el carcinoma genital y de células escamosas que aparece asociado con la presencia del virus del papiloma humano (VPH). En este caso, nuestro desconocimiento del VPH y del cáncer cervical ha disminuido sensiblemente la posibilidad real de conseguir en un futuro cercano una vacuna frente a la infección viral, que disminuiría la prevalencia de la infección. Actualmente se encuentra en fase de desarrollo clínico un preparado vacunal (Oncocine HspE7), que tiene como objetivo los cánceres originados por el VPH. Su mecanismo de acción está basado en las llamadas proteínas de choque térmico presentadoras de antígenos del virus. Sin embargo, su utilidad clínica es muy restringida13.
En todos los ejemplos anteriores, la vacunación contra los virus más relevantes deberá prevenir la tumorogénesis, tal y como se ha manifestado en diversos ensayos clínicos
realizados2.
Hay un segundo tipo de cánceres sensibles a las vacunas, incluidos tumores espontáneos como el melanoma, que expresan antígenos tumorales endógenos. Pero la inmunoterapia dirigida contra el tumor puede presentar problemas aunque los últimos avances permiten un cierto optimismo. Muchos antígenos tumorales han sido identificados en melanomas. En varios ensayos clínicos donde los antígenos tumorales específicos de células T citotóxicas eran generados por diferentes protocolos de vacunación, se consiguió la completa o parcial remisión de los tumores en alrededor de un 30% de los pacientes2.
Las posibles modalidades de aplicación de las vacunas contra el cáncer, así como su situación actual, se reflejan en la tabla 2.
Vacuna contra la malaria
El paludismo o malaria es una enfermedad parasitaria que afecta de forma endémica a muchos países del mundo e infecta a 300-500 millones de personas al año según la OMS. Los casos de malaria siguen incrementándose, especialmente en los países del África Subsahariana, debido a la aparición de resistencias tanto a los fármacos utilizados para combatir la enfermedad como a los insecticidas utilizados para combatir al mosquito transmisor de la enfermedad, así como a una serie de cambios de tipo sociosanitario y económico16.
En este contexto, el desarrollo de una vacuna frente a la malaria se ha convertido en una de las prioridades de la comunidad científica.
El abordaje de las estrategias de diseño de vacunas contra la malaria tiene como primera referencia a la vacuna sintética SPf66, compuesta por 45 aminoácidos derivados de proteínas de Plasmodium falciparum en fase asexual eritrocítica. Señalamos que la eficacia de esta vacuna varía según los diferentes ensayos clínicos realizados con ella; destacan valores del 31% en el estudio realizado en Tanzania17, mientras que en el ensayo clínico llevado a cabo en Gambia solamente se alcanzaron valores de eficacia del 3%18.
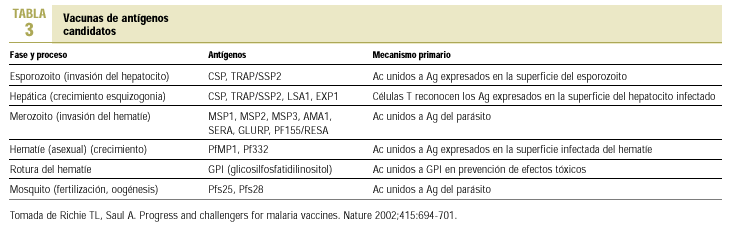
Desde entonces continúa la investigación de diversas vacunas de antígenos candidatas, siguiendo diversas estrategias, intentando averiguar cuál de ellas es capaz de producir la respuesta inmune adecuada. La búsqueda de antígeno debe reunir unos criterios específicos, tales como accesibilidad al sistema inmunológico, capacidad de inducir una respuesta inmunológica protectora en modelos animales, así como mecanismo primario de acción dependiendo de las fases de parásito (tabla 3). Otras líneas de trabajo se basan en la combinación de antígenos de diferentes estados del parásito, o en la combinación de varios antígenos de una misma fase de Plasmodium19.
Recientemente se ha dado a conocer el desarrollo de una nueva vacuna contra la malaria. La RTS,S/AS02 es una vacuna preeritrocítica basada en la proteína de superficie del esporozoito de P. falciparum combinado al HBsAg y con la incorporación de un adyuvante (AS02)20. Según los resultados obtenidos, induce una fuerte respuesta de anticuerpos frente a la proteína del circumsporocito, así como una importante respuesta de las células T. Se observó que el tiempo de aparición de la primera infección por P. falciparum era inferior en el grupo control que en el grupo de estudio. Los autores destacan que es una vacuna segura y bien tolerada e inmunógena, convirtiéndose en la primera vacuna preeritrocítica que infiere un efecto protector frente a la infección natural provocada por el parásito.
Para finalizar, no debemos olvidar que dentro de los grandes retos de la vacunología en los próximos años, y sin pasar por alto las prioridades en el desarrollo de vacunas, tenemos que destacar las necesidades y disponibilidad de éstas tanto en los países desarrollados como en aquellos en vías de desarrollo, y en estos últimos es prioritario un muy bajo coste del preparado vacunal, facilitar el acceso a la vacunación y favorecer la labor de educación para la salud en la población21.
Correspondencia:Ángel Gil de Miguel. Unidad de Docencia e Investigación en Medicina Preventiva y Salud Pública. Facultad de Ciencias de la Salud. Universidad Rey Juan Carlos. Avda. de Atenas, s/n. 28922 Alcorcón (Madrid). España. Correo electrónico: a.gildemiguel@cs.urjc.es