Introducción
El neumococo (Streptococcus neumoniae)1 es un germen grampositivo, capsulado, colonizador de las vías aéreas superiores y causante de múltiples patologías como bacteriemias/sepsis, neumonía, meningitis, artritis, peritonitis, otitis, sinusitis, endocarditis y empiema, entre otras.
La cápsula es el principal factor de virulencia capaz de inhibir la fagocitosis leucocitaria, pasar a la sangre y colonizar órganos diversos.
Se conocen más de 90 serotipos, aunque sólo 23 tienen un papel patogénico importante. Aunque los serotipos son constantes, su distribución geográfica varía de unos países a otros. El interés de esta variabilidad geográfica es que las vacunas actuales y, sobre todo, las nuevas vacunas conjugadas, serán tanto más eficaces en cuanto incluyan los serotipos más prevalentes en cada país2.
El neumococo coloniza las vías respiratorias superiores a veces sin causar síntomas (portadores asintomáticos) y éstos son el reservorio y los responsables de la mayoría de los casos de transmisión a otras personas. Situaciones como la pérdida de la integridad del epitelio respiratorio por infecciones, tabaquismo, alteraciones de la deglución presente en pacientes alcohólicos, por fármacos o senilidad, favorecen la aparición de infecciones por neumococo en las vías respiratorias bajas. Se calcula que está colonizado un 64% de los niños menores de 24 meses3.
La enfermedad invasiva se define fundamentalmente por episodios de bacteriemia, sepsis, meningitis y neumonía bacteriémica. Las enfermedades no invasivas más importantes corresponden a otitis y sinusitis aguda en niños, neumonía no bacteriémica y reagudizaciones infecciosas en pacientes con patología de base (enfermedad pulmonar crónica, exacerbaciones de bronquitis, complicaciones de la gripe, peritonitis, etc.).
Se estima una incidencia de infección neumocócica invasiva en los países desarrollados de 50-60 casos por 100.000 habitantes y año. Una de las infecciones más características es la neumonía, que constituye un problema sanitario de primera magnitud, ya que es una de las principales causas de mortalidad e ingreso hospitalario4. Según datos del estudio EPINE5, las neumonías representan el 13-16% de las infecciones comunitarias hospitalizadas. La incidencia de neumonía adquirida en la comunidad (NAC) se estima en 50-100 casos por 100.000 habitantes y año, con una mortalidad del 5%, aunque en pacientes ingresados puede llegar al 25%. El riesgo de infección neumocócica es superior en pacientes menores de 4 años y mayores de 65, independientemente de la enfermedad de base6. La bacteriemia supone alrededor de un tercio de las infecciones neumocócicas y el origen más frecuente de la neumonía.
A pesar de las discrepancias existentes en la bibliografía en función del tipo de estudio y métodos diagnósticos utilizados7-9, el neumococo es el germen más frecuente de las NAC. Según datos declarados en España (1996) el 21% de todas las neumonías correspondió al neumococo10. Asimismo, de todas las neumonías que requieren hospitalización, un 30-50% es causada por neumococo.
El neumococo también es la causa más frecuente de meningitis en mayores de 25 años y el germen más frecuente de peritonitis espontánea.
Sobre la incidencia en niños, en Cataluña se ha encontrado una incidencia de enfermedad invasora de 61/100.000 en niños menores de 2 años y una incidencia de meningitis neumocócica en lactantes de 7-9/100.00011. Aproximadamente en un 40% de las otitis medias se aísla el neumococo.
También hay que destacar el incremento de resistencias del neumococo a los antibióticos de uso más frecuente, como penicilinas, cefalosporinas, macrólidos, cotrimoxazol y quinolonas.
Las dos estrategias para hacer frente a las infecciones neumocócicas son la utilización racional de los antibióticos y el uso de vacunas.
Vacuna de polisacáridos
Aunque las investigaciones para la obtención de vacuna se iniciaron hace más de cien años, fue en 1977 cuando se comenzó a utilizar una vacuna 14-valente. En 198312 apareció una vacuna 23-valente que contiene 23 serotipos de polisacáridos capsulares con 25 µg de cada uno de ellos en una solución salina isotónica. Los 23 serotipos incluidos en la vacuna son los causantes del 90% de las infecciones neumocócicas graves. En España se registró en 1999.
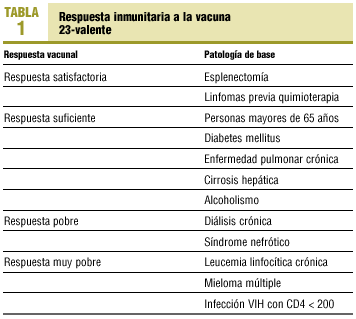
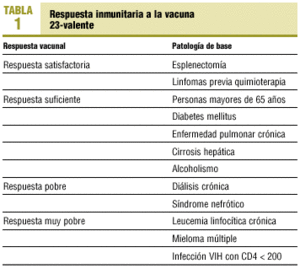
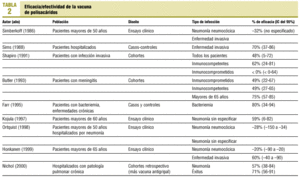
Respecto a la inmunogenicidad de la vacuna, la respuesta inmunitaria inducida por ésta no es igual en todos los pacientes ni para todos los serotipos. Además, la inmunogenicidad varía en función de la patología de base del paciente. En la tabla 1 se explicita la respuesta vacunal en función de la patología de base preexistente. La respuesta inmunitaria es mayor en sujetos inmunocompetentes que en inmunodeprimidos. No induce respuesta en niños menores de 2 años. Al ser una vacuna de polisacáridos no induce memoria inmunológica.
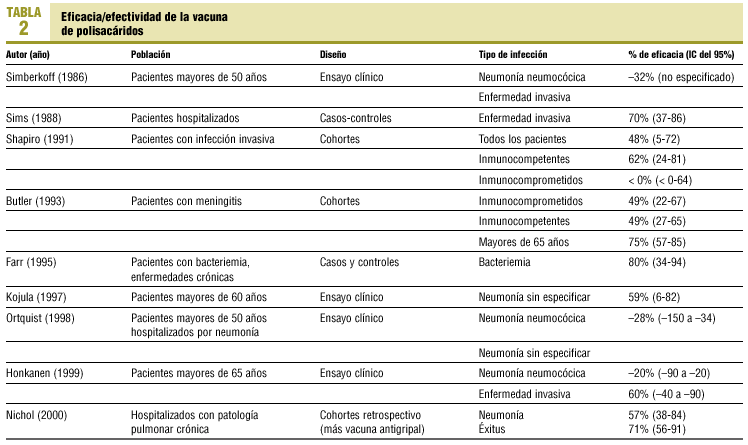
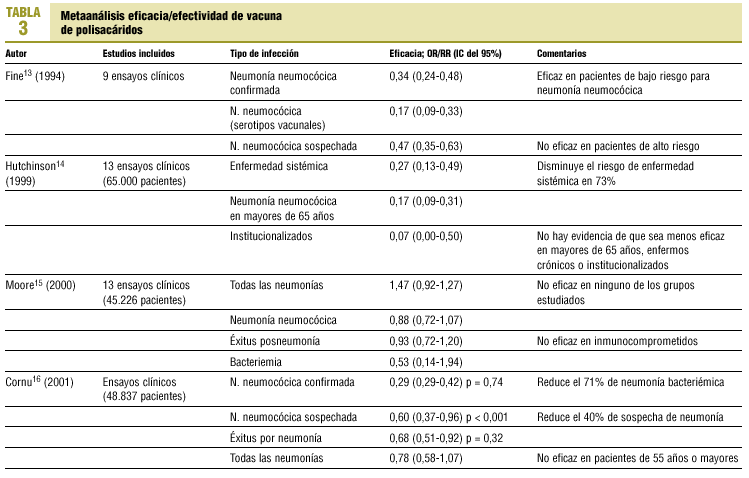
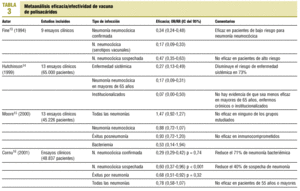
Los datos disponibles sobre la eficacia/efectividad son uno de los puntos más controvertidos. En la tabla 2 se resumen algunos de los trabajos publicados. Es eficaz en pacientes inmunocompetentes para la prevención de bacteriemia/sepsis o neumonía bacteriémica (47-70%). Respecto a la eficacia en la prevención de neumonía no bacteriémica o en pacientes inmunodeprimidos o mayores de 65 años, los datos son contradictorios. Se han dado a conocer 4 metaanálisis (tabla 3) de los trabajos publicados para depurar la información respecto a la eficacia/efectividad de la vacuna de polisacáridos. La vacuna parece ser eficaz en inmunocompetentes para prevenir la enfermedad neumocócica invasiva y la neumonía bacteriémica. Respecto a la eficacia en mayores de 65 años e inmunodeprimidos y/o de alto riesgo para enfermedad neumocócica, los datos son contradictorios.
Esta discordancia entre los estudios publicados se refleja en la disparidad de las recomendaciones para la vacunación (especialmente en mayores de 65 años) que han aprobado los diversos organismos y autoridades sanitarias12,17-19.
A pesar de la ingente cantidad de información contradictoria actualmente disponible sobre la eficacia/efectividad de la vacuna, hay algunas cuestiones no resueltas20:
Aun con las dudas que genera su eficacia, es la única forma de prevenir la enfermedad.
La no significación de algunos ensayos clínicos y metaanálisis puede deberse tanto a la metodología utilizada como a la falta de potencia estadística o a muestras insuficientes en subgrupos de los pacientes evaluados.
Se necesitan más estudios en grupos específicos, sobre todo en mayores de 65 años y/o pacientes institucionalizados para conocer la eficacia real y el coste/efectividad de la vacuna.
La extrapolación de los resultados publicados a nuestro país con coberturas de vacunación muy bajas impide conocer su efectividad real en nuestro medio.
Aunque la eficacia en pacientes mayores de 65 años e inmunocomprometidos es baja, habría que considerar la elevada prevalencia de episodios de enfermedad neumocócica en estos pacientes.
Se desconoce el beneficio de la vacunación en pacientes no vacunados, portadores nasofaríngeos asintomáticos y en la resistencia del germen a los antibióticos más comúnmente utilizados.
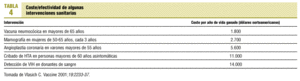
Se debe valorar el coste/eficacia de la vacunación antineumocócica en comparación con otras intervenciones sanitarias (tabla 4).
Indicaciones12,17-19
Adultos con alto riesgo de morbimortalidad por neumococo
Personas mayores de 65 años, especialmente en aquellos que estén o vayan a ser institucionalizados. Las autoridades sanitarias españolas (Ministerio de Sanidad)17 no la recomiendan. Sin embargo, y dado que la política vacunal es competencia de las comunidades autónomas, la decisión de vacunar a este grupo etario difiere en cada comunidad. Actualmente están vacunando sistemáticamente a los mayores de 65 años las comunidades de Cataluña, Galicia, Comunidad Valenciana y Cantabria.
Inmunodeprimidos: asplenia, infección por VIH, linfomas, mieloma múltiple, anemia de células falciformes.
Pacientes con enfermedades crónicas: insuficiencia cardíaca, neumopatías crónicas, cirrosis hepática, diabetes mellitus, insuficiencia renal, alcoholismo, pacientes con fístulas de LCR.
Niños mayores de 2 años con alto riesgo de morbimortalidad por neumococo
Asplenia funcional u orgánica.
Niños con enfermedades crónicas: neumopatías crónicas, cardiopatías, insuficiencia renal, síndrome nefrótico.
Infección por VIH.
Anemia depranocítica.
Niños inmunodeprimidos: leucemia, linfomas, trasplantados.
La dosis a administrar es de 0,5 ml por vía intramuscular o subcutánea y se puede simultanear con otras vacunas, siempre que el lugar de inoculación sea diferente (vacuna antigripal, Haemophylus influenzae, toxoide tetánico y/o diftérico, triple viral, hepatitis B). Respecto a la revacunación, se recomienda una dosis de recuerdo siempre que hayan transcurrido más de 5 años de la primovacunación en aquellos pacientes con alto riesgo de enfermedad neumocócica. Los mayores de 65 años recibirán una segunda dosis si han pasado más de 5 años de la primera y tenían menos de 65 años. Los pacientes mayores de 65 años no vacunados recibirán una sola dosis y no está indicada la revacunación.
La tolerancia es buena; se han descrito reacciones locales hasta en el 50% de los vacunados, consistentes en dolor e induración en el punto de inoculación. Las reacciones de carácter general son muy infrecuentes (menos del 1%) y consisten en fiebre, mialgias y excepcionalmente anafilaxia. En definitiva, se trata de una vacuna de polisacáridos con discrepancia sobre su eficacia en algunos grupos (inmunodeprimidos, mayores de 65 años), no eficaz en menores de 2 años y que no induce memoria inmunológica. Si embargo, es la única vacuna existente actualmente para adultos. La solución a estos interrogantes probablemente esté en el desarrollo de vacunas conjugadas para su uso en adultos.
Vacuna conjugada
Uno de los problemas que plantea la vacuna de polisacáridos es su ineficacia en niños menores de 2 años, cuando se trata de un grupo de alta incidencia de enfermedad neumocócica21. Para hacer frente a este problema se han desarrollado vacunas conjugadas. La vacuna actualmente comercializada en España es una vacuna heptavalente que conjuga los serotipos 4-6B-9V-14-18C-19F-23F con un carrier proteico CRM 197 que es una mutante atóxica de toxina diftérica; de esta forma la convierte en un antígeno T-dependiente, más inmunógena y generadora de memoria (estimula a las células B y T de memoria) creando inmunidad permanente. Se aprobó en Estados Unidos en febrero del año 2000 y está disponible en España desde junio de 2001.
Las indicaciones aprobadas por las autoridades americanas22 son:
1. Todos los niños de 0-24 meses de edad.
2. Niños de 24-59 meses de edad pertenecientes a las siguientes categorías:
Anemia falciforme, aplasia congénia/funcional.
Infección VIH.
Enfermedades crónicas: cardíacas, pulmonares, diabetes, fístulas de LCR.
Inmunodeficiencias congénitas, adquiridas, insuficiencia renal, síndrome nefrótico, tumores, leucemias, quimioterapia, radiaciones y trasplante.
3. Debe considerarse en niños de 24-59 meses si presentan las siguientes circunstancias:
Asistencia a guarderías.
Grupos étnicos con elevada incidencia de infección neumocócica como afroamericanos y originarios de Alaska.
En España se ha aprobado su uso en niños menores de 2 años con condiciones de riesgo para la enfermedad neumocócica invasora que incluye bacteriemia, sepsis, meningitis y neumonía bacteriémica.
Se administra por vía intramuscular (zona anterolateral del muslo en lactantes y deltoides en niños mayores).
La pauta de administración es la siguiente:
Niños menores de 6 meses: 3 dosis de 0,5 ml con intervalo de al menos un mes entre dosis. Se recomienda una cuarta dosis en el segundo año de vida.
Niños de 7-11 meses: 2 dosis de 0,5 ml con intervalo de al menos un mes. Se recomienda una tercera dosis en el segundo año de vida.
Niños de 12-23 meses: 2 dosis con al menos 2 meses de intervalo entre ambas.
La vacuna puede administrarse juntamente en lugares diferentes con otras vacunas: DTP-Hib, DT, TV, VHB.
Respecto a la eficacia, el estudio Kaiser23 evaluó la eficacia de la vacuna conjugada en la prevención de la enfermedad neumocócica invasiva en 37.868 niños, demostrándose una eficacia del 97% (IC del 95%, 82-99). En el ensayo finlandés24 se estudió la eficacia vacunal en la prevención de la otitis media. Fue eficaz en un 57% para prevenir la otitis media aguda (OMA) por los serotipos incluidos en la vacuna, disminuyendo al 34% para la OMA producida por cualquier neumococo y del 6% en la reducción de los episodios de OMA de cualquier etiología.
Los datos disponibles sobre la seguridad indican que los principales efectos son locales; aparecen en un 10-15% de los casos y consisten en eritema e induración en el área de inoculación. El efecto secundario sistémico más frecuente es la fiebre de 38 oC que se presenta en la cuarta parte de los vacunados. Estos efectos son más frecuentes cuando se asocian simultáneamente con otras vacunas (DT, DTPa). Dichos efectos son similares en niños prematuros o de bajo peso.
En resumen, la vacuna conjugada actualmente disponible es más inmunógena y eficaz que la de polisacáridos y se puede utilizar en niños menores de 2 años. Actualmente está aprobada para vacunación sistemática en Estados Unidos, Canadá, Sudáfrica y Finlandia. Respecto a nuestro país, se necesita conocer la incidencia de infecciones neumocócicas y los serotipos que las producen, así como estudios de coste/eficacia para definir el esquema vacunal más apropiado25.
Conclusiones
Las diversas manifestaciones clínicas de las infecciones originadas por neumococo constituyen un problema sanitario de primera magnitud. Las dos estrategias actuales para hacer frente a este problema son la prevención mediante vacunas y la utilización racional de los antibióticos. La vacuna de polisacáridos plantea algunas cuestiones no resueltas: no es eficaz en niños menores de 2 años y tiene una eficacia moderada en mayores de 65 años e inmunodeprimidos. La reciente aparición de vacunas conjugadas resuelve parcialmente estos problemas: es eficaz en menores de 2 años e induce memoria inmunológica. Sin embargo, se han de resolver algunas cuestiones antes de plantearse su introducción en el calendario vacunal sistemático: número de dosis, coste/eficacia, asociación con otras vacunas, etc.
La posible solución a la baja eficacia de la vacuna de polisacáridos en mayores de 65 años e inmunodeprimidos quizá radica en el desarrollo de vacunas conjugadas para adultos.
Correspondencia: José Javier Gómez Marco. C/ Cobos de Segovia, 7, portal 6, 5.o A. 28005 Madrid. España. Correo electrónico: jjgomezm@medynet.com