Presentamos el caso de un varón de 50años con diabetes mellitus (DM) tipo2 de 8 años de evolución enviado desde urgencias al Hospital de Día de Diabetes de nuestro centro por hiperglucemia de 392mg/dl. En los antecedentes personales destacaba trasplante cardiaco realizado 7 años antes por miocardiopatía dilatada de origen isquémico no revascularizable, momento en el que comenzó tratamiento insulínico. Además, presentaba antecedentes de hipertensión arterial (HTA), era ex fumador, con dislipidemia y obesidad grado I según la clasificación de la OMS. Entre los antecedentes familiares destacaba un hijo con DM tipo2. No tenía antecedentes conocidos de dislipidemia familiar o patología cardiovascular de aparición temprana en parientes de primer grado. Tampoco existían datos de nefropatía o retinopatía diabética en su seguimiento previo por endocrinología. Clínicamente tan solo refería parestesias en miembros inferiores, y la última ecocardiografía realizada mostraba disfunción ventricular derecha leve.
Su tratamiento domiciliario era insulina NPH (Neutral Protamine Hagedorm), 22 unidades en desayuno y cena; insulina aspártica, 14 unidades antes de desayuno, almuerzo y cena; metformina, 850mg/12h; tacrolimus, 0,5mg/12h; micofenolato mofetilo, 1.000mg/12h; prednisona, 2,5mg/24h; losartán, 50mg/hidroclorotiazida 12,5mg/24h; doxazosina, 8mg/24h; fluvastatina, 80mg/24h; omeprazol, 20mg/24h; citalopram, 20mg/24h; lorazepam, 1,5mg/24h. No realizaba dieta diabética y tenía un hábito sedentario.
La exploración física a su llegada a nuestra unidad fue la siguiente: peso, 106,7kg; talla, 177,5cm (índice de masa corporal, 33,86 kg/m2); presión arterial, 163/89mmHg; frecuencia cardíaca, 102lpm; cintura, 114cm. La auscultación cardiaca mostró un corazón rítmico a buena frecuencia, sin soplos ni extratonos, y los miembros inferiores conservaban pulsos y sensibilidad. No se palpaban adenopatías o bocio. En los resultados analíticos destacaban los siguientes: glucosa, 348mg/dl; urea, 50mg/dl; creatinina, 1,50mg/dl (aclaramiento de creatinina estimado según fórmula de Cockroft-Gault, 59,18ml/min/1,73m2); HbA1c, 11,0%; índice microalbúmina/creatinina, 96,4mg/g; colesterol total, 190mg/dl; colesterolHDL, 21mg/dl; colesterolLDL, 91mg/dl; triglicéridos, 644mg/dl; colesterol total/colesterolHDL, 9;05mg/dl; colesterol noHDL, 169mg/dl.
Teniendo en cuenta todos estos datos, realizamos los siguientes diagnósticos: diabetes mellitus tipo 2 descompensada, hipertensión arterial, dislipidemia mixta, obesidad gradoI, síndrome metabólico, enfermedad renal crónica gradoIII, trasplante cardiaco.
El tratamiento prescrito fue dieta diabética hipocalórica de 1.500 kcal, ejercicio físico aeróbico de forma regular, pauta de insulinización bolo-basal con insulina detemir 30unidades en desayuno y después de cenar, e insulina aspártica 18unidades en desayuno, almuerzo y cena, así como realización de controles glucémicos. Fue sometido al programa educativo impartido por el equipo de enfermería especializado en diabetes de nuestra unidad. Siguió con el resto del tratamiento que realizaba previamente, con la retirada de la insulina NPH, y se añadieron a las estatinas ácidos grasos omega-3 para la reducción de la hipertrigliceridemia.
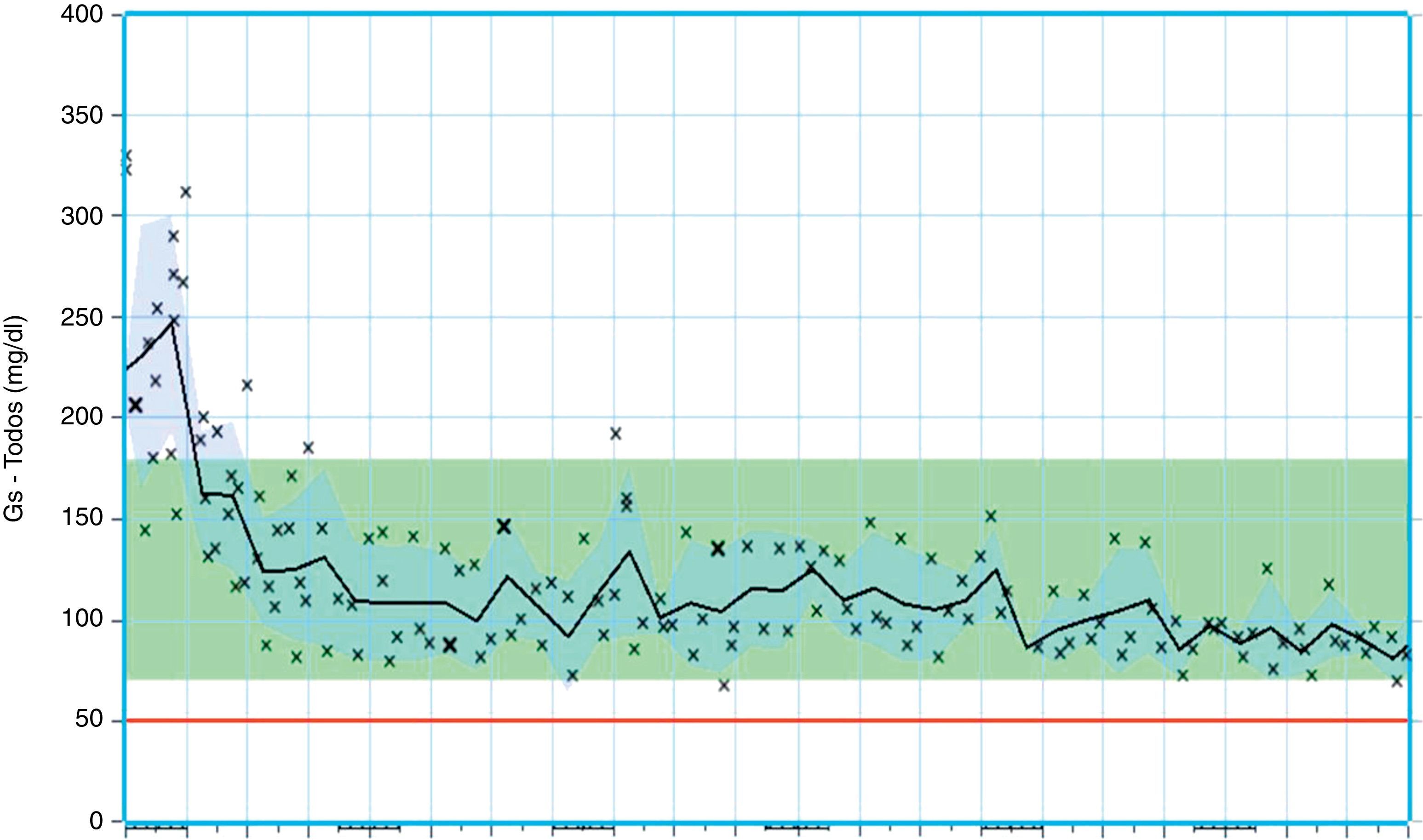
Durante 3meses el paciente acudió a 5visitas, en las que se procedió a titular la dosis de insulina, que se incrementó hasta 50-0-70unidades de insulina detemir y 30-32-30unidades de insulina aspártica (más pauta correctora según controles glucémicos preprandriales). Con ello se consiguió una reducción de la glucemia media de 326±57 a 176±45mg/dl, con un descenso de la HbA1c hasta el 7,5%. La figura 1 muestra la evolución del perfil glucémico en los 3meses de seguimiento. Mantuvimos el tratamiento con metformina, 850mg cada 12h, con el objeto de disminuir la resistencia insulínica, requiriendo pregabalina, 75mg en desayuno y 150mg en cena, para el control del dolor neuropático en los miembros inferiores.
El paciente tuvo una pérdida de peso de 1,7kg al cabo de estos 3 meses. No obstante, el control de la presión arterial no fue óptimo, y durante el seguimiento mantuvo cifras diastólicas en torno a 90mmHg. La función renal se mantuvo estable durante el seguimiento evolutivo. La retinografía digital realizada no determinó la presencia de retinopatía diabética.
DiscusiónLa importancia de este caso reside en la presencia concomitante de trasplante cardiaco en tratamiento inmunosupresor, DM tipo2 en el contexto de síndrome metabólico y enfermedad renal crónica de nuevo diagnóstico, lo cual muestra la complejidad en el manejo que puede requerir un paciente de este tipo. La probabilidad de desarrollar insuficiencia renal crónica (IRC) terminal en pacientes con DM tipo2 de raza caucásica se encuentra en el rango del 15-20%, y es frecuente la presencia de HTA asociada y arteriosclerosis previa al diagnóstico1. Por otro lado, hay que recordar que la IRC con Cr ≥2mg/dl aparece en el 24-33% de los trasplantados cardiacos, con progresión a enfermedad renal terminal del 3-8% de los casos. Entre los factores que determinan esta evolución encontramos la importante presencia de comorbilidad en estos pacientes, ya que a los 5años del injerto el 95% presenta HTA, el 81% hiperlipidemia y el 32% DM (en nuestro caso, ya con DM tipo2 previa). En cuanto al uso de fármacos inmunosupresores para evitar el rechazo del injerto, la terapia con glucocorticoides y tacrolimus está asociada a un empeoramiento de las cifras glucémicas, lo que dificulta el control metabólico2. Este inhibidor de la calcineurina tiene un efecto deletéreo sobre la secreción pancreática de insulina y toxicidad directa sobre la célula beta. Sin embargo, los estudios realizados al respecto con micofenolato mofetilo han mostrado resultados pocos concluyentes3. Por otro lado, el tacrolimus per se parece tener un perfil menos perjudicial para la función renal que la utilizada clásicamente ciclosporina4.
Es importante destacar que el adecuado control metabólico y de la presión arterial, así como el tratamiento con un IECA o un ARA-II y la precaución en el manejo de los medios diagnósticos o nefrotóxicos, han demostrado su utilidad sobre la evolución de la nefropatía y sus complicaciones1. Nuestra postura fue abordar este caso de una forma integral, haciendo especial hincapié en el control glucémico y de la tensión arterial, según las recomendaciones de la ADA5, con tratamiento insulínico intensivo y el empleo de metformina. Utilizamos los análogos de insulina de acción prolongada para reducir el riesgo de hipoglucemia por su perfil más plano y para eliminar la necesidad de suplementación con hidratos de carbono entre las comidas principales, reduciendo el riesgo de incremento de peso. A este respecto es destacable la importancia de la educación diabetológica para evitar la ganancia ponderal que suele ocurrir con la intensificación del tratamiento insulínico, hecho que conseguimos evitar en nuestro paciente. El importante incremento en la dosis de insulina se justifica por el pésimo control metabólico previo del paciente y la insulinorresistencia que caracteriza a un paciente obeso, circunstancia que se agrava con el uso de fármacos inmunosupresores y corticoides.
En cuanto a las biguanidas, pese a las recomendaciones clásicas que alertan del riesgo de su utilización de en la IRC, un estudio realizado en el Reino Unido con 12.482pacientes defiende la aceptable seguridad de la metformina en IRC grado III (aclaramiento de creatinina 30-59ml/min/1,73m2), aunque alerta a los clínicos acerca de la necesaria consideración de otros factores de riesgo para el inicio o mantenimiento de dicho tratamiento6. Tras 3 meses de seguimiento los resultados obtenidos con este enfoque multifactorial del riesgo cardiovascular nos permiten albergar esperanzas para la estabilización de la nefropatía y la perdurabilidad del injerto cardiaco.