El pulmonary vein ablation catheter (PVAC) es un catéter decapolar circular que pretende simplificar el procedimiento de ablación de venas pulmonares «punto a punto».
MétodosAnálisis retrospectivo de las ablaciones de fibrilación auricular con PVAC en un centro. Se avanzó el PVAC a la aurícula izquierda mediante punción transeptal. Se identificaron los antros con una angiografía retrógrada. Se analizó la conducción venoatrial mediante estimulación desde el seno coronario y desde la aurícula derecha alta o en ritmo sinusal.
ResultadosSe incluyeron 18 pacientes (58±15 años) con fibrilación auricular paroxística (13; 72%) o persistente (5; 28%). Se ablacionaron 65 venas. Tras abatir los electrogramas antrales, se demostró bloqueo en 47 venas (72%). Hubo un hematoma femoral como única complicación. El 70% de los pacientes mantienen ritmo sinusal sin fármacos antiarrítmicos (seguimiento 5±1,9 meses).
DiscusiónLa experiencia inicial con el PVAC es positiva con respecto a su eficacia y seguridad.
Pulmonary vein ablation catheter (PVAC) is a circular decapolar catheter developed in order to simplify the “point by point” pulmonary vein ablation.
MethodsRetrospective analysis of the first atrial fibrillation ablations with PVAC in a single centre. PVAC was introduced in the left atrium through a transeptal puncture. The antra were identified by a retrograde angiography. Vein-atrium conduction was analyzed by pacing from coronary sinus and from high right atrium or sinus rhythm.
ResultsEighteen patients (58±15 years old) with paroxysmal (13; 72%) or persistent (5; 28%) atrial fibrillation were included. A total of 65 veins were ablated. After examining the antrum electrograms, block was demonstrated in 47 veins (72%). There was a femoral haematoma as a single complication. The majority (70%) of the patients remained in sinus rhythm without antiarrhythmic drugs (follow-up 5±1.9 months).
DiscussionOur first experience regarding safety and efficacy is positive.
La ablación de venas pulmonares realizada tradicionalmente «punto a punto» es un procedimiento largo que precisa varios catéteres en la aurícula izquierda, un navegador y una curva de aprendizaje prolongada, y en él es difícil obtener lesiones contiguas y transmurales. Existen nuevas herramientas específicamente diseñadas para la ablación de venas pulmonares que pretenden simplificar el procedimiento. Una de ellas es el pulmonary vein ablation catéter troga(PVAC, Ablation Frontiers, Medtronic). Es un catéter 9F deflectable con 5 pares de electrodos dispuestos en un sistema circular que avanza sobre una guía hasta cada vena pulmonar (fig. 1A).
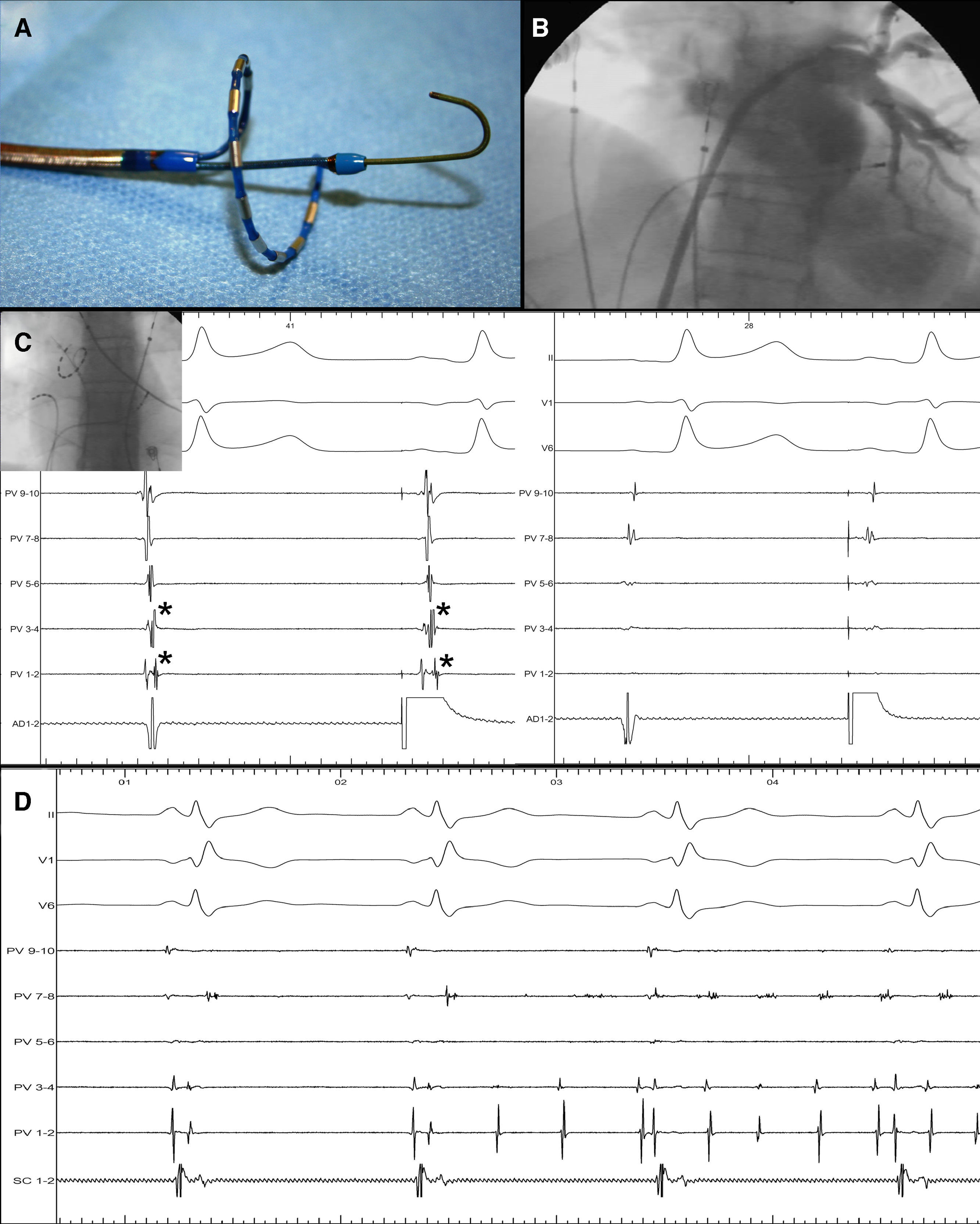
A) Catéter pulmonary vein ablation catheter (PVAC). B) Ejemplo de venografía retrógrada. C) Ejemplo de desconexión en una vena superior derecha antes (a la izquierda) y después de la ablación (a la derecha). Se observa que los electrogramas auriculares disminuyen de tamaño y el electrograma venoso (*) desaparece. Nótese que la estimulación desde la aurícula derecha permite separar el componente venoso. D) Bloqueo de salida diagnosticado tras iniciarse fibrilación auricular en una de las venas ablacionadas, mientras el paciente mantiene el ritmo sinusal.
La peculiaridad principal de este catéter es que puede registrar la actividad eléctrica de las venas, y a través de una fuente específica (GENius, Ablation Frontiers, Medtronic) liberar radiofrecuencia de forma ciclada en modo bipolar (entre cada par de electrodos), permitiendo crear lesiones circunferenciales contiguas y en modo monopolar, con lo que se consigue ablacionar en profundidad. La proporción de energía liberada en bipolar y en monopolar es programable. La temperatura objetivo se mide en cada par de electrodos y está preprogramada en 60°C, de manera que la entrega de energía es automática y se autorregula en función de la temperatura objetivo en cada dipolo, sin ser nunca mayor de 10 vatios.
Actualmente son pocos los centros en España que han iniciado la ablación con esta técnica. Se presenta este estudio descriptivo cuyo objeto es la comunicación de los resultados de los primeros procedimientos de ablación de fibrilación auricular (FA) realizados con PVAC en un centro español.
MétodosSe obtuvo un escáner de venas pulmonares antes de cada ablación. Bajo anestesia general, se realizó un ecocardiograma transesofágico para descartar trombosis de la orejuela y para guiar la punción transeptal, según el protocolo habitual de nuestro laboratorio en los procedimientos de ablación de FA. Se avanzó el PVAC a la aurícula izquierda mediante punción transeptal, a través de una vaina 10F. Se realizó una angiografía retrógrada inyectando contraste en la aurícula izquierda tras inducir asistolia con adenosina (fig. 1B). Se identificaron los antros combinando los datos angiográficos y los eléctricos, en base al tamaño de los electrogramas de vena y de aurícula.
Se analizó la conducción basal en cada una de las venas. El procedimiento finalizaba tras conseguir el abatimiento de los electrogramas antrales (valoración subjetiva por el electrofisiólogo) y posteriormente la desconexión eléctrica (demostrada al menos en sentido aurícula-vena). Se analizó la conducción aurículo-venosa mediante estimulación desde el seno coronario (venas izquierdas) o desde la pared posterior de la aurícula derecha (venas derechas) (fig. 1C), y la veno-auricular mediante estimulación desde dentro de la vena o tras actividad espontánea en la vena (fig. 1D).
El seguimiento clínico fue realizado con un ECG y un Holter de 24h a los 3 y 6meses. Se mantuvo anticoagulación oral y tratamiento antiarrítmico en los 3meses posteriores a la ablación, y luego se mantenían o no en base a criterios CHADS y a la respuesta clínica, respectivamente.
Se utilizó el test de chi cuadrado con la corrección de Yates para la comparación de los porcentajes de desconexión entre los primeros y los últimos procedimientos
ResultadosSe incluyeron 18 pacientes consecutivos (edad: 58±15 años; 10 varones) con FA paroxística (13; 72%) o persistente (5; 28%), tras fracaso de al menos un antiarrítmico por ineficacia o intolerancia. El 61% estaban en tratamiento anticoagulante previo. Todos tenían una FEVI normal y un diámetro anteroposterior de aurícula izquierda medio de 39±4mm. Se ablacionaron 65 venas pulmonares, de las cuales 7 eran troncos comunes (6izquierdos y uno derecho).
Las primeras aplicaciones se realizaron por todos los pares de electrodos, con una ratio bipolar/monopolar de 4:1 o 2:1, con la precaución de ir girando el catéter de manera que el gap existente entre el primer y el último electrodo, a través de los cuales no se libera radiofrecuencia. Una vez abatidos los electrogramas del antro, las aplicaciones fueron «focales», es decir, únicamente desde el par o pares de electrodos donde se registraba conducción desde la aurícula hasta la vena. Se demostró la presencia de bloqueo, al menos de entrada, en 47 venas (72%; 6 troncos). En los primeros 8 procedimientos se demostró desconexión en 21 de 35 venas (60%), y en los últimos 8 procedimientos se demostró en 26 de 30 venas (87%), siendo esta diferencia estadísticamente significativa (p=0,034).
Se realizaron una media de 33 aplicaciones de 1min por procedimiento (10 aplicaciones por vena). Los procedimientos se prolongaron entre 135 y 360min (media 209±50min) y el tiempo de fluoroscopia fue de entre 34 y 99min (media 66±14min).
Hubo una única complicación grave: un hematoma femoral en los días siguientes al procedimiento, que requirió transfusión.
De los 10 pacientes que han completado un seguimiento superior a 3 meses (media 5±1,9 meses), 7 mantienen ritmo sinusal sin fármacos antiarrítmicos, si bien uno de ellos, en quien no se obtuvo reconexión en dos de las venas, precisó un segundo procedimiento «punto a punto». La eficacia, por tanto, de un único procedimiento PVAC es del 60%. Dos de los 3pacientes que tuvieron recurrencias experimentaron mejoría subjetiva (crisis menos frecuentes y de menor duración). Las características de los pacientes y los resultados de los procedimientos se resumen en la tabla 1.
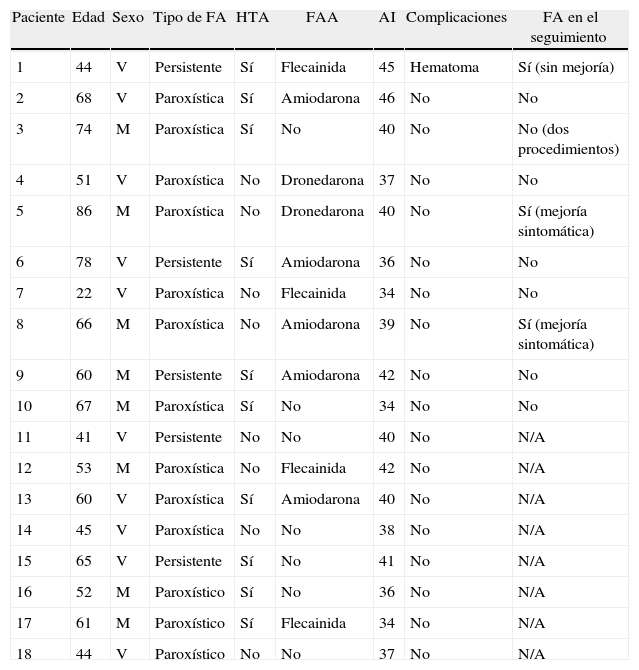
Características basales de los pacientes y resultado de la ablación
| Paciente | Edad | Sexo | Tipo de FA | HTA | FAA | AI | Complicaciones | FA en el seguimiento |
| 1 | 44 | V | Persistente | Sí | Flecainida | 45 | Hematoma | Sí (sin mejoría) |
| 2 | 68 | V | Paroxística | Sí | Amiodarona | 46 | No | No |
| 3 | 74 | M | Paroxística | Sí | No | 40 | No | No (dos procedimientos) |
| 4 | 51 | V | Paroxística | No | Dronedarona | 37 | No | No |
| 5 | 86 | M | Paroxística | No | Dronedarona | 40 | No | Sí (mejoría sintomática) |
| 6 | 78 | V | Persistente | Sí | Amiodarona | 36 | No | No |
| 7 | 22 | V | Paroxística | No | Flecainida | 34 | No | No |
| 8 | 66 | M | Paroxística | No | Amiodarona | 39 | No | Sí (mejoría sintomática) |
| 9 | 60 | M | Persistente | Sí | Amiodarona | 42 | No | No |
| 10 | 67 | M | Paroxística | Sí | No | 34 | No | No |
| 11 | 41 | V | Persistente | No | No | 40 | No | N/A |
| 12 | 53 | M | Paroxística | No | Flecainida | 42 | No | N/A |
| 13 | 60 | V | Paroxística | Sí | Amiodarona | 40 | No | N/A |
| 14 | 45 | V | Paroxística | No | No | 38 | No | N/A |
| 15 | 65 | V | Persistente | Sí | No | 41 | No | N/A |
| 16 | 52 | M | Paroxístico | Sí | No | 36 | No | N/A |
| 17 | 61 | M | Paroxístico | Sí | Flecainida | 34 | No | N/A |
| 18 | 44 | V | Paroxístico | No | No | 37 | No | N/A |
AI: diámetro anteroposterior de la aurícula izquierda en milímetros; FA: fibrilación auricular; FAA: fármacos antiarrítmicos; HTA: hipertensión arterial; M: mujer; N/A: no aplicable por seguimiento <3 meses; V: varón.
Esta técnica de ablación de venas pulmonares, en comparación con la tradicional «punto a punto», evita la manipulación de dos catéteres dentro de la aurícula izquierda, dado que el catéter de mapeo y el de ablación se integran en uno solo. Tampoco es necesaria la reconstrucción anatómica de la cavidad con un navegador. Ambos hechos permiten comenzar la ablación poco tiempo después de la punción transeptal, una vez adquirida la angiografía.
La capacidad diagnóstica del catéter es teóricamente menor que la de un catéter circular tipo «Lasso» por presentar la mitad de electrodos, una distancia interelectrodo más larga y un gap entre el primer y el último electrodo del sistema. No obstante, se pudo analizar fiablemente la conducción venoatrial en la mayoría de los pacientes y demostrar desconexión. Aun así, el porcentaje de desconexiones demostradas es bajo con respecto a otras series1,2, principalmente porque en los primeros pacientes se concentraron los esfuerzos en la manipulación del catéter (que exige una nueva curva de aprendizaje) y no se había sistematizado adecuadamente el análisis de la conducción antes y después de la ablación en cada vena. Ello explica el aumento significativo del porcentaje de venas con desconexión demostrada en la segunda mitad de los pacientes intervenidos.
Un estudio aleatorizado ha mostrado que el PVAC disminuye los tiempos del procedimiento con respecto a la ablación convencional3. Nuestros tiempos han ido acortándose de forma progresiva según iba aumentando nuestra experiencia, por lo que nuestros resultados iniciales apuntan también en esta dirección.
La única complicación grave (hematoma femoral) tuvo lugar en un paciente con obesidad mórbida en quien las punciones femorales fueron difíciles. Nuestra impresión con respecto a la seguridad del catéter es por tanto favorable, al igual que en las principales series1,2. No obstante, existen datos recientes sobre la aparición de embolias cerebrales subclínicas tras la ablación con PVAC4,5 (en torno al 38%), que pueden abrir un debate sobre su seguridad en el futuro.
LimitacionesLas limitaciones del estudio son el escaso número de pacientes, el tratarse de un análisis retrospectivo, así como de un seguimiento clínico relativamente corto y realizado con sistemas de monitorización de ventana estrecha.
ConclusiónLos resultados a medio plazo en cuanto a la eficacia y seguridad de nuestros primeros procedimientos con PVAC han sido favorables.
Conflicto de interesesLa Dra. Marta de Riva es titular de una beca de investigación de Medtronic. Los Dres. López-Gil, Salguero y Arribas han recibido honorarios de Medtronic en el pasado, en concepto de contratos de consultoría y formación. El resto de los autores no manifiestan conflictos de intereses.