El término insuficiencia cardiaca (IC) avanzada se refiere a aquellos pacientes con compromiso circulatorio clínicamente significativo que pueden requerir trasplante cardíaco ortotópico (TCO), terapia inotrópica intravenosa continua o intermitente, asistencia ventricular mecánica (AVM), cirugía del remodelado ventricular o terapia paliativa1.
Los pacientes con IC avanzada o refractaria al tratamiento médico óptimo presentan una elevada morbimortalidad. El TCO es el único tratamiento que mejora el pronóstico en estos casos, pero solo puede aplicarse a un número reducido de pacientes. Por este motivo la AVM se ha convertido en una de las mejores opciones para pacientes con IC avanzada. También hemos asistido recientemente a la presentación de nuevas técnicas percutáneas para el tratamiento del remodelado ventricular.
Asistencia ventricular mecánicaLa AVM se define como todos aquellos dispositivos capaces de generar flujo circulatorio para sustituir parcial o totalmente la función del corazón en situaciones agudas o crónicas de fracaso cardiaco severo que no responde a otros tratamientos. Las AVM pueden proporcionar apoyo hemodinámico al ventrículo izquierdo (VI), al ventrículo derecho (VD) o a ambos, e incluso pueden sustituir completamente sus funciones tras la explantación cardiaca2,3.
¿Cuáles son las estrategias de implantación de la asistencia ventricular mecánica?- 1.
Como puente al trasplante cardiaco (PTC)
La estrategia fundamental para la implantación de una AVM es de forma temporal como puente al TCO ante la presencia de shock cardiogénico (SC) a pesar de dosis máximas de inotrópicos y balón de contrapulsación intraaórtico (BCIAo).
- 2.
Como puente a la recuperación
El uso de la AVM es una opción en aquellas situaciones clínicas en las que podemos conseguir una recuperación del funcionalismo cardíaco, como la miocarditis aguda, el fallo cardíaco poscardiotomía, el fallo agudo del injerto pos-TCO, el infarto agudo de miocardio (IAM) y la miocardiopatía periparto.
- 3.
Como puente a la decisión
Ante la dificultad de discernir si el fallo multiorgánico asociado a un shock cardiogénico es reversible, se debe evaluar la decisión de implantar una AVM temporal para poder confirmar si las contraindicaciones para un TCO son agudas, transitorias y potencialmente reversibles.
- 4.
Como terapia definitiva o de destino (TD)
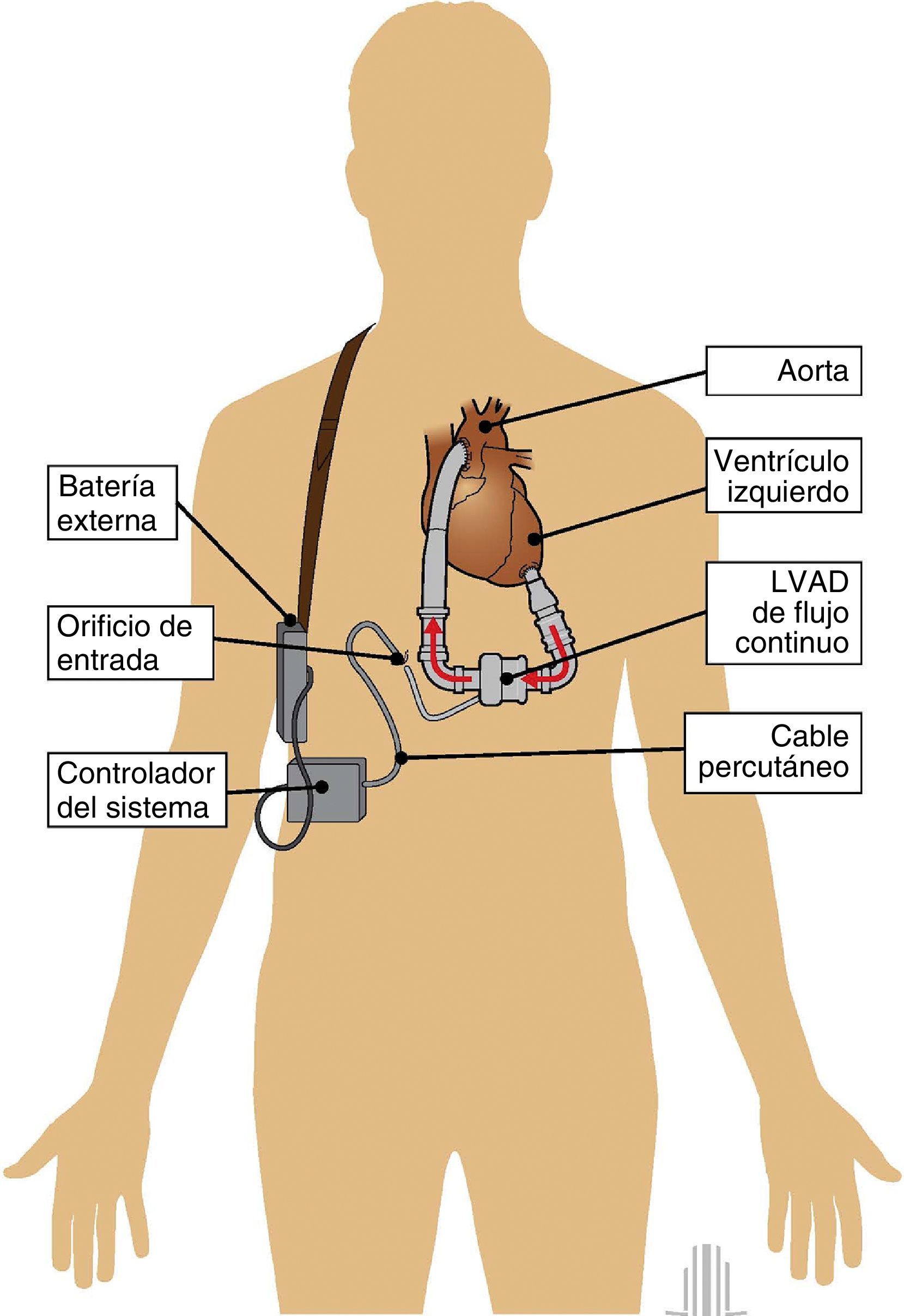
La AVM como soporte del VI mediante bombas de flujo continuo se ha convertido en una opción eficaz y permanente para los pacientes con IC avanzada. Su función es reemplazar el corazón insuficiente con objeto de poder alcanzar un gasto cardíaco óptimo (fig. 1).
A lo largo de estos años hemos visto un crecimiento exponencial del uso de AVM como TD en pacientes con IC avanzada. En el último registro de la Interagency Registry for Mechanically Assisted Circulatory Support (INTERMACS) se describen más de 10.000 pacientes, de los cuales el 40% son indicación como TD. Con el avance de la tecnología se han conseguido mejores resultados, lográndose supervivencias a 1 y 2 años del 80 y del 70%, respectivamente4.
- 5.
Como puente a ser candidato (bridge to candidacy)
Existen diferentes escenarios clínicos en los cuales es difícil prever la evolución final del paciente tras la implantación de una AVM. Ante la incertidumbre clínica, esta terminología facilita la comunicación sobre las opciones potenciales con el paciente y/o la familia.
- 6.
Como puente al puente
Esta estrategia se plantea en pacientes que llegan en situación crítica y a los que se implanta una AVM de corta duración. Tras la mejora neurológica y de los órganos del paciente, se puede plantear el TCO. Una vez descartadas las potenciales contraindicaciones para el mismo y si no se ha recuperado la función cardiaca del paciente, habría que evaluar una AVM de larga duración como PTC.
- 1.
Indicaciones según la escala de INTERMACS
Tras la creación de registro INTERMACS en el año 2006, este ha jugado un papel decisivo en la estandarización de las definiciones en los perfiles de riesgo de los pacientes candidatos a una AVM. La clasificación INTERMACS tiene 7 categorías según el perfil clínico del paciente, junto 3 factores que ayudan a establecer el pronóstico: si se ha requerido un soporte circulatorio temporal, las hospitalizaciones repetidas y la presencia de arritmias graves2,3.
- 2.
Indicaciones de implante urgente de la asistencia ventricular mecánica
La indicación de implantar una AVM y el momento idóneo debe ser tomada por un equipo multidisciplinar ante diferentes situaciones clínicas2,3.
SC post-IAM o en un paciente con IC o que presenta una descompensación, con los siguientes parámetros:
- •
Criterios hemodinámicos:
- -
Índice cardiaco inferior a 2 l/min/m2.
- -
Presión arterial sistólica inferior a 90mmHg o media inferior a 60mmHg.
- -
Presión capilar pulmonar superior a 20mmHg.
- -
Oliguria (diuresis <30ml/h) a pesar de tratamiento diurético.
- -
- •
Implante de BCIAo.
- •
Máximo tratamiento inotrópico.
- •
Revascularización máxima percutánea o quirúrgica.
- •
Candidato a TCO.
- •
Poscardiotomía: siempre que se considere que hay miocardio con capacidad de recuperar su función con la AVM.
Existen diferentes sistemas que se pueden diferenciar por su modo de funcionamiento, tipo de soporte, estrategia de uso y durabilidad (tablas 1 y 2)2.
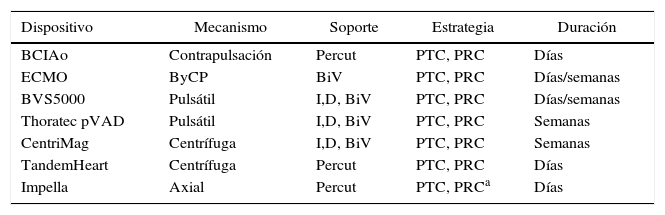
Dispositivos de AVM para soporte hemodinámico de corta duración
| Dispositivo | Mecanismo | Soporte | Estrategia | Duración |
|---|---|---|---|---|
| BCIAo | Contrapulsación | Percut | PTC, PRC | Días |
| ECMO | ByCP | BiV | PTC, PRC | Días/semanas |
| BVS5000 | Pulsátil | I,D, BiV | PTC, PRC | Días/semanas |
| Thoratec pVAD | Pulsátil | I,D, BiV | PTC, PRC | Semanas |
| CentriMag | Centrífuga | I,D, BiV | PTC, PRC | Semanas |
| TandemHeart | Centrífuga | Percut | PTC, PRC | Días |
| Impella | Axial | Percut | PTC, PRCa | Días |
AVM: asistencia ventricular mecánica; BCIAo: balón de contrapulsación intraaórtico; ByCP: bypass cardiopulmonar; D:derecha; ECMO: extracorporeal membrane oxygenator; I: izquierda; Percut: soporte circulatorio percutáneo; PRC: puente a la recuperación; PTC: puente al trasplante cardíaco.
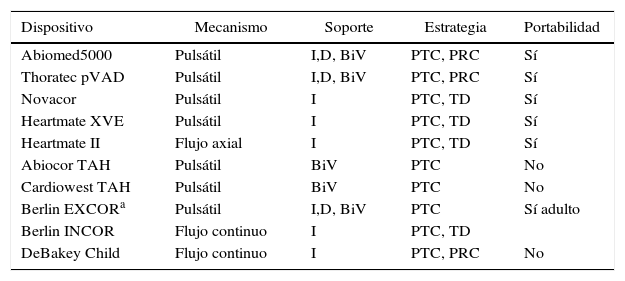
Dispositivos de AVM para soporte hemodinámico de media-larga duración
| Dispositivo | Mecanismo | Soporte | Estrategia | Portabilidad |
|---|---|---|---|---|
| Abiomed5000 | Pulsátil | I,D, BiV | PTC, PRC | Sí |
| Thoratec pVAD | Pulsátil | I,D, BiV | PTC, PRC | Sí |
| Novacor | Pulsátil | I | PTC, TD | Sí |
| Heartmate XVE | Pulsátil | I | PTC, TD | Sí |
| Heartmate II | Flujo axial | I | PTC, TD | Sí |
| Abiocor TAH | Pulsátil | BiV | PTC | No |
| Cardiowest TAH | Pulsátil | BiV | PTC | No |
| Berlin EXCORa | Pulsátil | I,D, BiV | PTC | Sí adulto |
| Berlin INCOR | Flujo continuo | I | PTC, TD | |
| DeBakey Child | Flujo continuo | I | PTC, PRC | No |
AVM: asistencia ventricular mecánica; D: derecha; I: izquierda; Percut: soporte circulatorio percutáneo; PRC: puente a la recuperación; PTC: puente al trasplante cardíaco; TAH: total artificial heart; TD: terapia de destino.
- 1.
Sistemas de flujo continuo
Bombas de rodillos
El extracorporeal membrane oxigenator (ECMO) es un sistema ampliamente disponible que utiliza las mismas cánulas, conexiones y cabeza rotora que la máquina de cirugía extracorpórea convencional. El ECMO es una AVM que se usa tanto en población adulta como pediátrica, y sustituye simultáneamente tanto la función cardiaca como la pulmonar al estar provisto de un oxigenador.
Bombas centrífugas (Levitronix CentriMag, Tandem-Heart, HeartWare HVAD): son dispositivos de flujo continuo en los que la sangre es impulsada por la inercia derivada de un vórtice creado artificialmente. No producen hemólisis importante y, según el dispositivo, pueden utilizarse durante breves períodos de días, semanas y hasta años.
Sistemas axiales
Estos dispositivos emplean una cánula con una turbina eléctrica en su interior que, girando a gran velocidad, expulsa por inercia la sangre desde el VI a la aorta. Pueden generar gastos de hasta 10 l/min y son fácilmente implantables por su pequeño tamaño, además de ser duraderos. Están controlados y alimentados desde consolas portátiles y se han utilizado en numerosos casos como TD, y con ellos se han conseguido buenas supervivencias.
- 2.
Sistemas de flujo pulsátil
También llamados ventrículos artificiales, son AVM complejas con válvulas de entrada y salida similares a las prótesis valvulares convencionales. Han sido usados en aplicaciones a largo plazo; ofrecen un soporte durante días a meses y, en un pequeño número de casos, durante años. La energía que impulsa la sangre es neumática (Abiomed BVS 5000, Thoratec VAD System, Excor Berlin Heart). No obstante, estos sistemas están quedando cada vez más obsoletos delante de las bombas de flujo continuo.
- 3.
Corazón artificial total (CAT)
Actualmente hay 3 dispositivos: Abiocor, Syncardia o CardioWest y Carmat. Su implante es muy complejo y precisa la extracción del corazón nativo y su sustitución total. El Syncardia o CardioWest consiste en un dispositivo neumático implantado en posición ortotópica, con una carcasa rígida que contiene una doble cámara esférica de poliuretano, válvulas y conexiones transcutáneas a la consola de control que monitoriza las presiones y el funcionamiento de la bomba. Su principal limitación es su gran tamaño, que impide su uso en pacientes con una superficie corporal inferior a 1,5 m2.
- 1.
Problemas hemorrágicos, hematológicos y neurológicos
La mayoría de las AVM precisan anticoagulación y antiagregación plaquetaria. Por este motivo, los episodios de sangrado complican su implantación. Hay una incidencia de hemorragia perioperatoria en el 30% y sangrado gastrointestinal entre el 19-40%. El ictus isquémico puede llegar a tener una incidencia del 8%, y el ictus hemorrágico es una complicación grave que ha sido reportada en todos los dispositivos de flujo continuo (2-11%)2,3.
- 2.
Infecciones
La infección de los cables que conectan la bomba con el sistema eléctrico de baterías, especialmente en el lugar de su salida a través de la piel, sigue siendo uno de los talones de Aquiles de estos dispositivos. Este tipo de infecciones siguen siendo un problema significativo, ya que la incidencia más baja está alrededor del 11%. La prevención es sumamente importante, por lo que se precisa el cuidado meticuloso del lugar de salida del cable, así como evitar la tracción del cable de transmisión2,3.
- 3.
Problemas valvulares y arritmias
En el caso de una insuficiencia tricuspídea de grado moderado-severo al implantar una bomba de flujo continuo, muchos grupos realizan rutinariamente anuloplastia de la válvula tricúspide. En el caso de una insuficiencia aórtica (IAo) moderada-severa al implantar la bomba de flujo continuo se recomienda su corrección, ya sea mediante el cierre de la válvula aórtica o sustitución de la misma con una bioprótesis. Si no se corrige la IAo se produce la recirculación del volumen de sangre desde la cánula de salida en la raíz de la aorta hacia el VI, lo que provoca a su vez recurrencia de los síntomas de IC y sobrecarga hemodinámica del VI.
La función de una bomba de flujo continuo para soporte del VI no se ve directamente afectada por una taquicardia ventricular (TV) o una fibrilación ventricular (FV). No obstante, estas arritmias tienen el potencial de afectar negativamente a la función sistólica del VD. Por último, la configuración inapropiada por excesiva velocidad de las bombas de flujo continuo puede descomprimir excesivamente el VI, provocando fenómenos de succión y a su vez arritmias2,3.
El daño isquémico miocárdico puede conllevar una asinergia de la pared ventricular y con el tiempo se produce un cambio en la forma del VI. De esta forma el corazón se vuelve cada vez más esférico, con volúmenes ventriculares mayores y con disminución de la función contráctil, lo que conlleva disfunción ventricular y clínica de IC. A todo este proceso se le llama remodelado ventricular izquierdo, y su abordaje clínico consiste en estrategias de revascularización máximas y el tratamiento farmacológico de la IC5. Otras terapéuticas para evitar el remodelado del VI son la cirugía de reconstrucción ventricular y las nuevas técnicas percutáneas, como el PARACHUTE y el sistema REVIVENT.
Recientemente se han publicado los primeros resultados con el uso del PARACHUTE en 39 pacientes que muestra su seguridad y eficacia en reducción de volúmenes diastólicos del VI y en la mejora de la clase funcional a 3 años de seguimiento6.
El sistema REVIVENT consiste en la exclusión del área aneurismática del VI mediante la implantación quirúrgica de varios anclajes de titanio que traccionan el VI. Su acción se basa en la ley de Laplace y reduce la tensión de la pared miocárdica. Para su implante se precisa esternotomía, pero no entrar en bomba de circulación extracorpórea. Se ha desarrollado la forma percutánea de implantación no invasiva que reduce el riesgo para el paciente. Los resultados iniciales en más de 70 pacientes también muestran datos clínicos positivos, lo que ha generado expectativas para el tratamiento del remodelado ventricular de origen isquémico.