Se presenta el caso de una paciente de 55 años con insuficiencia cardiaca severa, secundaria a miocarditis, con fracción de eyección severamente deprimida, remitida a nuestro hospital para valoración pretrasplante cardiaco. Debido a la presencia de resistencias vasculares pulmonares elevadas, a pesar de la optimización del tratamiento médico vasodilatador, se decide implantar un EXCOR® como puente al trasplante. Con el presente artículo pretendemos revindicar la importancia de los dispositivos de asistencia ventricular de larga duración, para solventar la contraindicación que supone la hipertensión pulmonar severa en el trasplante cardiaco. Además, nuestra paciente presentó las 2 complicaciones de etiología inmunológica más frecuentes que pueden surgir a corto-medio plazo, exponiendo en el caso clínico las diferentes técnicas diagnósticas y las opciones de tratamiento disponibles para hacer frente al rechazo tanto humoral como celular hacia el órgano trasplantado.
We present the case of a 55 year-old patient with severe heart failure secondary to myocarditis with severely depressed ejection fraction, referred to our Hospital for Cardiac pretransplant evaluation. Due to the presence of elevated pulmonary vascular resistance despite optimization of vasodilator medical treatment, an EXCOR® was implanted as a bridge to transplantation. This article aims to highlight the importance of ventricular assist devices to solve long-term contraindication posed severe pulmonary hypertension for heart transplantation. In addition, we will discuss the complications of immune etiology that may arise in the short-medium term and the different diagnostic techniques and treatment options available to address both humoral and cellular rejection to the transplanted organ.
Mujer de 55 años sin antecedentes personales de interés, salvo reumatismo palindrómico, con factor reumatoide positivo, que ingresa en 2004 en su hospital de referencia por insuficiencia cardiaca (IC) debido a miocarditis aguda vírica, con fracción de eyección (FEVI) severamente deprimida (33%), y regurgitación mitral severa funcional. A pesar del tratamiento médico óptimo, la evolución posterior de la paciente es desfavorable, con múltiples hospitalizaciones por descompensación de IC, donde se objetiva deterioro de la función ventricular y persistencia del grado de insuficiencia mitral. Ante esta situación se decide colocación de MitraClip® con resultado no satisfactorio, permaneciendo en clase funcional III de la NYHA. Se deriva a nuestro hospital para valoración pretrasplante cardiaco.
Tras cateterismo derecho, donde se registran RVP elevadas (5 UW), que contraindican el trasplante, se optimiza el tratamiento vasodilatador (sildenafilo) y se decide implantar un segundo MitraClip®. Sin embargo, la paciente reingresa por IC, objetivándose de nuevo insuficiencia mitral severa en la ecocardiografía. En el nuevo cateterismo derecho persisten 5 UW, encontrándose en situación INTERMACS 3. Se opta, entonces, por implementar tratamiento médico (sildenafilo y bosentán inicialmente, sustituyéndose el segundo fármaco por macitentán, así como bolos de levosimendán) pero, ante la ausencia de respuesta a las medidas anteriores, se decide implantar un dispositivo de asistencia ventricular (DAV) izquierda tipo Berlin Heart EXCOR®. La indicación con la que se coloca el EXCOR®-LVAD fue la conocida como «bridge to candidacy», con el fin de disminuir las resistencias vasculares pulmonares, que suponían una contraindicación absoluta para el trasplante cardiaco, haciéndola candidata al mismo.
A los 40 días, la paciente presenta una importante mejoría, estimándose por ecocardiografía una presión arterial pulmonar media de 25mmHg. Fue tan llamativo el resultado que no se consideró necesario el estudio hemodinámico. Ante los hallazgos, pudo ser incluida en lista de espera (Alarma-1).
Al mes de la inclusión, la paciente entra en Alarma-0 debido a la aparición de trombos en la cánula de salida y a la presencia de signos de infección local en la misma. A los 5 días se realiza el trasplante cardiaco con evolución inmediata favorable en la UCI.
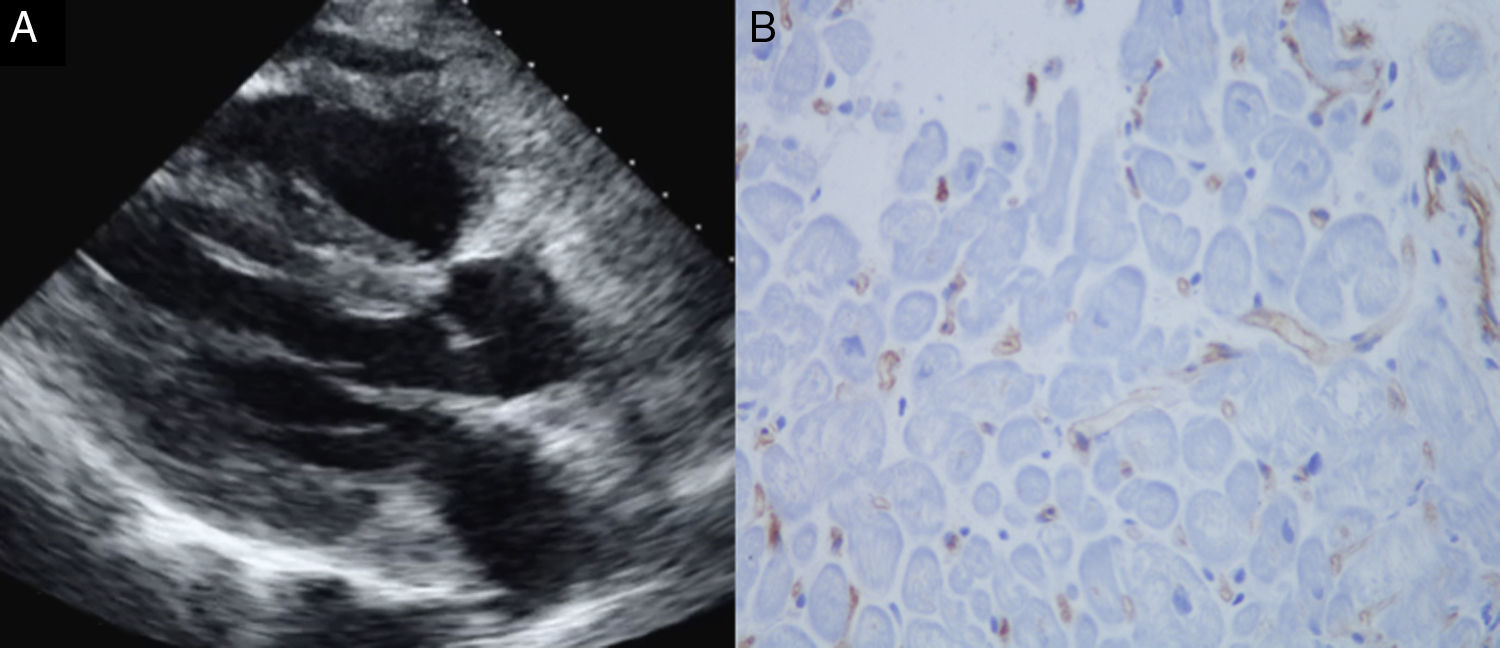
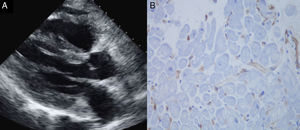
En los días posteriores comienza de nuevo con datos de IC severa y episodios frecuentes de FA que precisan medicación anti-arrítmica, objetivándose en la ecocardiografía hipertrofia severa concéntrica de ambos ventrículos (septum 18mm) (fig. 1A), no presente previamente. Esta situación se mantiene a pesar de la intensificación del tratamiento inmunosupresor (además de tacrolimus+everolimus+prednisona oral, se administran bolos de corticoides intravenosos), realizándose biopsia endomiocárdica que es informada como rechazo humoral agudo C4d+ estadio 3 (pAMR2, de una escala entre pAMR0 y pAMR3) (fig. 1B), que explica la resistencia al tratamiento corticoideo.
Con respecto a su situación inmunológica, existía compatibilidad ABO, y presentaba anticuerpos anti-HLA donante específicos de clase I, concretamente frente a la molécula A2 del donante, en alta carga.
La paciente respondió favorablemente a plasmaféresis (4 sesiones con recambio de 2.500ml por solución de albúmina, bien toleradas) y rituximab (2 dosis de 375mg/m2), además de la optimización del tratamiento inmunosupresor basal y los bolos de corticoides iv. Normalizó el grosor miocárdico y la FEVI, desapareciendo las crisis de FA, y decidiéndose ante la buena evolución, el alta a domicilio a los 21 días del inicio del tratamiento.
Desde entonces, y a 6 meses del alta, ha continuado con revisiones periódicas, con biopsias endomiocárdicas de control, sin rechazo humoral, aunque con datos de rechazo celular de grado ligero (IB), controlado actualmente con tratamiento inmunosupresor (triple terapia).
DiscusiónLa experiencia del DAV de media-larga duración Berlin Heart EXCOR®, muestra resultados favorables en su indicación, como puente al trasplante, en aquellos pacientes con contraindicación para el mismo por RVP elevadas, refractarias a tratamiento médico-óptimo1, siendo los principales efectos adversos infecciones y fenómenos embólicos, que requieren extracción del sistema.
En pacientes trasplantados con sospecha de rechazo agudo del injerto (IC, FA, …), resistente a tratamiento corticoideo, debemos pensar en la posibilidad de rechazo agudo humoral C4d+2, entidad poco frecuente, pero que debe estar siempre presente en el diagnóstico diferencial.
El ser portador de un dispositivo de asistencia ventricular constituye uno de los factores de riesgo conocidos para el desarrollo de rechazo humoral, así como el hecho de ser multípara y haber necesitado múltiples trasfusiones de hemoderivados.
En esta situación, las sesiones de plasmaféresis3 y el tratamiento con anticuerpos monoclonales han demostrado efecto beneficioso con resolución del cuadro4,5. En cualquier caso, el paciente trasplantado requiere seguimiento estrecho, para diagnosticar y poder tratar si aparecen complicaciones inmunológicas a medio-largo plazo.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.