Implantar asistencias ventriculares (AV) en situaciones anatómicas no convencionales asociadas a cardiopatía congénita puede constituir un problema para obtener un funcionamiento óptimo de la AV. Reparar la cardiopatía al mismo tiempo puede solventar estos inconvenientes.
Describimos un caso de un niño de 3 años afecto de insuficiencia cardiaca terminal, secundaria a miocardiopatía restrictiva, y de drenaje venoso pulmonar anómalo parcial (DVPAP) derecho donde se realizó una intervención conjunta para la resolución del DVPAP y la colocación de una AV izquierda como puente a trasplante, ya que, el implante de una AV aislada habría dejado sin reparar un cortocircuito importante izquierda-derecha, que alteraría el funcionamiento de la AV.
El empleo de AV en pacientes con insuficiencia cardiaca terminal y cardiopatía congénita, como puente al trasplante, es una alternativa terapéutica que en ciertas ocasiones precisa la reparación de las anomalías congénitas para lograr un funcionamiento óptimo de la asistencia.
Implantation of heart ventricular assists device (VAD) in unconventional anatomical situations associated with congenital heart disease may be a problem to obtain optimal functioning of the VAD. Repairing heart disease at the same time can solve these problems.
We describe the case of a 3-year-old boy with end-stage heart failure, secondary to restrictive cardiomyopathy, and partial right-sided abnormal pulmonary venous connection (PAPVC), where a joint intervention was performed to resolve PAPVC and the placement of a left VAD as bridge to transplant, since the implantation of an isolated VAD would have left without repair a major left-right shunt, which would alter the functioning of the VAD.
The use of VAD in patients with end-stage heart failure and congenital heart disease, as a bridge to transplantation, is a therapeutic alternative that sometimes requires the repair of congenital anomalies to achieve optimal performance.
El primer trasplante cardiaco infantil se realizó en 1967 y desde entonces tanto la técnica quirúrgica como las indicaciones, los tratamientos farmacológicos adyuvantes y el tipo de pacientes han evolucionado y cambiado, pero sigue presente la escasez de órganos para pacientes pediátricos afectos de cardiopatía estructural congénita asociada, hecho que conlleva que permanezcan en lista de espera para trasplante cardiaco más tiempo del deseado, presenten descompensaciones y precisen en bastantes ocasiones una asistencia ventricular (AV) mecánica1,2, para conseguir un correcto soporte como puente al trasplante. Actualmente, en este grupo de pacientes, hasta en la mitad de los casos3,4 se precisa un dispositivo de asistencia, y como es conocido su empleo no es indefinido ni está exento de complicaciones5.
La asociación de un fracaso tipo miocardiopatía y una cardiopatía congénita estructural, debe hacernos plantear una estrategia y un abordaje individualizado para cada paciente6, valorar qué tipo de AV emplear, pero sobre todo establecer si es necesario reparar o paliar la cardiopatía estructural de base para que el funcionamiento de la AV sea óptimo. En muchas ocasiones, estos pacientes han sido sometidos a cirugías y están corregidos o paliados7, pero otros no lo están y es en ellos donde hay que valorar si la reparación quirúrgica es necesaria. Esto a veces no mejora el pronóstico del paciente per se, aunque sí optimiza el funcionamiento de la AV y disminuye sus complicaciones.
ObjetivoEn este caso clínico se plantea la problemática donde un niño con miocardiopatía restrictiva severa y un drenaje venoso pulmonar anómalo parcial (DVPAP) no reparado precisaba una AV para llegar al trasplante cardiaco. El objetivo es describir el proceso y la intervención conjunta para la resolución del DVPAP y la colocación de AV izquierda como puente al trasplante.
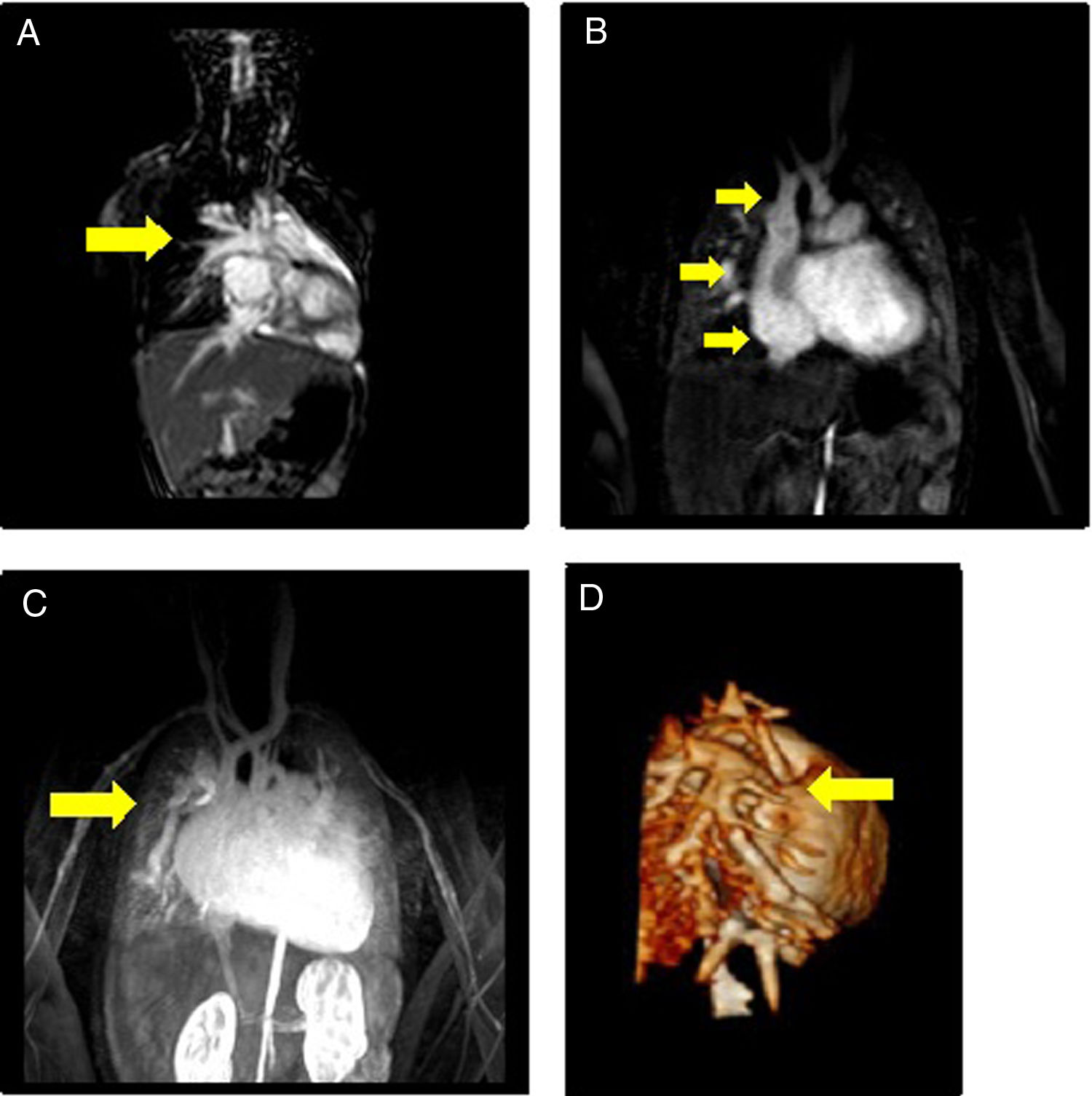
Caso clínicoSe trata de un niño de 3 años sin cardiopatía previa conocida, que comienza con cuadro de insuficiencia cardiaca congestiva secundaria a miocardiopatía restrictiva y DVPAP derecho a vena cava superior sin comunicación interauricular (CIA), que evoluciona hacia fase terminal. Elevación de presiones de llenado derechas e izquierdas, resistencias pulmonares normales, disfunción diastólica restrictiva severa del ventrículo izquierdo y presencia en la resonancia magnética cardiaca de drenaje venoso anómalo de lóbulos pulmonares derechos superior y medio, con dilatación significativa de ambas aurículas y del ventrículo derecho (fig. 1).
Imágenes de resonancia magnética (A-C son cortes sagitales): A) Arteria pulmonar. B) Vena cava superior, aurícula derecha y vena cava inferior. C) Desembocadura de venas pulmonares (VVPP) anómalas a vena cava superior. D) Reconstrucción tridimensional de la llegada de las VVPP anómalas a vena cava superior.
Tras finalizar el estudio pre-trasplante, fue aceptado en sesión médico-quirúrgica y listado para trasplante cardiaco. Durante el tiempo de espera, desarrolló empeoramiento rápido, progresivo y con ausencia de respuesta al tratamiento convencional de la insuficiencia cardiaca, múltiples infecciones intercurrentes, deterioro respiratorio, varios ingresos hospitalarios en planta y en unidad de cuidados intensivos para intensificar tratamiento anticongestivo intravenoso y proporcionar soporte ventilatorio.
El paciente se encontraba en situación de insuficiencia cardiaca secundaria a miocardiopatía restrictiva y DVPAP derecho no reparado, en franca, agresiva e irreversible progresión a estadio terminal. Por ello, ante esta veloz evolución se decidió la implantación de una AV para conseguir soporte hemodinámico hasta la llegada del órgano8. Dentro de las posibles alternativas del mercado en relación a dispositivos9, estrategias terapéuticas, y teniendo en cuenta las características del paciente5,10, así como la experiencia de nuestro centro se optó por implantar una AV izquierda de larga duración y la reparación del DVPAP derecho en el mismo acto quirúrgico, para obtener por una parte soporte hemodinámico hasta la llegada del órgano, y por otra, con la corrección de la cardiopatía, reproducir la fisiología correcta e intentar optimizar el funcionamiento de la AV.
La intervención consistió en el implante de una AV izquierda tipo Berlin-Heart Excor® y en la reparación completa del DVPAP derecho mediante técnica de Warden modificada. Presentaba cardiomegalia severa con dilatación biventricular importante y DVPAP de 3 venas pulmonares (VVPP) provenientes de los lóbulos superior y medio derechos, inferiores a la vena ácigos y a 10-15mm de la confluencia vena cava superior-aurícula derecha, y ausencia de CIA. Mediante una esternotomía media se canularon la aorta, la vena innominada y la vena cava inferior para establecer la circulación extracorpórea con pinzado aórtico. Se realizó transección de la cava superior por encima de las VVPP, se suturó el cabo proximal y se septo el tabique interauricular con un parche de politetrafluoroetileno expandido desde la entrada de la cava superior hasta una CIA creada previamente, redirigiendo el flujo desde las VVPP anómalas hacia la aurícula izquierda. Se reimplantó la cava en la orejuela derecha mediante un conducto de Dacron® y se preservó la vena ácigos, de cara a las conexiones del futuro trasplante bicavo.
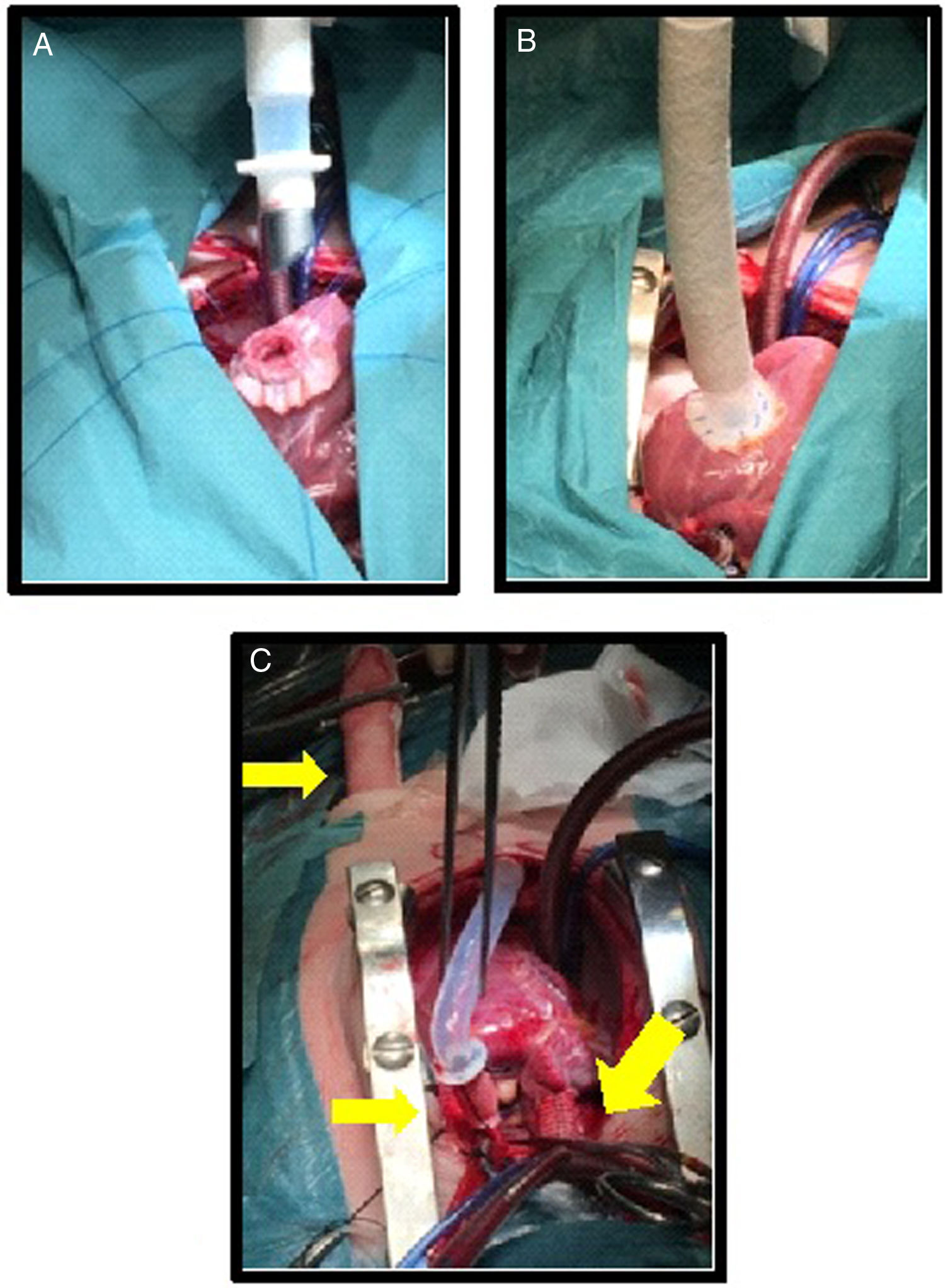
A continuación, se implantó la cánula del ápex del ventrículo izquierdo, y se despinzó el corazón. Una vez latiendo y con pinzado aórtico parcial se implantó la cánula en aorta. Seguidamente se conectaron las cánulas del ventrículo izquierdo y aorta con la bomba ventricular paracorpórea de 15cc (fig. 2), comprobándose mediante ecocardiografía intraoperatoria el correcto funcionamiento de la AV y la adecuada respuesta del corazón (mejoría en la función contráctil biventricular, sin dilatación del ventrículo derecho ni aumento de insuficiencia tricúspide y presión pulmonar estimada de 40mmHg), por lo que no consideramos necesario implantar otra bomba para asistir al lado derecho.
Esternotomía media, imágenes intraoperatorias: A) Orificio en ápex del ventrículo izquierdo para colocar cánula 9/12mm de Berlin-Heart Excor®. B) Cánula del ventrículo izquierdo insertada. C) Reparación DVPAP (Warden modificado) e implante de cánula 6mm en aorta con clampaje aórtico parcial.
Tras la reparación del DVPAP y el implante de la AV izquierda, el paciente presentó recuperación de las reagudizaciones de la insuficiencia cardiaca y de las infecciones intercurrentes consiguiendo estabilizar el proceso de deterioro y ganar tiempo para llegar al trasplante. Un mes más tarde, se realizó el trasplante cardiaco ortotópico con técnica bicava, respetando la reparación del DVPAP derecho, pero eliminando cualquier vestigio de material protésico que pudiera ser susceptible de infección (endocarditis) en un entorno de inmunosupresión debido al trasplante. No se presentaron incidencias reseñables y la evolución postoperatoria fue satisfactoria, permitiendo que el niño fuese dado de alta a domicilio.
DiscusiónComo ha sido referido en múltiples publicaciones, el empleo de la AV en pacientes pediátricos afectos de insuficiencia cardiaca terminal refractaria a tratamiento convencional ha crecido significativamente en los últimos años, tanto como puente a recuperación, decisión o trasplante2.
En el supuesto concreto del empleo de AV en pacientes con insuficiencia cardiaca terminal acompañado de cardiopatía congénita, como puente a trasplante, hasta donde llega nuestro conocimiento hay escasa experiencia reportada de reparación conjunta de una cardiopatía congénita junto al implante de una AV como puente al trasplante cardiaco3.
El razonamiento establecido implicaba que implantar solamente una AV izquierda aislada habría dejado sin reparar un cortocircuito importante izquierda-derecha. La reparación del shunt asociaría disminución del hiperaflujo al lado derecho del corazón, y mejoría en la función del ventrículo derecho en una situación de correcta oxigenación. Con esta estrategia el ventrículo derecho respondió adecuadamente y evitamos una AV derecha, al tiempo que redujimos otras complicaciones asociadas a un doble Berlin-Heart Excor®.
Satisfactoriamente se pudo llevar a cabo la intervención propuesta (reparación del DVPAP derecho e implante de AV izquierda), brindando soporte hemodinámico que permitió la supervivencia del paciente, recuperación de las afecciones intercurrentes y realizar el trasplante ortotópico un mes después. La evolución postrasplante fue favorable, siendo dado de alta a domicilio a los 34 días. Los controles ecocardiográficos, angiográficos, analíticos y clínicos posteriores fueron adecuados hasta la fecha de comunicación de este caso clínico.
Creemos que la reparación de las anomalías congénitas es una alternativa terapéutica que en ciertas ocasiones se precisa para lograr un funcionamiento óptimo de la asistencia.
Responsabilidades éticasLos autores declaran que para la publicación de este trabajo obtuvieron el consentimiento informado de los progenitores del paciente y que siguieron los protocolos de su centro de trabajo sobre la publicación de datos de pacientes, preservando en todo momento su anonimato.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.