La reparación de la coartación aórtica con/sin hipoplasia de arco en neonatos/lactantes es controvertida. Los abordajes quirúrgicos mediante toracotomía o esternotomía, respectivamente, evitan o requieren circulación extracorpórea. Presentamos nuestros resultados, analizando si existen diferencias significativas entre ambas técnicas.
MétodosEstudio retrospectivo; 132 lactantes con anatomía de corazón biventricular y cirugía del arco aórtico durante el período 2004-2014: 65-esternotomías y 67 toracotomías. En las esternotomías usamos rutinariamente perfusión cerebral selectiva (PCS). La parada circulatoria es excepcional.
ResultadosGrupos no homogéneos: el abordaje esternal asocia más cardiopatía, más hipoplasia de arco y mayor complejidad. Técnicas quirúrgicas: por esternotomía 83% pacientes recibieron anastomosis término-lateral y por toracotomía 87% anastomosis termino-terminal. Mortalidad hospitalaria: 10,7% esternotomía y 4,5% toracotomía (ns). Morbilidad hospitalaria: sin diferencias en complicaciones neurológicas ni en recoartación precoz, pero las esternotomías tienen más lesión del nervio recurrente laríngeo y mayores estancias hospitalarias que las toracotomías (p<0,05). Seguimiento medio: 37±26 meses. Tres pacientes mueren tardíamente (1 esternotomía, 2 toracotomía). Las toracotomías presentan más recoartación tardía (30%) que las esternotomías (17%) (ns) y habitualmente se soluciona con angioplastia percutánea.
ConclusionesLa PCS en cirugía del arco por esternotomía permite realizar la anastomosis con precisión. Respecto a la toracotomía, no hay diferencia significativa en la mortalidad hospitalaria ni en las secuelas neurológicas, pero sí asocia mayor lesión recurrencial y un postoperatorio prolongado. La permeabilidad del arco a largo plazo es mejor con la esternotomía pero esta diferencia no resultó significativa. Recomendamos esternotomía media con PCS si existe hipoplasia del arco proximal y/o si hay cardiopatía asociada que requiera cirugía.
Surgical approach of infants with coarctation±hypoplastic aortic arch is a challenge. Choosing between sternotomy or thoracotomy is associated, respectively, with the need of extracorporeal circulation or not. We present our results and compare both surgical techniques.
MethodsA retrospective analysis was conducted on 132 infants with biventricular heart and surgical reconstruction of aortic arch during 2004-2014: 65-sternotomy and 67-thoracotomy. Selective cerebral perfusion (SCP) was used in the sternotomy group instead of circulatory arrest in order to minimize cerebral injury.
ResultsBoth groups are different: sternotomy-group has more associated cardiac diseases, more hypoplastic arch, and higher complexity. Surgical techniques: sternotomy patients received an end-to-side anastomosis (83%), and thoracotomy patients received an end-to-end anastomosis (87%). Hospital mortality: 10.7% in sternotomy and 4.5% in thoracotomy (ns). Hospital morbidity: there are no differences in neurological complications or early re-coarctation, but sternotomy-group presents more recurrent laryngeal nerve lesion and longer postoperative stay than thoracotomies (P<.05). Mean follow-up: 37±26 months. Three patients died in the follow-up (1-sternotomy, 2-thoracotomy). Late re-coarctation is more frequent in thoracotomy (30%) than in sternotomy (17%) (ns) and is generally treated with percutaneous angioplasty.
ConclusionsSCP in sternotomy approach of arch surgery allows the surgeon to perform the anastomosis in a bloodless field, and preserves neurological function. Sternotomy, in comparison with thoracotomy, has similar mortality, a higher recurrent nerve lesion, and prolonged hospital stay. Sternotomy seems to be associated with a lower incidence of re-coarctation in the follow-up. Sternotomy with SCP is recommended if there is hypoplastic aortic arch and/or associated cardiac diseases needing surgery.
La patología del arco aórtico constituye un espectro de anomalías anatómicas que originan la presencia de un estrechamiento u obstrucción de la luz aórtica, localizada o a distintos niveles, suponiendo el 5-8% del total de las cardiopatías congénitas. La sintomatología suele aparecer en período neonatal cuando la perfusión de la aorta descendente es ductus dependiente y el cierre del mismo tras el nacimiento desencadena un cuadro de bajo gasto severo, al depender de su permeabilidad la circulación de la aorta toraco-abdominal. Ante la sospecha de esta patología, es obligado instaurar tratamiento con prostaglandina-E1 intravenosa (PGE1), para mantener abierto el ductus, recuperar y estabilizar al niño antes de la cirugía.
Las cardiopatías congénitas que incluyen coartación1 con hipoplasia de arco asociada y las interrupciones de arco aórtico (IAA), siguen siendo un reto quirúrgico actualmente2. Pueden presentarse bien de manera aislada o asociadas a otras malformaciones intracardíacas. Es frecuente que exista cierto grado de hipoplasia de cavidades izquierdas con válvula aórtica bicúspide y las distintas anomalías que conforman el síndrome de Shone.
La reconstrucción quirúrgica del arco aórtico en neonatos y lactantes exige gran precisión técnica para realizar una anastomosis perfecta en arterias de escasos milímetros de calibre. Las alternativas quirúrgicas implican un abordaje por toracotomía o esternotomía media, que, respectivamente, evitan o requieren usar la circulación extracorpórea (CEC). En general, el arco distal y el itsmo se amplían bien desde los 2 abordajes, pero el arco proximal solo puede ser ampliado eficazmente por esternotomía.
La reconstrucción del arco aórtico por esternotomía históricamente se realizaba con hipotermia profunda y parada circulatoria, que como efecto secundario puede causar daño cerebral. Este último se manifiesta como un desarrollo neurológico alterado tanto en el sistema motor, en las áreas del lenguaje y/o en la coordinación visual-espacial3. Las técnicas de perfusión cerebral selectiva (PCS)4 permiten realizar la anastomosis aórtica con visibilidad similar a la que proporciona la parada circulatoria exanguinando el campo quirúrgico, pero sin el «efecto cronómetro» que en esta última modalidad obligaba al cirujano a tardar menos de 30-45 min para evitar el daño cerebral. Con la PCS, alcanzada la temperatura cerebral y sistémica deseada, la perfusión arterial se reduce limitándose al tronco braquiocefálico. El cerebro recibe siempre sangre oxigenada, protegiéndose gracias a la competencia del polígono de Willis, y el resto del cuerpo se perfunde por circulación colateral desde el tronco innominado. La PCS permite reducir o eliminar la parada circulatoria.
El objetivo de este trabajo es describir nuestra experiencia con estas operaciones, los resultados quirúrgicos inmediatos y el seguimiento posterior, analizando si existen diferencias significativas entre ambos abordajes (esternotomía y toracotomía).
MétodosRevisamos retrospectivamente las intervenciones quirúrgicas del arco aórtico realizadas en menores de un año durante la última década en nuestro hospital. Excluimos a los pacientes con anatomía univentricular para homogeneizar el grupo de estudio.
Seguimos los criterios de Moulaert et al.5 para definir como hipoplasia del arco aórtico proximal, distal o del itsmo al que tiene un diámetro menor que el 60, el 50 y el 40% del de la aorta ascendente respectivamente. Clasificamos las IAA según Celoria y Patton6.
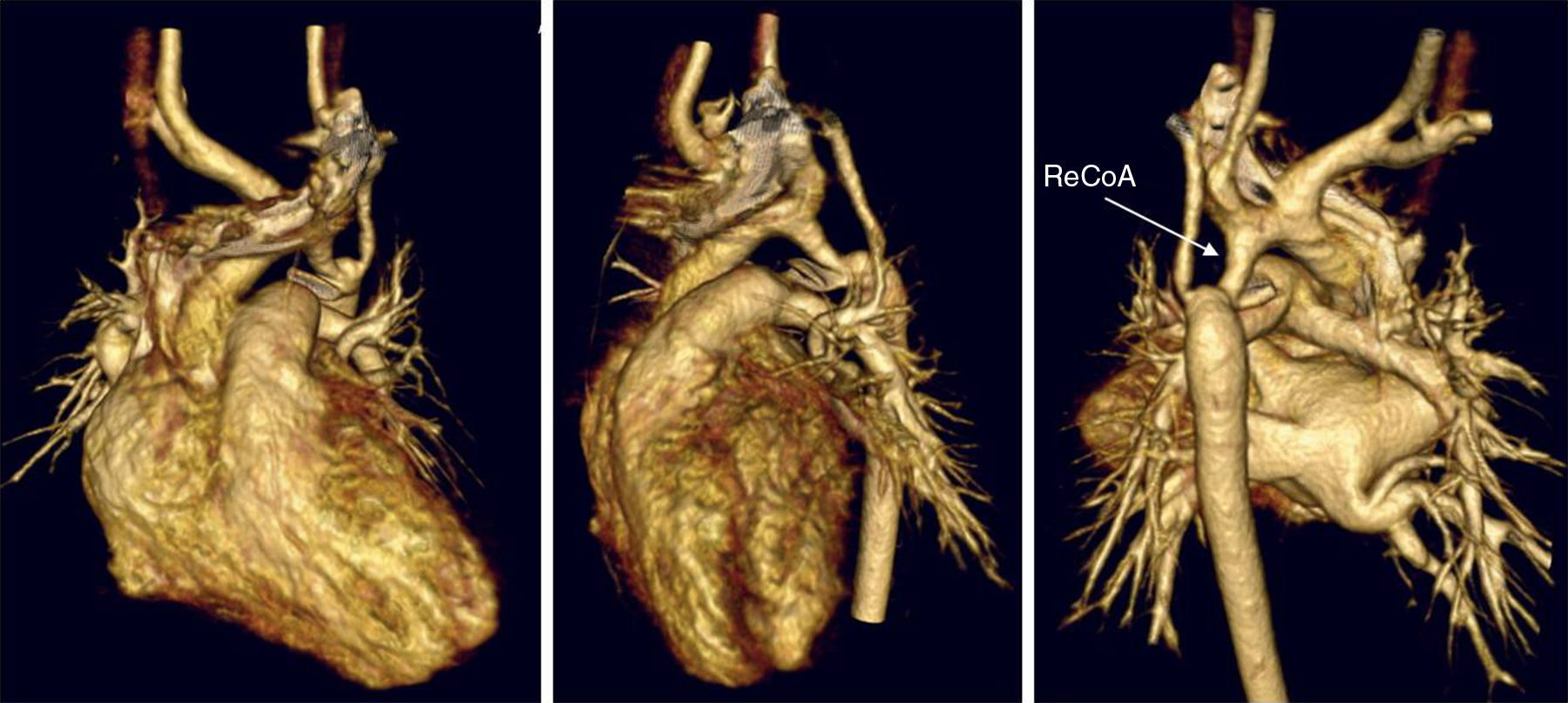
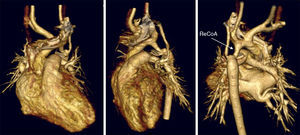
El diagnóstico de estos pacientes se basa en la clínica y la exploración física. Ante un neonato pálido y mal perfundido, con disminución o ausencia de pulsos en los miembros inferiores y clínica de bajo gasto cardíaco y shock, hay que descartar patología del arco aórtico. La ecocardiografía transtorácica habitualmente será diagnóstica: mide los diámetros aórticos en sus distintas porciones, los gradientes patológicos con extensión diastólica, el flujo en aorta descendente, valora la existencia de ductus y de patología asociada. En casos seleccionados en los que persistan dudas anatómicas con la ecocardiografía, otras técnicas de imagen como la tomografía computarizada nos ayudarán en el diagnóstico (fig. 1).
Ante la sospecha de esta patología, se debe instaurar tratamiento con PGE1 por vía intravenosa, para mantener abierto el ductus, recuperar y estabilizar al niño antes de la cirugía. El tratamiento médico va dirigido a corregir las alteraciones del equilibrio ácido-base y normalizar la creatinina.
Indicamos reparación quirúrgica neonatal si aparecen síntomas o se requiere perfusión de PGE1 mantenida. En niños asintomáticos y sin PGE1, haremos la operación superado el mes de vida. Abordamos por toracotomía la coartación aislada±hipoplasia de arco distal y las IAA-A. Intervenimos por esternotomía media con CEC y PCS la coartación con hipoplasia de arco proximal o el arco bovino, la IAA-B o C, y/o si existe cardiopatía asociada que requiera cirugía concomitante.
Los pacientes que se reparan mediante toracotomía izquierda, habitualmente reciben una resección de la coartación y sutura término-terminal extendida7. Menos frecuentes son otras técnicas, como la aortoplastia con parche sintético, o con parche de subclavia izquierda (Waldhausen).
Los pacientes que son reparados mediante esternotomía requieren CEC e hipotermia moderada-severa y la anastomosis aórtica se hace con PCS generalmente de manera término-lateral (avance aórtico) o término-terminal8. En el momento de realizar la anastomosis aórtica comienza la PCS, con perfusión exclusiva por el tronco braquiocefálico, disminuyendo el flujo de CEC al 30-40% del total correspondiente a la temperatura del paciente. Durante la PCS la presión arterial radial derecha y la saturación cerebral nos informan de la adecuada perfusión cerebral. La perfusión del resto del cuerpo en esos momentos depende de la circulación colateral desde el tronco braquiocefálico. El uso de la PCS nos permite hacer la anastomosis aórtica en un campo exangüe, eliminar completamente el tejido ductal, manteniendo en todo momento la perfusión cerebral con sangre oxigenada.
Todos los pacientes se siguieron posteriormente en consultas externas de cardiología, con exploración física y neurológica, empleando ecocardiografía transtorácica para valoración cardíaca y del arco aórtico. No perdimos información de ningún paciente en las revisiones, por tanto, el seguimiento es completo en el 100% de los casos.
Estudiamos en nuestros pacientes diversas variables pre, intra y postoperatorias, analizando con especial interés la cirugía realizada y sus resultados, en cuanto a morbimortalidad hospitalaria y el seguimiento a medio plazo. Para el análisis estadístico hemos utilizado el programa SPSS versión 15.0 (SPSS Inc. Chicago 2007). Se expresan de forma descriptiva las variables estudiadas, presentando las cuantitativas como media±desviación estándar, y las cualitativas en porcentajes. La comparación entre los grupos se ha realizado mediante las pruebas estadísticas de la chi al cuadrado, el test de Fischer o la prueba de t de Student, según precise cada caso. La supervivencia actuarial y los pacientes libres de reintervención se muestran con curvas de Kaplan-Meier.
ResultadosPresentamos un estudio retrospectivo de las historias clínicas de 132 neonatos y lactantes (edad igual o menor a 12 meses) con corazón anatómicamente biventricular, en los que se realizó reconstrucción quirúrgica del arco aórtico durante el período 2004-2014: 65 fueron operados mediante esternotomía y los 67 restantes mediante toracotomía.
Grupo operado por esternotomíaLos pacientes tenían una edad media de 1,1±1,8 meses (rango: 4 días-9 meses), siendo más de la mitad (45, 69%) neonatos (≤ 30 días), y pesaban 3,3±1,3kg (rango: 1,6-9kg). El 55% (36) fueron varones.
Solo en el 29% de los casos la coartación con arco aórtico hipoplásico fue una patología aislada. El 71% restante asociaba cardiopatías diversas, siendo lo más frecuente una comunicación interventricular (CIV).
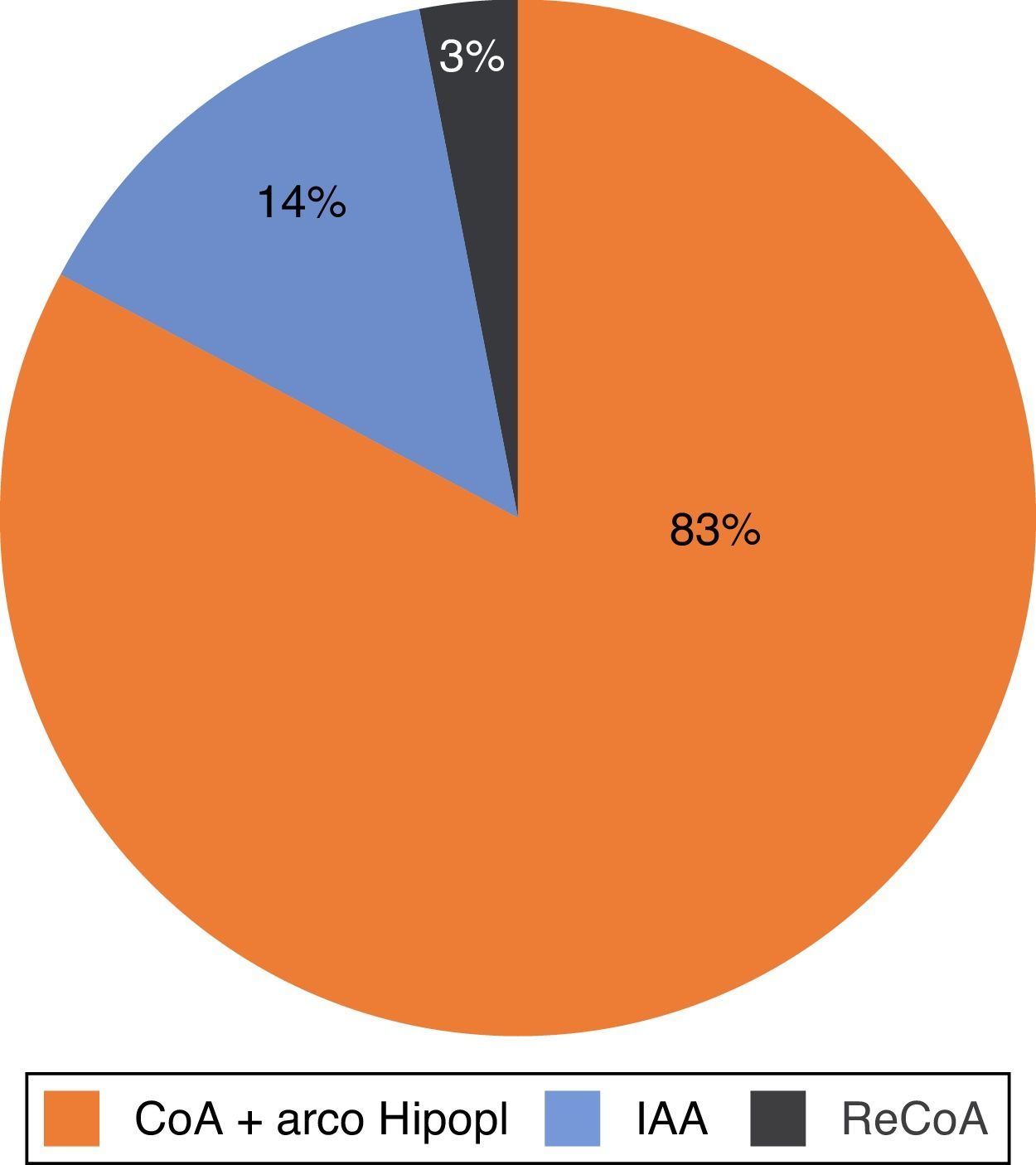
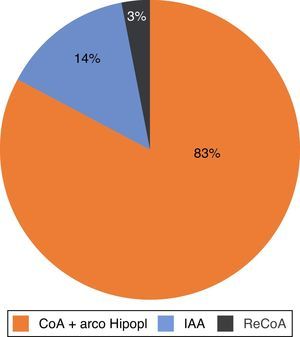
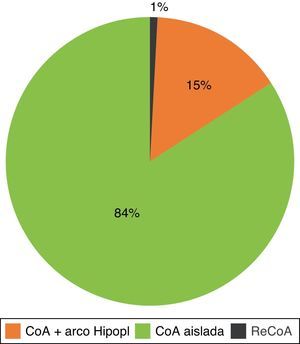
Atendiendo a la anatomía del arco aórtico, la mayoría presentaba coartación aórtica con arco hipoplásico, seguida por IAA, y recoartación posquirúrgica en orden descendente de frecuencia (fig. 2). El 71% de los niños necesitaron perfusión de PGE1 para mantener el ductus abierto, y a través de este la perfusión de la aorta distal.
Todos estos pacientes se operaron con CEC. La cánula arterial se colocó directamente en el tronco innominado en 55 pacientes (85%), y en los 10 restantes (15%) se colocó en la aorta ascendente progresándola al tronco braquiocefálico durante la anastomosis aórtica. La canulación venosa se hizo a través de la aurícula derecha hasta las cavas. Tanto el enfriamiento como el calentamiento se hicieron progresivamente; el control, el ajuste del pH y los gases se hicieron con la estrategia α-stat. En la mayoría de los casos se pinzó la aorta y se paró el corazón mediante cardioplejía para completar la anastomosis aórtica y el resto de la cirugía asociada (en 4 pacientes se hizo la anastomosis con el corazón latiendo sin pinzar la aorta).
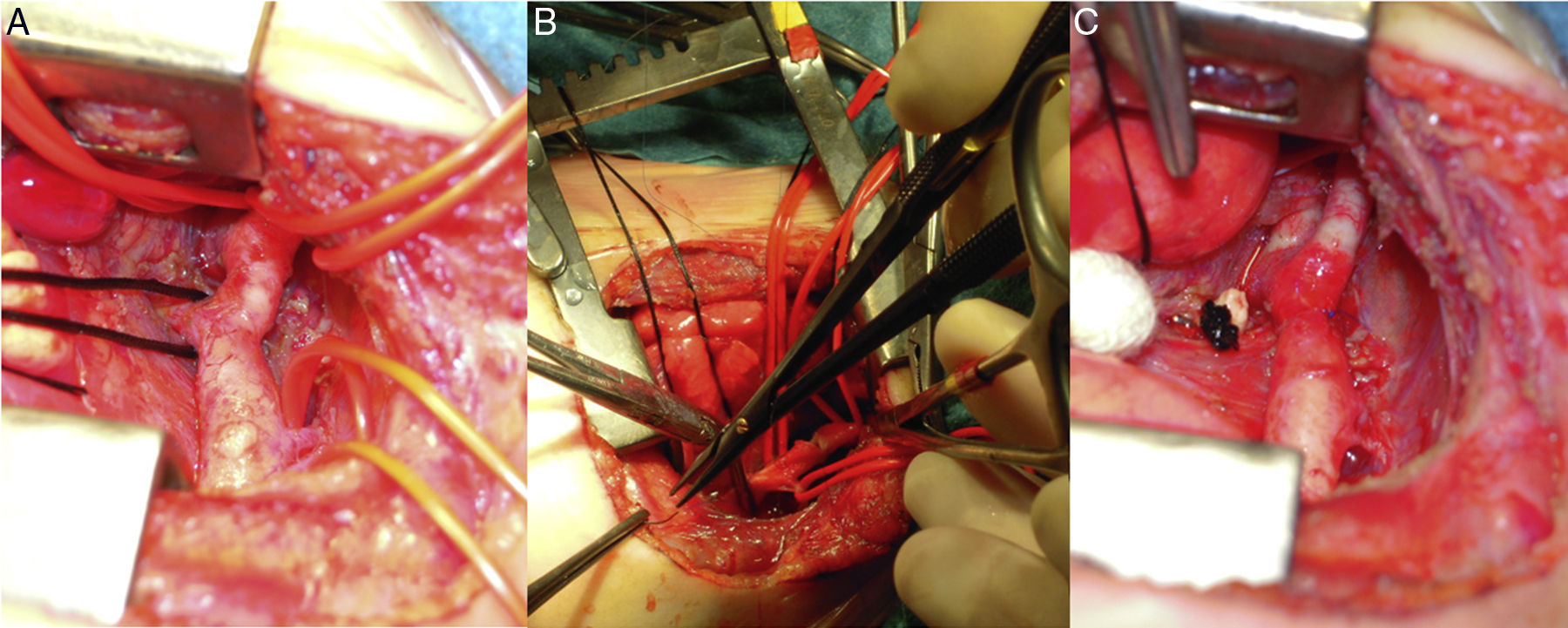
En la reconstrucción quirúrgica del arco, se hizo anastomosis término-lateral (avance aórtico) (fig. 3) en 54 pacientes (83%), sutura término-terminal en 10 (15,5%) y aortoplastia con parche en 1 (1,5%). Recibieron cirugía asociada 56 pacientes (86%): cierre de defectos septales, reparación completa según Jatene de D-transposición de grandes arterias, etc.
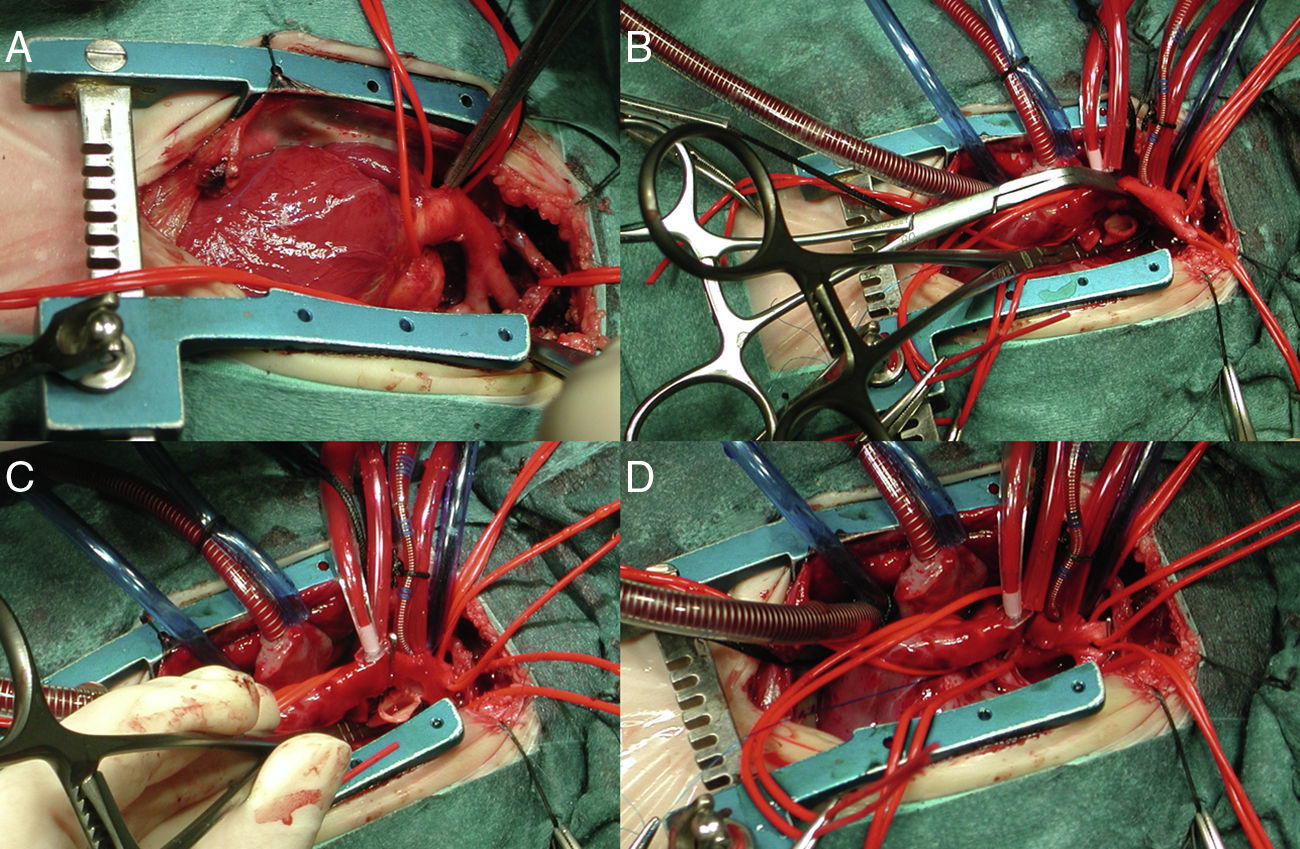
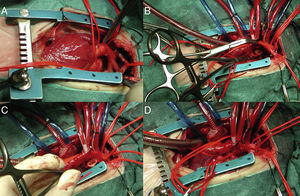
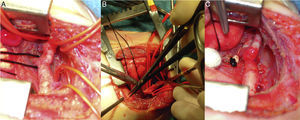
Imágenes intraoperatorias de neonato con D-transposición de grandes arterias+comunicación interventricular+interrupción de arco aórtico tipo A, operado por esternotomía. Vista del arco tras la apertura del pericardio (A). Cánula arterial en tronco braquiocefálico y cánulas venosas en ambas cavas, pinzadas la aorta ascendente y la descendente con el tejido ductal resecado (B). Anastomosis latero-terminal (avance aórtico) observándose las bocas anastomóticas (C) y anastomosis completa habiendo retirado la pinza distal (D).
Los tiempos quirúrgicos medios ± desviación estándar fueron 146±79 min de CEC, y 67±50 min de pinzado aórtico. La PCS duró una media de 31±8 min (rango: 18-63), a una temperatura mínima rectal de 22±2°C, manteniendo flujos de 30-40ml/kg/min. Se realizó hemodilución parcial, con hematocritos mínimos de 26±2,7% durante la CEC.
La estimación del riesgo quirúrgico según la escala de RACHS-19 sitúa al 98,5% de nuestros pacientes en la categoría 4, que tiene una mortalidad hospitalaria (MH) esperada del 19,4%. La mortalidad real de nuestro grupo fue del 10,7%, ya que fallecieron 7 pacientes durante el ingreso hospitalario, todos ellos operados con menos de 1,5 meses. Especialmente letal fue la anatomía de Taussig-Bing+coartación como causa de fallecimiento en 4 pacientes, hipertensión pulmonar severa en 2 y bronquiolitis severa por virus respiratorio sincitial en otra paciente.
En 26 niños (40%) se dejó el tórax abierto de manera electiva, para cerrarlo diferidamente el 2.°-3.er día en la Unidad de Cuidados Intensivos. La media de extubación es el 5.° día, del alta de cuidados intensivos el día 13 y del alta hospitalaria el día 29 postoperatorio.
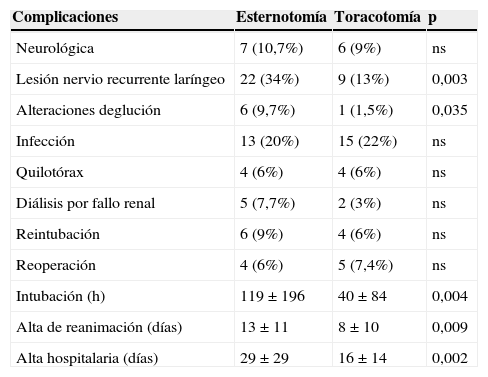
Con respecto a la morbilidad del postoperatorio inmediato (véase la tabla 1), destacamos complicación neurológica en 7 pacientes (10,7%) y lesión del nervio recurrente laríngeo izquierdo en 22 (34%). Observamos recoartación precoz en 5 niños (7,7%): 2 necesitaron reintervención quirúrgica los días +1 y +40, respectivamente, realizándose aortoplastia con parche; los otros 3 se solucionaron percutáneamente (angioplastia con balón). Se reoperó a 4 pacientes en el postoperatorio inmediato: 3 precisaron aortoplastia con parche (2 recoartaciones comentadas previamente y una estenosis de aorta ascendente distal al avance) y uno cierre de CIV.
Morbilidad hospitalaria de los pacientes operados del arco aórtico por esternotomía o por toracotomía
| Complicaciones | Esternotomía | Toracotomía | p |
|---|---|---|---|
| Neurológica | 7 (10,7%) | 6 (9%) | ns |
| Lesión nervio recurrente laríngeo | 22 (34%) | 9 (13%) | 0,003 |
| Alteraciones deglución | 6 (9,7%) | 1 (1,5%) | 0,035 |
| Infección | 13 (20%) | 15 (22%) | ns |
| Quilotórax | 4 (6%) | 4 (6%) | ns |
| Diálisis por fallo renal | 5 (7,7%) | 2 (3%) | ns |
| Reintubación | 6 (9%) | 4 (6%) | ns |
| Reoperación | 4 (6%) | 5 (7,4%) | ns |
| Intubación (h) | 119±196 | 40±84 | 0,004 |
| Alta de reanimación (días) | 13±11 | 8±10 | 0,009 |
| Alta hospitalaria (días) | 29±29 | 16±14 | 0,002 |
Se expresa el número de pacientes y entre paréntesis el porcentaje. En la columna de la derecha se expresa el valor p.
ns: no significativa.
El seguimiento medio, excluida la MH, es de 35±24 meses. La mortalidad tardía fue del 1,7% (un paciente con síndrome de Shone severo, operado de Ross-Konno a los 5 meses tras avance aórtico, fallece por hipertensión pulmonar severa refractaria a tratamiento).
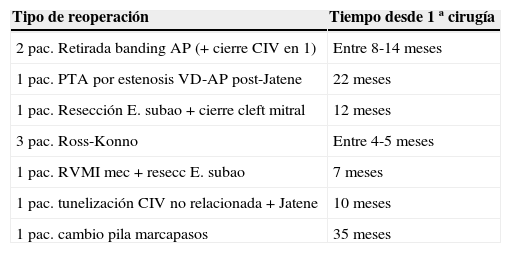
En la evolución posterior se han recoartado 10 pacientes (17%), precisando todos los casos angioplastia percutánea con balón entre los 3-11 meses poscirugía. Durante este tiempo además se ha reoperado a 10 pacientes (17%) por complicaciones de su cardiopatía asociada, manteniendo adecuada permeabilidad del arco todos ellos (véase la tabla 2). Generalmente, estos pacientes asocian cierto grado de hipoplasia del corazón izquierdo, que es causa frecuente de sus reoperaciones.
Reoperaciones durante el seguimiento en los pacientes operados del arco aórtico por esternotomía
| Tipo de reoperación | Tiempo desde 1ª cirugía |
|---|---|
| 2 pac. Retirada banding AP (+ cierre CIV en 1) | Entre 8-14 meses |
| 1 pac. PTA por estenosis VD-AP post-Jatene | 22 meses |
| 1 pac. Resección E. subao+cierre cleft mitral | 12 meses |
| 3 pac. Ross-Konno | Entre 4-5 meses |
| 1 pac. RVMI mec+resecc E. subao | 7 meses |
| 1 pac. tunelización CIV no relacionada+Jatene | 10 meses |
| 1 pac. cambio pila marcapasos | 35 meses |
AP: arteria pulmonar; CIV: comunicación interventricular; E. subao: estenosis subaórtica; pac: paciente; PTA: parche transanular; RVMI mec: recambio valvular mitral mecánico; VD: ventrículo derecho.
En su última revisión cardiológica, todos mantienen buen grado funcional y el gradiente pico medido en el arco es de 16±8,7mmHg.
Grupo operado por toracotomíaLos pacientes tenían una edad media de 1,4±1,9 meses (rango: 6 días-9 meses), siendo más de la mitad (45, 67%) neonatos, y pesaban 3,7±1,4kg (rango: 1,4-8kg). El 73% (49) fueron varones.
En el 75% de los casos la coartación fue una patología aislada y en el 25% restante se asociaban cardiopatías diversas (sobre todo CIV).
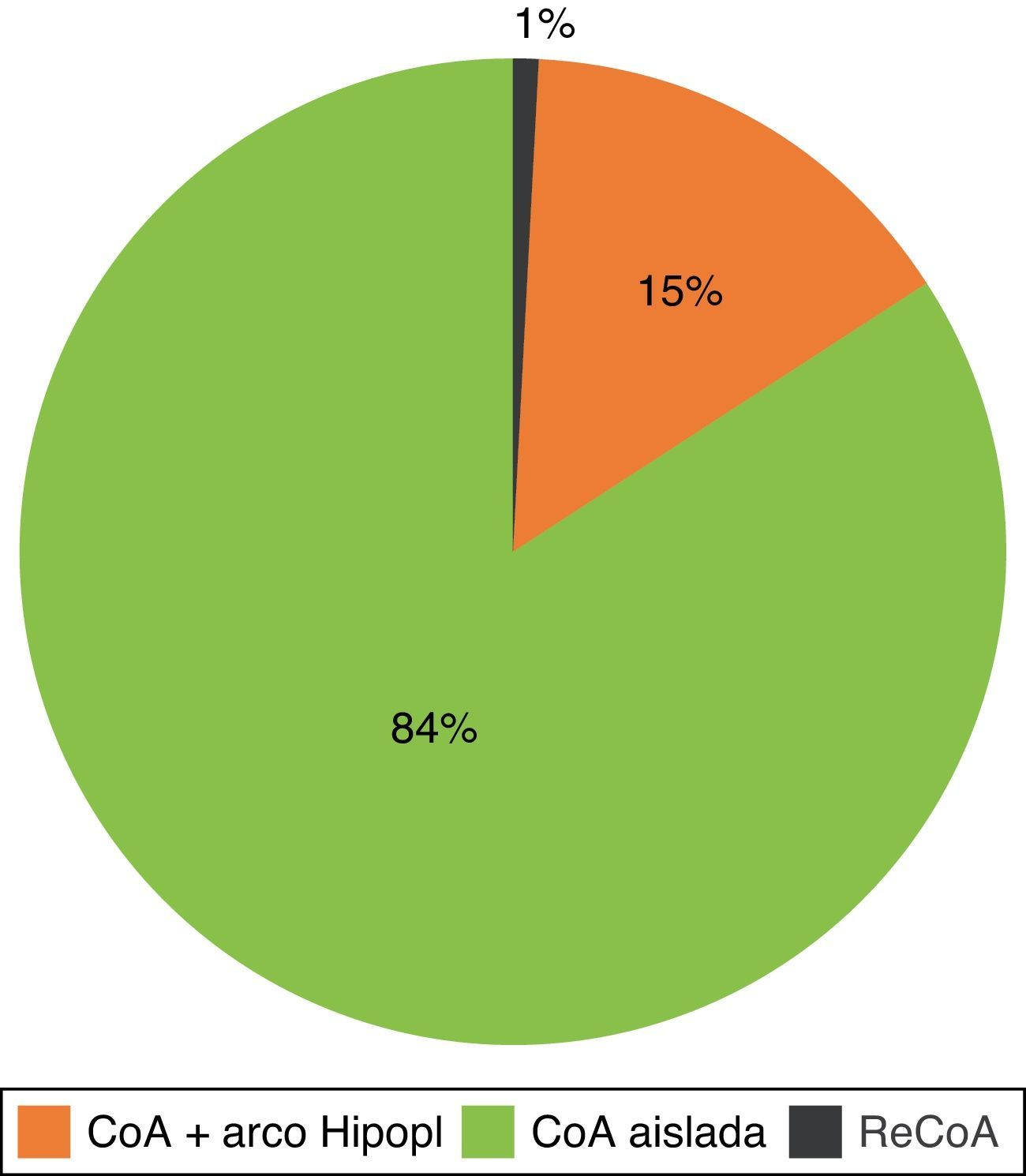
Atendiendo a la anatomía del arco aórtico, la mayoría presentaba coartación aislada, siendo menos frecuentes la coartación con arco hipoplásico y la recoartación posquirúrgica (fig. 4). El 40% de los niños necesitaron perfusión de PGE1.
Comparando a los pacientes operados por esternotomía y toracotomía, la edad y el peso son similares, pero ambos grupos no son homogéneos. El abordaje mediante esternotomía media presenta significativamente más cardiopatía asociada, más hipoplasia de arco y mayor requerimiento de PGE1 (p<0,05).
Los pacientes se intervinieron mediante toracotomía lateral izquierda a la altura del 3.er-4.° espacio intercostal. Respecto a la técnica quirúrgica, en 58 pacientes (87%) se hizo resección de la coartación y sutura término-terminal extendida (fig. 5), en 8 pacientes (12%) aortoplastia con parche y en un paciente (1%) técnica de Waldhausen. En 4 pacientes (6%) se hizo cirugía asociada, fundamentalmente cerclaje de arteria pulmonar.
Imágenes intraoperatorias: lactante de 2 meses con coartación de aorta aislada operada por toracotomía. Disección del itsmo aórtico, aorta descendente y ligamento ductal (A). Aorta pinzada proximal y distal, resecada la coartación, y realizada la parte posterior de la anastomosis (B). Anastomosis término-terminal completa y despinzada la aorta, muñón del ligamento ductal con ligadura de seda (C).
La estimación del riesgo quirúrgico según la escala de RACHS-1 sitúa al 69% de nuestros pacientes en la categoría 2, que tiene una MH esperada del 3,8% (RACHS-1: 1 en 20 pacientes [30%] y 3 en un paciente [1%]). La mortalidad real de nuestro grupo fue del 4,5%: fallecieron 3 neonatos durante el ingreso hospitalario. Aunque la MH es del 10,7% en el abordaje esternal y del 4,5% en abordaje por toracotomía, la diferencia entre ambas no es significativa (p = 0,12). Sin embargo, la complejidad medida con la escala de RASCHS-1 es significativamente más alta en grupo intervenido por esternotomía media que en el operado por toracotomía (p<0,001).
Tras la reparación del arco por toracotomía, la media de extubación es el 2.° día, del alta de intensivos es el día 8 y del alta hospitalaria el día 16 postoperatorio, todo ello significativamente inferior al grupo intervenido por esternotomía media (p<0,002). Con respecto a la morbilidad del postoperatorio inmediato (véase la tabla 1), en general, es menor respecto a los pacientes operados por vía esternal, aunque la complicación neurológica es similar. Observamos recoartación precoz en 3 niños (4,5%), tratados uno con angioplastia percutánea y los otros 2 con reintervención quirúrgica. Además, se reoperaron 3 pacientes por su cardiopatía asociada (Ross-Konno, banding pulmonar y reparación completa de canal aurículo-ventricular).
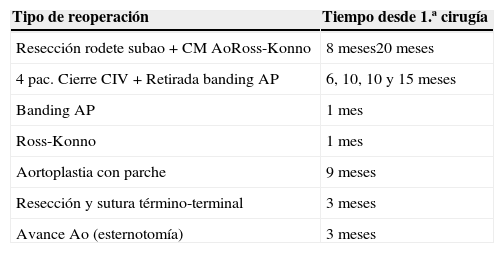
El seguimiento medio, excluida la MH es de 38±28 meses. La mortalidad tardía fue del 3% (2 pacientes). En la evolución posterior, se han recoartado 21 pacientes (31%), precisando 17 de ellos angioplastia percutánea con balón, uno angioplastia con stent y 3 otra reoperación. Durante este tiempo se ha reoperado a 10 pacientes (16%): los 3 recoartados y además otros 7 por complicaciones de su cardiopatía asociada (véase la tabla 3).
Reoperaciones durante el seguimiento en los pacientes operados del arco aórtico por toracotomía
| Tipo de reoperación | Tiempo desde 1.ª cirugía |
|---|---|
| Resección rodete subao+CM AoRoss-Konno | 8 meses20 meses |
| 4 pac. Cierre CIV+Retirada banding AP | 6, 10, 10 y 15 meses |
| Banding AP | 1 mes |
| Ross-Konno | 1 mes |
| Aortoplastia con parche | 9 meses |
| Resección y sutura término-terminal | 3 meses |
| Avance Ao (esternotomía) | 3 meses |
Ao: aórtica; AP: arteria pulmonar; CIV: comunicación interventricular; CM: comisurotomía; pac: paciente.
En su última revisión cardiológica, ningún niño muestra limitación de su actividad física, estando todos en grado funcional i, y el gradiente pico medido en el arco es de 21±9mmHg.
Centrándonos solo en la incidencia de recoartación, si comparamos ambos grupos (tabla 4), los pacientes operados por esternotomía media muestran una tendencia hacia una mayor recoartación precoz, pero menor recoartación tardía, aunque la diferencia entre ambos abordajes no es estadísticamente significativa.
DiscusiónEl manejo de la coartación±arco aórtico patológico en neonatos y lactantes continúa siendo un gran desafío para todas las personas que participan en sus cuidados10. La anatomía del arco aórtico puede ser variada, desde una estenosis localizada a nivel del itsmo aórtico (coartación) asociada o no a distintos grados de hipoplasia del arco, hasta la obstrucción completa de la luz de la aorta (interrupción)11. Son patologías complejas que habitualmente comienzan en el período neonatal tras el cierre ductal, manifestándose clínicamente como un cuadro de shock y bajo gasto sistémico. Ante la simple sospecha, es recomendable mantener abierto el ductus y trasladar al bebé a un centro con cardiología pediátrica y cirugía cardíaca infantil. Allí se estabilizará al niño, se confirmará y/o completará el diagnóstico y se elegirá el momento más adecuado para la intervención quirúrgica.
La patología del arco aórtico puede aparecer aislada o asociada a otras lesiones, como CIV, transposición de grandes arterias, doble salida del ventrículo derecho y ventrículo único. La asociación más frecuente es la válvula aórtica bicúspide, que aparece entre el 30-80% de los casos, que no suele dar problemas a corto-medio plazo, pero se asocia tardíamente a complicaciones en la aorta ascendente durante la edad adulta12.
En este grupo de edad la aortoplastia percutánea asocia a elevadas tasas de recoartación13, por lo que el tratamiento de elección es quirúrgico. Reparar el arco mediante esternotomía media o toracotomía es una decisión compleja, que implica elegir la vía de abordaje óptima en cada caso. La coartación aórtica aislada o con hipoplasia asociada del arco distal se resuelve adecuadamente con una resección y sutura término-terminal por toracotomía14.
La reparación quirúrgica por esternotomía media es obligada en los casos de hipoplasia del arco proximal y/o si existen anomalías asociadas que precisan cirugía, como una CIV significativa, transposición de grandes vasos, etc. Estas cirugías se hacen con CEC y la parte intracardíaca con pinzado aórtico y parada cardíaca cardiopléjica. Para obtener buenos resultados, la reconstrucción del arco aórtico exige una visibilidad perfecta y gran precisión técnica, puesto que se suturan arterias de escasos milímetros y tejido friable (secundario a fragilidad neonatal, persistencia de tejido ductal, retención hídrica por las prostaglandinas). Por estos motivos, tradicionalmente estas anastomosis aórticas se realizaban con hipotermia profunda y parada circulatoria. Diversos estudios han demostrado daño hipóxico-isquémico cerebral asociado a la parada circulatoria y a la duración de la misma15. La afectación neurológica tardía aparece en el 21-69% de las cardiopatías complejas reparadas en el período neonatal-infancia, y se manifiesta como problemas con el control del movimiento fino-grueso, de la integración visual-motora, problemas de atención y comportamiento, dificultad para hablar y aprender, bajo rendimiento escolar, dificultad para la integración, etc.16.
Dentro de las estrategias adoptadas para minimizar el daño cerebral en estos pacientes17, está el mantenimiento de flujos altos de perfusión y hematocritos altos durante la CEC, sustituir la parada circulatoria por la PCS y la monitorización neurológica con saturación cerebral y Doppler transcraneal18. Definimos la PCS como un conjunto de técnicas usadas junto a la CEC para perfundir el cerebro en las cirugías de reconstrucción del arco aórtico, evitando la parada circulatoria y, por tanto, minimizar el daño neurológico asociado a la misma19. De esta manera, se hace la anastomosis aórtica en un campo exangüe, eliminando el tejido ductal casi en su totalidad; en todo momento llega sangre oxigenada a la cabeza desde la cánula arterial colocada en el tronco braquiocefálico y a los órganos subdiafragmáticos por circulación colateral20. Actualmente, aunque la PCS es prometedora, ningún estudio publicado demuestra su superioridad frente a la parada circulatoria21.
Nuestra experiencia con la reparación quirúrgica del arco por esternotomía media es favorable a corto-medio plazo. Usamos un protocolo de PCS similar al descrito en otros hospitales22,23 y nuestros resultados son similares a los publicados por otros centros extranjeros. La mortalidad hospitalaria de estas cardiopatías complejas es aceptable, absolutamente mejor que la de pacientes similares operados en parada circulatoria y menor que la esperada según la escala de RACHS-1. La reconstrucción del arco por esternotomía media con CEC y PCS asegura la permeabilidad del arco en un grupo de pacientes más complejos, sin aumentar la mortalidad hospitalaria ni las complicaciones neurológicas, respecto a los arcos reparados por toracotomía. Sin embargo, y como corresponde a su mayor complejidad, este abordaje asocia un postoperatorio inmediato complicado, con tiempos de intubación y de estancia hospitalaria prolongados. Destacamos la lesión del nervio recurrente laríngeo izquierdo en el 36% de los pacientes, posiblemente relacionada con la disección y la movilización ductal y de la aorta descendente para hacer la anastomosis aórtica sin tensión. Es importante seguir la evolución de estos lactantes para valorar si posteriormente recuperan la función de la cuerda vocal, o si, por el contrario, la disfunción persiste en el tiempo, ya que puede estar relacionada con alteraciones de la deglución que padezcan estos pacientes24.
Destacamos la importancia de las anomalías cardíacas asociadas en la cirugía y su evolución posterior, ya que un número importante de pacientes (17% en nuestra serie) se reoperan por estos motivos. El seguimiento cardiológico de estos niños se debe hacer de por vida25, primeramente en las unidades de cardiología pediátrica y, posteriormente, en las unidades de cardiopatías congénitas del adulto. En las revisiones, es esencial la valoración ecocardiográfica exhaustiva tanto del arco como de la cardiopatía asociada, para establecer correctamente las indicaciones de reintervención, antes de que aparezcan síntomas o lesiones irreversibles.
Atendiendo solamente a la evolución del arco aórtico, tanto el abordaje por esternotomía como la toracotomía para su reparación quirúrgica son efectivos y duraderos, permitiendo el crecimiento de los niños con buen grado funcional. La reparación mediante toracotomía parece asociar menores cifras de recoartación precoz y mediante esternotomía media menores cifras tanto de recoartación tardía como global. Cuando aparece una recoartación, habitualmente se soluciona de manera percutánea (angioplastia con balón) y solo excepcionalmente se requiere una nueva cirugía.
ConclusionesLa reparación quirúrgica del arco por esternotomía media permite reparar casos más complejos, sin asociar mayores tasas de recoartación que la toracotomía.
El abordaje esternal con PCS permite reparar el arco y la cardiopatía asociada sin diferencias significativas en la mortalidad hospitalaria, ni de lesión neurológica, respecto al abordaje por toracotomía. Como desventaja, en la morbilidad destacan la lesión del nervio recurrente laríngeo y una prolongada hospitalización posquirúrgica.
Recomendamos abordaje esternal con CEC y PCS si el arco proximal es hipoplásico y/o si hay cardiopatía asociada que requiera cirugía. Recomendamos el abordaje por toracotomía si la coartación es aislada, el arco proximal es de buen tamaño y no se requiere cirugía intracardíaca concomitante.
El seguimiento de los pacientes es fundamental para detectar la recoartación y tratarla adecuadamente, de manera percutánea o quirúrgica. Además, un porcentaje importante de pacientes requiere nueva operación como tratamiento de su cardiopatía asociada.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.