Analizar retrospectivamente los resultados a corto y medio plazo de los pacientes en los que se realizó cirugía de revascularización miocárdica utilizando injerto de arteria mamaria bilateral.
Material y métodosEntre abril/05 y abril/14, 1.041 pacientes consecutivos fueron tratados con revascularización miocárdica aislada, en 497 (47,7%) de los cuales se utilizaron ambas arterias mamarias.
ResultadosLa edad media fue 63,3±10 años con 248 pacientes (49,9%)<65 años, 111 (22,3%) de 65-70 años y 138 (27,8%)>70 años. El 83% de las cirugías se realizó con circulación extracorpórea, con 4±1 puentes/paciente. La prevalencia de diabetes, obesidad, vasculopatía periférica y enfermedad pulmonar obstructiva crónica fue del 31, 18, 15 y 8%, respectivamente. La mortalidad hospitalaria fue del 1,4% (7/497) con EuroSCORE I medio del 4,1%. Durante el postoperatorio presentaron mediastinitis 4 pacientes (0,8%), ictus 10 pacientes (2%), infarto perioperatorio 8 pacientes (1,6%) y precisaron diálisis 13 pacientes (2,6%). No hubo diferencias significativas entre los grupos de edad. La supervivencia a 1, 5 y 7 años fue del 98, 95 y 88%, respectivamente. El análisis multivariante identificó la vasculopatía periférica (p=0,04) como factor de riesgo de mortalidad hospitalaria, y la insuficiencia renal preoperatoria (p=0,03) y un tiempo de circulación extracorpórea≥200min (p=0,004) como factores de riesgo de mediastinitis.
ConclusionesLa cirugía de revascularización miocárdica con doble mamaria presenta unos excelentes resultados a corto y medio plazo independientemente de la edad. En pacientes con elevada comorbilidad, especialmente vasculopatía e insuficiencia renal, se debería individualizar la decisión del uso de doble mamaria.
Retrospective analysis of the early and mid-term outcomes of patients undergoing isolated coronary artery bypass grafting using bilateral internal thoracic artery graft.
MethodsBetween April 2005 and April 2014, 1,041 consecutive patients underwent an isolated coronary artery bypass grafting in our institution. In 497 patients (47.7%) both internal mammary arteries were used.
ResultsMean age was 63.3±10 years, with 248 patients (49.9%)<65 years, 111 (22.3%) between 65-70 years, and 138 (27.8%)>70 years. Cardiopulmonary bypass was performed on 83%, with 4±1 grafts/patient. The prevalence of diabetes, obesity, peripheral vascular disease, and chronic obstructive pulmonary disease was 31.8%, 18%, 15.1%, and 8%, respectively. Hospital 30-day mortality was 1.4% (7/497) with a mean EuroSCORE I of 4.1%. The rates of deep sternal wound infection, stroke, myocardial infarction, and postoperative dialysis were 0.8%, 2.0%, 1.6%, and 2.6%, respectively, with no significant differences between age groups. Overall survival at 1, 5, and 7 years was 98%, 95%, and 88%, respectively. Multivariate analysis identified peripheral vascular disease (P=.04) as a risk factor for hospital mortality and preoperative renal failure (P=.03) and CPB time≥200min (P=.004) as risk factors for deep sternal wound infection.
ConclusionsThe coronary artery bypass grafting with double mammary artery has excellent early and mid-term results, regardless of age. In highly comorbid patients, especially those with vascular disease and renal failure, the indications of double mammary artery grafting should be individualised.
La cirugía de revascularización miocárdica (CRM) continúa siendo la técnica de elección en la enfermedad coronaria multivaso en pacientes con un riesgo quirúrgico aceptable. El uso del injerto de arteria mamaria interna izquierda a la arteria descendente anterior es el patrón oro de la cirugía coronaria, mejorando la supervivencia a largo plazo y reduciendo la incidencia posterior de infarto agudo de miocardio (IAM), angina recurrente y necesidad de nueva revascularización en comparación con injerto de vena safena interna1–6.
La necesidad de utilizar más de un injerto en la enfermedad coronaria multivaso sumado a la limitada permeabilidad a largo plazo de los injertos venosos y a los excelentes resultados demostrados con la arteria mamaria interna izquierda impulsaron el empleo de otros injertos arteriales para la revascularización miocárdica. Entre los injertos arteriales utilizados existe una progresiva evidencia a favor del uso de arteria mamaria interna bilateral (AMIB)7. En 1999, Lytle et al.8 demostraron que los pacientes tratados con ambas mamarias comparado con una sola mamaria e injertos venosos presentaban una mayor permeabilidad, supervivencia y libertad de reoperación a corto y largo plazo. Desde entonces han sido publicados múltiples estudios confirmando estos hallazgos, especialmente cuando el segundo injerto arterial es usado en el territorio de la arteria circunfleja7,9,10. Este beneficio en la supervivencia se extiende, incluso, hasta la segunda y la tercera década de seguimiento10,11.
Clásicamente, la limitación en la utilización de ambas mamarias en la cirugía coronaria ha sido el riesgo de aumentar la morbimortalidad postoperatoria, especialmente el incremento de la incidencia de infección profunda de la herida esternal/mediastinitis en diferentes subgrupos de riesgo (edad avanzada, sexo femenino, reoperación, obesidad, enfermedad pulmonar obstructiva crónica [EPOC] y especialmente diabetes)12,13. Sin embargo, en publicaciones recientes, con el empleo de la técnica de esqueletización de los injertos mamarios, no han encontrado diferencias significativas en la morbimortalidad postoperatoria entre injerto mamario único o doble, con una mayor supervivencia a medio-largo plazo con el uso de doble mamaria, incluidos estos subgrupos de riesgo14–17.
La evidencia actual a favor de la AMIB es reflejada inequívocamente por las guías de revascularización miocárdica europeas (revascularización arterial completa en pacientes con expectativa de vida razonable, clase IA)18 y americanas (uso de AMIB clase IIaB)19.
No obstante, el uso actual de AMIB en la práctica clínica es muy escaso, aproximadamente del 15-20% en Europa20 y menos del 5% en EE. UU.21 y la inmensa mayoría de los injertos de revascularización coronaria, a excepción de la AMI a la descendente anterior, se realizan con vena safena.
Las respuestas definitivas de la superioridad o no del uso de AMIB serán probablemente respondidas por el estudio ART22, que ha aleatorizado a 3.102 pacientes para injerto único o doble de mamaria con el objetivo primario de supervivencia a 10 años. Los resultados preliminares a un año han mostrado una mortalidad similar en ambos grupos (≈2%) con ligero aumento en la incidencia de infección esternal en el grupo asignado a injerto bilateral de mamaria (el 1,9% frente al 0,6%).
Analizamos retrospectivamente los resultados de la CRM con AMIB, determinando los predictores de riesgo de morbimortalidad hospitalaria y la supervivencia a medio plazo.
MétodosDesde abril/05 hasta abril/14, 1.041 pacientes consecutivos fueron tratados con CRM aislada por enfermedad coronaria multivaso. De estos, en 497 pacientes (47.7%) se utilizaron AMIB. Si bien se individualizó la indicación de doble mamaria, el criterio general de nuestro Centro es emplear ambas mamarias en todo paciente tratado mediante CRM aislada≤75 años sin elevada comorbilidad (fundamentalmente que no presenten varios factores de riesgo de mediastinitis, no desestimándose la indicación por la presencia aislada de un solo factor de riesgo, especialmente diabetes). En un reducido número de pacientes también se utilizaron ambas mamarias pese a no presentar indicación a priori para su uso, pero con ausencia de disponibilidad de otros injertos (p. ej., safenectomía o varices de ambas venas safenas).
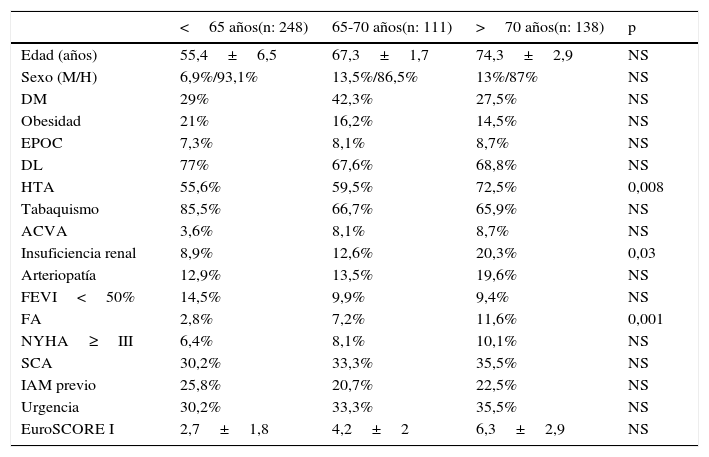
Secundariamente, para analizar los resultados en función de la edad, se estratificaron los pacientes en 3 grupos: <65 años (248 pacientes [49,9%]), entre 65-70 años (111 [22,3%]) y >70 años (138 [27,8%]).
Técnica quirúrgicaLa revascularización miocárdica se realizó con circulación extracorpórea (CEC) en el 83,7% de los pacientes. La CEC se estableció mediante canulación en aorta ascendente y venosa arteriocava a hipotermia ligera (32-34°C). La protección miocárdica durante el pinzamiento aórtico fue con cardioplejía sanguínea fría intermitente anterógrada y retrógrada. Se tendió a esqueletizar ambas arterias mamarias, utilizando la segunda arteria mamaria fundamentalmente para completar la revascularización de árbol coronario izquierdo. El resto de injertos utilizados (especialmente para el territorio de la arteria coronaria derecha) fueron de vena safena o arteria radial. El injerto de arteria radial se seleccionó para arterias coronarias ocluidas o con estenosis críticas, y fue descartado en pacientes con test de Allen patológico, hemodiálisis y enfermedad de Raynaud o Dupuytren. En nuestra serie se empleó en el 23,3% de los pacientes. La profilaxis antibiótica utilizada fue cefazolina 2g intravenosos, 30min antes del inicio de la cirugía y posteriormente cada 8h durante un máximo de 48h (o hasta que el paciente abandone la unidad de cuidados postoperatorios). En alérgicos a penicilina se sustituye por vancomicina 1g intravenoso preincisión y a las 12h.
SeguimientoLos datos clínicos, la aparición de eventos cardiovasculares definidos como recurrencia de angina, IAM y/o necesidad de nueva revascularización y la supervivencia fueron obtenidos mediante revisión de nuestra base de datos, historias clínicas, entrevistas personales y/o telefónicas con los pacientes, familiares y cardiólogos/médicos de atención primaria. Se consiguió un seguimiento del 96,3% de los pacientes supervivientes al alta hospitalaria (472/490 pacientes) con un seguimiento medio de 5,3±2,4 años.
Análisis estadísticoEl programa estadístico SPSS versión 22.0 (IBM/SPSS Inc., Chicago, IL, EE. UU.), fue utilizado para el análisis. Las variables continuas con distribución normal fueron expresadas como media±desviación típica y analizadas mediante el test t de Student. Las variables continuas con distribución no normal fueron expresadas como mediana y el rango intercuartílico y analizadas mediante pruebas no paramétricas (U de Mann-Whitney). Las variables categóricas fueron expresadas como proporciones y analizadas usando el test de χ2. Se realizó el análisis univariante de las variables perioperatorias para determinar los posibles factores de riesgo de mortalidad hospitalaria y mediastinitis estadísticamente significativos (p<0,05). Los resultados fueron sometidos a un análisis de regresión logística para determinar los factores de riesgo independientes. La supervivencia a medio plazo global y de cada grupo de edad fue expresada mediante las curvas de Kaplan-Meier.
ResultadosLas características clínicas y demográficas preoperatorias de los pacientes globales y estratificadas por edad se muestran en las tablas 1 y 2. La edad media de los pacientes fue 63,3±10 años. La prevalencia de diabetes mellitus, obesidad, vasculopatía periférica y EPOC fue de 31,8; 18; 15,1; y 8%, respectivamente. El grupo de pacientes>70 años presentaba mayor prevalencia de hipertensión arterial (p=0,008), fibrilación auricular permanente (p=0,001) e insuficiencia renal preoperatoria (p=0,03) sin diferencias significativas en el resto.
Características preoperatorias de los pacientes (n: 497)
| Edad (años) | 63,3±9,6 |
| Sexo (M/H) | 10/90% |
| DM | 31% |
| Obesidad | 18% |
| EPOC | 8% |
| DL | 73% |
| HTA | 61,2% |
| Tabaquismo | 76,1% |
| ACVA | 6,1% |
| Insuficiencia renal | 12,9% |
| Arteriopatía | 15% |
| FEVI<50% | 12,1% |
| FA | 6,5% |
| NYHA≥III | 7,8% |
| SCA | 32,5% |
| IAM previo | 24,1% |
| Urgencia | 32,5% |
| EuroSCORE I | 4,1±2,6 |
ACVA: accidente cerebrovascular agudo; DL: dislipidemia; DM: diabetes mellitus; EPOC: enfermedad pulmonar obstructiva crónica; FA: fibrilación auricular; FVC: capacidad vital forzada; FEVI: fracción de eyección ventrículo izquierdo; H: hombre; HTA: hipertensión arterial; IAM: infarto agudo de miocardio; IMC: índice de masa corporal; M: mujer; NYHA: clase funcional para disnea de la New York Heart Association; SCA: síndrome coronario agudo.
EPOC: diagnosticada mediante pruebas de función respiratoria: FEV1/FVC<70% y/o FEV1<80%.
Insuficiencia renal crónica: filtración glomerular<60ml/min/1,73m2.
Obesidad: IMC≥30kg/m2.
Características preoperatorias de los pacientes estratificados por edad
| <65 años(n: 248) | 65-70 años(n: 111) | >70 años(n: 138) | p | |
|---|---|---|---|---|
| Edad (años) | 55,4±6,5 | 67,3±1,7 | 74,3±2,9 | NS |
| Sexo (M/H) | 6,9%/93,1% | 13,5%/86,5% | 13%/87% | NS |
| DM | 29% | 42,3% | 27,5% | NS |
| Obesidad | 21% | 16,2% | 14,5% | NS |
| EPOC | 7,3% | 8,1% | 8,7% | NS |
| DL | 77% | 67,6% | 68,8% | NS |
| HTA | 55,6% | 59,5% | 72,5% | 0,008 |
| Tabaquismo | 85,5% | 66,7% | 65,9% | NS |
| ACVA | 3,6% | 8,1% | 8,7% | NS |
| Insuficiencia renal | 8,9% | 12,6% | 20,3% | 0,03 |
| Arteriopatía | 12,9% | 13,5% | 19,6% | NS |
| FEVI<50% | 14,5% | 9,9% | 9,4% | NS |
| FA | 2,8% | 7,2% | 11,6% | 0,001 |
| NYHA≥III | 6,4% | 8,1% | 10,1% | NS |
| SCA | 30,2% | 33,3% | 35,5% | NS |
| IAM previo | 25,8% | 20,7% | 22,5% | NS |
| Urgencia | 30,2% | 33,3% | 35,5% | NS |
| EuroSCORE I | 2,7±1,8 | 4,2±2 | 6,3±2,9 | NS |
ACVA: accidente cerebrovascular agudo; DL: dislipidemia; DM: diabetes mellitus; EPOC: enfermedad pulmonar obstructiva crónica; FA: fibrilación auricular; FEVI: fracción de eyección ventrículo izquierdo; H: hombre; HTA: hipertensión arterial; IAM: infarto agudo de miocardio; M: mujer; NYHA: clase funcional para disnea de la New York Heart Association; SCA: síndrome coronario agudo.
Las características intraoperatorias globales y estratificadas por edad se muestran en las tablas 3 y 4. La media de injertos/paciente fue de 3,8±0,9, realizándose una revascularización completa en el 94,8% de los pacientes. El 98,3% de las arterias mamarias internas izquierdas y derechas fueron disecadas de forma esqueletizada. En 423 pacientes (85,3%) ambas arterias mamarias fueron utilizadas para revascularizar el sistema coronario izquierdo. La AMI fue utilizada como injerto in situ en el 98,8% de los casos y la anastomosis proximal de la arteria mamaria derecha se hizo sobre el cuerpo de la AMI (como injerto en T o Y) en el 60%, la aorta ascendente en el 32,4% o in situ en el 7,6%.
Características intraoperatorias de los pacientes (n: 497)
| Con CEC | 83,7% |
| Tiempo de CEC (min) | 111,8±35,5 |
| Tiempo de isquemia (min) | 91,9±28,8 |
| Número de injertos, media | 3,8±0,9 |
| Número de injertos arteriales, media | 2,9±0,9 |
| Revascularización completa | 94,8% |
| Injerto de arteria radial | 23,3% |
| Revascularización arterial completa | 46,7% |
| Arteria mamaria esqueletizada | 98,3% |
CEC: circulación extracorpórea.
Características intraoperatorias de los pacientes estratificados por edad
| <65 años(n: 248) | 65-70 años(n: 111) | >70 años(n: 138) | p | |
|---|---|---|---|---|
| Con CEC | 83,5% | 89,2% | 79,7% | NS |
| Tiempo de CEC (min) | 115,1±36,3 | 107,3±37,3 | 109,4±31,6 | NS |
| Tiempo de isquemia (min) | 94,9±29,2 | 88,7±28,4 | 88,8±27,9 | NS |
| Número de injertos, media | 3,8±0,9 | 3,7±0,9 | 3,8±1 | NS |
| Número de injertos arteriales, media | 3±1 | 2,9±0,9 | 2,9±0,9 | NS |
| Revascularización completa | 94,8% | 94,6% | 94,9% | NS |
| Injerto de arteria radial | 32,3% | 23,4% | 7,2% | 0,03 |
| Revascularización arterial completa | 52,4% | 45% | 37,7% | NS |
| Arteria mamaria esqueletizada | 98,6% | 97,7% | 98,3% | NS |
CEC: circulación extracorpórea.
La mortalidad hospitalaria global fue del 1,4% (7/497) con un EuroSCORE I23 logístico medio de 4,1%. Tres pacientes fallecieron por causa cardiológica (2 por shock de componente mixto [distributivo/cardiogénico] y uno por IAM masivo secundario a espasmo difuso del lecho coronario e injertos), 2 por accidente cerebrovascular agudo (ACVA), uno por un tromboembolismo pulmonar masivo y uno por isquemia mesentérica.
Durante el postoperatorio presentaron mediastinitis 4 pacientes (0,8%), ACVA 10 pacientes (2%), IAM perioperatorio 8 pacientes (1,6%) y precisaron diálisis 13 pacientes (2,6%). La mediana de estancia hospitalaria postoperatoria fue de 5 (4,5-7) días.
El análisis univariante evidenció como factores de riesgo perioperatorios de mortalidad hospitalaria la diabetes, EPOC y la vasculopatía periférica, y como factores de riesgo de mediastinitis la insuficiencia renal preoperatoria, un tiempo de CEC≥200min y un bajo gasto cardiaco postoperatorio. El análisis multivariante identificó la vasculopatía periférica (p=0,04; RR: 1,69) como factor de riesgo de mortalidad hospitalaria y la insuficiencia renal preoperatoria (p=0,03; RR: 1,75) y un tiempo de CEC≥200min (p=0,004; RR: 2,1) como factores de riesgo de mediastinitis. Las complicaciones presentadas durante el postoperatorio se muestran en la tabla 5.
Complicaciones hospitalarias postoperatorias globales (n: 497)
| Mortalidad | 7 (1,4%) |
| BGC | 34 (6,8%) |
| Mediastinitis | 4 (0,8%) |
| Infección superf. herida | 17 (3,4%) |
| Infección urinaria | 12 (2,4%) |
| ACVA | 10 (2,0%) |
| IAM | 8 (1,6%) |
| Reoperación por sangrado | 14 (2,8%) |
| Insuficiencia renal (diálisis) | 13 (2,6%) |
| Neumonía | 13 (2,6%) |
| Estancias | 5 (4,5-7) días |
ACVA: accidente cerebrovascular agudo; BGC: bajo gasto cardiaco; IAM: infarto agudo de miocardio; BGC: bajo gasto cardiaco.
Estratificando por grupos de edad (<65, 65-70 y >70 años), la mortalidad hospitalaria fue del 1,2% (3/248); 1,8% (2/111); y 1,45% (2/138), respectivamente, menor que la mortalidad esperable según el EuroSCORE I logístico medio (2,65; 4,28; 6,29%, respectivamente; p<0,001). No hubo diferencias significativas en cuanto a la incidencia de morbimortalidad postoperatoria entre los 3 grupos de edad (tabla 6).
Complicaciones hospitalarias postoperatorias estratificadas por edad
| <65 años(n: 248) | 65-70 años(n: 111) | >70 años(n: 138) | p | |
|---|---|---|---|---|
| Mortalidad | 3 (1,2%) | 2 (1,8%) | 2 (1,4%) | NS |
| Bajo gasto cardiaco | 22 (8,8%) | 6 (5,4%) | 6 (4,3%) | NS |
| Mediastinitis | 2 (0,8%) | 1 (0,9%) | 1 (0,7%) | NS |
| Infeccción superf. herida | 8 (3,2%) | 6 (5,4%) | 3 (2,2%) | NS |
| Infección urinaria | 5 (2%) | 0 (0%) | 7 (5,1%) | NS |
| ACVA | 6 (2,4%) | 1 (0,9%) | 3 (2,2%) | NS |
| IAM | 5 (2%) | 1 (0,9%) | 2 (1,4%) | NS |
| Reoperación por sangrado | 5 (2%) | 5 (4,5%) | 4 (2,9%) | NS |
| Insuficiencia renal (diálisis) | 7 (2,8%) | 2 (1,8%) | 4 (2,9%) | NS |
| Neumonía | 6 (2,4%) | 1 (0,9%) | 6 (4,3%) | NS |
| Estancias, días | 5 (4-6,5) | 6 (5-8) | 5 (4,5-7) | NS |
ACVA: accidente cerebrovascular agudo; IAM: infarto agudo de miocardio.
En el 96,3% de los pacientes supervivientes (472/490 pacientes) se realizó un seguimiento medio de 5,3±2,4 años (rango: 2-111 meses), con una mortalidad global del 8,3% (39/472). La supervivencia actuarial de los pacientes supervivientes hospitalarios fue del 98,3%±0,7; 95%±1,2; y 88,9%±2,2 a los uno, 5 y 7 años, respectivamente (fig. 1). Las causas de mortalidad durante el seguimiento se muestran en la tabla 7. La supervivencia de eventos cardiacos de la serie a uno, 5 y 7 años fue del 99,5%±0,4; 98,2%±0,8; y 97,5%±0,7.
La supervivencia de los pacientes <65, 65-70 y >70 años de edad fue del 98,5±0,8%, del 97,7±1,6% y del 98,1±1,3% a un año; del 96,6±1,4%, del 95,9±2,4% y del 89±3,5% a 5 años; y del 91,6±2,8%, del 88,9±4,5% y del 83,6 ±5,1% a 7 años, respectivamente (fig. 2).
Durante el seguimiento, el 3,6% de los pacientes precisaron revascularización percutánea (tablas 8 y 9).
Características durante el seguimiento estratificadas por edad (n: 472)
| <65 años(n: 239), n (%) | 65-70 años(n: 105), n (%) | >70 años(n: 128), n (%) | |
|---|---|---|---|
| Mortalidad | 14 (6) | 8 (7,6) | 17 (13) |
| Angina (CCS≥II) | 6 (2,5) | 7 (6,6) | 6 (4,7) |
| Necesidad de revascularización percutánea | 6 (2,5) | 7 (6,6) | 4 (3,1) |
CCS: Canadian Cardiovascular Society.
Los predictores independientes de mortalidad durante el seguimiento fueron EPOC (p:0,014), mala clase funcional preoperatoria, New York Heart Association>II (p=0,04), FA preoperatoria (p=0,034) e insuficiencia renal postoperatoria (p=0,05).
DiscusiónEn la CRM, el uso del injerto de arteria mamaria interna izquierda a la arteria descendente anterior es el patrón oro por la evidencia demostrada del incremento en la supervivencia y en la reducción de la incidencia posterior de eventos cardiológicos a largo plazo comparada con el injerto de vena safena1–6.
A partir de estos excelentes resultados obtenidos con la arteria mamaria interna izquierda y a la limitada permeabilidad a largo plazo de los injertos venosos se impulsó el empleo de otros injertos arteriales. Entre los injertos arteriales utilizados, existe una progresiva evidencia a favor del uso de ambas mamarias7. Desde la publicación de Lytle et al.8, donde se objetivó una mayor supervivencia y libertad de reoperación a corto-largo plazo en los pacientes tratados con ambas mamarias en comparación con una sola mamaria e injertos venosos, una creciente cantidad de publicaciones han confirmado estos resultados. Puskas et al.24 evidenciaron una reducción del 35% en el riesgo de mortalidad a largo plazo en pacientes con doble mamaria frente a una sola mamaria y Grau et al.10 demostraron unas diferencias significativas en la supervivencia a 5, 10 y 15 años entre pacientes con doble injerto de mamaria comparado con injerto de mamaria único (96 vs. 91%, 89 vs. 79% y 79 vs. 61%, respectivamente). Este beneficio en la supervivencia se extiende, incluso, a más de 20 años de seguimiento10,11,25.
Nuestra serie retrospectiva de 497 pacientes con AMIB presenta unos buenos resultados a medio plazo, superponibles a las series contemporáneas con una supervivencia a los 5 y 7 años del 95% y el 88,9%. Grau et al.10 con una serie de 1.459 pacientes con doble injerto de mamaria presentaban una supervivencia a 5 años del 96% y Medalion et al.16 evidenciaron una supervivencia a 5 años del 88%.
Una posible explicación del beneficio del uso de ambas mamarias es la prolongada permeabilidad26 secundaria a su inherente efecto ateroprotector, a través del incremento de la síntesis de vasodilatadores como el óxido nítrico y la reducción de la producción de vasoconstrictores como la endotelina-1 y la angiotensina-ii27.
Otras probables razones, de ámbito más técnico, pero con un papel fundamental en el incremento de la supervivencia y en la libertad de eventos cardiológicos a largo plazo, son la realización de una revascularización completa y la utilización de la arteria mamaria derecha como injerto para el territorio de la circunfleja9,11,28. En nuestra serie se realizó una revascularización completa en el 94,8% de los casos con una media de injertos/paciente de 3,8±0,9; ligeramente mayor a la mayoría de las grandes series publicadas10,22,29 y con un 85,3% de los pacientes con ambas arterias mamarias utilizadas para revascularizar el sistema coronario izquierdo, hechos que han podido influir en los buenos resultados a medio plazo.
Pese a estos potenciales beneficios en la supervivencia a largo plazo, el uso de AMIB en la práctica clínica actual es muy limitado. Una de las principales razones de esta reducida utilización es el riesgo de incrementar la morbimortalidad postoperatoria, especialmente en la incidencia de mediastinitis, debido a que la disección de ambas arterias mamarias condiciona una reducción de la vascularización esternal, aumentando potencialmente el riesgo de infección con la elevada mortalidad inherente a esta complicación. Este riesgo es más acusado en determinados subgrupos de pacientes (edad avanzada, obesidad, EPOC y especialmente diabetes)12,13. Diferentes estudios observacionales y metaanálisis encontraron un leve aumento de la incidencia de mediastinitis en los pacientes tratados con AMIB comparada con mamaria aislada12,13,30. En cambio, publicaciones recientes, con la mejoría de la profilaxis antibiótica, la optimización de la glucemia perioperatoria y específicamente con la aplicación de la técnica de esqueletización en la disección de ambas mamarias (preservando las colaterales y el sistema venoso esternal), han evidenciado una reducción del riesgo de infección esternal, sobre todo en diabéticos30,31, sin encontrar diferencias significativas en la morbimortalidad postoperatoria entre injerto mamario único o doble, incluidos los subgrupos de pacientes de alto riesgo13–17,22.
En nuestra experiencia con AMIB, pese a no haber sido comparada con el grupo de pacientes en donde solo utilizamos una sola mamaria, observamos una baja mortalidad postoperatoria hospitalaria (1,4%), en similitud con las grandes series publicadas recientemente que presentan una mortalidad hospitalaria<1,5%, siendo, en la mayoría de ellas, significativamente inferior a la mortalidad hospitalaria observada en pacientes con injerto único de mamaria10,21,22.
Del mismo modo, la frecuencia de complicaciones hospitalarias de nuestra serie fue comparable a la publicada por otros grupos, con una incidencia de ACVA, IAM y mediastinitis postoperatoria≤2%10,16,21,22,30. Itagaki et al. analizaron una cohorte histórica de más de un millón de pacientes tratados con CRM, donde el 3,9% de los pacientes recibieron AMIB21. Los predictores independientes de mediastinitis fueron la insuficiencia cardiaca preoperatoria, EPOC, insuficiencia renal y la diabetes mellitus avanzada con complicaciones crónicas. Medalion et al. señalaron como predictores de mediastinitis en 1.714 pacientes con doble injerto de mamaria la reoperación, EPOC, vasculopatía periférica y la diabetes mellitus16. Ambos trabajos no pudieron demostrar una asociación significativa entre AMIB y mediastinitis.
En nuestro caso, los predictores independientes de mediastinitis fueron la insuficiencia renal preoperatoria (p=0,03; RR:1,75) y un tiempo de CEC≥200min (p=0,004; RR: 2,1). Pese a tener una considerable prevalencia preoperatoria de pacientes diabéticos (31%), la incidencia de mediastinitis fue del 0,8% (4 pacientes, 2 de ellos diabéticos) no pudiendo inferirse, en este reducido número de casos, una relación estadísticamente significativa entre diabetes y mediastinitis. Una de las posibles razones de esta baja incidencia de mediastinitis, como en otras series actuales, fue la realización de la disección de ambas mamarias de forma esqueletizada en casi la totalidad de los pacientes (98,3%).
Otro grupo de pacientes en los que la utilización del doble injerto de arteria mamaria es controvertido son los ancianos debido a su limitada expectativa de vida y a los excelentes resultados obtenidos utilizando injerto de mamaria única. En el trabajo de Lytle et al8, aunque el número de pacientes>60 años intervenidos con doble mamaria fue relativamente bajo, la supervivencia a largo plazo mejoró con respecto a los pacientes>60 años con mamaria única. Kurlansky et al.11 compararon a 1.497 pacientes≥65 años con una o 2 mamarias, evidenciando menor mortalidad hospitalaria (6,4 vs. 3,1%) y mejor supervivencia a 4 años (60,7 vs. 69,7%) en el grupo de doble mamaria. El estudio más reciente y numeroso, comparando AMIB en diferentes grupos de edad (≤65, 66-75, y >75 años), ha sido reportado por Medalion et al.16. Su mortalidad hospitalaria fue del 1,2; 4,1; y 5,8%, respectivamente, sin diferencias en la incidencia de mediastinitis entre los grupos de edad y con una supervivencia a 10 años del 85, 65 y 40%, similar a la expectativa de vida de la población general en Israel. Los autores concluyeron que la edad no es una contraindicación para la utilización de doble mamaria.
Nosotros estratificamos nuestra serie en <65, 65-70 y >70 años con un 50% de los pacientes≥65 años. Aunque los pacientes más añosos fueron un grupo seleccionado, no se evidenciaron diferencias significativas en morbimortalidad hospitalaria entre los 3 grupos de edad con mortalidades de 1,2% (<65 años); 1,8% (65-70 años); y 1,45% (>70 años), respectivamente, y una incidencia de mediastinitis de 0,8; 0,9; y 0,7%, con una buena supervivencia a medio plazo (91,6; 88,9; y 83,6% a 7 años).
En definitiva, el incremento actual de la incidencia de la cardiopatía isquémica a edades cada vez más tempranas y el aumento progresivo de la esperanza de vida de la población nos obligan a intentar aportar una revascularización miocárdica de calidad, eligiendo aquella estrategia quirúrgica con una mayor durabilidad potencial y una ajustada morbimortalidad hospitalaria. En espera de los resultados de ensayos aleatorizados, como el ART22, que darán las respuestas definitivas de la superioridad o no del uso de AMIB, la evidencia actual indica que la utilización de ambas mamarias, en comparación con mamaria única con injertos venosos, aporta mayor supervivencia a largo plazo con una reducida morbimortalidad precoz. Una juiciosa selección de los pacientes, evitando el uso de AMIB en pacientes con varios factores de riesgo de mediastinitis asociados, especialmente diabetes con EPOC y/o obesidad, y la realización de la esqueletización de ambas arterias mamarias pueden reducir significativamente la incidencia de complicaciones de la herida esternal.
LimitacionesEste artículo está sujeto a todas las limitaciones de un estudio observacional, retrospectivo y no aleatorizado. Pese a presentar unos resultados a corto y medio plazo similares a las grandes series publicadas utilizando AMIB, nosotros no realizamos una comparación estadística con el grupo de pacientes contemporáneos en los cuales utilizamos injerto de mamaria único. Durante el seguimiento solo en un pequeño número de casos (3,6%, pacientes sintomáticos para angina) se realizaron coronariografías posteriores.
ConclusionesLa CRM aislada utilizando injerto de AMIB presenta unos excelentes resultados a corto y medio plazo independientemente de la edad, pudiendo ser la técnica de elección en todo paciente con una razonable expectativa de vida. En pacientes con elevada comorbilidad, especialmente vasculopatía e insuficiencia renal, se debería individualizar la decisión del uso de doble arteria mamaria.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.