Introducción
La gastropatía hipertrófica asociada a hipoproteinemia fue descrita por primera vez por Ménétrier1 en 1889. Esta enfermedad gástrica de etiología desconocida es muy infrecuente. Se la considera una condición preneoplásica, ya que se asocia a cáncer gástrico en un 10-15% de los pacientes2,3. La actitud terapéutica no está claramente definida. Presentamos un nuevo caso de enfermedad de Ménétrier (EM) asociado a cáncer gástrico y realizamos una puesta al día.
Caso clínico
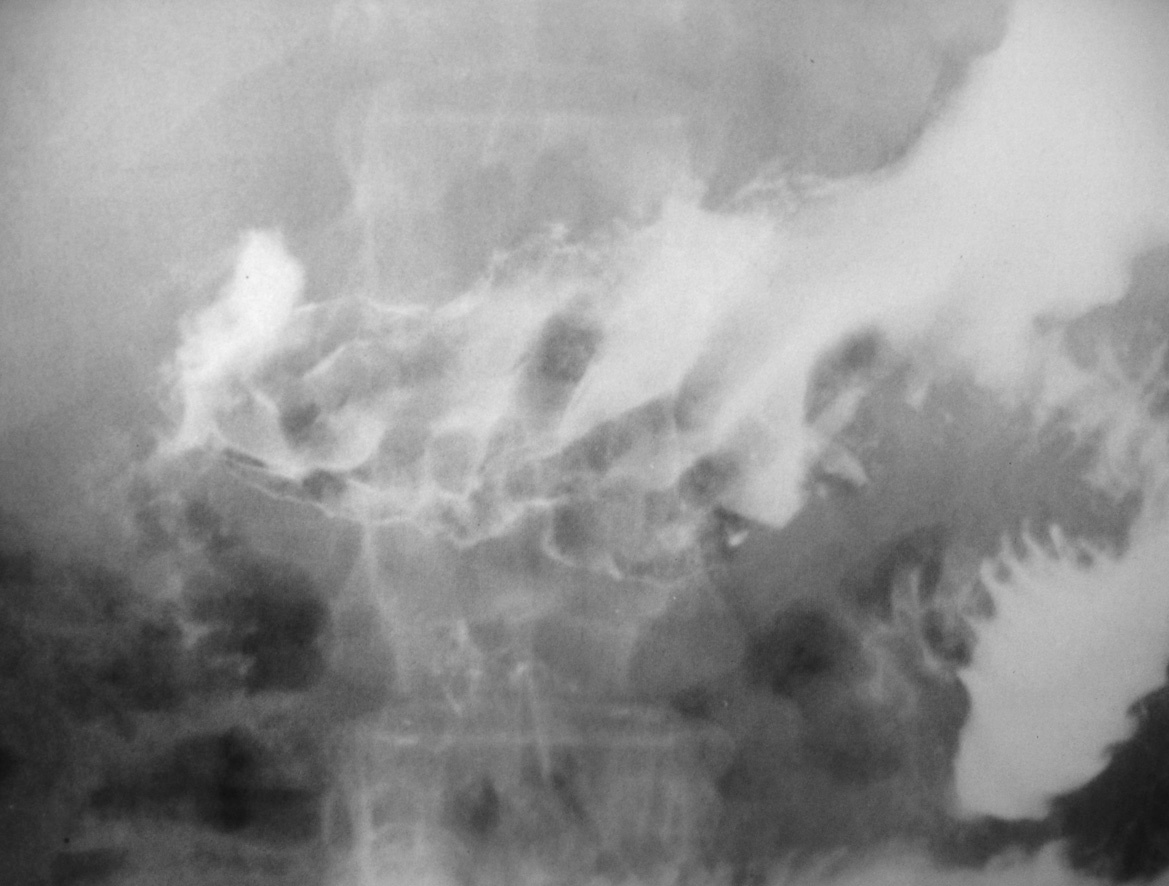
Varón de 66 años con EM diagnosticada 13 años antes, que se inició clínicamente con un cuadro de melenas. En la endoscopia que se le practicó, se observaba una gran área de pliegues engrosados en la curvatura mayor, compatible con EM. La biopsia confirmó la sospecha endoscópica. El paciente rehusó tratamiento quirúrgico y eligió tratamiento médico y seguimiento endoscópico, sin haber presentado cambios destacables. Adelantó su cita anual, ya que presentaba pesadez y dolor epigástrico, pirosis retroesternal, vómitos oscuros y melenas. Se le realizó tránsito gastroduodenal (fig. 1) y endoscopia digestiva alta, en la que se observó pliegues muy engrosados en ambas curvaturas, con la mucosa muy hiperémica, y una masa de aspecto infiltrativo en curvatura menor, con signos de sangrado reciente, que estenosaba casi totalmente la luz gástrica. Se biopsió la masa descrita, que histológicamente corresponde a un adenocarcinoma. En la analítica destacaban: fosfatasa alcalina, 502 UI/l; lactato deshidrogenasa, 491 UI/l, y proteínas totales, 4,3 g/dl. Se realizó tomografía computarizada abdominal, en la que se apreciaron metástasis hepáticas múltiples y adenopatías peripancreáticas de aspecto patológico. Debido al cuadro obstructivo, se decidió realizar cirugía paliativa mediante gastroenteroanastomosis y biopsia de una de las múltiples lesiones hepáticas de aspecto metastásico. La pared resecada para efectuar la derivación quirúrgica presenta el aspecto histológico típico de EM (gastropatía hiperplásica con hipertrofia foveolar), y la lesión hepática es compatible con adenocarcinoma. En el postoperatorio presentó dos cuadros de hematemesis autolimitada. Falleció a los 6 meses de la intervención por progresión de la neoplasia.
Fig. 1. Tránsito esofagogástrico: pliegues antrales muy engrosados.
Discusión
La EM es una variante muy infrecuente de gastropatía hiperplásica, caracterizada por la aparición de pliegues engrosados en la mucosa gástrica asociada a una pérdida de proteínas e hipoclorhidria1-3. Existen dos variantes: la forma difusa y la localizada, en la cual habitualmente hay afectación de la curvatura mayor y fundus2-4. Es más frecuente en varones de 55 a 60 años4. La etiología de la EM se desconoce, y se han postulado factores infecciosos (citomegalovirus, Helicobacter pylori), autoinmunitarios (exposición a alérgenos, anticuerpos contra las células parietales), hormonales y genéticos, entre otros1-5.
Los síntomas más frecuentes son: dolor abdominal, pérdida de peso, anorexia, vómitos y hemorragia digestiva1,2. En los pacientes con EM parece haber una mayor incidencia de infecciones graves y enfermedades tromboembólicas. En la analítica destacan la hipoproteinemia y en ocasiones hipoclorhidria1,3.
En la endoscopia, macroscópicamente se observa un engrosamiento de los pliegues gástricos o engrosamiento nodular de la mucosa, y se debe efectuar una biopsia de todo el espesor de la mucosa afectada. Microscópicamente hay un incremento del grosor epitelial, hiperplasia foveolar, atrofia glandular y un leve infiltrado inflamatorio3. En la tomografía computarizada abdominal, se observan los pliegues engrosados habitualmente localizados en el fundus y la curvatura mayor4. Se debe plantear un diagnóstico diferencial con otras enfermedades gástricas que puedan causar engrosamiento de pliegues: síndrome de Zollinger-Ellison, síndrome de Stiempen, gastritis crónica linfocitaria, sífilis, sarcoidosis, linfoma y carcinoma infiltrante difuso (Bormann IV)1,2,4.
El riesgo de malignización de la EM es controvertido. Como únicamente hay casos aislados o series cortas, no se puede obtener datos epidemiológicos fiables. La concurrencia de cáncer gástrico y EM publicada oscila en el 0-10%. Pero es difícil valorar en la literatura si realmente es una malignización de la EM o un cáncer coincidente1.
El tratamiento de la EM no está claramente establecido. En los casos de EM asociados a infección por H. pylori, se ha comunicado el control de los síntomas con la terapia antibiótica de eliminación5,6. Otros tratamientos médicos empleados han sido: dieta rica en proteínas, antiácidos, anticolinérgicos, octreotida e incluso anticuerpos monoclonales anti-EGFR1,2. Pero, la recomendación más admitida es el tratamiento quirúrgico, especialmente en los pacientes con pérdida no controlable de proteínas o sangrado, ya que además se elimina el teórico riesgo de malignización3.
Otra cuestión no resuelta es la extensión de la gastrectomía a realizar. Los partidarios de la gastrectomía total defienden su realización porque se elimina el riesgo de malignización, la localización habitual es fúndica, y se obvia la realización de un anastomosis con una mucosa hipertrofiada1. Por el contrario, los defensores de una cirugía más económica afirman que permite controlar los síntomas con menor morbilidad. Quizá la postura más razonable sea adaptar la técnica a la localización de la EM y el grado de displasia. Así, en los casos difusos, localizados cerca del cardias, como ocurre habitualmente, o con displasia/neoplasia, la gastrectomía total es la técnica a realizar. Por el contrario, en las lesiones antrales sin signos de displasia, la gastrectomía subtotal es suficiente.
Correspondencia: Dr. J.M. Ramia.
General Perón, 22, 3.o C. 28020 Madrid. España.
Correo electrónico: jose_ramia@hotmail.com
Manuscrito recibido el 18-10-2005 y aceptado el 17-1-2006.