Realizamos una revisión sistemática de la literatura y un metaanálisis a través de las bases de datos MEDLINE, EMBASE y COCHRANE LIBRARY identificando los ensayos clínicos publicados entre 2005 y 2010 que comparan los resultados a corto plazo de la escisión mesorrectal total laparoscópica convencional (EMTL) y asistida por robot (EMTR) en el tratamiento del cáncer de recto no complicado.
Seleccionamos 5 ensayos con un total de 380 pacientes, de los que 169 fueron sometidos a EMTR y 211 a EMTL. No hemos encontrado diferencias significativas aunque la EMTR se asocia con menor tasa de conversión, mayor margen de resección circunferencial y mayor número de ganglios linfáticos aislados, así como una menor tasa global de complicaciones. No existe evidencia de que la EMTR aporte ventajas que compensen la mayor duración de la intervención y el mayor coste del procedimiento. Son necesarios estudios prospectivos aleatorizados y con mayor número de pacientes.
A systematic literature review and meta-analysis was performed using the MEDLINE, EMBASE and COCHRANE LIBRARY data bases, and identifying clinical trials, published between the years 2005 to 2010, that compared the short term results of conventional laparoscopic total mesorectal excision (L-TME) and robot-assisted total mesorectal excision (RA-TME) in the treatment of non-complicated rectal cancer.
Five trials with a total of 380 patients were selected, of whom 169 were subjected to RA-TME and 211 to L-TME. No significant differences were found, although RA-TME was associated with a lower conversion rate, a greater resection margin circumference, and higher number of isolated lymph nodes, as well as a lower overall rate of complications. There was no evidence that RA-TME had advantages that compensated for the longer duration of the surgery and the higher cost of the procedure. More randomised prospective studies and a greater number of patients are needed.
La escisión total del mesorrecto (EMT), que implica la extirpación del mesorrecto intacto mediante disección cortante en el plano avascular existente entre la fascia presacra y la fascia propia del recto, se considera actualmente el gold standard en el tratamiento quirúrgico del cáncer de recto. El objetivo es eliminar el tumor obteniendo márgenes circunferenciales libres de afectación tumoral, preservando al tiempo el plexo nervioso hipogástrico. Su implantación ha supuesto una disminución de las recidivas locales mejorando de manera significativa el pronóstico de estos pacientes1,2.
En las 2 últimas décadas la cirugía mínimamente invasiva (CMI) ha revolucionado la técnica quirúrgica3. El abordaje laparoscópico se emplea también en el tratamiento de tumores malignos, aunque muchas de estas técnicas laparoscópicas precisan acreditar sus resultados. Así, las recientes controversias en el cáncer de colon, resueltas en su mayor parte, se trasladan ahora al cáncer de recto.
Aunque la CMI es una opción terapéutica válida para el tratamiento del cáncer de recto con innegables ventajas postoperatorias a corto plazo, no ha logrado una amplia implantación. Este hecho se debe en parte a la complejidad técnica de la EMT laparoscópica al tener que trabajar en un campo quirúrgico profundo y estrecho, con instrumentos rígidos y una visión bidimensional, a la larga y difícil curva de aprendizaje y a la preocupación general de que estas dificultades puedan comprometer los resultados oncológicos4–9. El ensayo inglés CLASICC10 indica que la EMT por laparoscopia conlleva una alta tasa de conversión (34%) y una tendencia hacia una mayor positividad del margen circunferencial, aunque señalan tasas similares de recurrencia local, SLE y supervivencia total.
La cirugía asistida por un telemanipulador es una tecnología emergente que permite realizar procedimientos laparoscópicos en muchas indicaciones. El sistema Da Vinci (Intuitive Surgical Inc., Sunnyvale, CA, USA) es un robot esclavo (no es inteligente por lo que no realiza la operación por sí mismo) que se viene utilizando en todo el mundo desde que fuera aprobado por la FDA para uso clínico en operaciones abdominales en julio del 2000 y que proporciona numerosas ventajas técnicas frente al abordaje laparoscópico convencional: plataforma estable para la cámara, posición ergonómica del cirujano, visión tridimensional magnificada, eliminación del temblor de las manos, capacidad ambidiestra con mayor precisión, instrumental articulado con más grados de movimiento, menos errores y menos sangrado operatorio11,12. Además, se ha señalado que la curva de aprendizaje es más corta que con la laparoscopia convencional permitiendo que un mayor número de cirujanos pueda realizar procedimientos laparoscópicos. Entre sus inconvenientes cabe citar la falta de sensación táctil y tensional por el cirujano, la dificultad para una conversión rápida a cirugía abierta ante una complicación grave como hemorragia severa, la mayor duración de la intervención y el alto coste del equipo y de su mantenimiento. El Da Vinci consta de 3 elementos: la consola maestra (la interfase entre el cirujano y el robot), la columna de visión con un doble sistema óptico que permite la visión tridimensional ampliada, y 3 o 4 brazos articulados acoplados a los instrumentos a través de puertos laparoscópicos. Los movimientos que realiza el cirujano en los manipuladores o «guante maestro» se transmiten con extrema precisión al campo quirúrgico vía software y con los mismos 7 grados de libertad que las manos del cirujano en cirugía abierta. Para Satava M et al.11 la laparoscopia sería una fase de transición hacia la «cirugía basada en la informática». La robótica no solo mejora la calidad de la cirugía, sino que la convierte en un proceso informático y las ventajas conocidas actualmente solo son la punta del iceberg de los cambios a los que vamos a asistir en breve en la cirugía.
En el abordaje laparoscópico del cáncer de recto, la asistencia robótica podría ser especialmente útil compensando algunas limitaciones técnicas de la laparoscopia, si bien estos beneficios no están del todo aclarados12–29. Algunos cirujanos, al ser la resección anterior una intervención que precisa un trabajo multicuadrante, con el fin de evitar el reposicionamiento del robot y ahorrar tiempo, emplean una técnica híbrida que consiste en aislar y ligar los vasos mesentéricos inferiores y movilizar el colon descendente-sigmoides con laparoscopia convencional y luego, hacer la EMT con el robot. Otros, en cambio, prefieren movilizar el ángulo esplénico y aislar el mesorrecto sin cambiar la posición del robot30,31.
El entusiasmo inicial que ha despertado esta nueva tecnología debe reforzarse con una evidencia científica de sus beneficios mediante el empleo de ensayos clínicos prospectivos controlados y aleatorizados. Para tratar de dilucidar las incertidumbres que se plantean, nos proponemos comparar ambas técnicas utilizando para ello el metaanálisis.
Material y métodosSelección de estudiosHemos realizado una revisión de la literatura científica en MEDLINE, EMBASE y COCHRANE LIBRARY desde 2005 a 2010 analizando ensayos clínicos controlados que comparan la escisión mesorrectal total laparoscópica (EMTL) con la asistida con robot (EMTR) en pacientes con cáncer de recto. Se han utilizado para la búsqueda los siguientes términos: «laparoscopia», «cirugía robótica», «cáncer de recto», «escisión mesorrectal total», «estudio comparativo». La función «artículos relacionados» ha permitido ampliar la búsqueda.
Extracción de datosDos revisores independientes (A.G., J.M.) han extraído los siguientes datos de cada estudio: primer autor, año de publicación, características de la población a estudio incluyendo sexo, edad, variables clínicas, operatorias y patológicas, número de sujetos operados con cada técnica, diseño del estudio y criterios de inclusión y exclusión.
Criterios de inclusiónConsideramos para el metaanálisis aquellos estudios que: 1) incluyan datos suficientes para las distintas variables elegidas tanto operatorias como patológicas y clínicas, 2) comparen las dos técnicas -laparoscopia tradicional y asistida por robot- en la resección de cáncer de recto, 3) realicen EMT. Cuando hay 2 estudios realizados por la misma institución se elige el de mayor calidad o el de publicación más reciente.
Criterios de exclusiónSe excluyen los ensayos que no comparan ambas técnicas, los que no realizan EMT en el cáncer de tercio superior, los que incluyen cirugía de colon y recto, los que consideran enfermedad benigna y maligna y los que incluyen resecciones con carácter paliativo.
Variables de interés y definicionesSe consideran 3 tipos de variables para comparar el grupo con cirugía laparoscópica del cáncer de recto con el grupo de cirugía robótica:
- a)
Variables clínicas: edad, sexo, índice de masa corporal (IMC), distancia del tumor al margen anal, QT-RT neoadyuvante, estancia hospitalaria media (días) y tasa global de complicaciones.
- b)
Variables operatorias: tiempo operatorio, pérdida de sangre estimada (PSE), tasa de conversión y complicaciones perioperatorias.
- c)
Variables patológicas: márgenes de resección distal (MRD) en cm y margen circunferencial en mm (MRC) y n.° de ganglios aislados en el espécimen.
La afectación del margen circunferencial (MRC) se define como MRC < o igual a 1mm. La fuga anastomótica clínica se define como la dehiscencia anastomótica verificada por enema con contraste o exploración quirúrgica indicada cuando el drenaje era fecaloideo o el paciente presentaba signos de sepsis.
Análisis estadísticoEl metaanálisis se ha realizado considerando las variables para las que se encuentren datos suficientes siguiendo la metodología recomendada por la Cochrane Collaboration y las guías de Quality of Reporting of Meta-Analyses3. En el análisis estadístico de las variables categóricas se emplea la odds ratio (OR) y en el caso de variables cuantitativas, la diferencia ponderada de medias, ambas con intervalos de confianza del 95%. Los resultados se representan mediante una forest plot o gráfica de efectos que muestra el efecto estimado es cada estudio junto con el valor obtenido combinando los resultados de todos los estudios, acompañados por sus respectivos intervalos de confianza (IC). En ella aparece la línea vertical del valor correspondiente a la ausencia de efectos (RR=1 o diferencia de medias=0).
Para la valoración de la heterogenicidad entre los estudios empleamos las siguientes estrategias: 1) estadístico Q de Der Simonian y Laird, cuyo valor se confronta con la distribución teórica correspondiente, de forma que si el valor de p es >0,05 se puede asumir la hipótesis de homogeneidad; 2) gráfico de Galbraith para representar la precisión de cada estudio frente al estandarizado mediante una banda de confianza, localizando a la derecha los estudios que por su mayor precisión tienen más importancia para el metaanálisis; 3) para la combinación de resultados el método estadístico preferido en investigación quirúrgica es el modelo de efectos aleatorios, debido a que los pacientes que se operan en centros diferentes tienen distintos perfiles de riesgo y criterios de selección para cada técnica quirúrgica; 4) para evaluar el sesgo de publicación utilizamos el funnel plot o gráfico de embudo, que representa el tamaño muestral de cada estudio frente al tamaño del efecto detectado, y el test de Egger que valora si hay asimetría significativa; 5) la consistencia se valora mediante el análisis de sensibilidad que permite reanalizar los resultados del metaanálisis excluyendo en cada paso uno de los estudios incluidos en la revisión. Si los resultados son similares tanto en magnitud del efecto como en significación estadística, el análisis es consistente32.
Para el procesamiento estadístico de los datos hemos utilizado el programa EPIDAT 3.0.
ResultadosEstudios seleccionadosLa investigación inicial, una vez excluidos los estudios que consideran tanto enfermedad benigna como maligna, enfermedad cólica y rectal y ensayos con errores graves, identifica 6 estudios. Tras la revisión, seleccionamos 5 ensayos33–36,38 que cumplen los criterios de inclusión con datos suficientes en las variables consideradas, con un total de 380 pacientes de los que 169 fueron intervenidos con asistencia robótica y 211 con laparoscopia convencional. La serie de Patriti et al.37 con 66 pacientes (R29/ L37) se ha desestimado para el metaanálisis ya que los autores realizaron en unos casos EMT y en otros parcial, según la localización del tumor en el recto.
Variables patológicas- •
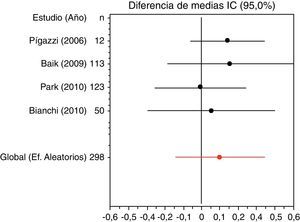
Margen distal de resección (MRD) en cm: los cinco ensayos recogen esta variable. No hay diferencias estadísticamente significativas en el MRD. El resultado en cuanto a la diferencia estandarizada de medias (DEM) es 0,0137cm (IC 95%) que expresa la diferencia entre el margen obtenido con robot y con laparoscopia convencional, lo que supone un margen ligeramente inferior en el grupo robótico, como corrobora el análisis de sensibilidad (0,0137cm). No hay evidencia de heterogenicidad estadística (Q=2,8408; p=0,5848 (>0,05) o sesgo (Egger=0,8065; p>0,05).
- •
Margen circunferencial (MRC) en mm: aquí ocurre al revés (-0,934mm) ya que el robot da mejores resultados siendo su valor en el análisis de sensibilidad de -2,1mm. Sin embargo, los estudios en este caso no son homogéneos (si se suprime el estudio de Baik et al.33 no hay prácticamente diferencias).
- •
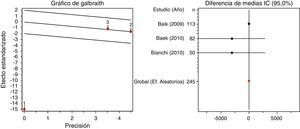
Ganglios linfáticos aislados: el número de ganglios aislados es ligeramente superior en la EMTR (0,137 ganglios), dato corroborado por el análisis de sensibilidad (0,223 ganglios en promedio).
En conclusión, en cuanto a las variables patológicas, la EMTR consigue mayor margen circunferencial y menor margen longitudinal que la EMTL, no siendo las diferencias significativas. El número de ganglios resecados es ligeramente superior en la EMTR.
Variables operatorias- -
Duración de la intervención (minutos)
- -
Pérdida de sangre (ml)
- -
Tasa de conversión a cirugía abierta
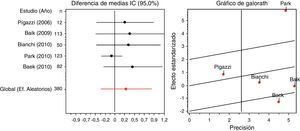
En lo referente a las variables operatorias, cabe señalar que los estudios son heterogéneos en cuanto a la duración de la intervención. Fijándonos en los estudios más precisos (Baik et al.33 y Park et al.34), así como en los resultados, la EMTR conlleva mayor tiempo quirúrgico que la laparoscopia convencional. La pérdida de sangre solo se reseña en 2 estudios (Baek et al.36 y Pigazzi et al.38) de ahí su homogeneidad. En ambos, la pérdida es menor con el robot, si bien al ser solo 2 estudios no hay análisis de sensibilidad. En cuanto a la tasa de conversión a cirugía abierta (TCA), el gráfico de Galbraith muestra que los estudios no son homogéneos, siendo el trabajo de Baik et al.33 el que causa la distorsión. Los resultados son más favorables en la EMTR con una menor tasa de conversión.
Variables clínicas- -
Edad (promedio y rango)
- -
Sexo
- -
IMC
- -
Estancia hospitalaria media
- -
Tasa global de complicaciones
- -
Distancia del tumor al margen anal (media en cm y desviación típica)
- -
Quimiorradioterapia neoadyuvante
Los estudios que tratan las variables edad carecen de homogeneidad, si bien a medida que se van incluyendo trabajos prácticamente no se observan diferencias entre la edad de los pacientes operados por uno u otro método. El IMC se comporta de forma similar a la edad. Los estudios no son homogéneos pero el resultado final indica que los pacientes operados con el robot tienen menor masa corporal aunque la diferencia es tan mínima que si se suprime el estudio de Pigazzi et al.38 cambia el resultado. La variable sexo se ha obviado ya que no parece relevante en este tipo de estudio. En cuanto a la QT-RT preoperatoria, los estudios son homogéneos, siendo ligeramente mayor el número de pacientes que reciben tratamiento neoadyuvante en el grupo EMRL. La distancia del tumor al margen anal solo se refleja en 2 estudios con resultados dispares, existiendo gran diferencia entre ellos en el número de pacientes incluidos. La estancia hospitalaria media es ligeramente inferior en el grupo robótico si bien los estudios no son homogéneos. Lo mismo sucede con la tasa global de complicaciones, sobre todo si se suprime el estudio de Pigazzi et al.38.
DiscusiónEl objetivo de este estudio es tratar de determinar las ventajas reales de la asistencia robótica en el tratamiento laparoscópico del cáncer de recto a través de una revisión sistemática de la literatura. Hemos seleccionado 5 estudios por incluir datos suficientes sobre las variables consideradas y no presentar criterios de exclusión. En cuanto a la calidad metodológica de los mismos, solamente uno de ellos (Baik et al.33) es un ensayo controlado aleatorizado. Los restantes son ensayos no aleatorizados, que asignan un determinado tratamiento según la disponibilidad del robot, sin utilizar un método de aleatorización estándar. Todos son abiertos, sin enmascaramiento.
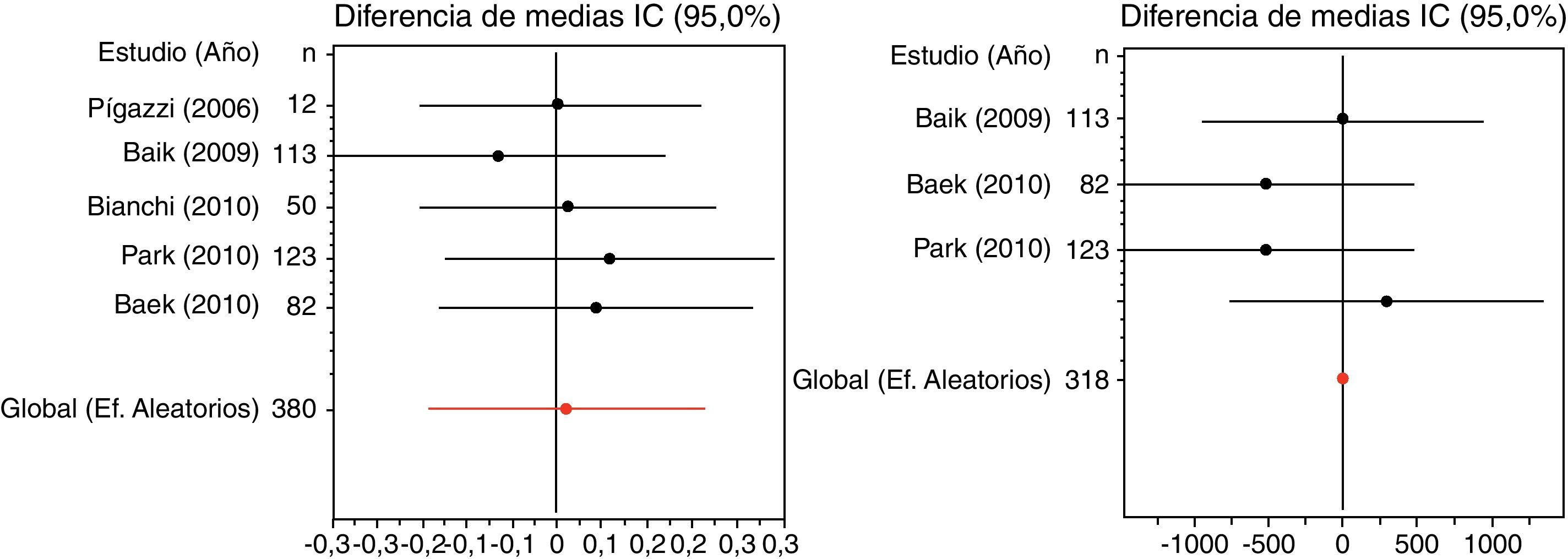
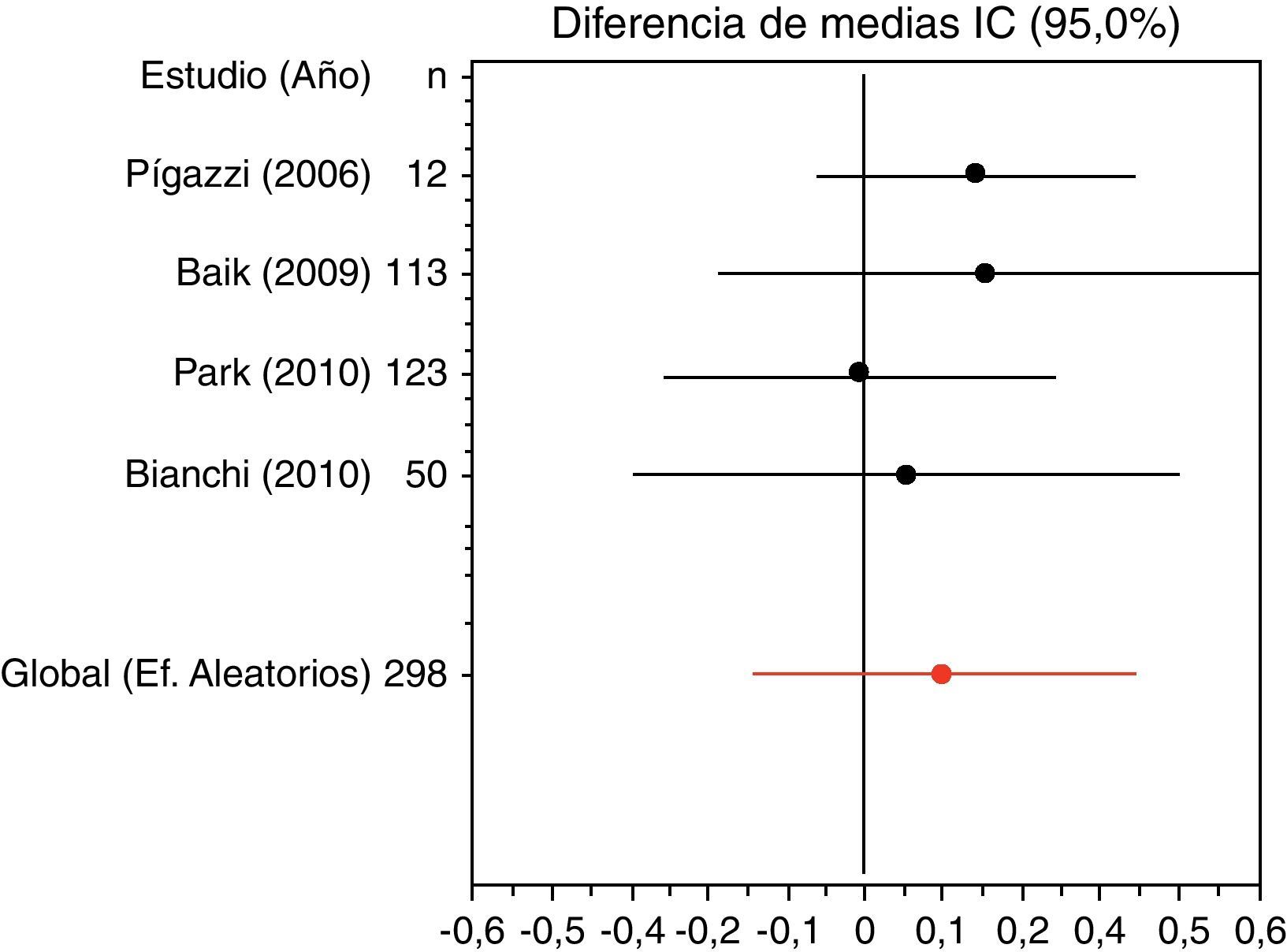
Si consideramos las variables patológicas, el robot consigue un MRC algo mayor, aunque los estudios no son homogéneos, siendo el heterogéneo el de Baik et al.33, ya que si se suprime este ensayo los resultados son prácticamente los mismos. No obstante, estos autores señalan que la calidad macroscópica del espécimen del mesorrecto es mayor en el grupo robótico. En cuanto al MRD, es más pequeño en el grupo tratado con laparoscopia convencional (fig. 1). El número de ganglios extirpados también es ligeramente superior en el grupo de EMTR, dato que también apoya el análisis de sensibilidad (0,1223 ganglios en promedio). Si suprimimos el estudio de Park et al.34 habría un mínimo cambio en el resultado (fig. 2). Es necesario un seguimiento más largo y en más pacientes para valorar si estos factores influyen en la supervivencia a largo plazo y en las tasas de recurrencia local.
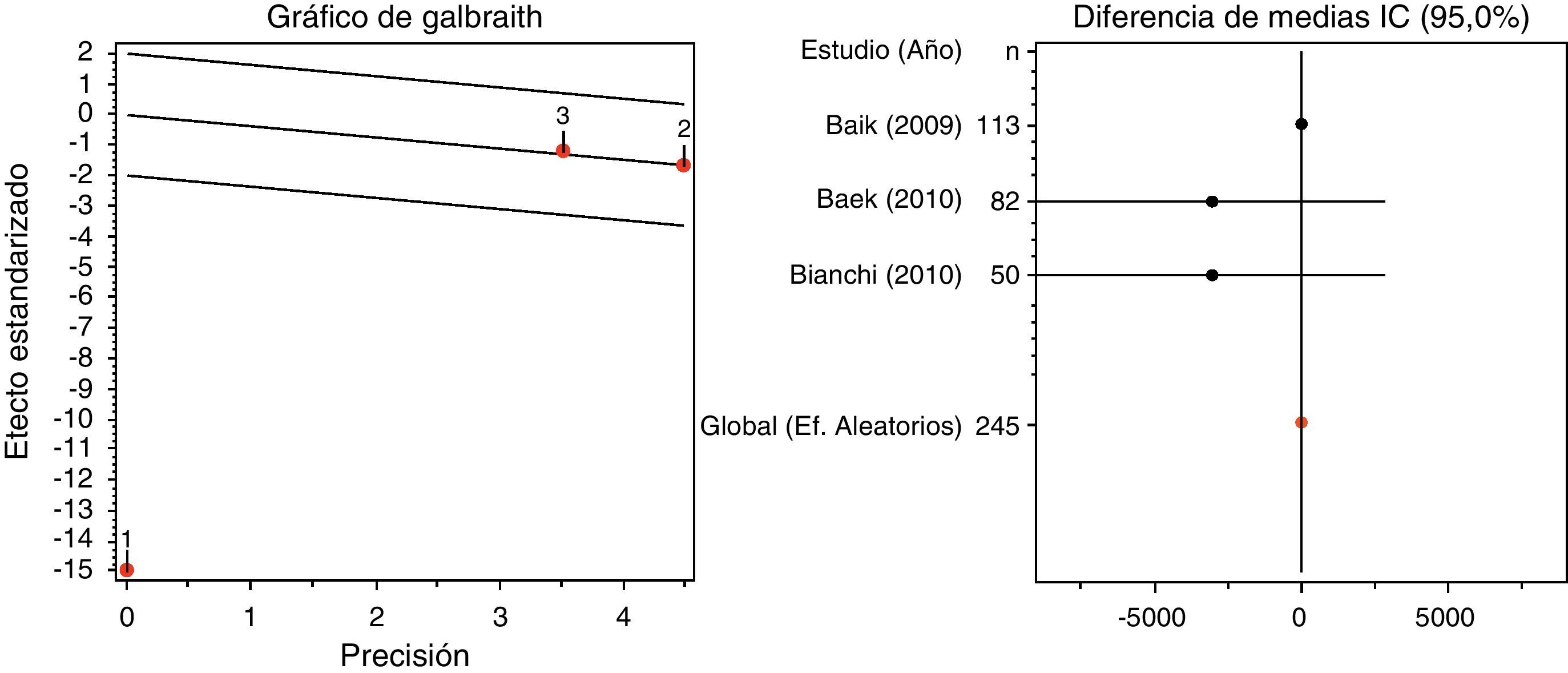
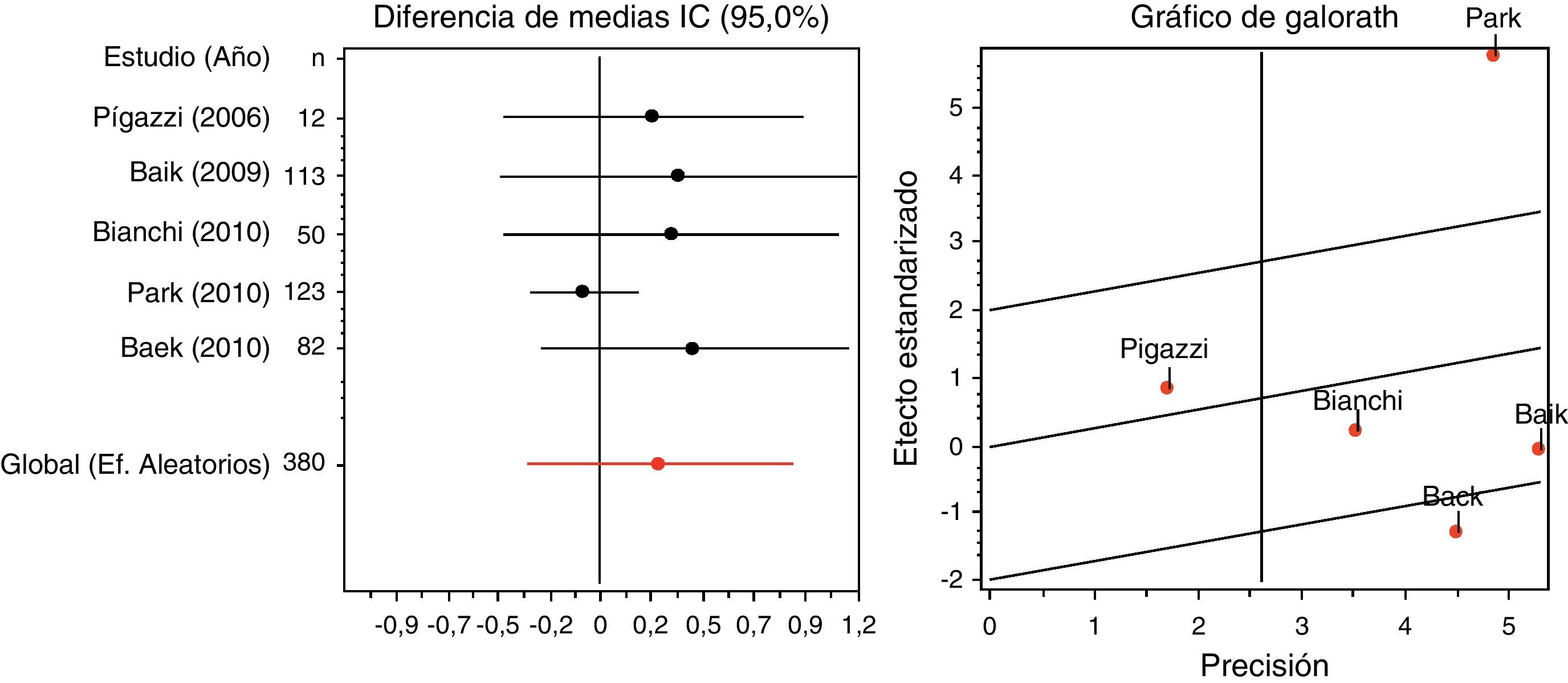
En cuanto a las variables operatorias, la TCA es el parámetro utilizado en el ensayo ROLARR39 para evaluar las ventajas de la robótica. Esta variable es inferior en la EMTR si bien los estudios son heterogéneos (fig. 3 izquierda) siendo el trabajo de Baik et al.33 el no homogéneo. Si solo tenemos en cuenta los estudios homogéneos, los resultados se decantan claramente a favor de la cirugía asistida por robot (fig. 3 derecha). Aunque la TCA es un indicador de la dificultad técnica quirúrgica, parece claro que el empleo del Da Vinci se asocia con menor fatiga del cirujano y, aunque es difícil de demostrar, el estrés de una operación difícil puede ser una causa indirecta de conversión. Considerando la duración de la operación, los estudios son heterogéneos. Si nos fijamos en los estudios más precisos de Park y Baik se aprecia que la EMTR es una intervención más larga (fig. 4 izquierda) pero si suprimimos estos estudios que según el gráfico de Galbraith distorsionan los resultados (fig. 4 derecha) la menor duración correspondería al grupo robótico (tablas 1–3).
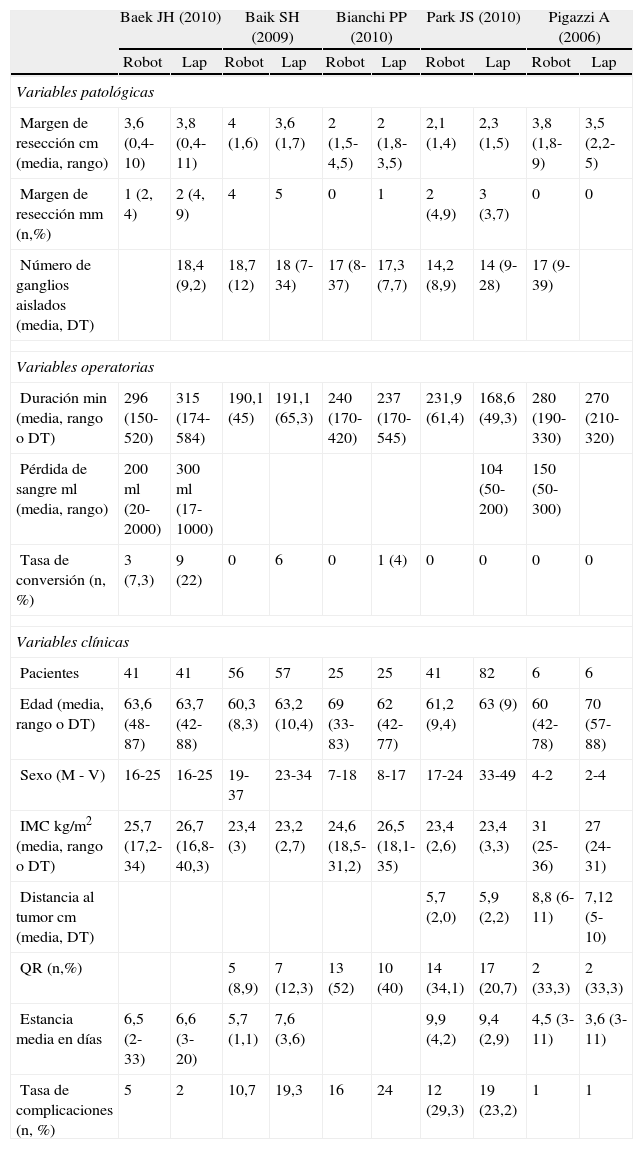
Variables que cumplen los criterios de inclusión
| Baek JH (2010) | Baik SH (2009) | Bianchi PP (2010) | Park JS (2010) | Pigazzi A (2006) | ||||||
| Robot | Lap | Robot | Lap | Robot | Lap | Robot | Lap | Robot | Lap | |
| Variables patológicas | ||||||||||
| Margen de resección cm (media, rango) | 3,6 (0,4-10) | 3,8 (0,4-11) | 4 (1,6) | 3,6 (1,7) | 2 (1,5-4,5) | 2 (1,8-3,5) | 2,1 (1,4) | 2,3 (1,5) | 3,8 (1,8-9) | 3,5 (2,2-5) |
| Margen de resección mm (n,%) | 1 (2, 4) | 2 (4, 9) | 4 | 5 | 0 | 1 | 2 (4,9) | 3 (3,7) | 0 | 0 |
| Número de ganglios aislados (media, DT) | 18,4 (9,2) | 18,7 (12) | 18 (7-34) | 17 (8-37) | 17,3 (7,7) | 14,2 (8,9) | 14 (9-28) | 17 (9-39) | ||
| Variables operatorias | ||||||||||
| Duración min (media, rango o DT) | 296 (150-520) | 315 (174-584) | 190,1 (45) | 191,1 (65,3) | 240 (170-420) | 237 (170-545) | 231,9 (61,4) | 168,6 (49,3) | 280 (190-330) | 270 (210-320) |
| Pérdida de sangre ml (media, rango) | 200 ml (20-2000) | 300 ml (17-1000) | 104 (50-200) | 150 (50-300) | ||||||
| Tasa de conversión (n, %) | 3 (7,3) | 9 (22) | 0 | 6 | 0 | 1 (4) | 0 | 0 | 0 | 0 |
| Variables clínicas | ||||||||||
| Pacientes | 41 | 41 | 56 | 57 | 25 | 25 | 41 | 82 | 6 | 6 |
| Edad (media, rango o DT) | 63,6 (48-87) | 63,7 (42-88) | 60,3 (8,3) | 63,2 (10,4) | 69 (33-83) | 62 (42-77) | 61,2 (9,4) | 63 (9) | 60 (42-78) | 70 (57-88) |
| Sexo (M - V) | 16-25 | 16-25 | 19-37 | 23-34 | 7-18 | 8-17 | 17-24 | 33-49 | 4-2 | 2-4 |
| IMC kg/m2 (media, rango o DT) | 25,7 (17,2-34) | 26,7 (16,8-40,3) | 23,4 (3) | 23,2 (2,7) | 24,6 (18,5-31,2) | 26,5 (18,1-35) | 23,4 (2,6) | 23,4 (3,3) | 31 (25-36) | 27 (24-31) |
| Distancia al tumor cm (media, DT) | 5,7 (2,0) | 5,9 (2,2) | 8,8 (6-11) | 7,12 (5-10) | ||||||
| QR (n,%) | 5 (8,9) | 7 (12,3) | 13 (52) | 10 (40) | 14 (34,1) | 17 (20,7) | 2 (33,3) | 2 (33,3) | ||
| Estancia media en días | 6,5 (2-33) | 6,6 (3-20) | 5,7 (1,1) | 7,6 (3,6) | 9,9 (4,2) | 9,4 (2,9) | 4,5 (3-11) | 3,6 (3-11) | ||
| Tasa de complicaciones (n, %) | 5 | 2 | 10,7 | 19,3 | 16 | 24 | 12 (29,3) | 19 (23,2) | 1 | 1 |
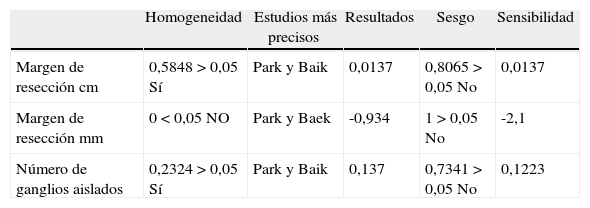
Resultados de variables patológicas
| Homogeneidad | Estudios más precisos | Resultados | Sesgo | Sensibilidad | |
| Margen de resección cm | 0,5848>0,05 Sí | Park y Baik | 0,0137 | 0,8065>0,05 No | 0,0137 |
| Margen de resección mm | 0<0,05 NO | Park y Baek | -0,934 | 1>0,05 No | -2,1 |
| Número de ganglios aislados | 0,2324>0,05 Sí | Park y Baik | 0,137 | 0,7341>0,05 No | 0,1223 |
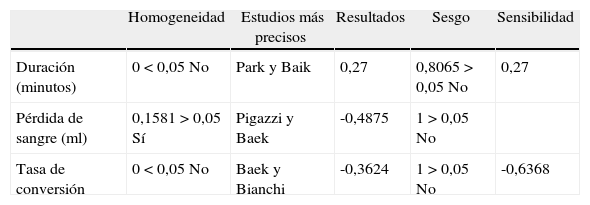
Resultados de variables operatorias
| Homogeneidad | Estudios más precisos | Resultados | Sesgo | Sensibilidad | |
| Duración (minutos) | 0<0,05 No | Park y Baik | 0,27 | 0,8065>0,05 No | 0,27 |
| Pérdida de sangre (ml) | 0,1581>0,05 Sí | Pigazzi y Baek | -0,4875 | 1>0,05 No | |
| Tasa de conversión | 0<0,05 No | Baek y Bianchi | -0,3624 | 1>0,05 No | -0,6368 |
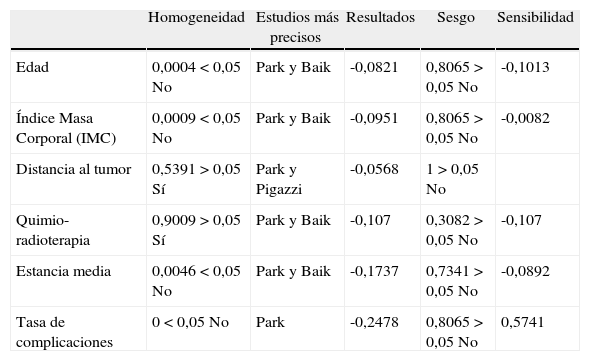
Finalmente, de las 6 variables clínicas incluidas en el análisis, solo hay ligera diferencia en la tasa global de complicaciones (tabla 4), que es algo menor en la EMTR, aunque los estudios no son homogéneos.
Resultados de variables clínicas
| Homogeneidad | Estudios más precisos | Resultados | Sesgo | Sensibilidad | |
| Edad | 0,0004<0,05 No | Park y Baik | -0,0821 | 0,8065>0,05 No | -0,1013 |
| Índice Masa Corporal (IMC) | 0,0009<0,05 No | Park y Baik | -0,0951 | 0,8065>0,05 No | -0,0082 |
| Distancia al tumor | 0,5391>0,05 Sí | Park y Pigazzi | -0,0568 | 1>0,05 No | |
| Quimio-radioterapia | 0,9009>0,05 Sí | Park y Baik | -0,107 | 0,3082>0,05 No | -0,107 |
| Estancia media | 0,0046<0,05 No | Park y Baik | -0,1737 | 0,7341>0,05 No | -0,0892 |
| Tasa de complicaciones | 0<0,05 No | Park | -0,2478 | 0,8065>0,05 No | 0,5741 |
Los resultados del metaanálisis sugieren que no existen diferencias significativas en los resultados de las variables consideradas entre la EMTL convencional y la EMTR en pacientes intervenidos por cáncer de recto.
Sin embargo, el número de estudios válidos y el número de pacientes incluidos en el metaanálisis es demasiado pequeño para obtener conclusiones útiles. Es necesario evaluar los resultados de grandes estudios aleatorizados de mayor calidad, con mayor número de pacientes y con un seguimiento a largo plazo para evaluar la tasa de recidiva local y la supervivencia en ambos grupos de tratamiento. Actualmente, y desde marzo del 2010, está en marcha en el Reino Unido un estudio multicéntrico internacional llamado Robotic versus Laparoscopic Resection for Rectal Cancer (ROLARR)39 que incluye 400 pacientes para realizar un ensayo prospectivo, controlado, aleatorizado y con enmascaramiento sobre el tratamiento quirúrgico del cáncer de recto realizando la EMT con laparoscopia convencional o asistida por robot. Los resultados de este estudio pueden aclarar muchas de las dudas que se plantean sobre los beneficios reales que aporta la asistencia robótica en el tratamiento quirúrgico del cáncer de recto.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.