Objetivos
Métodos
Resultados
Conclusiones
Objectives
Methods
Results
Conclusions
La colitis isquémica (CI) es la forma más frecuente de isquemia del aparato digestivo1,2 y es el resultado de un desequilibrio entre el aporte sanguíneo al colon y sus necesidades. Hay múltiples causas, desde la ligadura de la arteria mesentérica inferior durante una cirugía aórtica hasta el vasospasmo asociado al shock, aunque habitualmente se desarrolla sin obstrucción de los grandes vasos y se la considera una forma de isquemia no oclusiva. En la mayoría de los casos es difícil establecer el desencadenante. La CI puede aparecer a cualquier edad, aunque es más frecuente en la séptima y octava décadas de la vida y en pacientes con antecedentes cardiovasculares. La expresión clínica depende del grado de hipoxia en la pared del colon y de la longitud del segmento involucrado. En los casos leves y moderados, que suponen el 80% del total, la afección se limita a la mucosa o submucosa y es reversible con tratamiento conservador. Sin embargo, en los casos graves, la hipoxia progresa en la pared del colon, y puede afectar al plano muscular o incluso todas las capas (necrosis transmural); puede presentarse con un amplio espectro sintomático. En estos casos, el único tratamiento es la cirugía, para resecar los segmentos de colon no viable, y se acompaña de altas tasas de mortalidad y morbilidad.
El cuadro típico consiste en un paciente de edad avanzada, con antecedentes cardiovasculares y que comienza con dolor abdominal y rectorragia3–7. El diagnóstico se basa en la sospecha y se confirma con una colonoscopia8,9. En los casos más graves se han empleado técnicas de imagen (radiografía simple de abdomen, angiografía o tomografía computarizada) con variadas sensibilidad y especificidad10.
Presentamos una serie amplia de pacientes diagnosticados de CI grave que requirieron cirugía urgente en nuestro hospital, con el objetivo de describir el proceso diagnóstico y los resultados, y evaluar los posibles factores predictores de mortalidad.
MétodosSe trata de un estudio retrospectivo observacional en el que se incluyó a los pacientes operados con diagnóstico de CI en el Servicio de Cirugía de Urgencias del Hospital General Universitario Gregorio Marañón entre 1991 y 2006. Los datos fueron extraídos de la base de datos de CI de nuestro centro. Los hallazgos de la tomografía computarizada (TC) considerados indicativos de CI fueron engrosamiento mural del colon, áreas de insuficiente vascularización de la pared del colon y neumatosis del colon o neumoperitoneo.
A los pacientes que no requerían una laparotomía inmediata se les realizó TC abdominal, colonoscopia o ambas, con una indicación liberal. Los hallazgos de la TC fueron considerados diagnósticos según los antecedentes personales y el riesgo de presentar colitis de otro origen (seudomembranosa, infecciosa, etc.).
Dividimos a los pacientes en dos grupos, supervivientes (grupo A) y no supervivientes (grupo B), y los comparamos mediante la prueba de la χ2 o la t de Student según la variable. Consideramos estadísticamente significativa una p<0,05. El programa utilizado para todo ello fue el SPSS, en su versión 14.0 para windows.
ResultadosLas características generales de la serie están resumidas en la tabla 1. Más del 90% de los pacientes tenían antecedentes cardiovasculares (hipertensión arterial [HTA], diabetes mellitus [DM], cardiopatía isquémica o arrítmica); 66 (65%) pacientes presentaban al menos dos de dichos antecedentes, la HTA fue el más frecuente, seguido de la fibrilación auricular. No encontramos relación con ningún fármaco concreto o familia de fármacos, aunque casi todos los pacientes tomaban alguna medicación. Los fármacos más empleados fueron los diuréticos del asa, inhibidores de la enzima de conversión de angiotensina [IECA] y broncodilatadores, seguidos de antiagregantes y anticoagulantes orales.
Tabla 1. Características generales y pruebas diagnósticas (n=101)
| Varones/mujeres, n | 49/52 |
| Edad (años), media±DE | 73±12 |
| Formas de presentación | |
| Espontánea | 79 |
| Hospitalaria | 35 |
| Postoperatoria | 22 |
| Tras cirugía aórtica | 17 |
| Tras otra cirugía | 5 |
| Clínica | |
| Rectorragia | 34 |
| Dolor abdominal típico | 52 |
| Dolor abdominal atípico | 47 |
| Exploración abdominal | |
| Inespecífica | 38 |
| Defensa abdominal | 63 |
| Signos vitales | |
| Hipotensión (PAS<90 mmHg) | 19 |
| Fiebre | 18 |
| Taquicardia (>100 lat/min) | 31 |
| Datos analíticos | |
| Acidosis metabólica | 62 |
| Leucocitosis | 71 |
| Elevación de LDH | 32 |
| Elevación de amilasa | 34 |
| Colonoscopia (n=39) | |
| Diagnóstica | 36 (92%) |
| TC (n=55) | |
| Diagnóstica | 18 (33%) |
DE: desviación estándar; LDH: lactato deshidrogenasa; PAS: presión arterial sistólica; TA: tomografía computarizada.
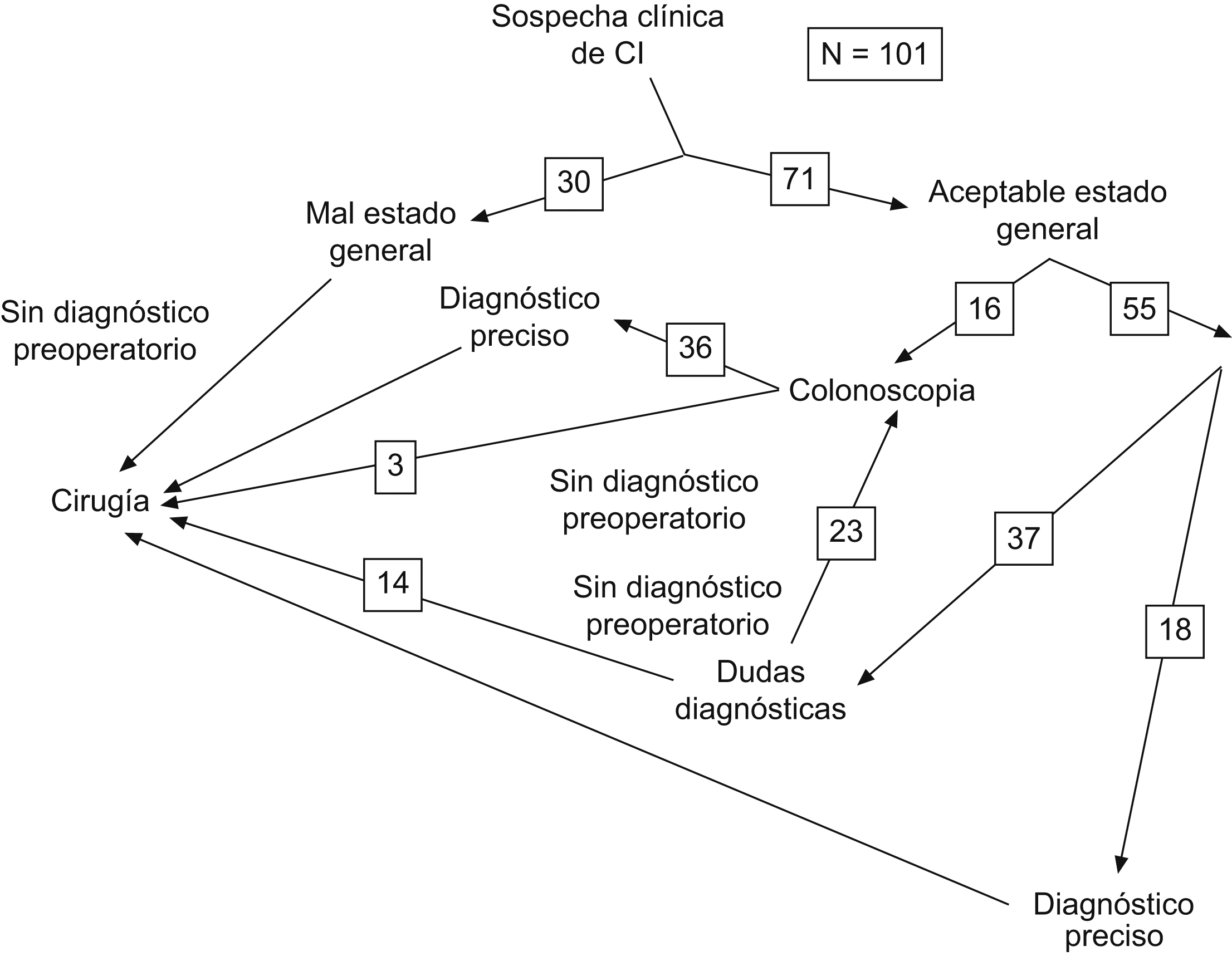
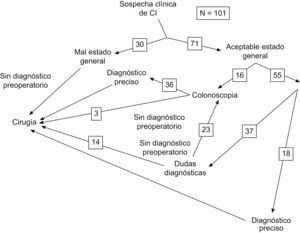
La indicación de cirugía se basó en el cuadro clínico en exclusiva (47 pacientes) o en las pruebas complementarias (54 pacientes). Las pruebas de imagen realizadas están reflejadas en la Figura 1. Se llevó al quirófano a 47 (46%) pacientes con diagnóstico de abdomen agudo, de los que 17 tenían alguna prueba de imagen (fig. 1). Estos datos no se han modificado en ambos períodos; 18 (46%) pacientes, sin diagnóstico preoperatorio en el primer período y 29 (46%), en el segundo. La presencia de neumoperitoneo o neumatosis en la TC y de lesiones gangrenosas extensas en la colonoscopia condujeron a un tratamiento quirúrgico independientemente de la clínica del paciente.
Figura 1. Pruebas de imagen realizadas.
La tabla 2 muestra el tratamiento quirúrgico y los resultados. En el momento de la cirugía 67 pacientes tenían necrosis transmural. Lo más habitual fue la afección de más de un segmento de colon; el colon derecho estaba afectado en 45 ocasiones; el colon transverso, en 35 casos; el colon izquierdo, en 57; el sigma, en 48, y el recto, en 5 casos.
Tabla 2. Tratamiento quirúrgico y resultados
| N=101 | ||
| Técnica quirúrgica | Hemicolectoma derecha | |
| Con anastomosis | 17 | |
| Con ileostomía terminal | 2 | |
| Hemicolectomia izquierda con anastomosis | 6 | |
| Hartmann | 35 | |
| Sigmoidectomía con anastomosis | 2 | |
| Colectomía subtotal | ||
| Con anastomosis | 14 | |
| Con ileostomía terminal | 19 | |
| Laparotomía exploradora | 6 | |
| Laparostomía para “second look” | 10 | |
| Estancia hospitalaria media/mediana (días) | 29/17 | |
| Tiempo hasta diagnóstico media/mediana (horas) | 31/20 | |
| Recidiva a los 3 meses | 7 | |
| Morbilidad | 40 | |
| Mortalidad | 42 |
Las complicaciones quirúrgicas que han presentado los pacientes fueron necrosis del estoma, dehiscencia anastomótica, íleo prolongado, absceso intraabdominal, infección de la herida, evisceración, neumonía e infección del tracto urinario.
No encontramos diferencias en cuanto a sexo, edad, antecedentes, formas de presentación o tiempo hasta el diagnóstico entre los grupos A y B (tabla 3). De entre los pacientes que fallecieron, 20 (47%) estaban ingresados en el hospital por otra causa cuando comenzaron los síntomas; 15 (36%) de ellos, en el postoperatorio de otra cirugía no relacionada. Observamos una tendencia a menores cifras de presión arterial, bicarbonato y pH, y a mayores cifras de lactato deshidrogenasa (LDH), creatinfosfocinasa (CPK), frecuencia cardíaca y temperatura entre los pacientes que fallecieron, aunque sin significación estadística. El tiempo medio desde el inicio de los síntomas al diagnóstico es mayor en los pacientes que fallecieron, sin significación estadística (36 h frente a 28 h). El 93% de los pacientes que fallecieron tenían necrosis transmural, así como el 49% de los pacientes que sobrevivieron (p<0,05). También hallamos una mayor mortalidad (68%) entre los pacientes con CI diagnosticada en el postoperatorio (p<0,01).
Tabla 3. Factores relacionados con la mortalidad
| Fallecidos (n=42) | Supervivientes (n=59) | p | |
| Edad (años) | 73±12 | 72±11 | 0,83 |
| Mujeres/varones | 23/19 | 29/30 | 0,57 |
| Antecedentes cardiovasculares | 0,82 | ||
| Ninguno | 3 | 5 | |
| Uno | 17 | 25 | |
| Dos o más | 22 | 29 | |
| Síntomas | 0,59 | ||
| Típicos | 19 | 29 | |
| Atípicos | 23 | 30 | |
| Exploración abdominal | 0,19 | ||
| Inespecífica | 12 | 25 | |
| Defensa | 30 | 34 | |
| Leucocitos/μl (media) | 16.700 | 16.800 | 0,97 |
| Acidosis | 0,17 | ||
| Presente | 29 | 33 | |
| Ausente | 13 | 26 | |
| Tiempo hasta el diagnóstico (h) | 36±9 | 28±6 | 0,5 |
| Necrosis transmural | 39 (93%) | 29 (49%) | <0,05 |
| Postoperatoria/espontánea | 15/27 | 7/52 | <0,01 |
| Técnica quirúrgica | >0,5 | ||
| Hemicolectomía derecha | 5 | 14 | |
| Hemicolectomía izquierda | 6 | 13 | |
| Hartmann | 8 | 14 | |
| Sigmoidectomía | 0 | 2 | |
| Colectomía subtotal | 17 | 16 | |
| Laparotomía exploradora | 6 | 0 |
De los 17 casos diagnosticados tras cirugía aórtica, 11 iniciaron con dolor abdominal atípico y 14 impresionaban de gravedad en la exploración. No encontramos diferencias en los datos del laboratorio ni en las complicaciones postoperatorias. La mortalidad en este grupo fue de 10 (59%) pacientes.
Dividiendo el estudio en dos períodos iguales, observamos que entre 1991 y 1998 se operó a 39 pacientes, mientras que entre 1999 y 2006 operamos a 62 pacientes.
DiscusiónLa CI es la forma más frecuente de isquemia del tracto digestivo1, con una incidencia estimada de 6–47 casos por 100.000 habitantes/año2. El aumento de su incidencia durante los últimos años puede explicarse por un progresivo envejecimiento de la población, aunque hay que resaltar que nuestra serie sólo refleja los casos más graves.
Algunos autores han descrito series en las que la CI grave mostraba una amplia expresión clínica, y encuentran una clara correlación entre los hallazgos en la exploración física y la gravedad de la enfermedad5,11. Sin embargo, nuestros datos difieren, ya que demustran que incluso los casos más graves pueden presentarse con una exploración inespecífica. Esto subraya la importancia de realizar una colonoscopia tan pronto como se sospeche estar frente a una CI12. De ahí que la mayoría de las publicaciones relacionadas con la CI se hayan centrado en determinar los factores de riesgo y los antecedentes que nos permitan detectarla precozmente3,11,13–15. Otras series6,7 han demostrado una firme relación entre la CI y los antecedentes cardiovasculares, asociación confirmada en nuestro estudio, en el que más del 90% de los pacientes presentaban dichos antecedentes. No hemos hallado una asociación directa con ningún fármaco o familia farmacológica concreta y el riesgo de CI, aunque la mayoría de nuestros pacientes estaban bajo algún tipo de tratamiento debido a sus antecedentes. Tampoco hemos encontrado una asociación importante de CI con otras enfermedades (como síndrome de colon irritable, diverticulosis12, cáncer de colon, estenosis o vólvulos colónicos), como la señalada en la bibliografía7,16 (aproximadamente, el 75% de nuestros pacientes no presentaban ninguna de esas dolencias). Otros autores han observado una mayor gravedad de la CI cuando afectaba al colon derecho17, aunque no hemos podido confirmarlo en nuestra serie.
La prueba de referencia diagnóstica es la colonoscopia8,9. La alta prevalencia de los síntomas típicos, el carácter leve de la mayor parte de los casos y la disponibilidad reducida de la colonoscopia en muchos servicios de urgencias hacen que muchos pacientes con CI leve o moderada reciban el alta sin un diagnóstico definitivo, y esto puede causar un retraso diagnóstico en los casos graves. Desgraciadamente, no se ha encontrado aún un marcador de laboratorio específico para isquemia intestinal, por lo cual la colonoscopia sigue siendo el método diagnóstico de elección en caso de sospecha clínica de CI. Algunos autores han dado mucha importancia a la TC, tanto en el diagnóstico como en el pronóstico de la CI10, aunque en nuestro estudio su sensibilidad fue muy baja, lo que nos plantea dudas respecto a la utilidad de la TC ante una sospecha de CI. En cualquier caso, esto puede cambiar con el desarrollo tecnológico futuro.
Mención aparte merece la medición continua de pH intramucoso del sigma con un tonómetro. El hecho de que el sensor explore una región específica y que mida las condiciones locales de la zona donde probablemente se originen los cambios patológicos puede ayudar a realizar un diagnóstico más precoz18,19. Ha sido empleado en el intraoperatorio de la cirugía aórtica20, para detectar dehiscencia anastomótica en cirugía colorrectal21 y para evaluar la necrosis de la plastia tras esofagectomía en nuestro centro22.
En cuanto a la técnica quirúrgica, la más empleada fue la intervención de Hartmann. Dadas las dificultades para asegurar la extensión de la afectación durante la cirugía, creemos que una colectomía izquierda, con resección de la zona crítica de vascularización del ángulo esplénico, debe realizarse cuando la CI afecte aparentemente sólo al colon sigmoide23; otra posibilidad es la de realizar un second look para evaluar la vascularización del colon 24 a 48 horas después de la primera intervención, como hicimos en 10 pacientes. En 6 casos la intervención se limitó a una laparotomía exploradora ante una afección generalizada del colon y en pacientes con un estado general crítico; todos ellos fallecieron pocas horas después de la cirugía. No observamos diferencias en cuanto a mortalidad o número de reintervenciones en función de la técnica empleada (tabla 3), por lo que consideramos que la decisión de realizar un estoma (colostomía o ileostomía) o una anastomosis primaria, así como la de dejar una laparostomía para un second look precoz, debe tomarla el cirujano basándose en el aspecto macroscópico de la mucosa del colon y la situación clínica del enfermo. No realizamos colecistectomía profiláctica, como proponen Menegaux et al en los casos de CI tras cirugía aórtica, basándose en la fisiopatología compartida con la colecistitis alitiásica (microtrombosis y lesión mural)23, aunque tampoco registramos ningún caso complicado por afección aguda de la vesícula en el postoperatorio.
La mortalidad general de nuestra serie fue del 42%, y coincide con las cifras que se encuentran en la bibliografía2,5,9,11. Sólo un alto índice de sospecha puede mejorar estos resultados, lo que supone un reto para la práctica clínica de cualquier cirujano, máxime si tenemos en cuenta que el 66% de los pacientes de este estudio no tenían rectorragia, y el 47% presentaba un dolor abdominal atípico.
Una de las limitaciones de nuestro estudio retrospectivo, en cuanto a la sensibilidad de la TC, es que durante el período de estudio se han empleado distintos equipos, incluida una TC de nueva generación, durante los últimos 5 años. Por otra parte, la técnica quirúrgica empleada también varía en función de las condiciones generales del paciente, con intervenciones más rápidas (Hartmann, por ejemplo) en los pacientes más afectados.
ConclusionesLa CI grave tiene un pronóstico malo, su diagnóstico suele ser tardío y su incidencia parece estar aumentando. La mayoría de los pacientes son añosos y presentan antecedentes cardiovasculares. El hallazgo intraoperatorio de necrosis transmural y el desarrollo de la CI en el postoperatorio inmediato de otras cirugías son predictores de mortalidad. La taquicardia, la acidosis y la fiebre indican una mayor gravedad del caso, aunque los datos no fueron estadísticamente significativos. Teniendo en cuenta la ausencia de nuevos tratamientos, el diagnóstico precoz parece ser la única manera de mejorar los resultados.
Autor para correspondencia.
Daniel Serralta De Colsa
Dirección: lallamaquellama79@hotmail.com