La cirugía antirreflujo se asocia con frecuencia a tasas significativas de recurrencia y complicaciones, habiéndose propuesto varias técnicas quirúrgicas para minimizarlas. El objetivo del estudio es evaluar los resultados a tres años de una funduplicatura con disección extensa de la unión esofagogástrica (UEG).
MétodosEstudio observacional retrospectivo que incluyó a 178 pacientes con enfermedad por reflujo gastroesofágico (ERGE) o hernia de hiato (HH) a los que se les realizó una funduplicatura con disección extensa de la UEG entre 2015 y 2020. La recidiva herniaria, los síntomas y la calidad de vida al primer año y a los tres siguientes de la cirugía fueron evaluados mediante tránsito baritado, endoscopia y cuestionarios para síntomas y calidad de vida (Gastro Esophageal Reflux Disease-Health Related Quality of Life [GERD-HRQL]).
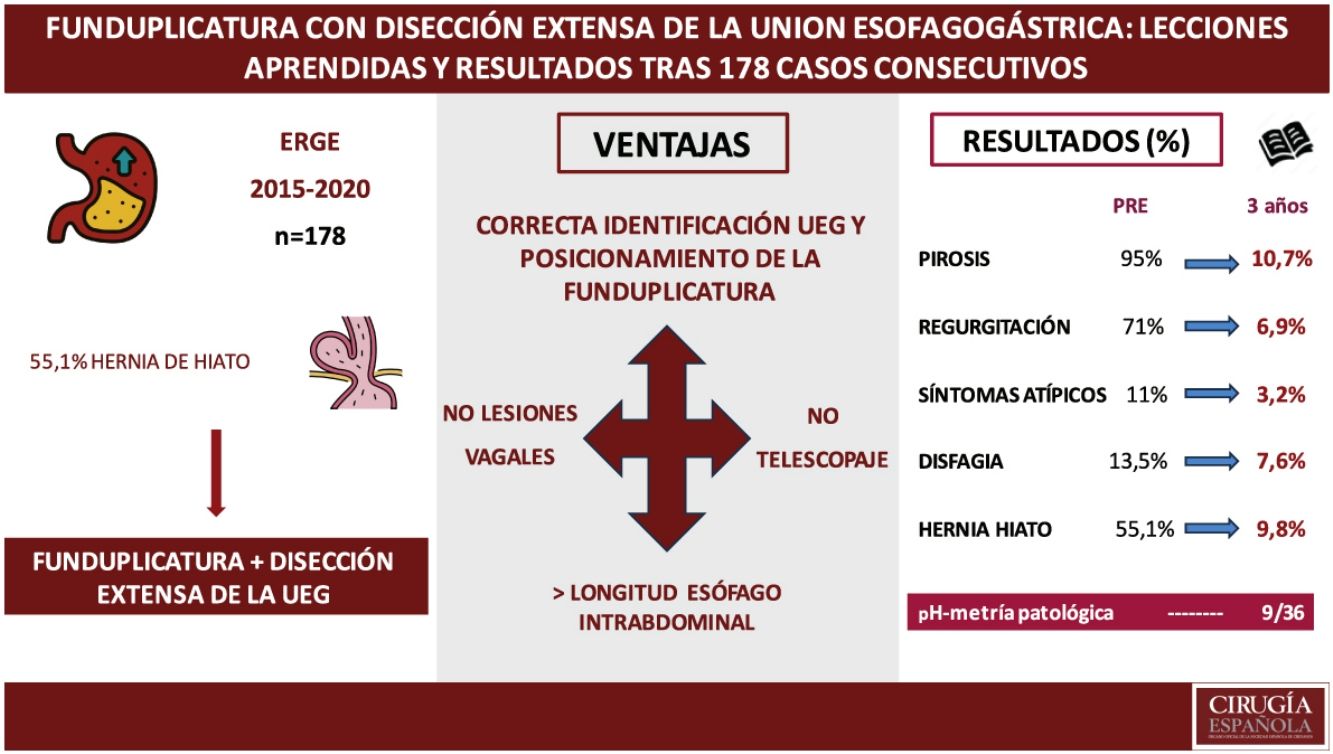
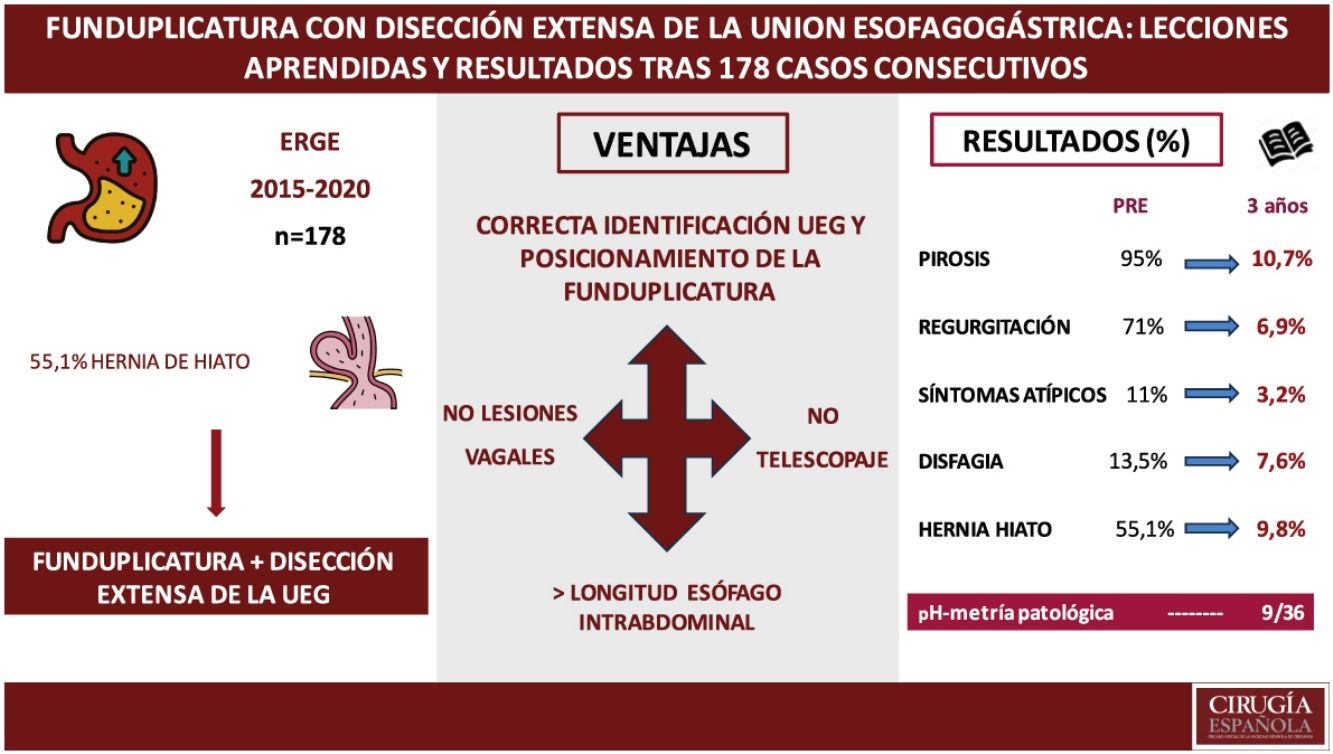
ResultadosLa tasa de pirosis fue de 7,5 y 10,7% al año y a los tres siguientes, respectivamente, regurgitación de 3,8 y 6,9% y disfagia de 3,7 y 7,6%. La presencia de hernia hiatal se evidenció preoperatoriamente en 55,1% y en 7,8 y 9,6% en el seguimiento y la mediana de la escala GERD-HRQL fue de 27, 2 y 0, respectivamente. No aparecieron casos de telescopaje de la funduplicatura ni síntomas que sugieran lesión vagal. No se encontraron diferencias al comparar los distintos tipos de funduplicatura en términos de recidiva del reflujo, complicaciones o recurrencia de la hernia.
ConclusionesLa funduplicatura con disección extensa de la UEG contribuye a su correcto posicionamiento y mejor anclaje, lo que asocia bajas tasas de recidiva herniaria y del reflujo, así como disminuye la posibilidad de telescopaje y lesión vagal.
Antireflux surgery is commonly associated with significant recurrence and complication rates, and several surgical techniques have been proposed to minimize them. The aim of this study is to evaluate the results of a fundoplication with extensive dissection of the esophagogastric junction 1 and 3 years after the procedure.
MethodsRetrospective observational study including 178 patients with gastroesophageal reflux disease or hiatal hernia who underwent fundoplication with extensive dissection of the esophagogastric junction between 2015 and 2020. Hernia recurrence, symptoms and quality of life at 1 and 3 years after surgery were assessed by barium transit, endoscopy and questionnaires for symptoms and quality of life (GERD-HRQL).
ResultsHeartburn rate was 7.5% and 10.7% at 1 and 3 years respectively, regurgitation 3.8% and 6.9% and dysphagia was 3.7% and 7.6%. The presence of hiatal hernia was evident preoperatively in 55.1% and in 7.8% and 9.6% at follow-up and the median GERD-HRQL scale was 27, 2 and 0, respectively. There were no cases of slippage of the fundoplication or symptoms suggestive of vagal injury. No differences were found when comparing the different types of fundoplication in terms of reflux and recurrence or complications.
ConclusionsFundoplication with extensive dissection of the esophagogastric junction contributes to correct positioning and better anchorage of the fundoplication, which is associated with low rates of hiatal hernia and reflux recurrence, as well as absence of slippage and lower possibility of vagal injury.
La enfermedad por reflujo gastroesofágico (ERGE) es uno de los problemas de salud más frecuentes con tasas de prevalencia en Europa de entre 8,8 y 25,9%1. Los síntomas típicos son la pirosis y la regurgitación2, aunque también puede presentarse con dolor abdominal o torácico, disfagia3 o manifestaciones extraesofágicas como tos o faringitis crónica. Puede desempeñar un papel en las exacerbaciones del asma4, la aparición de anemia o hemorragia digestiva alta5.
Los inhibidores de la bomba de protones (IBP) son la base del tratamiento médico6,7, aunque un alto porcentaje de los pacientes con pirosis8 y regurgitación9 no responden al mismo. La cirugía es el único abordaje eficaz ante el fracaso de los IBP10,11.
Desde que en 1937 Rudolph Nissen12 realizó la primera funduplicatura, se han propuesto muchas alternativas de la técnica para controlar los síntomas de la ERGE y minimizar las complicaciones derivadas del procedimiento13.
En 1988, Rossetti et al. describieron una variante técnica para tratar a pacientes con ERGE y úlcera gastroduodenal asociada o esofagitis grave, en la cual realizaban una disección de la unión esofagogástrica (UEG) y una vagotomía proximal selectiva vinculada a la funduplicatura14. Un año más tarde, añadieron una modificación situando este procedimiento entre la UEG y la parte proximal de la curvatura menor y los troncos vagales para mejorar su anclaje y disminuir el riesgo de deslizamiento15.
Dada la ausencia de información en la literatura acerca los resultados a medio y largo plazo de dicha modificación técnica, sistematizamos en nuestra unidad la disección extensa de la UEG previa a la confección de una funduplicatura que queda anclada entre los troncos vagales y el esófago distal. Esto puede aportar una serie de ventajas: la ganancia de longitud adicional de esófago intrabdominal, evitar el malposicionamiento de las valvas, una disminución en la aparición o recidiva de una hernia de hiato (HH) al obstaculizar el deslizamiento del fundus sobre la funduplicatura (telescopaje), y la identificación y preservación de los nervios vagos.
El objetivo de este estudio fue evaluar los resultados clínicos, la recidiva herniaria, la calidad de vida y el grado de satisfacción a uno y tres años en pacientes sometidos a una funduplicatura con disección extensa de la UEG.
MétodosPacientes y técnica quirúrgicaFueron incluidos todos aquellos pacientes intervenidos entre 2015-2020 con diagnóstico confirmado de ERGE sintomático con o sin HH, aquellos con HH tipos I-IV sintomática a los que se les efectuó una funduplicatura como técnica antirreflujo y las cirugías de revisión en las que se incluía la realización de una funduplicatura como parte del procedimiento.
Se consideraron criterios de exclusión: pacientes menores de 18 años, aquellos con resecciones gástricas previas, sujetos con dos o más cirugías antirreflujo anteriores o algunas que requirieron conversión a abordaje abierto.
El estudio fue aprobado por el comité ético institucional.
Técnica quirúrgicaNo se utilizaron sondas nasogástrica, de calibración esofágica, ni urinaria durante la cirugía.
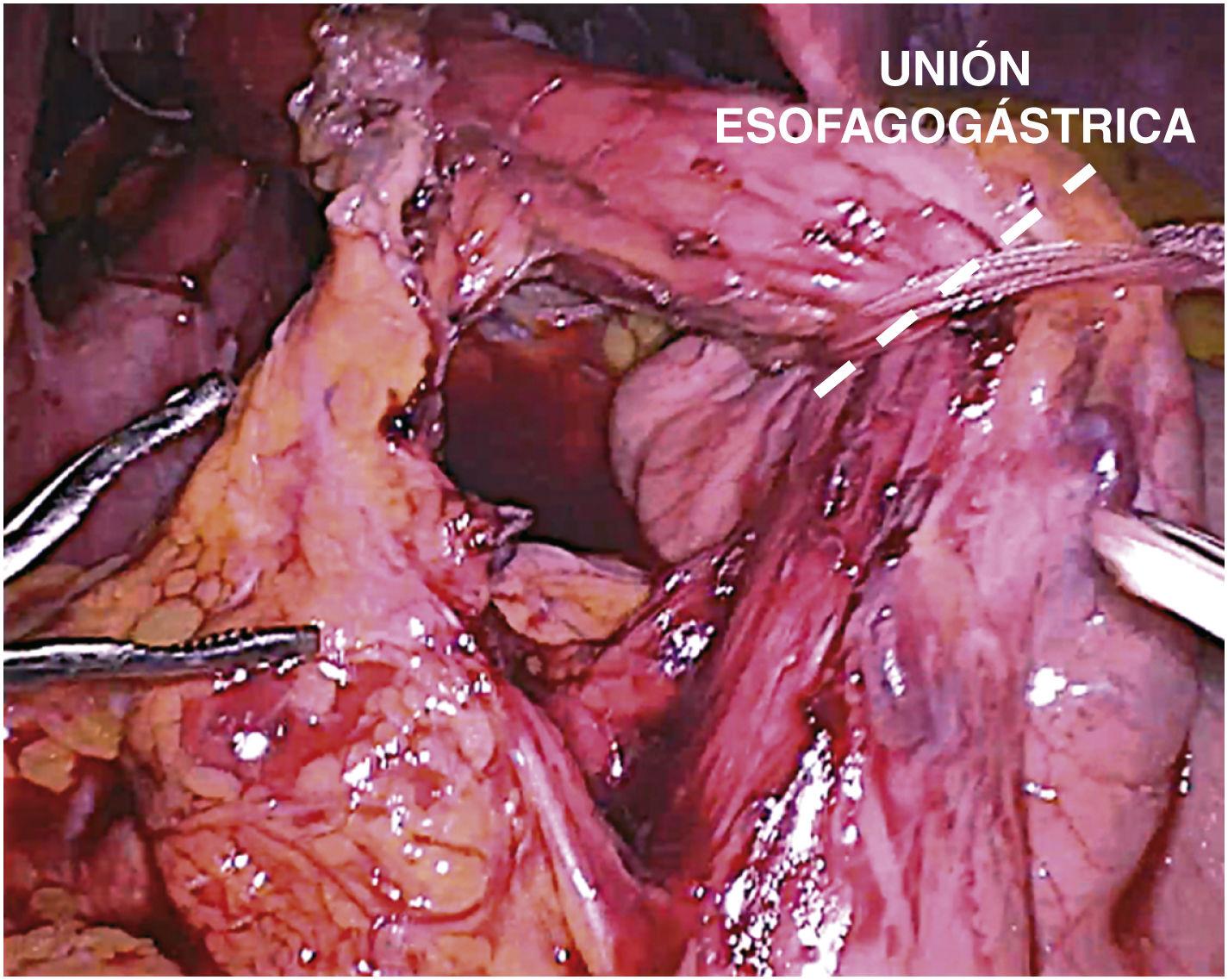
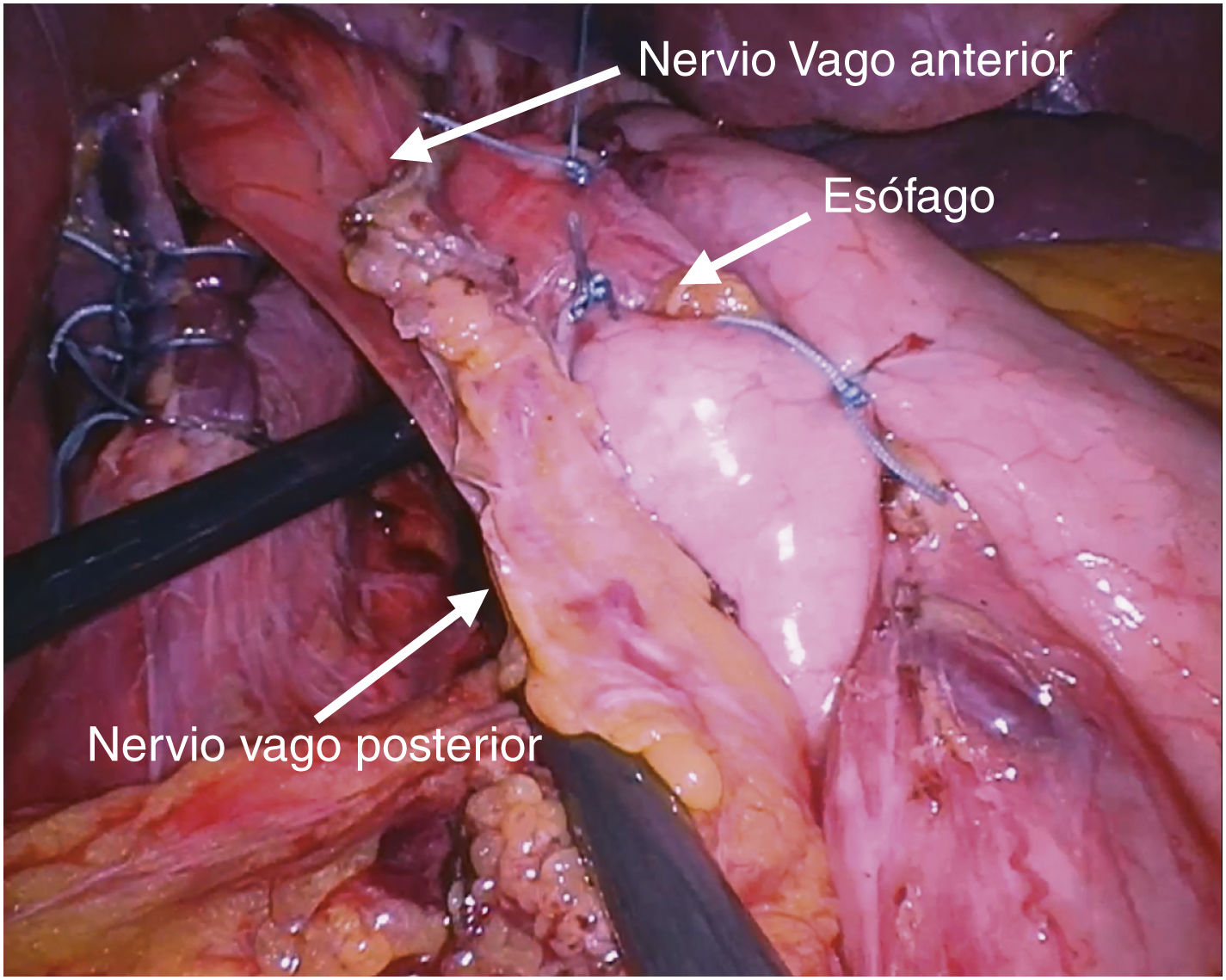
La disección extensa de la UEG comienza en el tercio proximal de la curvatura menor. Se diseca y rechaza posteriormente la almohadilla grasa (fat pad) y se identifican y lateralizan ambos troncos vagales (fig. 1).
Los vasos cortos son seccionados y, posteriormente, se realiza una hiatorrafia con puntos sueltos irreabsorbibles.
Finalmente, en pacientes con trastorno motor severo, se efectuó una funduplicatura parcial tipo Toupet 270°. En aquellos con motilidad conservada, se confeccionó una funduplicatura modificada consistente en la fijación anterior de ambas valvas con un punto sobre el esófago distal y la UEG, y la sutura de cada una de las mismas a la cara anterolateral del esófago. Esta modificación descrita por Luketich16, a la que denominaremos en lo sucesivo funduplicatura 320°, tiene como propósito minimizar el riesgo de disfagia asociado a los procedimientos completos de 360°, manteniendo un correcto control del reflujo (fig. 2).
Evaluación preoperatoria y seguimientoDe manera basal, se llevó a cabo una evaluación clínica, una endoscopia digestiva alta (EDA), tránsito esofagogastroduodenal (TEGD) y un estudio funcional esofágico con manometría y pHmetría de 24 horas. Después de un mes, se realizó una reevaluación clínica y TEGD, y al año y a los tres siguientes de la cirugía se llevó a cabo una nueva valoración, EDA, TEGD y un estudio funcional a aquellos pacientes con sospecha clínica de recidiva. Las complicaciones posoperatorias fueron recogidas y clasificadas según los grados de la escala Clavien-Dindo17. Asimismo, se documentaron las reintervenciones quirúrgicas y los reingresos no programados a 30 y 90 días.
Evaluación de los síntomasEl seguimiento de los pacientes fue realizado por tres cirujanos senior de la Unidad de Cirugía Esofagogástrica mediante una entrevista presencial o telefónica en la que se evaluaron los síntomas posoperatorios, la toma de IBP y la calidad de vida mediante la escala para síntomas y calidad de vida (Gastro Esophageal Reflux Disease-Health Related Quality of Life [GERD-HRQL]) descrita por Velanovich18 que incluye 10 preguntas acerca de la pirosis, disfagia, o la toma de medicación otorgando una puntuación de entre 0 y 45.
Los síntomas típicos, atípicos y otros como la disnea o el dolor abdominal fueron evaluados como variables cuantitativas dicotómicas.
La disfagia se catalogó basándose en la clasificación de Visick en: 1) leve (grado II de Visick), 2) moderada (Visick III) y 3) severa (Visick IV y V)19 (fig. 3).
Endoscopia y estudio radiológicoSe realizaron EDA y TEGD, preoperatoriamente y durante el seguimiento, para el estudio de la esofagitis, el esófago de Barrett y la presencia o recidiva de HH.
Para evaluar la esofagitis y el esófago de Barrett se emplearon la clasificación de Los Ángeles20 y la de Praga21, respectivamente. La toma de biopsias en el esófago de Barrett se realizó según el protocolo de Seattle22.
La evaluación radiológica fue llevada a cabo por dos miembros del Servicio de Radiología. Se definió la recidiva de la HH como el ascenso de la cámara gástrica por encima del nivel del diafragma.
Estudio funcionalLa presencia de reflujo patológico se definió como una puntuación > 14,72 según la escala descrita por Johnson et al.23. Se realizó una manometría convencional en el periodo 2015-2016 y una manometría de alta resolución (HRM) entre 2017-2020, para detectar trastornos de la motilidad esofágica.
A los pacientes con trastornos severos de la motilidad, definidos como tal por el informe de la manometría o con una integral de contractilidad distal<450 en la HRM, se les practicó una funduplicatura parcial tipo Toupet 270°.
Análisis estadísticoLas variables cualitativas se expresan como porcentajes y las cuantitativas como valores medios con desviación estándar (DE) en el caso de distribución normal, utilizándose la mediana con el rango intercuartílico (IQR) para la variable de calidad de vida. Las cualitativas se compararon mediante la prueba X2 de Pearson con corrección de continuidad o la prueba F de Fisher cuando al menos 25% de los valores mostraban una frecuencia esperada inferior a 5. Se empleó el test de la mediana para comparar la calidad de vida según la técnica.
Los análisis estadísticos se realizaron con el software informático paquete estadístico para las ciencias sociales (SPSS Statistics Base para Windows Versión 17.0), versión 17.0. Se asumió un nivel de significación de 5% (p<0,05).
ResultadosUn total de 229 pacientes fueron sometidos a cirugía antirreflujo en nuestro centro entre octubre de 2015 y diciembre de 2020. De ellos, a 178 (77,7%) se les realizó una funduplicatura con disección extensa de la UEG. Todos los casos se efectuaron por vía laparoscópica.
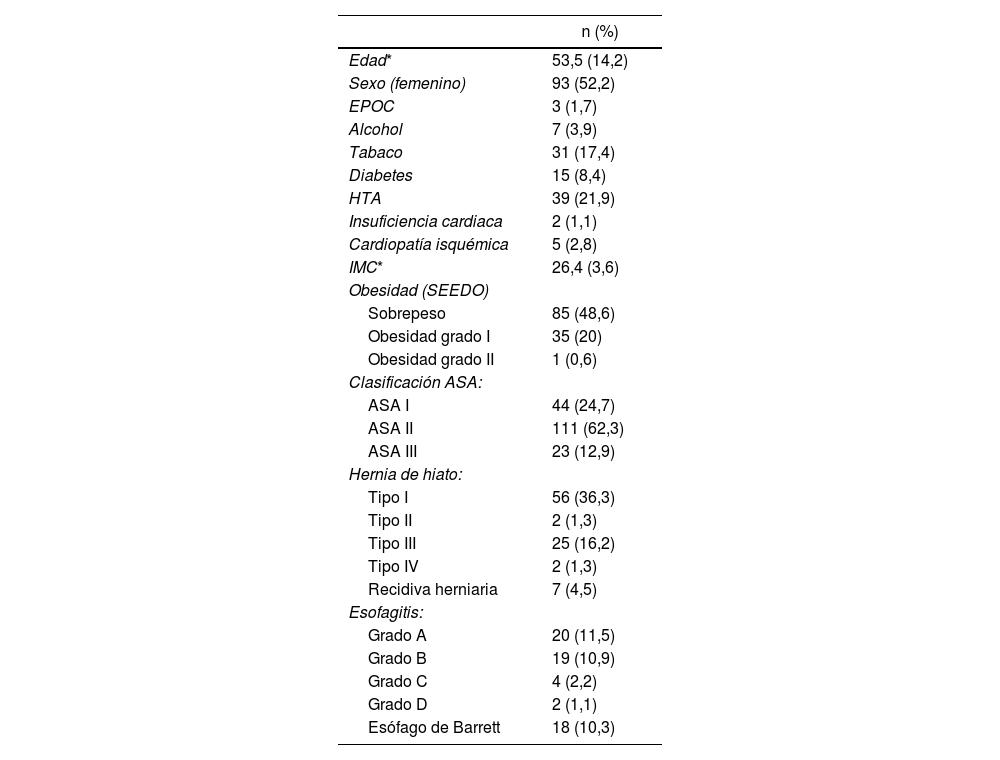
La edad media de los pacientes fue de 53,3 años y 52,2% fueron mujeres. Las características demográficas se encuentran reflejadas en la tabla 1.
Características demográficas de los pacientes
| n (%) | |
|---|---|
| Edad* | 53,5 (14,2) |
| Sexo (femenino) | 93 (52,2) |
| EPOC | 3 (1,7) |
| Alcohol | 7 (3,9) |
| Tabaco | 31 (17,4) |
| Diabetes | 15 (8,4) |
| HTA | 39 (21,9) |
| Insuficiencia cardiaca | 2 (1,1) |
| Cardiopatía isquémica | 5 (2,8) |
| IMC* | 26,4 (3,6) |
| Obesidad (SEEDO) | |
| Sobrepeso | 85 (48,6) |
| Obesidad grado I | 35 (20) |
| Obesidad grado II | 1 (0,6) |
| Clasificación ASA: | |
| ASA I | 44 (24,7) |
| ASA II | 111 (62,3) |
| ASA III | 23 (12,9) |
| Hernia de hiato: | |
| Tipo I | 56 (36,3) |
| Tipo II | 2 (1,3) |
| Tipo III | 25 (16,2) |
| Tipo IV | 2 (1,3) |
| Recidiva herniaria | 7 (4,5) |
| Esofagitis: | |
| Grado A | 20 (11,5) |
| Grado B | 19 (10,9) |
| Grado C | 4 (2,2) |
| Grado D | 2 (1,1) |
| Esófago de Barrett | 18 (10,3) |
ASA: American Society of Anesthesiologist; EPOC: enfermedad pulmonar obstructiva crónica; HTA: hipertensión arterial; IMC: índice de masa corporal; SEEDO: Sociedad Española para el Estudio de la Obesidad.
Habían sido intervenidos previamente de cirugía antirreflujo siete pacientes y cuatro presentaron un telescopaje de la funduplicatura.
En el momento del diagnóstico, 166 sujetos (93,3%) presentaban pirosis, 127 (71,3%) regurgitación y 24 (13,5%) disfagia, 16 leve (Visick II), cinco moderada (Visick III) y tres severa (Visick IV-V). Referían laringitis 22 (12,4%) y 12 (6,7%) disnea secundaria a una HH grande.
La mediana (IQR) de la escala GERD-HRQL preoperatoria fue 27(15).
Todos los pacientes tomaban IBP. De ellos, 48% no respondía al tratamiento y 39,3% presentaba respuesta parcial.
La pHmetría fue patológica en 156 personas (87,6%). La manometría esofágica reveló un trastorno moderado o severo de la motilidad en 36% de los casos.
Se realizó un TEGD preoperatorio en 154 pacientes, mostrando una HH en 85 (55,1%), siendo la más frecuente la de tipo I en 56 (36,6%) (tabla 1).
Se efectuaron 174 EDA (97,7%). Presentaron esofagitis grado A como alteración más frecuente 20 pacientes (11,5%), evidenciándose esófago de Barrett en 18 casos (10,1%). Dos sujetos padecieron displasia de bajo grado (DBG).
La técnica más frecuente fue la funduplicatura tipo Toupet en 105 casos (58,9%) seguida de la 320° (73 casos, 41,1%).
Durante el periodo posoperatorio, seis pacientes (3,3%) presentaron complicaciones médicas, siendo las más frecuentes las respiratorias en tres casos (1,8%, Clavien-Dindo I y II) y cardiovasculares en dos casos (1,2%, Clavien-Dindo II).
Se observaron complicaciones quirúrgicas en siete (3,9%) pacientes, siendo las más habituales la hemorragia en dos casos (1,2%, Clavien-Dindo II) y la infección del sitio quirúrgico en dos sujetos (1,2%, Clavien-Dindo I).
Un paciente mostró una evisceración que requirió cirugía durante el ingreso (Clavien-Dindo IIIb).
Se registró un reingreso a 30 días por una volvulación aguda que necesitó reintervención urgente en otro centro (Clavien-Dindo IVa). No se registraron otros reingresos a 90 días.
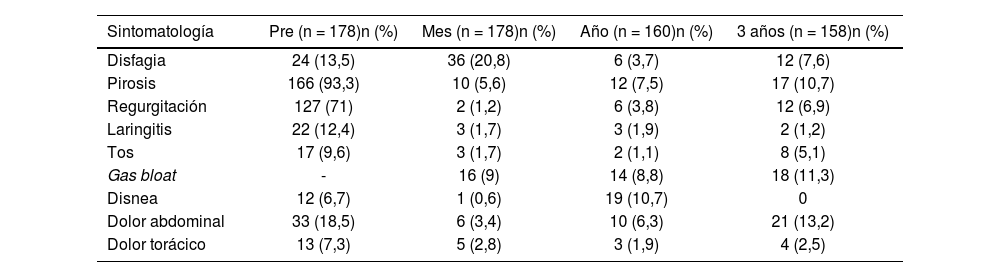
Seguimiento al año de la cirugíaSe obtuvo el seguimiento de 160 (89%) pacientes. De ellos, 10 (7,5%) presentaron pirosis, seis (3,7%) regurgitación y tres (1,9%) laringitis. Referían disfagia seis (3,7%), en cinco casos fue leve (Visick II) y en uno moderada (Visick III). En 14 (8,8%) se observaron síntomas relacionados con el síndrome gas-bloat (tabla 2).
Síntomas presentados preoperatoriamente, al primer mes, al año y a los 3 años de seguimiento
| Sintomatología | Pre (n = 178)n (%) | Mes (n = 178)n (%) | Año (n = 160)n (%) | 3 años (n = 158)n (%) |
|---|---|---|---|---|
| Disfagia | 24 (13,5) | 36 (20,8) | 6 (3,7) | 12 (7,6) |
| Pirosis | 166 (93,3) | 10 (5,6) | 12 (7,5) | 17 (10,7) |
| Regurgitación | 127 (71) | 2 (1,2) | 6 (3,8) | 12 (6,9) |
| Laringitis | 22 (12,4) | 3 (1,7) | 3 (1,9) | 2 (1,2) |
| Tos | 17 (9,6) | 3 (1,7) | 2 (1,1) | 8 (5,1) |
| Gas bloat | - | 16 (9) | 14 (8,8) | 18 (11,3) |
| Disnea | 12 (6,7) | 1 (0,6) | 19 (10,7) | 0 |
| Dolor abdominal | 33 (18,5) | 6 (3,4) | 10 (6,3) | 21 (13,2) |
| Dolor torácico | 13 (7,3) | 5 (2,8) | 3 (1,9) | 4 (2,5) |
Se realizó pHmetría en 41 (25,6%) pacientes siendo patológica en seis. Mantenían tratamiento con IBP 16,2%.
Se efectuó EDA a 40 personas (25%). En 84,6% de los casos desapareció la esofagitis y en 16,6% la metaplasia. Un paciente desarrolló DBG de novo que remitió en un control a los tres meses tras un tratamiento intensivo con IBP.
A 153 (85,6%) sujetos se les realizó el TEGD mostrando recidiva herniaria en 12 (7,8%).
La mediana (IQR) de la escala de calidad de vida GERD-HRQL fue 2 (5).
Seguimiento a los tres añosFueron evaluados 158 pacientes (88,7%). De ellos, 17 (10,7%) referían pirosis, 12 (7,6%) regurgitación y dos (1,2%) laringitis. Se llevó a cabo una pHmetría a 34 (21,5%) siendo patológica en nueve. Presentaban disfagia 12 (7,6%); en dos casos era moderada (Visick III) y en uno severa (Visick IV-V), requiriendo dilataciones endoscópicas con buen resultado clínico.
Se realizaron 49 EDA (31%). En 85,7% desapareció la esofagitis y 83,4% mantenían la metaplasia. Ningún caso presentó displasia y no se registró esofagitis de novo. Un total de 22,7% continuó el tratamiento con IBP.
Se efectuaron 142 (89,8%) TEGD revelando HH en 14 (9,8%). La mediana (IQR) de la escala GERD-HRQL fue 0 (2).
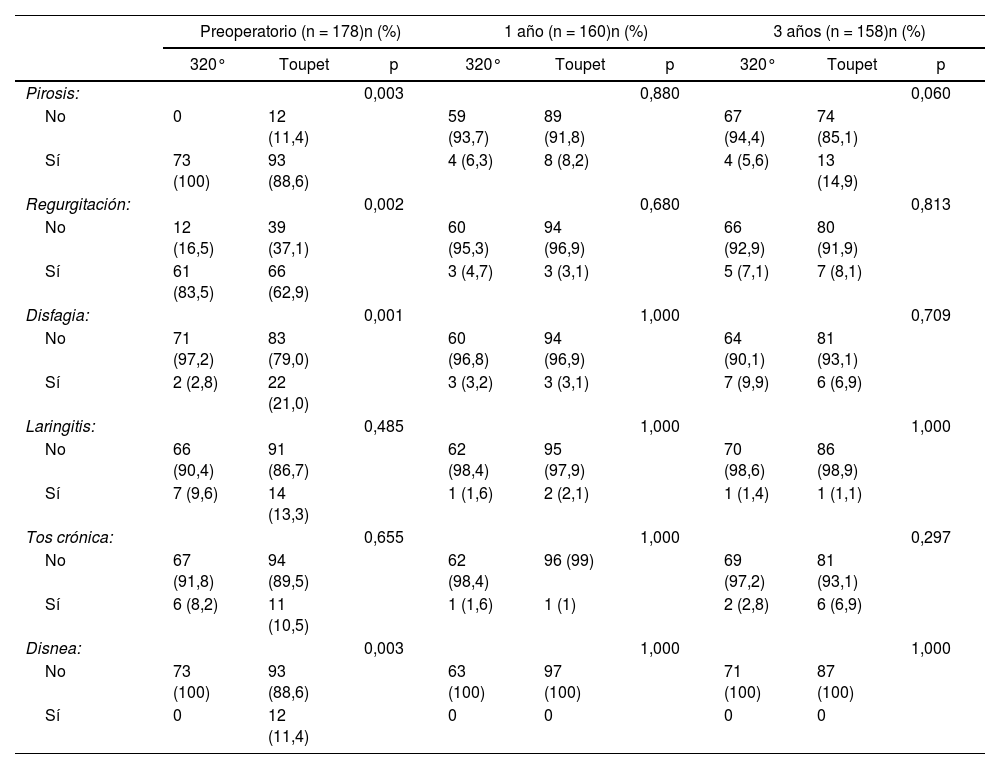
Resultados en función del tipo de funduplicaturaEn nuestro estudio existe una diferencia clínicamente relevante, sin alcanzar significación estadística, en la mayor aparición de pirosis a los tres años en aquellos pacientes a los que se les realizó una funduplicatura parcial (5,6 vs. 14,9%; p = 0,060) (tabla 3).
Sintomatología en función del tipo de funduplicatura
| Preoperatorio (n = 178)n (%) | 1 año (n = 160)n (%) | 3 años (n = 158)n (%) | |||||||
|---|---|---|---|---|---|---|---|---|---|
| 320° | Toupet | p | 320° | Toupet | p | 320° | Toupet | p | |
| Pirosis: | 0,003 | 0,880 | 0,060 | ||||||
| No | 0 | 12 (11,4) | 59 (93,7) | 89 (91,8) | 67 (94,4) | 74 (85,1) | |||
| Sí | 73 (100) | 93 (88,6) | 4 (6,3) | 8 (8,2) | 4 (5,6) | 13 (14,9) | |||
| Regurgitación: | 0,002 | 0,680 | 0,813 | ||||||
| No | 12 (16,5) | 39 (37,1) | 60 (95,3) | 94 (96,9) | 66 (92,9) | 80 (91,9) | |||
| Sí | 61 (83,5) | 66 (62,9) | 3 (4,7) | 3 (3,1) | 5 (7,1) | 7 (8,1) | |||
| Disfagia: | 0,001 | 1,000 | 0,709 | ||||||
| No | 71 (97,2) | 83 (79,0) | 60 (96,8) | 94 (96,9) | 64 (90,1) | 81 (93,1) | |||
| Sí | 2 (2,8) | 22 (21,0) | 3 (3,2) | 3 (3,1) | 7 (9,9) | 6 (6,9) | |||
| Laringitis: | 0,485 | 1,000 | 1,000 | ||||||
| No | 66 (90,4) | 91 (86,7) | 62 (98,4) | 95 (97,9) | 70 (98,6) | 86 (98,9) | |||
| Sí | 7 (9,6) | 14 (13,3) | 1 (1,6) | 2 (2,1) | 1 (1,4) | 1 (1,1) | |||
| Tos crónica: | 0,655 | 1,000 | 0,297 | ||||||
| No | 67 (91,8) | 94 (89,5) | 62 (98,4) | 96 (99) | 69 (97,2) | 81 (93,1) | |||
| Sí | 6 (8,2) | 11 (10,5) | 1 (1,6) | 1 (1) | 2 (2,8) | 6 (6,9) | |||
| Disnea: | 0,003 | 1,000 | 1,000 | ||||||
| No | 73 (100) | 93 (88,6) | 63 (100) | 97 (100) | 71 (100) | 87 (100) | |||
| Sí | 0 | 12 (11,4) | 0 | 0 | 0 | 0 | |||
No se encontró diferencia estadísticamente significativa en la respuesta a los IBP, el estudio de calidad de vida, o recidiva de la HH.
DiscusiónMediante la correcta localización de la UEG y el anclaje de las valvas que aporta la funduplicatura con disección extensa de la misma hemos obtenido a los tres años de seguimiento, índices de pirosis en torno a 10%, regurgitación 7,6% y clínica atípica menor a 5%, manteniendo las tasas de disfagia alrededor de 7%. La tasa de recidiva de HH fue de 9,8% y en más de 80% de los casos ha desaparecido la esofagitis previa, mejorando todo ello la calidad de vida de los pacientes lo que queda evidenciado en una disminución en la mediana en la escala GERD-HRQL de 27 a 0. No hemos encontrado diferencias estadísticamente significativas comparando las distintas variantes de funduplicatura.
El correcto posicionamiento de la funduplicatura ha contribuido a lograr bajas tasas de recidiva clínica de reflujo. Dallemagne et al.24, reflejan tasas de éxito del control del reflujo de 93% tras la funduplicatura de Nissen y 82% después de la de Toupet. En la misma línea, Luketich et al.25 reportan, en 18 meses de seguimiento, pirosis persistente en 23 y 27,6% y regurgitación en 8,8 y 10% de los pacientes sometidos a funduplicatura de Nissen y Toupet, respectivamente.
Por otro lado, en diversas series26,27 se reportan tasas de resolución de la sintomatología atípica tras la cirugía antirreflujo menores a 50%.
La conformación de la funduplicatura con las valvas ancladas entre los troncos vagales y el esófago ha contribuido probablemente a la baja tasa de HH a los tres años de seguimiento.
Las altas tasas de recidiva herniaria descritas en la literatura siguen siendo poco conocidas variando entre 5 y 59%28–30 y continúa siendo uno de los problemas sin resolver de esta patología.
Ningún paciente de nuestro estudio ha presentado telescopaje o malposicionamiento de la funduplicatura durante el seguimiento.
Horgan et al.31 describen hasta 16% de pacientes con telescopaje (hernia tipo Ib de la clasificación de fallos anatómicos) y de 6,4% de sujetos con malposición (hernia tipo III). Pennathur et al.32 reflejan un malposicionamiento de las valvas sobre el cuerpo gástrico en 13,8% de los casos en una serie de 80 cirugías de revisión.
No se ha evidenciado sintomatología relacionada con lesiones vagales durante el seguimiento, como diarrea crónica sin otra causa comprobada o clínica derivada del retraso en el vaciado gástrico.
Lindeboom et al.33 reportan lesiones del nervio vago hasta en 10%, aunque no siempre asociado a un retraso en el vaciado gástrico. Van Rijn et al.34 observaron, del mismo modo, lesiones iatrogénicas del nervio vago en 20% de una serie de 125 pacientes, con un retraso significativo del vaciado gástrico posoperatorio en el grupo con lesión vagal.
Entre las limitaciones del estudio, cabe señalar, en primer lugar, que la recurrencia del reflujo se evaluó basándose en la evolución clínica, realizándose pruebas funcionales de control únicamente en pacientes con sospecha clínica de recidiva. Sin embargo, como señalaron Morgenthal et al.35, la evolución clínica de los sujetos parece ser un método útil y fiable en el seguimiento, ya que únicamente 22 a 29% de los sintomáticos presentaban una pHmetría patológica.
El periodo de seguimiento establecido a tres años puede suponer otra limitación. No obstante, los estudios que evalúan el éxito en términos de control del reflujo y complicaciones de la funduplicatura sugieren que estos resultados a largo plazo se asemejan a los mostrados tres años después de la cirugía36.
Finalmente, representa una limitación la no utilización de cuestionarios validados para la evaluación de los síntomas típicos o atípicos. Lógicamente, al no usar estos, no se ha podido describir con detalle las características de la recidiva clínica, aunque sí su impacto en la calidad de vida mediante el cuestionario GERD-HRQL. No se emplearon, asimismo, herramientas específicas para la valoración de la disfagia.
Como conclusión, la disección extensa de la UEG contribuye al correcto posicionamiento y a un mejor anclaje de la funduplicatura, obteniéndose tasas bajas de recidiva herniaria y de reflujo en este estudio. Ninguno de los pacientes presentó telescopaje de la funduplicatura ni síntomas que sugirieran lesión vagal. Nuevos estudios con un mayor número de participantes y un seguimiento más prolongado nos permitirán obtener hallazgos más sólidos y concretos acerca de los resultados de la técnica.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interésLos autores declaran no tener ningún conflicto de intereses.