Hablar de diabetes es referirse a una de las mayores causas de preocupación de médicos, enfermos y, en general, de cualquiera que tenga responsabilidades en el mundo sanitario. Las cifras son realmente mareantes: 190 millones de diabéticos en el mundo con unas previsiones de alcanzar los 330 en 2025; causa 3,2 millones de muertes al año o, lo que es lo mismo, 6 muertes al minuto; sólo en España hay unos 2 millones de afectados, entre el 5 y el 6% de la población; es la principal causa de ceguera en los países desarrollados y de insuficiencia renal crónica en el mundo, y quienes la padecen tienen una probabilidad muy aumentada de padecer infarto de miocardio (principal causa de muerte, del 50% en los tipo 2) y/o una hemorragia cerebral (el 15% de muertes), así como de sufrir amputaciones (entre 15 y 40 veces más que la población general hasta afectar al 25% de los diabéticos).
Como es lógico, las repercusiones económicas de esta epidemia del siglo XXI son igualmente impresionantes. Se estima entre el 6,3 y el 7,4% del gasto sanitario español se dedica a esta enfermedad (porcentajes similares en los países de nuestro entorno), que al año consume entre 2.400 y 2.675 millones de euros o, lo que es lo mismo, cifras cercanas al medio billón de las antiguas pesetas. Los pacientes con diabetes tienen el triple de probabilidades de ingreso hospitalario que el resto de la población, y el coste por enfermo y año fue, en 2003, de 1.289-1.476 euros frente a los 865 del paciente no diabético.
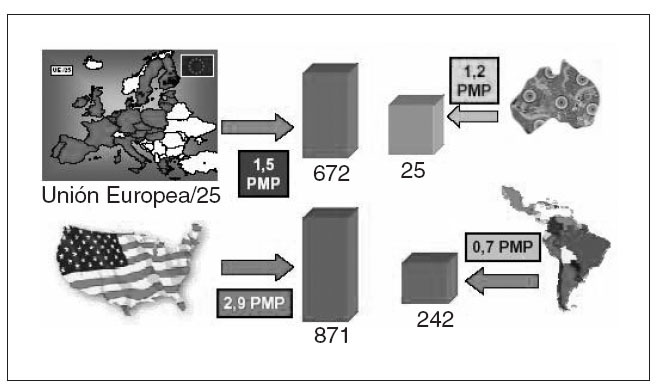
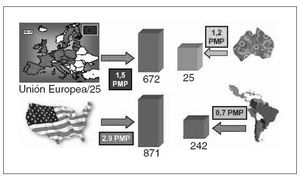
Fig. 1. Actividad de trasplante de páncreas en diversas zonas del mundo en 2003, en cifras absolutas y por millón de habitantes (pmp). Datos del Consejo de Europa.
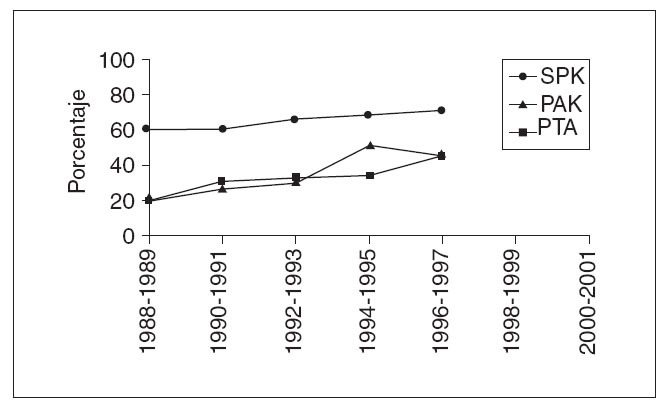
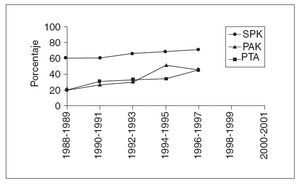
Fig. 2. Trasplante de páncreas en Estados Unidos. Supervivencia del injerto a los 5 años según el período de realización. Datos IPTR/UNOS. SPK: trasplante simultáneo páncreas-riñón; PAK: páncreas después de riñón; PTA: páncreas aislado.
Los estándares modernos del tratamiento de la diabetes tipo 1 quedaron establecidos tras la publicación del Diabetes Control and Complications Trial Research Group (DCCT), en 1993. En este trabajo quedó perfectamente establecido que el tratamiento insulínico intensivo de estos pacientes conlleva ventajas evidentes sobre los convencionales, al tiempo que se apuntó la indicación del trasplante de páncreas como la mejor opción terapéutica en determinados pacientes seleccionados. Cuando el trasplante tiene éxito se consigue un mejor control y/o evolución de los valores de hemoglobina glucosilada, así como de la nefropatía, la neuropatía, las complicaciones de grandes vasos y la calidad de vida. Estas evidencias no hicieron sino consolidarse a lo largo de los años noventa, a medida que las mejoras tanto quirúrgicas como de inmunosupresión introducidas en esta terapéutica fueron mejorando los resultados.
El trasplante de páncreas ha tenido una evolución histórica bastante más tórpida que la del resto de órganos sólidos. Iniciado, como el resto de los grandes órganos extrarrenales, en la década de los sesenta, el trabajo pionero correspondió en 1966 a Richard Lillehei, en Minneapolis (Minnesota). Ocho años más tarde, en 1974, se inicia la técnica en España a cargo del profesor Laureano Fernández Cruz, en el Hospital Clinic i Provincial de Barcelona. De las dificultades iniciales de esta técnica puede dar idea el hecho de que en este centro se realizaran nada menos que el 75% de todos los trasplantes en España durante los 20 años siguientes, algo impensable en cualquier otro órgano.
En parte condicionado por las dificultades quirúrgicas derivadas del trasplante del páncreas exocrino, pronto se planteó la hipótesis de que lo ideal sería implantar tan sólo la parte endocrina previo aislamiento a partir del órgano extraído de un cadáver o del propio enfermo, en casos de autotrasplante por enfermedad pancreática. El primer trasplante de islotes data de 1974, mientras que en España se realizó en 1992, en el Hospital Clínico de Madrid. Los resultados no acompañaron a las expectativas: apenas un 10% de los enfermos permanecían libres de insulina al año de recibir el implante de islotes. Por ello, la publicación, en julio de 2000, por parte de Shapiro, de los primeros resultados del llamado protocolo de Edmonton con un régimen de inmunosupresión sin esteroides a base de tacrolimus, sirolimus y dacliximab, y con un 80% de enfermos sin insulina al año, marcó un antes y un después en esta terapéutica. De nuevo, el interés de gran parte de la comunidad médica y no médica se concentró en los islotes, y en todo el mundo se comenzó a trabajar intensamente en este campo.
Trasplante de páncreasPero volviendo al trasplante de páncreas, solo o en combinación con el de riñón, según los datos del Registro de la Comisión de Trasplantes del Consejo de Europa, al año se llevan a cabo más de 1.800 intervenciones en las principales áreas del mundo, con un claro liderato en términos absolutos y relativos de Estados Unidos (algo también exclusivo del páncreas y que no ocurre con otros órganos). Durante 2003, en ese país se hicieron 871 trasplantes (2,9 pmp) por 672 (1,5 pmp) en los países de la Unión Europea, a distancia de los 242 (0,7 pmp) de América Latina y los 25 (1,2 pmp) de Australia. En España se llevaron a cabo 74 durante 2003 (y en el momento de escribir estas líneas se puede aventurar ya un número similar para 2004), lo que significa 1,7 pmp, superior a la media europea pero netamente inferior a la de Estados Unidos, pese a disponer de casi un 50% más de donantes en relación con la población. Ya tenemos aquí el primer dato que no acaba de cuadrar.
Frente a una línea creciente lenta pero firme en Estados Unidos, la evolución de la actividad trasplantadora de páncreas en el resto del mundo durante los años ochenta y primera mitad de los noventa describe líneas quebradas y con numerosos altibajos tanto en España como en el resto del mundo. Éste es un signo inequívoco de que no se trata de una empresa fácil y que muchos de los que iniciaron uno de estos programas lo abandonaron poco después o lo mantuvieron de forma testimonial a la vista de los pobres resultados obtenidos. De hecho, el International Pancreas Transplant Registry (IPTR) muestra cómo en los primeros años noventa, y pese a aumentar progresivamente el número de centros registrados en el mundo, la actividad total estaba claramente estancada, con una línea en meseta.
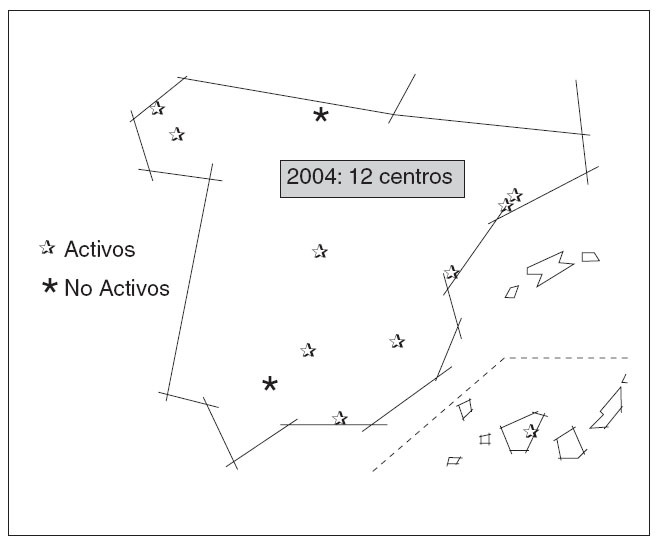
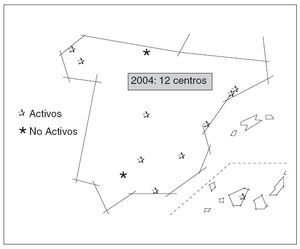
Fig. 3. Localización geográfica de los hospitales españoles con programas activos o inactivos de trasplante de páncreas durante 2004.
La década de los noventa, sin embargo, significó un antes y un después para esta técnica, con unos resultados claramente superiores como consecuencia de las mejoras introducidas tanto en cuanto a las técnicas quirúrgicas como a la inmunosupresión (fig. 2). Las supervivencias funcionales del injerto registradas en el IPTR, de alrededor del 70% a los 5 años, son superponibles a las de otros órganos sólidos y se han incrementado en todas las modalidades posibles (páncreas-riñón simultáneo, riñón seguido de páncreas o páncreas aislado).
Son 12 los hospitales que en España han realizado en algún momento trasplantes de páncreas, aunque 2 de ellos están ahora inactivos, por lo que quedan 10 centros, con la distribución geográfica que se puede observar en la figura 3. Este mapa tiene un interés superior al meramente anecdótico de saber dónde se llevan a cabo estos trasplantes, porque la distancia en kilómetros, en tiempo de isquemia y/o en recursos económicos entre el lugar donde se produce la donación y el hospital donde se debe realizar el acto quirúrgico ha condicionado en gran manera el desarrollo de esta terapéutica y lo sigue haciendo en la actualidad, un segundo dato importante que considerar en nuestro entorno.
TABLA 1. Criterios de utilización de islotes/páncreas
En la tabla 1 se especifican los criterios de aceptación manejados en el documento del Consejo de Europa actualmente en discusión sobre este tema y que, por tanto, se consideran razonables en el plano internacional, lo que desde luego no quiere decir que sean universalmente utilizados. De hecho la mayoría de los equipos quirúrgicos españoles todavía no se plantean, ni de lejos, estos tiempos de isquemia ni tampoco la aceptación de órganos con unos factores de riesgo que se pudieran considerar entre ligeros y moderados.
Las razones son o han sido claras, aunque cada vez lo sean menos. El trasplante de páncreas se ha movido hasta hace poco en un círculo vicioso en el que pese a que el número de enfermos diabéticos en diálisis se está incrementando progresivamente desde hace muchos años, los trasplantes de páncreas-riñón se han estado llevando a cabo con cuentagotas por parte de los clínicos (nefrólogos-endocrinólogos), en gran medida condicionados por las dificultades de la técnica y los resultados históricos no especialmente brillantes, salvo en centros muy concretos. Pocos enfermos en lista de espera, con unos criterios de inclusión no siempre uniformes y a veces condicionados por el especial conocimiento de la técnica en determinados centros o incluso por parte del propio paciente, han hecho que la percepción de necesidad de optimizar la obtención de páncreas en el donante cadáver haya sido más bien escasa.
A diferencia de lo que ocurre con cualquier otro órgano, en el páncreas la desproporción oferta/demanda se ha convertido históricamente en lo contrario: una cierta desproporción demanda/oferta, salvo excepciones de determinados equipos. Los páncreas se han obtenido localmente en la gran mayoría de los casos, algo que dejó de ocurrir hace mucho tiempo con otros trasplantes, sin que se plantease el desplazamiento del equipo o del órgano, salvo en circunstancias muy determinadas. Ni los equipos han percibido que lo tuvieran que hacer, ni las administraciones que los tuvieran que financiar, ni los coordinadores alejados de los centros de trasplante que tuvieran que optimizar su obtención si luego no se iban a extraer. No ha existido, ni existe, el compromiso mutuo que caracteriza el proceso de donación y trasplante de hígado, corazón, riñón o pulmones en los que todo el sistema se vuelca para optimizar su obtención y su utilización.
A ello se une el hecho de que los equipos de trasplante renal que no trasplantan páncreas contemplan con espíritu crítico el “desvío” de un porcentaje nada desdeñable de los riñones con mejores características a los pacientes diabéticos que, de esta forma, se verían sometidos a una presunta “discriminación positiva” frente al receptor joven no diabético que ante el progresivo envejecimiento de la población de donantes podría ver en muchos casos comprometida la probabilidad de recibir un riñón “óptimo” y quedar relegado en diálisis. Bien es cierto que la principal crítica que se hacía en los años noventa a la priorización de determinados pacientes diabéticos (los mediocres resultados que cabía esperar con ellos) ha dejado de tener sentido ante la mejor supervivencia que comentamos antes. En todo caso, los criterios de priorización de estos enfermos han estado, y están, mal definidos y peor cumplidos en la mayoría de las comunidades, sobre todo cuando hay más de un equipo de trasplante renal. A este respecto, cabe destacar (y en otros muchos del tema que estamos tratando) el ejemplo de Andalucía, donde estos criterios están perfectamente definidos y se cumplen con el soporte de la Organización Nacional de Trasplantes (ONT) sin problema alguno.
Por si fuera poco, la extracción quirúrgica del páncreas no es simple, requiere una cierta experiencia, prolonga bastante tiempo el proceso de explante de órganos y, según otros equipos quirúrgicos (en concreto los pulmonares y los de intestino), interfiere con la extracción o pone en peligro la viabilidad de otros órganos. Por último, y aunque esto en España sea aún un futurible, la cierta superposición de criterios de donación páncreas-islotes (tabla 1) hace que en algunos casos y en determinadas zonas pueda haber una cierta competencia entre estos destinos. Un panorama complicado.
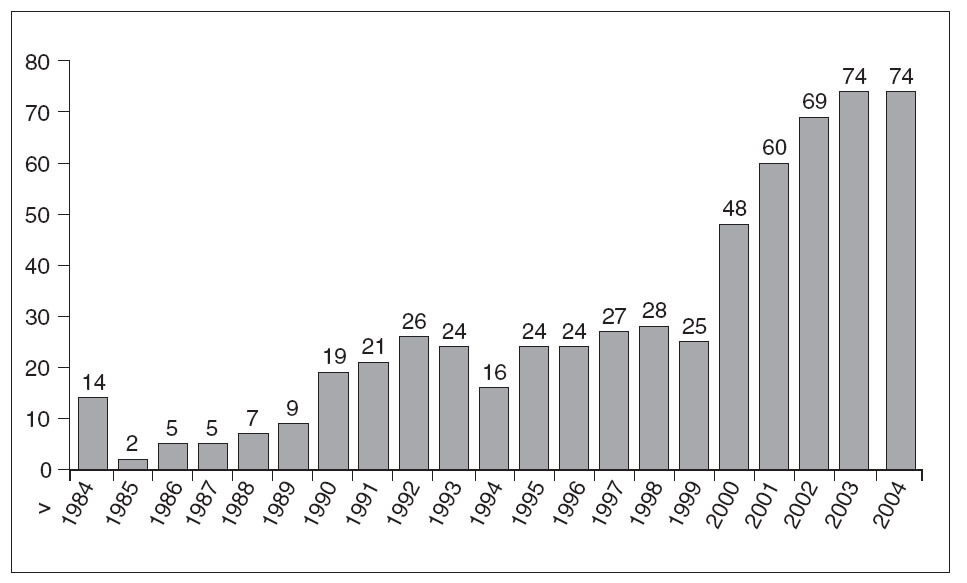
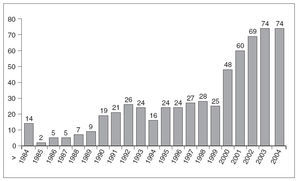
Fig. 4. Actividad de trasplante de páncreas en España.
Pese a todo, mientras los resultados no eran buenos, se hacían pocas indicaciones y en toda España no se llegaba a los 30 trasplantes de páncreas, la mayoría en Barcelona, la situación permanecía deficitaria aunque tranquila y estable. El siglo XXI ha venido a trastocar esta “arcadia feliz”: han aparecido mejores resultados, más indicaciones, más centros, más trasplantes (fig. 4), han crecido las listas de espera (entre 70 y 80 enfermos en toda España), se ha publicado el protocolo de Edmonton, se ha descubierto el aislamiento de islotes, se ha dado el fenómeno mediático de las células madre, la terapia celular confusa o intencionadamente mezclada con la investigación básica... Decididamente todo se complica.
¿Cuál es la situación real de la donación de páncreas en España? Si analizamos a los 1.443 donantes de órganos sólidos registrados en España durante 2003 y vamos excluyendo sucesivamente a los que cumplen los criterios estándares de exclusión a los que nos referíamos antes (edad, antecedentes de diabetes, parada cardíaca, etc.), nos encontramos con que en el mejor de los casos se podría haber utilizado el páncreas para trasplante en 264 donantes, un 18,3% del total. Esta estimación probablemente esté sobrevalorada por el hecho de que se trata de un análisis retrospectivo en el que no todos los donantes tenían, por ejemplo, valores de amilasa u otros datos que los habrían excluido desde el punto de vista clínico, sin contar con los criterios restrictivos de algunos equipos españoles a que antes aludíamos. En todo caso, ello nos da una idea de que estamos hablando de un donante “difícil”: menos de 1 caso de cada 5.
Como finalmente se hicieron 74 trasplantes de páncreas durante 2003, nos encontramos con que sólo se utilizó el 28% de los teóricamente válidos, el 5,1% del total de los donantes. Únicamente 1 de cada 20 donantes en España generó un trasplante pancreático durante 2003, proporción que se ha mantenido estable en 2004.
Fig. 5. Grado de utilización de los donantes potenciales de páncreas en España por comunidades autónomas (2003). Cifras ex presadas en porcentajes de utilización.
En la figura 5 se puede apreciar el grado de utilización por comunidades autónomas de los 264 donantes teóricamente válidos. Sólo en 5 comunidades se supera el 30% de utilización (Cataluña, Andalucía, Galicia, Madrid y Canarias, por este orden), mientras que en las 10 comunidades autónomas que no tenían un equipo de trasplante de páncreas, simplemente no se obtuvo ninguno de estos órganos, al no desplazarse los equipos de extracción. No hacen falta muchas conjeturas para señalar que otro punto fundamental que se debe considerar es que la situación es manifiestamente mejorable.
Sin embargo, ya no se discute seriamente la utilidad del trasplante de páncreas en sus diversas modalidades. La American Diabetes Association, en sus recomendaciones tanto de 2000 como de 2003, establece que se debe considerar la posibilidad del trasplante combinado de riñón y páncreas como tratamiento de elección para el enfermo diabético en diálisis, mientras que el trasplante aislado de páncreas se debe considerar en enfermos con un control metabólico y una calidad de vida inaceptable-mente pobres. En ambas ocasiones, el trasplante de islotes fue considerado como todavía experimental.
Trasplante de islotesComo comentábamos anteriormente, la infusión de islotes pancreáticos, para que regulen el metabolismo hidrocarbonato del paciente diabético, es una panacea largamente acariciada, pero que sólo ha empezado a tomar visos de realidad en la práctica clínica a partir de la publicación del histórico artículo de Shapiro et al, en 2000, con el ya famoso protocolo de Edmonton.
Aunque simple en teoría, la consecución de un aislamiento adecuado de los islotes en unas instalaciones adecuadas es uno de los pasos críticos del proceso. Los islotes se disocian del tejido exocrino mediante enzimas (colagenasa/liberasa) y se visualizan con colorante. Se separan entonces del tejido exocrino mediante gradientes de densidad hasta obtenerlos con el mayor grado posible de pureza. Los islotes se encuentran tanto mejor delimitados cuanto mayor es la edad del donante, lo que hace que el aislamiento sea complicado en los jóvenes y casi imposible en los niños.
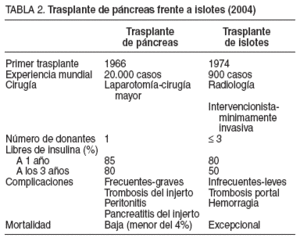
Una vez aislados y purificados, los islotes se inyectan en la porta mediante radiología intervencionista hasta su depósito en la periferia del hígado, en una maniobra que no requiere anestesia general y que tiene como complicaciones potenciales los fenómenos hemorrágicos o trombóticos locales (tabla 2). Aunque los resultados iniciales fueron realmente esperanzadores, son varios los nubarrones que se han cernido sobre este procedimiento y que hacen que en modo alguno se pueda considerar una terapia consolidada, sino aún en fase de ensayo clínico. En primer lugar, las supervivencias iniciales de un 80% al año de enfermos libre de insulina caen al 50% a los 3 años, valor manifiestamente inferior al conseguido con el trasplante de páncreas. Por otra parte, el efecto centro es evidente, con unas tasas de éxito muy distintas de unos a otros hospitales, de forma que la malfunción primaria estimada en la actualidad en un 17% ha oscilado entre el 0 y el 100%. Por si fuera poco, la mayoría de los enfermos requieren 2 o hasta 3 infusiones de islotes lo que complica, encarece y restringe el procedimiento.
TABLA 2. Trasplante de páncreas frente a islotes (2004)
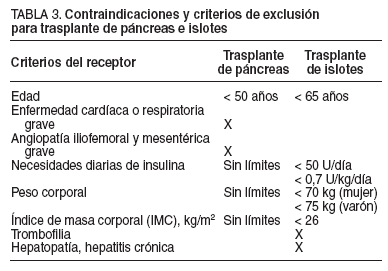
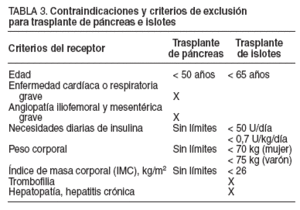
TABLA 3. Contraindicaciones y criterios de exclusión para trasplante de páncreas e islotes
Aunque existe la idea, más o menos generalizada, de que páncreas e islotes son competitivos en cuanto a la derivación de páncreas hacia uno u otro procedimiento o la adscripción de enfermos a una u otra terapéutica, en las tablas 1 a 3 puede observarse cómo la superposición es muy limitada, al menos en el momento actual. Ello no impide, sin embargo, que en el futuro se adivinen multitud de conflictos potenciales ya presentes en algunas zonas de Europa y Estados Unidos que, como ocurre tantas veces, pueden decantarse según las preferencias, las habilidades o los gustos locales y para los que cuanto antes se ponga una solución tanto mejor.
Los islotes estarían indicados preferentemente en el momento actual en el diabético lábil, con función renal normal, peso limitado y no excesivos requerimientos de insulina, lo que limita mucho las indicaciones. En cuanto a los donantes (tabla 1), aunque hay una cierta superposición, sobre todo en la edad, la tendencia evidente es a derivar a los pacientes más jóvenes al páncreas y a los mayores a los islotes. Todo hace pensar, sin embargo, que estos criterios se irán ampliando a medida que los resultados se vayan asentando.
Haciendo una estimación similar a la que describimos con el trasplante de páncreas y excluyendo a los donantes incluidos entre los potenciales para órgano entero, el número de donantes susceptibles de extracción de páncreas para islotes fue, en 2003, de 228 (un 15,8% del total), también en estimación al alza. Ello, unido al 18% de los páncreas, supondría que un 33,8% de los donantes, la tercera parte de los registrados en España (una cifra anual cercana 500) serían susceptibles de ser considerados donantes potenciales de páncreas o islotes.
Sin embargo, el número real que se podría utilizar y, sobre todo, el número de enfermos que es necesario tratar será mucho menor, aunque se optimice al máximo todo el proceso. Las distancias y los tiempos de isquemia existen, la mera distribución de donantes y receptores por grupo sanguíneo hace que sean difíciles de cuadrar en listas pequeñas y, por otra parte, la consideración de un órgano como no adecuado para trasplante depende de criterios y decisiones locales, a veces totalmente impredecibles, pero siempre inferiores a la consideración “de máximos” establecida aquí. En el caso de los islotes, la ya citada utilización de 2 o 3 páncreas por enfermo y el hecho de que el rendimiento de los páncreas utilizados para aislarlos no suela ser superior al 50%, junto con factores logísticos aún más exigentes que para el órgano entero, reduce drásticamente el número de enfermos susceptibles de ser tratados. Una mera estimación rápida de estas cifras y del enorme número de enfermos diabéticos muestra de una forma clara e inequívoca que en caso de que este procedimiento se consolide sólo podría beneficiarse de éste una proporción mínima de pacientes. La solución a gran escala tendría que esperar a la posibilidad de obtener células pancreáticas endocrinas a partir de células troncales, una posibilidad muchas veces apuntada pero que aún hoy se antoja lejana en la práctica clínica.
Situacion española y europeaEn España tan sólo se han llevado a cabo, según el protocolo de Edmonton, 2 implantes de islotes en el Hospital Carlos Haya de Málaga, en 2002. Los efectuados en el Hospital Clínico de Madrid en los noventa, lo fueron con los antiguos protocolos de aislamiento e inmunosupresión, previos al año 2000. Pese a ello, ya se están procesando páncreas con fines de investigación y eventual futuro implante en, al menos, 7 ciudades españolas (y en alguna en más de 1 centro), con intereses locales incipientes en algunas más.
Una simple división de los potenciales páncreas útiles por comunidades autónomas o áreas de influencia, de los necesarios para trasplantar a un solo enfermo y de su cadencia temporal pone de manifiesto que el camino emprendido de diversificación de esfuerzos no es precisamente el más indicado y que una cierta racionalización en estas fases iniciales de la terapéutica sería más que bienvenido.
Por si ello fuera poco, la publicación en los últimos años de hasta 3 directivas de la Unión Europea, orientadas de manera clara hacia la consecución de los máximos estándares de calidad del producto y de seguridad del ciudadano, ha hecho necesario reconsiderar de manera radical procedimientos como el de la infusión de islotes, encuadrables dentro del concepto de “terapia celular somática”. Según la directiva 2003/63 CE, la terapia celular somática se define como “el empleo en humanos de células vivas somáticas autólogas (del propio enfermo), alogénicas (de otro ser humano) o xenogénicas (de animales) cuyas características biológicas han sido sustancialmente alteradas como consecuencia de una manipulación para obtener un efecto diagnóstico, preventivo o terapéutico mediante procedimientos metabólicos, farmacológicos o inmunológicos”.
La inclusión del implante de islotes en este apartado, aunque discutible desde un punto de vista teórico y discutido en diversos ámbitos europeos, parece un proceso irreversible. Ello implica básicamente 2 cosas: por una parte que, como cualquier terapia celular, pasa a tener la consideración de medicamento y su empleo, a estar regulado por criterios similares a éstos en cuanto a estándares elevados (normas GMP), instalaciones, equipo, personal y metodología. Por otra parte, su consideración como medicamento obliga a iniciar su utilización en forma de ensayo clínico, de acuerdo con la directiva 2001/20 CE. Para cerrar el círculo, la recién aprobada directiva 2004/23 CE sobre la calidad y la seguridad de células y tejidos, aún no adaptada a nuestra normativa, establece los estándares correspondientes que se tendrán que cumplir en la donación, la obtención, la evaluación, el procesamiento, la conservación, el almacenamiento y la distribución de todo tipo de células y tejidos.
Por otro lado, la traducción práctica de la implementación de estas directivas es la necesidad, por una parte, de plantear el implante de islotes como un ensayo clínico, con todo lo que ello significa en cuanto a controles, autorizaciones, etc., y, por otra, de disponer de unas instalaciones acordes con los requisitos GMP. En el documento europeo a que antes aludíamos se valora el coste de estas instalaciones entre 1 y 2 millones de euros. A ello hay que unir que los costes de aislamiento de un páncreas pueden oscilar entre 10.000 y 20.000 euros y, teniendo en cuenta que sólo el 50% de los páncreas procesados proporciona islotes válidos y que la mayoría de los enfermos necesita, al menos, 2 infusiones, los costes de aislamiento para un enfermo pueden estimarse entre 40.000 y 80.000 euros. Desde el punto de vista administrativo, la autorización para iniciar uno de estos ensayos corresponde a la Agencia Española del Medicamento, previo informe de la ONT, como organismo técnico encargado de la aplicación clínica de la terapia celular en España.
Teniendo en cuenta los costes de las instalaciones necesarias para cumplir estos requisitos de calidad, la necesidad de experiencia suficiente y mantenida en el aislamiento, con una curva de aprendizaje prolongada como uno de los factores que explican las grandes diferencias entre centros y la necesidad de llevar a cabo una buena selección de enfermos se plantea como una opción más que racional el trabajo en red nacional o supranacional del tipo de las ya existentes (NICE, GRAGIL, etc.). Este esquema parte de la conveniencia de concentrar los centros de aislamiento siempre teniendo en cuenta los criterios de distancia a los hospitales donantes, tiempo de isquemia y costes, con miras a una optimización de los recursos existentes. En el centro de Europa, con unas características demográficas y de distancias desde luego distintas de las españolas, se ha evaluado la conveniencia de disponer de 1 centro de aislamiento y preservación de islotes cada 10-20 millones de habitantes, lo que daría la posibilidad de aislar 100-200 islotes/año/centro. Algunos expertos consideran que se deben procesar, al menos, 2 páncreas semanales para mantener un grado de entrenamiento adecuado del equipo, sin contar los costes básicos de mantener en alerta a toda una estructura de obtención y procesamiento.
Epílogo: acciones que se deben emprenderComo puede apreciarse la situación es tan compleja como apasionante, y desde luego es un ejemplo claro de necesidad de una acción coordinada tanto en el plano nacional como en el internacional, con vistas sobre todo a anticiparnos a los cambios y a la desproporción ofer-ta/demanda que inevitablemente se producirán a medio plazo. Desde el Consejo de Europa se ha comenzado a trabajar sobre el tema, razón de más para que en el plano nacional se afronte la situación sin más demoras.
Por todo ello, desde la Organizacion Nacional de Trasplantes hemos querido abrir un proceso de información y reflexión con todos los agentes implicados en el tema: cirujanos, endocrinólogos, nefrólogos, coordinadores, administraciones, investigadores, responsables del proceso de extracción y manipulación de islotes y, eventualmente, cualquier otro colectivo con interés en estos trasplantes. El objetivo es primero proporcionar toda la información disponible (que no es fácil de sintetizar dados los muy distintos aspectos que intervienen en este asunto), para crear después un grupo de trabajo multidisciplinario que elabore un documento donde se aborden todos estos puntos. Con posterioridad, se iniciaría un proceso de consenso de las recomendaciones elaboradas entre todos los implicados.
El día 10 de diciembre del 2004 se reunió por vez primera este grupo de trabajo en el que se incluye a representantes de:
– Organización Nacional de Trasplantes.
– Coordinaciones autonómicas (Comisión de Trasplantes del Consejo Interterritorial).
–Sociedad Española de Nefrología.–Asociación Española de Cirujanos.
–Asociación Española de Urología.
–Sociedad Española de Endocrinología.
–Sociedad Española de Diabetes.
–Red Española de Islotes Pancreáticos.
–Red Española de Terapia Celular.
–Sociedad Española de Inmunología.
En esta reunión, tras exponer ampliamente todos los aspectos referidos en este escrito, todos los presentes expresaron la conveniencia y la necesidad de este proceso y la apuesta de las respectivas sociedades representadas por llegar a un acuerdo global sobre el tema. Se formaron los grupos de trabajo correspondientes que ya han comenzado a elaborar una propuesta de documento. Los puntos que se deben abordar son muchos y se corresponden con el recorrido que hemos hecho en estas líneas por todo el proceso: criterios de indicación de una y otra terapéutica, de priorización, de distribución de órganos, de desplazamiento de equipos, de extracción de páncreas para trasplante o para islotes, de planificación de centros de islotes y un largo etcétera.
La existencia de este grupo no es óbice para que durante los primeros meses de 2005 se haga una exposición detallada del problema ante los diversos colectivos implicados, con el fin de que la iniciativa sea ampliamente conocida, y los resultados futuros gocen de un amplio consenso. La idea es continuar este proceso a lo largo de los próximos meses para finalizar en una reunión de consenso a la que serán invitados todos los interesados y a la que se dará una amplia difusión.
Dice un proverbio árabe que “lo fácil ya está hecho, lo difícil lo haremos y lo imposible lo venceremos”. Aunque son muchos y muy diversos los actores que intervienen en este problema, existe una amplia voluntad de entendimiento que sin duda conducirá a que encontremos las mejores soluciones en un plazo razonable. Son muchos los enfermos diabéticos que pueden beneficiarse de una optimización del proceso.
Este artículo también se ha publicado íntegramente en la revista Nefrología ( Nefrologia. 2005;25:1-8).
Correspondencia: Dr. R. Matesanz. Coordinador Nacional de Trasplantes. Organización Nacional de Trasplantes. Sinesio Delgado, 6. 28029 Madrid. España. Correo electrónico: rafmatesanz@yahoo.es
Manuscrito recibido el 30-12-2004 y aceptado el 10-1-2005.
Bibliografía recomendadaBland BJ. International Pancreas Transplant Registry (IPTR). Minneapolis, Minnesota. Disponible en: http://www.iptr.umn.edu
Committee of Experts on the Organisational Aspects of Co-Operation in Organ Transplantation (SP-CTO). Islet of Langerhans transplantation in Europe. Documento restringido en fase de preparación.
Matesanz R, Miranda B. Transplant Newsletter. Council of Europe. Madrid: Aula Médica; 2003. Organizacion Nacional de Trasplantes. Disponible en: http://www.ont. es/esp/estadisticas/f estadisticas.htm Robertson RP. Islet transplantation as a treatment for diabetes. A work in progress. N Engl J Med. 2004;350:694-705.
Shapiro AMJ, Lakey JRT, Ryan EA, et al. Islet transplantation in seven patients with type 1 diabetes mellitus using a glucocorticoid free immunosuppressive regimen. N Engl J Med. 2000;343:230-8.
The Diabetes Control and Complications Trial Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med. 1993;329:977-86.