La insuficiencia venosa crónica es una enfermedad muy prevalente, de una gran relevancia sanitaria y económica, y en la que en los últimos años se están produciendo importantes novedades terapéuticas. Aunque en la mayoría de los hospitales públicos su asistencia recae sobre los cirujanos generales, éstos no disponen de una formación continuada adecuada y continúan realizando habitualmente una cirugía clásica. Además, su presencia en el ámbito científico, organizativo y formativo es casi nula. Presentamos una actualización sobre las novedades en flebología y, aprovechando los resultados preliminares de una encuesta nacional, reflexionamos sobre la situación actual de la flebología y el futuro que los cirujanos generales tienen en este campo.
Chronic venous insufficiency is a highly prevalent condition, with significant health and economic repercussions. Although important therapeutic developments have been introduced in recent years, the majority are dealt with by general surgeons in national health hospitals. These surgeons do not have the required and continuous training, and continue to perform classic surgery techniques. Also, their presence at scientific, organisational meetings and training is almost nil. We present an update on developments in phlebology, and tapping into the preliminary results of a national survey, we reflect on the current status of phlebology and beyond for those general surgeons who should have a role in this field.
En nuestro hospital, donde al no haber angiología y cirugía vascular (ACV), operamos varices, nos llamaba la atención el poco peso que los cirujanos generales (CGD) le damos a esta enfermedad. Aunque hay unidades funcionales (UF) de enfermedades menos prevalentes, manteníamos infravalorada la flebología: no cuestionábamos la técnica clásica, no auditábamos resultados, nunca habíamos comunicamos nada sobre el tema. Después comprobamos que esta situación era común a otros hospitales, e incluso a escala institucional. Aunque en la AEC hay una sección de angiología y cirugía vascular, la inclusión de este tema en nuestros congresos, y en CirugíaEspañola, era testimonial.
Por este motivo, en 2007, decidimos poner en marcha una UF de varices. Desde ese momento descubrimos que la flebología es una especialidad de mucha actualidad, con importantes controversias sobre el manejo de estos pacientes, y que nos brindaba enormes posibilidades de mejora tanto asistencial como científica. Pero además, nos hemos convencido de que, dada la realidad de la ACV en nuestro país, implantada sólo en algunos hospitales1 y desbordada por enfermedades arteriales, los CGD debemos reivindicar mayor protagonismo en esta afección. Este trabajo tiene como objetivo polemizar sobre esta cuestión y hacer un repaso sobre las cuestiones más controvertidas en flebología. Además, presentamos datos de una encuesta postal enviada a todos los servicios de CGD públicos (fig. 1), y de la que llevamos recibidas 105 respuestas. Esperamos publicar los datos completos cuando finalice su recogida.
Importancia de la insuficiencia venosa crónicaLa insuficiencia venosa crónica (IVC) es una de las enfermedades más prevalentes que trata un cirujano. Un estudio transversal, realizado en Escocia sobre población general, estimó que un 40% de los varones y un 32% de las mujeres presentaban varices tronculares susceptibles de cirugía2. Esta alta prevalencia es mayor en España, donde otro estudio realizado en 20013 evidenció un 57% de pacientes con signos de IVC, y una actualización de 2006 lo elevaba al 62%4.
La IVC también tiene una importante repercusión socioeconómica, especialmente la úlcera venosa (UV), que afecta hasta el 1% de la población2. En Reino Unido la duración media de la úlcera es de 9 meses, que persiste más de 2 años en un 20% de los pacientes5. En Estados Unidos la UV causa 2 millones de días de baja laboral, con un coste de 3 billones de dólares/año6. En España, un 2,1% de los pacientes han tenido al menos 1 episodio de baja laboral relacionado con la IVC, y el 1,9% ha precisado al menos un ingreso hospitalario3.
Pese a ello, en nuestro país se le presta poca atención en el primer eslabón asistencial (atención primaria y mutuas laborales), como ponen de manifiesto estudios recientes llevados a cabo por médicos de primaria y CGD7,8. Esto conduce a que la IVC sea casi siempre derivada al cirujano y se convierta en uno de los diagnósticos más frecuentes en consulta. En concreto, en nuestro hospital, realizamos en enero de 2008 un estudio prospectivo, en que analizamos las primeras 100 visitas consecutivas, y comprobamos que la IVC suponía la segunda causa más frecuente de remisión (24%), después de la enfermedad anal (30%) (tabla 1).
Enfermedad que motiva la remisión como primera visita desde atención primaria
| Anorrecto (%) | 32 |
| Insuficiencia venosa crónica (%) | 24 |
| Problemas dermatológicos (%) | 14 |
| Pared abdominal (hernia-eventración) (%) | 12 |
| Mama (%) | 6 |
| Sinus pilonidal sacrococcígeo (%) | 4 |
| Colelitiasis (%) | 4 |
| Otros (%) | 4 |
Estudio prospectivo que analiza las primeras 100 visitas consecutivas (enero, 2008).
Esta alta frecuencia de pacientes en nuestras consultas sitúa al GRD 119, «ligadura y stripping de vena de miembros inferiores», entre los más frecuentes de un servicio de CGD en un hospital sin cirugía vascular9. Además, la demanda de cirugía de varices está creciendo en algunos países, como Reino Unido10, al demostrarse su beneficio en las 3 indicaciones principales que demandan los pacientes: mejora de la calidad de vida11, disminución del riesgo de enfermedad tromboembólica (ETE)12 y mejora estética13.
¿Quién trata en nuestro país a los pacientes con varices?Si fuéramos realistas, deberíamos responder que la medicina privada, por fracaso de la pública. Pero el ámbito de este trabajo es la medicina pública y a ella nos referiremos. Conocer las varices que operamos los CGD y las que operan los vasculares es muy difícil por falta de datos. Vamos a aproximarnos a la realidad analizando los datos sobre la dotación asistencial de cada hospital y la actividad realizada en cada grupo de hospitales.
Según la dotación asistencial del hospital, podemos diferenciar entre hospitales que dispongan o no de cirujanos vasculares.
Según los datos facilitados por la AEC en marzo de 2008, hay aproximadamente en nuestro país 270 hospitales públicos, todos ellos con CGD. Por el contrario, según datos publicados por los ACV, sólo 91 hospitales públicos disponen de vasculares1. Por lo tanto, en 179 hospitales públicos (el 66% del total) no hay vasculares. Como la cirugía de varices entra en la cartera de servicios de la sanidad pública, en 2/3 partes de los hospitales públicos son los CGD los que deben asumir esta especialidad.
Estos datos se asemejan a los de la encuesta: de los 105 hospitales que han respondido, en 59 (56,2%) no hay servicio de ACV. Podría ocurrir que los CGD de estos hospitales sin vascular derivasen a los pacientes a hospitales con CVA. Esto sólo ocurre en 8 de estos 59 hospitales (6 lo remiten a ACV del hospital de referencia, y 2 conciertan con la privada).
Pero, además, ocurre que en los 46 hospitales donde coexisten cirujanos vasculares y generales, ambos servicios asumen esta cirugía. Ello ocurre en 9 hospitales, y en ellos el porcentaje medio de varices que operan los CGD es del 31%, que oscila en el 5–90%.
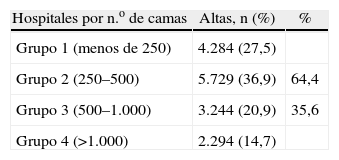
Según la categoría del hospital, los únicos datos generales estatales están en la página web del Ministerio de Sanidad y Consumo, que clasifica el número de altas por GRD y categoría del hospital14. Si consideramos que los hospitales con ACV están situados mayoritariamente en los grupos 3 y 4 (más de 500 camas), mientras que los hospitales de los grupos 2 (250–500 camas) y, sobre todo, los del grupo 1 (menos de 200 camas) no suelen contar con vasculares, el porcentaje de altas del GRD 119 en cada grupo nos sirve de referencia aproximada. En la tabla 2, observamos que el 64,4% de las intervenciones se realizan en hospitales pequeños y, muy probablemente, por un CGD. Por lo tanto, los CGD intervenimos en, aproximadamente, 2/3 de las operaciones de varices que se realizan en la sanidad pública.
Datos del Ministerio de Sanidad y Consumo sobre el número de altas del GRD 114, según el grupo de hospitales por número de camas14
| Hospitales por n.o de camas | Altas, n (%) | % |
| Grupo 1 (menos de 250) | 4.284 (27,5) | |
| Grupo 2 (250–500) | 5.729 (36,9) | 64,4 |
| Grupo 3 (500–1.000) | 3.244 (20,9) | 35,6 |
| Grupo 4 (>1.000) | 2.294 (14,7) |
Vamos a hacer referencia tanto al diagnóstico (clasificación CEAP, utilidad de la ecografía) como al manejo terapéutico (tratamiento compresivo, extensión y técnica de la safenectomía, técnicas menos invasivas, etc.).
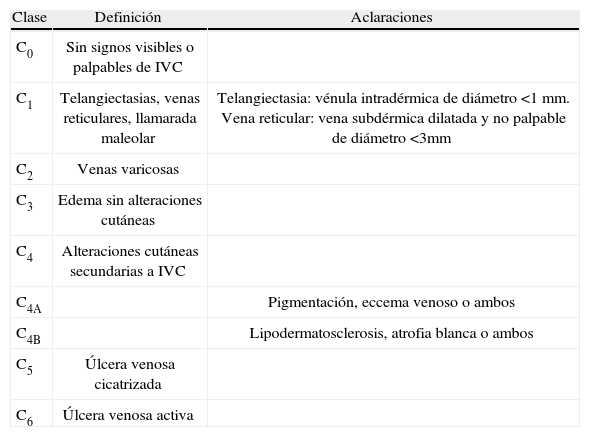
Clasificación CEAP (clinic, etiologic, anatomical y phisiopatologic): como enfermedad evolutiva, la IVC muestra una amplia escala de síntomas y signos lo que dificulta la estadificación de pacientes para comparar resultados. Recientemente el International Consensus Committee on Venosus Disease ha propuesto la clasificación CEAP15,16, la cual ha sido universalmente aceptada17. Dada su exhaustividad, en la práctica sólo se suele utilizar la clasificación clínica (C)18 (tabla 3).
Clasificación clínica (C) de la insuficiencia venosa crónica (IVC) propuesta por el International Consensus Committee on Venous Disease
| Clase | Definición | Aclaraciones |
| C0 | Sin signos visibles o palpables de IVC | |
| C1 | Telangiectasias, venas reticulares, llamarada maleolar | Telangiectasia: vénula intradérmica de diámetro <1mm. Vena reticular: vena subdérmica dilatada y no palpable de diámetro <3mm |
| C2 | Venas varicosas | |
| C3 | Edema sin alteraciones cutáneas | |
| C4 | Alteraciones cutáneas secundarias a IVC | |
| C4A | Pigmentación, eccema venoso o ambos | |
| C4B | Lipodermatosclerosis, atrofia blanca o ambos | |
| C5 | Úlcera venosa cicatrizada | |
| C6 | Úlcera venosa activa |
Importancia del tratamiento compresivo: la terapia compresiva no sólo mejora la clínica, sino que reduce el diámetro de las venas; incrementa el flujo venoso y disminuye el riesgo de trombosis. Asimismo, estimula el sistema fibrinolítico, con lo que mejora el flujo linfático y se reduce la filtración extravascular, esto minimiza el edema y los cambios cutáneos19. Además, en estadios precoces corrige la incompetencia valvular debida a la dilatación si aún no hay cambios fibrosos20. La terapia compresiva es útil, segura y barata, y debería recomendarse como primera línea de tratamiento y como tratamiento adyuvante de cualquier otro18. Un reciente ensayo aleatorizado demuestra mayor beneficio cuanto más avanzado es el estadio; se consigue prevenir la recidiva de la ulcera tras cirugía21. Junto con la terapia compresiva, también ha demostrado beneficio la mejora de las condiciones físicas (ejercicio, adelgazamiento, etc.)22. Los CGD debemos dedicar tiempo suficiente de nuestras consultas a conseguir su implantación.
Evolución del tratamiento quirúrgico: la cirugía de la IVC tiene 3 objetivos básicos: a) eliminación de venas dilatadas; b) mejora estética, y c) baja morbilidad y recidiva23. Dado que no hay consenso sobre la técnica ideal, se han descrito múltiples abordajes terapéuticos, como la ligadura, el arrancamiento (stripping) o la oclusión por calor o esclerosis18.
Tratamiento quirúrgico clásico (ligadura del cayado y safenectomía): la primera cirugía moderna data de 1905, y consistía en la extirpación exhaustiva del cayado y de toda la vena safena interna con ligadura de sus tributarias24. La agresividad de este tratamiento fue minimizada con la introducción del fleboextractor que arranca la safena con menor traumatismo quirúrgico25. Posteriormente, aunque algunos autores, basándose en que el mecanismo más trascendente de la IVC es el reflujo gravitatorio, defendieron la ligadura aislada del cayado, la publicación de mejores resultados cuando se combinaba la safenectomía frente a la simple ligadura26,27 consolidó definitivamente esta técnica.
Modificaciones al tratamiento clásico: aunque no hay discusión sobre la indicación de ligar un cayado insuficiente junto a sus colaterales, y extirpar la safena insuficiente para minimizar el riesgo de recidiva, sí hay controversia en cuanto a la extensión de la safenectomía13. Está aceptado que el grado de insuficiencia de la safena no es uniforme28 y suele limitarse a su porción más proximal; generalmente, la porción distal es competente29–31. Por ello, numerosos autores critican la exéresis sistemática de toda la safena, que imposibilita su uso posterior para revascularización miocárdica32–34. Además, la cirugía de la safena distal conlleva parestesias por lesión del nervio safeno interno35–38, que son 6 veces más frecuentes cuando la safenectomía se extiende hasta el tobillo29. Por ello se recomiendan 2 modificaciones técnicas:
- •
La safenectomía parcial, con limitación del stripping hasta el punto donde la safena suele tener sus perforantes en el tercio superior de la pierna, aproximadamente 20cm por debajo de la rodilla, aunque lo ideal es localizar el punto exacto mediante ecografía Doppler color (EDC)39–41.
- •
La safenectomía invertida mediante un fleboextractor dotado de un ojal al que se cose la vena, la cual se va invirtiendo conforme se tracciona de ella42, en vez de ser arrancada con la oliva clásica. Aunque hay controversia al cuantificar su beneficio43–45, su sencillez y economía aconsejan su conocimiento entre los CGD.
Método CHIVA (cura hemodinámica de la insuficiencia venosa crónica ambulatoria): tiene como objetivo restaurar la hemodinámica venosa sin extirpar la safena46–48. Para su realización precisa un detallado estudio de EDC. Aunque para sus defensores tiene más ventajas que la cirugía clásica47,49, otros estudios no encuentran mejores resultados en cuanto a recidivas ni estética50.
Procedimientos endovasculares: el hecho de que una de las principales causas de recidiva tras cirugía clásica sea la neovascularización a nivel de la herida inguinal51, así como la intención de minimizar la baja laboral, ha llevado a la reciente introducción de técnicas endovasculares. Básicamente, se trata de 2 procedimientos: la radiofrecuencia (RF) y el endoláser, que tienen como objetivo producir, mediante calor, una oclusión irreversible de la vena.
En ambos procedimientos se introduce distalmente (por debajo de la rodilla) un electrodo en la safena, hasta situarlo bajo control con EDC en el cayado. Luego, se va retirando el electrodo y se realiza un tratamiento secuencial del trayecto. Ambos se pueden realizar bajo anestesia locorregional o local tumescente52.
Tanto el endoláser, a diferentes longitudes de onda, como la RF son seguros y efectivos a corto-medio plazo, con una mayor satisfacción de los pacientes que con la cirugía tradicional53,54. Aunque la morbilidad es baja, conviene ser meticulosos en la técnica para evitar quemaduras de la piel. La RF, al precisar menor temperatura, tiene menos complicaciones55,56. Actualmente, se están publicando resultados satisfactorios a largo plazo, con tasas de curación de reflujo safeno del 86% a los 4 años con RF57,58. Aunque estos procedimientos tienen un mayor coste que la cirugía, estudios recientes demuestran su coste-efectividad al precisar una menor baja laboral59.
Esclerosis con espuma guiada por ultrasonidos (UGFS): aunque la esclerosis líquida se utiliza desde hace años para el tratamiento de varices de pequeño tamaño, su uso en grandes troncos obtenía pobres resultados60. Cabrera, basándose en estudios que demostraban que la espuma resultante de mezclar un esclerosante líquido con un gas era 4,5 veces más efectiva que el esclerosante solo61 y que el efecto del esclerosante era mayor cuando se aplicaba sobre una vena previamente vaciada62, popularizó en 1997 la UGFS63. Este tipo de esclerosis difiere de la esclerosis líquida en que la espuma no se diluye en la sangre de la vena, sino que la desplaza, lo que permite, gracias al EDC, un control preciso del lugar exacto y del tiempo en que actúa64.
Por su sencillez y bajo costo, el método más usado para obtener la espuma es el de Tessari65, mediante 2 jeringas desechables y una llave de 3 pasos. Tras llenar una jeringa con aire y la otra con un 1ml de esclerosante, se conecta ambas a una llave de 3 pasos, y se realiza 20 batidos rápidos del contenido entre las 2 jeringas, con lo que se obtiene una espuma estable que tiene mayor volumen y es más efectiva que el esclerosante líquido; se puede usar con control de EDC en cualquier vena de hasta 20mm de diámetro. El hecho de que esta espuma pueda utilizarse tanto en troncos venosos safenos como en venas reticulares, primarias o recidivadas, independientemente de su tamaño, tortuosidad o localización anatómica, de forma ambulatoria, en ambas piernas a la vez, y poder repetirse tanta veces como sea preciso, lo convierten, en opinión de muchos flebólogos, en el tratamiento del futuro66.
La tasa de recidivas a 10 años es de un 40%, comparable con la de la cirugía clásica67–69, aunque con la salvedad de que en estos casos una reesclerosis es tan eficaz y sencilla como el primer tratamiento18. No obstante, no está exenta de complicaciones y precisa, además del control ecográfico, de un flebólogo experimentado, ya que un paso excesivo de espuma al sistema profundo puede causar TVP70; se ha publicado un caso de muerte por embolia paradójica de una paciente con foramen oval permeable71.
Flebectomía ambulatoria: consiste en la avulsión mediante miniincisiones de venas varicosas no axiales mayores de 4mm72. Aunque es una técnica clásica, fue reintroducida en 1951 por Muller73, con 4 ventajas principales: ambulatoria, radical, económica y estética. Se puede utilizar como único procedimiento o combinado con otros (ligadura del cayado74, RF75, endoláser76, etc.). Los resultados a medio-largo plazo son mejores que los obtenidos con esclerosis77.
Tratamiento de las úlceras venosas mediante ligadura subfascial endoscópica de venas perforantes (SEPS)Pese a la importancia socioeconómica de la UV y el pobre resultado del tratamiento conservador, la cirugía ha realizado pocos progresos en el tratamiento de esta enfermedad78. La patogenia de la UV es fundamentalmente la incompetencia de las venas perforantes de la pierna79,80. El tratamiento tradicional ha sido la ligadura de dichas perforantes mediante la intervención de Linton81, con aceptables tasas de cicatrización82, pero con gran morbilidad y hospitalización prolongada. En 1985, Hauer83 describió un procedimiento endoscópico que posteriormente, coincidiendo con el desarrollo del material laparoscópico, ha experimentado mejoras técnicas84,85. El SEPS, al igual que el Linton, tiene como objetivo desconectar las perforantes insuficientes, pero accediendo al espacio subfascial desde una zona alejada de la piel dañada86. Para sus correctas indicación y realización exige un detallado estudio con EDC no sólo de las venas perforantes, sino también de los sistemas venosos superficial y profundo87.
Los estudios a corto plazo, alguno realizado por CGD85, muestran tasas de cicatrización del 100%, con mínima morbilidad. Estudios recientes88–90, algunos de ellos ensayos aleatorizados91,92, confirman estos buenos resultados (87–90%) con mínima morbilidad y ajustada estancia.
Con estos resultados es difícil justificar que los CGD, especialistas con más experiencia en técnicas videoquirúrgicas, permanezcamos ajenos al tratamiento de un problema tan prevalente en consulta. El problema no es su mayor coste, ya que los CGD disponemos de la mayor parte del material necesario (común al de la laparoscopia)85. La explicación podría estar en el poco interés que los CGD concedemos a la flebología y a la falta de formación en el manejo de la EDC, la cual es imprescindible para localizar las perforantes insuficientes y valorar su competencia85–92.
Manejo del EDC por parte del CGD-flebólogoAunque clásicamente se han descrito múltiples exploraciones en la IVC, todas ellas han sido desplazadas por la EDC. Su sencillez, rapidez, comodidad y ausencia de complicaciones, junto con una sensibilidad y una especificidad superiores al 95%, la convierten en una exploración indispensable en el estudio del paciente flebológico93. En palabras de Pizano, flebólogo colombiano: la EDC ha transformado la flebología en una ciencia formal, «convirtiendo la habilidad en ciencia»29. Como hemos comentado, la EDC es imprescindible en las técnicas endovasculares, y para poder cartografiar correctamente el sistema venoso del paciente y limitar la cirugía al territorio enfermo52. Al igual que no es concebible un servicio de ACV que no disponga de la EDC como exploración fundamental de su laboratorio vascular94, es imprescindible que el CGD-flebólogo tenga la formación necesaria para poder realizar una EDC.
Los CGD, al igual que otros especialistas (cardiólogos, digestólogos), hemos asumido la necesidad de realizar estudios ecográficos propios. No se entiende que un proctólogo o un cirujano hepático no realicen ecografía. En concreto, en nuestra encuesta se incluyó una pregunta sobre la actividad ecográfica en cirugía general. De los 96 hospitales que han respondido, el 60% reconoce usarla en alguna circunstancia. Ante esta realidad, nuestra AEC patrocinó en 2007 un curso de ecografía para cirujanos que se celebró en Zaragoza, y cuyos organizadores publicaron un manual completo95, y aunque ni en el curso ni en el libro se aborda la EDC flebológica, es de esperar que ésta se incluya en futuras ediciones, ya que, según los datos de nuestra encuesta, en el 11% de los servicios de cirugía general se realiza ya EDC.
En nuestro servicio, donde ya disponemos de una amplia experiencia en ecografía anorrectal, introducimos la EDC hace 1 año y, tras una pequeña curva de aprendizaje hemos constatado su enorme utilidad. Hemos pasado de operar varices con una EDC realizada por un radiólogo externo, que sólo informaba del cayado, a poder realizar una cartografía preoperatoria de estos pacientes.
¿Cuál es la situación actual de los CGD y la cirugía de varices?En nuestra opinión, la situación es pobre, ya que pese a ser los responsables del tratamiento de la mayoría de los pacientes, no estamos en el lugar que nos correspondería en el ámbito asistencial, científico, organizativo y formativo.
En cuanto a la asistencia, y según los datos de la encuesta, observamos que:
- •
Sólo un 7,6% de los servicios de cirugía general cuentan con una unidad de flebología, aunque en el 33% hay algún CGD-flebólogo.
- •
En 1/3 de los servicios que operan varices, esta cirugía la realizan todos los CGD por igual, mientras que en los 2/3 restantes sólo la hacen algunos de los cirujanos del servicio.
- •
La técnica más utilizada es la ligadura del cayado más safenectomía larga; sólo un 5% de los servicios realizan sistemáticamente safenectomía corta, y un 13,5% realiza safenectomía invertida.
- •
Sólo el 22% de los servicios que habitualmente operan varices tienen alguna experiencia con SEPS, y un 24%, con CHIVA.
Tampoco estamos a buen nivel científico. En los últimos 10 años sólo encontramos 5 trabajos sobre flebología en Cirugía Española85,96–99.
En cuanto a la organización, los CGD hemos dejado todo el protagonismo en manos de los vasculares. En el seno de la AEC hay una sección de angiología, cuya junta está formada exclusivamente por ACV. El órgano que representa a España en todos los foros flebológicos internacionales es el Capítulo Español de Flebología, dependiente de la Sociedad Española de Angiología y Cirugía Vascular (SEACV). Aunque admite a CGD, ya somos varios, sólo lo hace como miembros agregados (con voz pero sin voto).
Pero, posiblemente, el principal problema venga reflejado en la ausencia de formación continuada. Mientras que la SEACV organiza cursos para sus residentes, a los que difícilmente tienen acceso los residentes de cirugía general, la AEC no ofrece formación flebológica. Si en muchos hospitales no se operan varices, y no hay formación continuada, ¿cómo se formarán los futuros residentes? Lo mismo ocurre con la formación en EDC. La SEACV organiza cursos propios a los que los CGD no tenemos acceso.
En nuestra encuesta, cuando preguntamos sobre formación, obtenemos los siguientes resultados:
- •
Respecto a la formación flebológica durante el MIR, el 71% de las respuestas la consideran pobre; el 20%, regular, y sólo un 9%, buena.
- •
Respecto a si considera suficiente la formación continuada actual sobre flebología ofrecida por la AEC o la industria, el 88% de las respuestas son negativas, y un 83% opina que debería mejorarse.
Tan importante como saber lo que hacemos es saber qué queremos para el futuro. A la pregunta sobre si los CGD debemos tener un papel más importante. Sólo el 47% responde afirmativamente, mientras que el 40% responde negativamente y el 13% se abstiene. Esta dualidad se refleja en los comentarios adjuntos a la encuesta. Mientras que algunos hospitales nos dicen «gracias a Dios ya nos hemos librado de tener que operar más varices», otros se lamentan de la situación actual y nos animan a mejorar la formación flebológica. Llama la atención que las opiniones favorables a un mayor protagonismo provienen mayoritariamente de hospitales pequeños sin servicio de ACV.
ReflexiónLa flebología es un área quirúrgica de gran relevancia sociosanitaria, sometida a importante cambios al introducirse nuevos procedimientos, sobre los que ya existe una evidencia clínica demostrada y cuya demanda por parte de los pacientes va en aumento. Los CGD, aunque tenemos una gran responsabilidad asistencial, tenemos un pobre papel investigador, organizativo y formativo. Aunque reconocemos que la situación es mejorable, no acabamos de tener claro cuál debería ser nuestra posición en cuanto a esta enfermedad.
En nuestra opinión, los servicios de cirugía general en los que se realizase esta actividad deberían disponer de unidades de flebología, tal y como ya hay consolidadas otras UF (mama, cirugía bariátrica, pared abdominal, proctología, endocrino, etc.). Con respecto a la formación, la AEC debería asegurar que nuestros residentes, que en muchos casos van a acabar trabajando en un hospital sin ACV, obtengan una correcta formación, tanto en técnicas quirúrgicas como en la exploración básica en estos pacientes, la EDC.