Evaluar la morbimortalidad postoperatoria de la resección pancreática.
Material y métodosEstudio observacional prospectivo que incluye 117 pacientes intervenidos quirúrgicamente de forma consecutiva por presentar tumoración pancreática o periampular. En 61 de ellos se hizo pancreatectomía cefálica; en 15, pancreatectomía total; en uno, enucleación y en 40, resección corporocaudal.
ResultadosLa morbilidad global fue de 48,7% (59% para la pancreatectomía cefálica, 35% para la resección corporocaudal y 46,7% para la pancreatectomía total). Las complicaciones más frecuentes fueron las colecciones y abscesos intraabdominales, con un 15,38% y las complicaciones médicas, con un 13,68%. La incidencia de fístula pancreática fue de 9,83%, para la pancreatectomía cefálica y de 10% para la resección corporocaudal. La incidencia de reintervención fue de 14,53%. La mortalidad global fue de 5,12% (6,56% para la pancreatectomía cefálica, 2,5% para la resección corporocaudal y 6,67% para la pancreatectomía total). La presencia de complicaciones postoperatorias, la necesidad de reintervención y la edad superior a 70 años correlacionaron significativamente con la mortalidad.
DiscusiónLa resección pancreática tiene una morbilidad alta. La mortalidad es baja y está prácticamente limitada a los pacientes mayores de 70 años.
Assess the postoperative morbidity rates in pancreatic resection.
Material and methodProspective observational study which includes 117 patients who underwent surgery consecutively due to pancreatic or periampullary tumours. In 61 of the patients, cephalic pancreatectomy was carried out; 15 underwent total pancreatectomy; one underwent enucleation and 40 underwent distal pancreatectomy.
ResultsOverall morbidity was 48.7% (59% for cephalic pancreatectomy, 35% for distal pancreatectomy and 46.7% for total pancreatectomy). The most frequent complications were intra-abdominal abscesses and collections (15.38%) and medical complications (13.68%). The incidence of pancreatic fistula was 9.83% for cephalic pancreatectomy and 10% for distal pancreatectomy. The reintervention incidence was 14.53%. Overall mortality was 5.12% (6.56% for cephalic pancreatectomy, 2.5% for distal pancreatectomy and 6.67% for total pancreatectomy). The presence of postoperative complications, the need for reintervention and the fact of being over 70 years of age correlated significantly with mortality.
DiscussionPancreatic resection has high morbidity rates. Mortality is low and is practically limited to patients older than 70 years.
La resección pancreática es una operación técnicamente compleja, con una mortalidad que ha ido disminuyendo progresivamente hasta alcanzar valores inferiores al 5% en centros de referencia1–4, pero que, todavía en la actualidad, está gravada con una elevada incidencia de complicaciones postoperatorias, cuyo manejo adecuado requiere el concurso, de una manera integrada y coordinada, de cirujanos, radiólogos, endoscopistas y anestesistas. La continua mejoría de los resultados obtenidos con este tipo de cirugía en los últimos años se sustenta en la incorporación de aspectos novedosos de técnica quirúrgica y de manejo perioperatorio, basada en el conocimiento de la propia experiencia y de la de otros grupos. Por ello, creemos que es importante disponer de series que permitan conocer los resultados obtenidos en diversos centros y poder establecer comparaciones que contribuyan a la obtención de mejores resultados. En la literatura médica española no hay demasiadas series publicadas y, en este sentido, hemos creído apropiado aportar nuestra experiencia, planteando como objetivo la comunicación de los resultados obtenidos en nuestro centro con la resección pancreática, en cuanto a complicaciones postoperatorias y mortalidad.
Pacientes y métodosSe llevó a cabo un estudio observacional prospectivo en el que se incluyó a 117 pacientes tratados con resección pancreática, por presentar una tumoración pancreática o periampular, durante el periodo de tiempo comprendido entre enero de 2005 y diciembre de 2011. Los datos fueron recogidos de forma prospectiva en una base de datos anonimizada diseñada al comienzo del periodo de estudio y fueron analizados en junio de 2012. Se analizaron datos demográficos, drenaje biliar preoperatorio, técnica quirúrgica, requerimiento de transfusión, complicaciones, mortalidad y estancia postoperatoria.
Técnica quirúrgicaDuodenopancreatectomía cefálicaPara la duodenopancreatectomía cefálica (DPC) se hace una laparotomía subcostal y, después de descartar enfermedad metastásica, se expone el bloque duodenopancreático mediante descenso del ángulo hepático del colon y maniobra de Kocher hasta el borde izquierdo de la aorta, resecando en este momento, en continuidad con la pieza, los ganglios interaortocava, que únicamente se analizan intraoperatoriamente si son mayores de 1cm. A continuación se accede a la trascavidad de los epiplones tras seccionar el ligamento gastrocólico, se secciona el tronco gastrocólico a nivel de la vena mesentérica superior y se diseccionan la vena y la arteria mesentérica superiores, con sección de sus ramas accesibles. Posteriormente, se hace colecistectomía anterógrada y se disecciona el pedículo hepático, con esqueletización de sus elementos vasculares. La arteria gastroduodenal se secciona después de comprobar, mediante una prueba de pinzamiento, que no hay obstrucción del tronco celiaco. La vía biliar se secciona por debajo de la convergencia biliar y su porción proximal se mantiene ocluida con un clamp bulldog hasta el momento en que se hace la reconstrucción. La linfadenectomía del pedículo hepático se extiende desde la convergencia biliar hasta el origen de la arteria hepática. Después se secciona el antro gástrico, que se extirpará en bloque con la cabeza del páncreas (en ningún caso se hizo preservación pilórica). Se secciona el páncreas a la izquierda de la vena porta, comprobando que hay sangrado pulsátil por el borde de sección del cuerpo del páncreas. En caso de tumoración maligna, se hace biopsia intraoperatoria de los bordes de sección pancreático y biliar. Una vez completado este paso se secciona el yeyuno a unos 15cm del ligamento de Treitz y se traspone al lado derecho del eje mesentérico y, finalmente, se secciona la lámina retroportal hasta el borde derecho de la arteria mesentérica superior, completando la resección. La reconstrucción se inicia con la anastomosis pancreática. En todos los casos, excepto en 3, se hizo anastomosis ducto-yeyunal con puntos sueltos de ácido poliglicólico de 6/0 tutorizada con un drenaje intraluminal de unos 6-8cm de longitud y de calibre adaptado al diámetro del conducto pancreático. En los pacientes con ducto de gran diámetro no se utilizó tutor. En los pacientes con ducto de diámetro inferior a 1,5mm se invaginó el remanente pancreático en el estómago (un caso) o en el yeyuno (2 casos). A unos 8-15cm de la anastomosis pancreática se hace una hepaticoyeyunostomía terminolateral con puntos sueltos de ácido poliglicólico de 5/0 o 6/0. Por último se hace una gastroyeyunostomía terminolateral con 2 suturas continuas de material absorbible de 4/0. Al inicio de la serie se hacía una reconstrucción tipo Child, pero en los 2 últimos años se hizo una reconstrucción en Y de Roux, con un asa para la anastomosis pancreática y biliar, transmesocólica, y otra para la anastomosis gastroyeyunal, en posición antecólica. En todos los casos se dejaron 2 drenajes cerrados, uno en la fosa de Morrison y el otro, peripancreático.
Pancreatectomía corporocaudalEn caso de tumor benigno, se intentó conservar el bazo, si era posible con preservación de vasos esplénicos y si no lo era, mediante la técnica de Warshaw. En caso de tumor maligno se hizo esplenectomía en bloque y la operación comienza con la sección de la arteria esplénica en su origen, la sección del cuello del páncreas y la movilización de la pieza de resección de derecha a izquierda. Si la resección se hace por abordaje laparoscópico, el páncreas se secciona con endocortadora y se refuerza con puntos sueltos de material absorbible de 3/0. En todos los casos se dejó un drenaje aspirativo en la proximidad del remanente pancreático.
Duodenopancreatectomía totalSi hay que hacerla una vez completada la DPC porque el borde de sección pancreática está afectado por el tumor, se procede igual que para la pancreatectomía corporocaudal, extirpando el bazo en continuidad. Si la indicación se plantea desde el inicio, se comienza igual que para la DPC, comprobando que no hay infiltración vascular que contraindique la resección. A continuación se secciona la arteria esplénica en su origen y se movilizan el bazo y el páncreas en continuidad de izquierda a derecha y, finalmente, se secciona la lámina retroportal. La reconstrucción se hace del mismo modo que para la DPC y se dejan uno o 2 drenajes.
Resección multivisceralSe consideró como tal cuando, además del páncreas, se extirpó algún otro órgano distinto de vesícula biliar, duodeno, estómago distal o yeyuno proximal.
Resección vascularSe consideró indicada si había infiltración venosa, sin obstrucción del flujo portal, y el paciente tenía 70 o menos años. Se consideró contraindicada si había obstrucción del flujo portal, invasión de la arteria mesentérica superior, invasión del tronco celiaco o de la arteria hepática. Para la pancreatectomía corporocaudal, la invasión del tronco celiaco o de la arteria hepática proximal al origen de la arteria gastroduodenal no se consideraron una contraindicación para la resección, siempre y cuando hubiera flujo arterial hepático a través de la arteria gastroduodenal. Por lo general, en caso de DPC o pancreatectomía total se consideró contraindicada en pacientes mayores de 70 años.
Preparación preoperatoriaEn todos los pacientes se hizo profilaxis antibiótica, administrando el antibiótico en la hora que precede a la cirugía. Se utilizó la combinación de 2g de amoxicilina con 200mg de ácido clavulánico o bien la combinación de 1.500mg de metronidazol y 2g de ceftriaxona. La profilaxis se mantuvo durante 24h. También se administró una dosis de 40mg de enoxaparina y una dosis de 100mcg de octeótrido 12h antes de la cirugía, ambos por vía subcutánea.
Cuidados postoperatoriosNo se utilizó sonda nasogástrica de forma rutinaria. Se utilizó nutrición parenteral en los pacientes con DPC y pancreatectomía total, que se mantuvo hasta que el paciente toleró una dieta semiblanda. La sonda urinaria y el catéter venoso central se retiraron a las 24-48h de la cirugía y se inició la dieta oral a los 3-5 días. En caso de pancreatectomía corporocaudal la dieta se inició a las 24h. El octeótrido se mantuvo durante 7 días, excepto si se había heco pancreatectomía total, a dosis de 100 mcg cada 8h por vía subcutánea. La primera dosis postoperatoria se administró al terminar la cirugía. En pacientes con páncreas de consistencia blanda y ducto menor de 3mm se duplicó la dosis. La profilaxis con heparina se mantuvo durante el ingreso en caso de tumor benigno y durante 30 días en caso de tumor maligno. Los drenajes se retiraron entre el tercero y el octavo días, excepto en caso de fístula biliar o pancreática. Se hizo determinación de amilasa y bilirrubina en el contenido de los drenajes a partir del tercer día, así como en el contenido de cualquier colección que fuese drenada. No se utilizaron procinéticos de forma rutinaria.
MorbimortalidadFístula pancreática: se consideró que existía si, a partir del tercer día, los niveles de amilasa en el contenido del drenaje o en cualquier colección drenada eran superiores a 3 veces el valor en el suero5.
Fístula biliar: se consideró que existía si a partir del tercer día los niveles de bilirrubina en el contenido del drenaje o en cualquier colección drenada eran superiores a 3 veces el valor en suero6.
Retraso en el vaciamiento gástrico: se consideró que existía si era necesario mantener la sonda nasogástrica durante más de 3 días a partir del tercer día o si había intolerancia a la dieta oral más allá del séptimo día de postoperatorio7.
Hemorragia postoperatoria: se consideró que existía si se produjo una disminución de los niveles de Hb superior a 3g/dl8.
Análisis estadísticoEl análisis estadístico de los datos obtenidos se llevó a cabo mediante el paquete informático IBM SPSS (Statistical Package for Social Sciences Inc., Chicago, Illinois, EE. UU.) versión 20.0 para Mac. Se hizo un análisis descriptivo de las variables incluidas en el estudio. Se comprobó mediante la prueba de Saphiro-Wilk y el test de Kolmogorov si las variables cuantitativas se ajustaban a una distribución normal. Para las variables cuantitativas continuas se obtuvieron medidas de tendencia central y de dispersión, expresadas como medias, con IC al 95%, en el caso de variables con distribución normal, o como medianas, en caso contrario. Para las variables cualitativas se determinaron las proporciones, con sus intervalos de confianza al 95%. En el caso de variables no ajustadas a distribución normal se utilizó el test exacto de Fisher para la comparación de variables cualitativas; el test de Kruskall-Wallis o el test de Mann-Whitney para la comparación de variables cuantitativas entre grupos de pacientes, y el coeficiente de correlación de rangos de Spearman para la comparación de 2 variables cuantitativas. En el caso de variables ajustadas a distribución normal se utilizó el test chi-cuadrado para la comparación de variables cualitativas; el test de la t de Student para las variables cuantitativas y el coeficiente de correlación de Pearson para la comparación de 2 variables cuantitativas. Para analizar qué variables se relacionan con la mortalidad se recurrió a un modelo de regresión logística en el que se introdujeron las variables para las que el valor de p fue inferior a 0,20. Se consideró que había significación estadística para valores de p inferiores a 0,05.
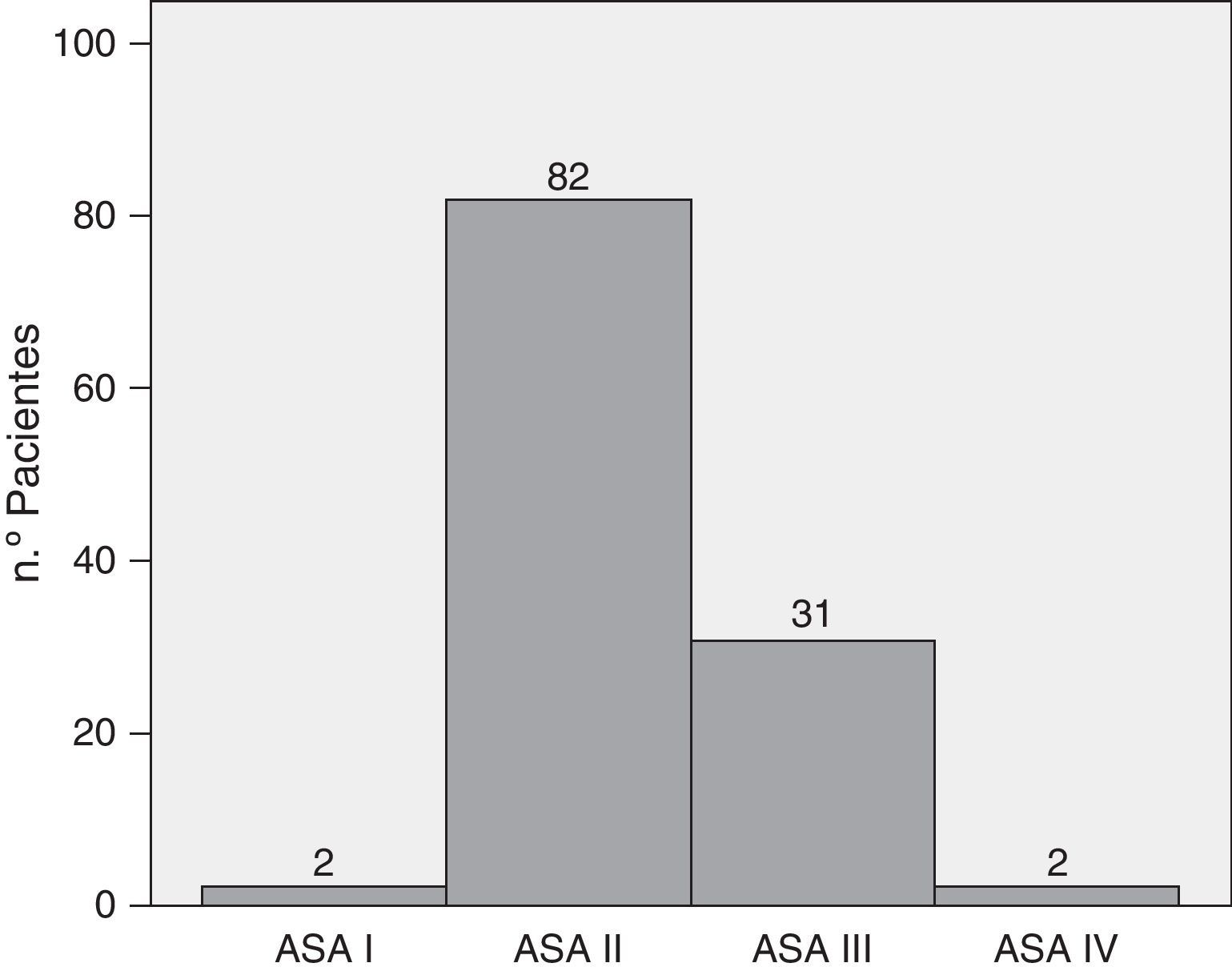
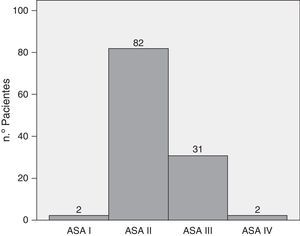
ResultadosLa serie incluyó 117 pacientes, con una mediana de 64,38 años (IC 95%: 62,3-66,47). El paciente más joven tenía 34 años y el de mayor edad, 82. El 53,8% eran varones y el 46,2%, mujeres. El IMC prequirúrgico medio fue de 25,97 (IC 95%: 25,36-26,59). Como se puede ver en la figura 1 el 70,1% de los pacientes eran ASA II y el 26,5%, ASA III. El índice de Charlson tenía una mediana de 0, con un percentil 75 de 1. Casi el 71% de los pacientes tenía un índice de Charlson de 0; el 17,9% tenían un índice de Charlson de 1; el 10,25% tenía un índice de 2 y solo un paciente tenía un índice de 3. En 31 pacientes (26,5%) se hizo drenaje biliar preoperatorio, en 29 de ellos por vía endoscópica y solo en 2 por vía percutánea.
La técnica quirúrgica realizada fue DPC en 61 pacientes (52,1%), pancreatectomía corporocaudal en 40 pacientes (34,2%), pancreatectomía total en 15 (12,8%) y enucleación en uno (0,9%). La pancreatectomía corporocaudal fue laparoscópica en 15 pacientes (37,5%); en 6 de ellos se hizo con preservación del bazo (40%), en 4 preservando los vasos esplénicos y en 2 mediante técnica de Warshaw. En 4 pacientes se hizo resección de vena porta o vena mesentérica superior (2 pacientes con DPC y 2 con pancreatectomía total). En 13 (11,1%) pacientes se hizo resección multivisceral (6 con DPC, 4 con pancreatectomía corporocaudal y 3 con pancreatectomía total). Cuarenta pacientes (34,18%) requirieron transfusión intraoperatoria con una mediana de un concentrado de hematíes (1-7). En todo el periodo postoperatorio fueron transfundidos 42 pacientes (35,9%), con una mediana de 2 concentrados de hematíes (1-27). Teniendo en cuenta todo el periodo perioperatorio se transfundieron 63 pacientes (53,8%). Los pacientes con pancreatectomía total fueron los que necesitaron transfusión con mayor frecuencia, tanto durante la cirugía como en el postoperatorio (60 y 46,7%, respectivamente), aunque solo de forma significativa respecto a la intraoperatoria (p=0,03). Los pacientes con pancreatectomía corporocaudal fueron los que con menor frecuencia necesitaron transfusión (29 y 30%, respectivamente), aunque no de forma significativa. Los pacientes con DPC necesitaron transfusión intraoperatoria en un 31,14% de los casos y postoperatoria en un 37,7%. La transfusión intraoperatoria se asoció significativamente con el tipo de resección (p=0,013), resección venosa (p=0,017) y resección multivisceral (p=0,011). En la pancreatectomía corporocaudal,la transfusión intraoperatoria fue significativamente menor si el abordaje fue laparoscópico.
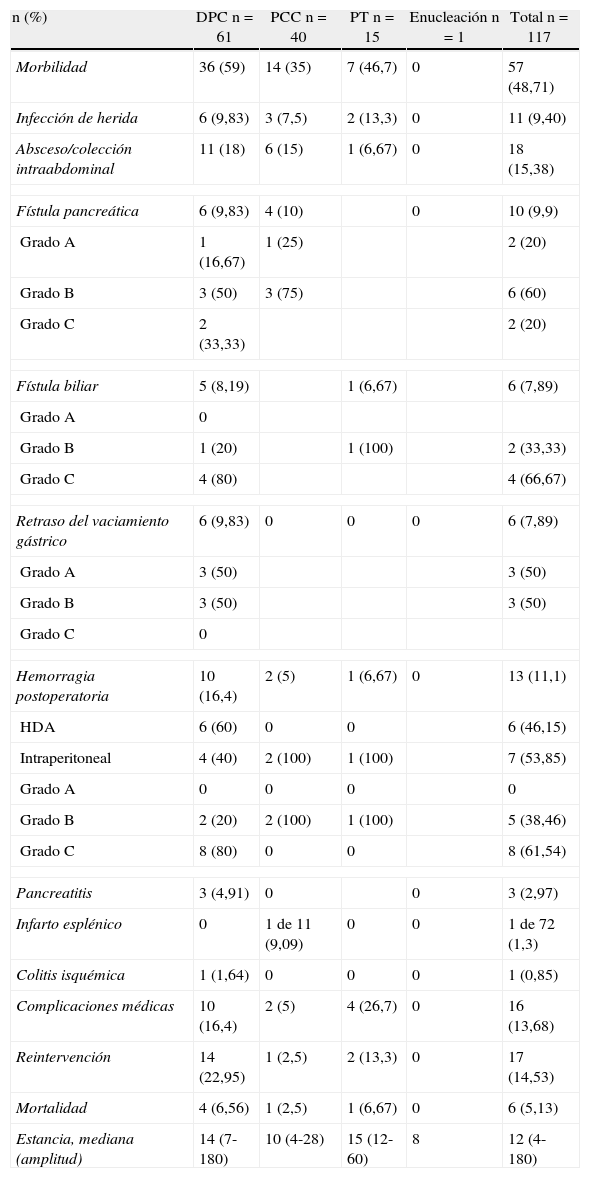
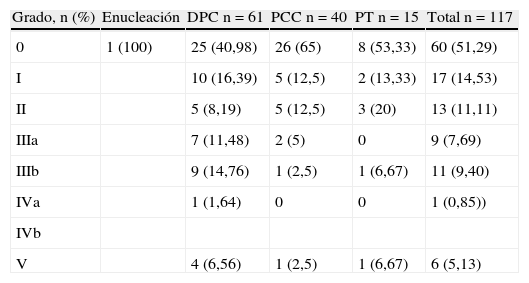
La incidencia global de complicaciones fue de 48,7%, siendo las más frecuentes los abscesos y colecciones intraabdominales, con un 15,38% y las complicaciones médicas, con un 13,68%. En la tabla 1 se muestran los datos de morbimortalidad según el tipo de resección y en la tabla 2 se muestra la morbilidad según la clasificación de Clavien-Dindo9, que tiene en cuenta su transcendencia y el tratamiento requerido para su control y resolución. Ninguna de las variables estudiadas mostró relación significativa con la morbilidad global. El absceso intraabdominal y la fístula biliar fueron significativamente más frecuentes cuando se hizo resección multivisceral (p=0,029 y p=0,018, respectivamente). La fístula pancreática no se asoció significativamente con ninguna de las variables estudiadas.
Morbimortalidad de la resección pancreática
| n (%) | DPC n=61 | PCC n=40 | PT n=15 | Enucleación n=1 | Total n=117 |
| Morbilidad | 36 (59) | 14 (35) | 7 (46,7) | 0 | 57 (48,71) |
| Infección de herida | 6 (9,83) | 3 (7,5) | 2 (13,3) | 0 | 11 (9,40) |
| Absceso/colección intraabdominal | 11 (18) | 6 (15) | 1 (6,67) | 0 | 18 (15,38) |
| Fístula pancreática | 6 (9,83) | 4 (10) | 0 | 10 (9,9) | |
| Grado A | 1 (16,67) | 1 (25) | 2 (20) | ||
| Grado B | 3 (50) | 3 (75) | 6 (60) | ||
| Grado C | 2 (33,33) | 2 (20) | |||
| Fístula biliar | 5 (8,19) | 1 (6,67) | 6 (7,89) | ||
| Grado A | 0 | ||||
| Grado B | 1 (20) | 1 (100) | 2 (33,33) | ||
| Grado C | 4 (80) | 4 (66,67) | |||
| Retraso del vaciamiento gástrico | 6 (9,83) | 0 | 0 | 0 | 6 (7,89) |
| Grado A | 3 (50) | 3 (50) | |||
| Grado B | 3 (50) | 3 (50) | |||
| Grado C | 0 | ||||
| Hemorragia postoperatoria | 10 (16,4) | 2 (5) | 1 (6,67) | 0 | 13 (11,1) |
| HDA | 6 (60) | 0 | 0 | 6 (46,15) | |
| Intraperitoneal | 4 (40) | 2 (100) | 1 (100) | 7 (53,85) | |
| Grado A | 0 | 0 | 0 | 0 | |
| Grado B | 2 (20) | 2 (100) | 1 (100) | 5 (38,46) | |
| Grado C | 8 (80) | 0 | 0 | 8 (61,54) | |
| Pancreatitis | 3 (4,91) | 0 | 0 | 3 (2,97) | |
| Infarto esplénico | 0 | 1 de 11 (9,09) | 0 | 0 | 1 de 72 (1,3) |
| Colitis isquémica | 1 (1,64) | 0 | 0 | 0 | 1 (0,85) |
| Complicaciones médicas | 10 (16,4) | 2 (5) | 4 (26,7) | 0 | 16 (13,68) |
| Reintervención | 14 (22,95) | 1 (2,5) | 2 (13,3) | 0 | 17 (14,53) |
| Mortalidad | 4 (6,56) | 1 (2,5) | 1 (6,67) | 0 | 6 (5,13) |
| Estancia, mediana (amplitud) | 14 (7-180) | 10 (4-28) | 15 (12-60) | 8 | 12 (4-180) |
DPC: duodenopancreatectomía cefálica; HDA: hemorragia digestiva alta; PCC: pancreatectomía corporocaudal; PT: pancreatectomía total.
Morbilidad según la clasificación de Clavien
| Grado, n (%) | Enucleación | DPC n=61 | PCC n=40 | PT n=15 | Total n=117 |
| 0 | 1 (100) | 25 (40,98) | 26 (65) | 8 (53,33) | 60 (51,29) |
| I | 10 (16,39) | 5 (12,5) | 2 (13,33) | 17 (14,53) | |
| II | 5 (8,19) | 5 (12,5) | 3 (20) | 13 (11,11) | |
| IIIa | 7 (11,48) | 2 (5) | 0 | 9 (7,69) | |
| IIIb | 9 (14,76) | 1 (2,5) | 1 (6,67) | 11 (9,40) | |
| IVa | 1 (1,64) | 0 | 0 | 1 (0,85)) | |
| IVb | |||||
| V | 4 (6,56) | 1 (2,5) | 1 (6,67) | 6 (5,13) |
DPC: duodenopancreatectomía cefálica; PCC: pancreatectomía corporocaudal; PT: pancreatectomía total.
La mortalidad global fue de 5,12% (6 pacientes). Según el tipo de resección, fue de 6,56% para la DPC (4 pacientes); 2,5% (un paciente) para la pancreatectomía corporocaudal y 6,67% (un paciente) para la pancreatectomía total. Únicamente la presencia de complicaciones postoperatorias, la necesidad de reintervención y la edad superior a 70 años correlacionaron significativamente con la mortalidad (p=0,005, p<0,0001 y p=0,007, respectivamente). Tras el análisis multivariante solo se mantuvo como significativa la necesidad de reintevención (OR: 23,29; IC 95%: 2,26-239,68).
La reconstrucción mediante técnica de Child o con Y de Roux, así como el tamaño de la neoplasia, no se asociaron con la aparición de complicaciones postoperatorias ni con la mortalidad.
La mediana de estancia global fue de 12 días (4-180). Para la DPC fue de 14 (4-180); para la pancreatectomía total de 15 (9-67) y para la pancreatectomía corporocaudal, 10 (4-42) (p=0,002). La estancia también fue significativamente mayor en pacientes con resección multivisceral (p=0,037), con complicaciones consideradas de forma global (p=0,000), absceso intraabdominal (p<0,0001), reintervención (p=0,001), fístula pancreática (p=0,015) y con la gravedad de las complicaciones (p<0,0001).
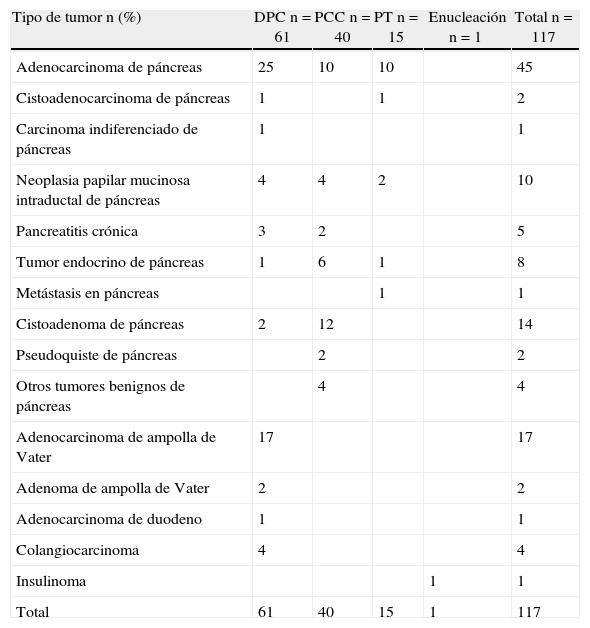
La indicación más frecuente para la resección pancreática fue el adenocarcinoma de páncreas (tabla 3). Solo en 3 pacientes se hizo radioquimioterapia neoadyuvante: 2 de ellos no tuvieron complicaciones postoperatorias y el tercero presentó un absceso intraabdominal.
Diagnóstico histológico
| Tipo de tumor n (%) | DPC n=61 | PCC n=40 | PT n=15 | Enucleación n=1 | Total n=117 |
| Adenocarcinoma de páncreas | 25 | 10 | 10 | 45 | |
| Cistoadenocarcinoma de páncreas | 1 | 1 | 2 | ||
| Carcinoma indiferenciado de páncreas | 1 | 1 | |||
| Neoplasia papilar mucinosa intraductal de páncreas | 4 | 4 | 2 | 10 | |
| Pancreatitis crónica | 3 | 2 | 5 | ||
| Tumor endocrino de páncreas | 1 | 6 | 1 | 8 | |
| Metástasis en páncreas | 1 | 1 | |||
| Cistoadenoma de páncreas | 2 | 12 | 14 | ||
| Pseudoquiste de páncreas | 2 | 2 | |||
| Otros tumores benignos de páncreas | 4 | 4 | |||
| Adenocarcinoma de ampolla de Vater | 17 | 17 | |||
| Adenoma de ampolla de Vater | 2 | 2 | |||
| Adenocarcinoma de duodeno | 1 | 1 | |||
| Colangiocarcinoma | 4 | 4 | |||
| Insulinoma | 1 | 1 | |||
| Total | 61 | 40 | 15 | 1 | 117 |
En las últimas décadas se han ampliado las indicaciones para la resección pancreática, fundamentalmente por 3 motivos. En primer lugar, actualmente se operan tumores malignos pancreáticos para los que antes se consideraba contraindicada la resección; en segundo lugar, se operan tumoraciones que antes se diagnosticaban con menor frecuencia, como las neoplasias papilares mucinosas intraductales, y, por último, se operan pacientes de mayor edad, incluso de 90 años10. En nuestra serie la indicación más frecuente fue el adenocarcinoma de páncreas, coincidiendo con lo publicado previamente11, aunque es de destacar el relativamente importante número de pacientes con neoplasia mucinosa papilar intraductal y de pacientes con tumores neuroendocrinos. Esta ampliación en las indicaciones de resección pancreática se ha podido llevar a cabo gracias a la mejoría de los resultados obtenidos que se ha conseguido en estos últimos años. Aunque para la DPC se considera un estándar de calidad una mortalidad inferior al 10% y una morbilidad menor del 50%12, en centros de referencia, con gran volumen de pacientes, la mortalidad es inferior al 5% 1–3 e incluso en torno al 1%4. En nuestra serie la mortalidad global es del 5,12%. Para la DPC es del 6,56%, y para la pancreatectomía total y la resección corporocaudal es del 6,67 y 2,5%, respectivamente. Estos datos son similares a los publicados en los últimos años por otros autores españoles11–14. En nuestro estudio la mortalidad es significativamente más alta en pacientes mayores de 70 años, en pacientes con complicaciones postoperatorias y en los pacientes que necesitan una reintervención, datos que coinciden con los publicados por otros autores14,15. No obstante, en el análisis multivariante la única variable que se mantiene significativamente asociada a la mortalidad es la reintervención. Aunque la fístula pancreática es reconocida como una de las principales causas de muerte16, en nuestra serie no hemos encontrado una relación significativa con la misma. La reducción en la mortalidad observada en los últimos años está ligada, fundamentalmente, a la mejoría en la técnica quirúrgica, en los cuidados postoperatorios y en el manejo de complicaciones, pero no se ha acompañado de una reducción sustancial en la incidencia de complicaciones, que sigue siendo muy alta. En centros con amplísima experiencia y gran reputación, como el John Hopkins y el Memorial Sloan-Kattering Center es del 38 y del 46%, respectivamente17,18. La incidencia de complicaciones es especialmente alta en la DPC y en la pancreatectomía total. En nuestra serie, la incidencia global de complicaciones es de 48,7%, con un 59% para la DPC, 46,7% para la pancreatectomía total y un 35% para la resección corporocaudal, en consonancia con los datos publicados por otros autores11,14. Entre las complicaciones de la resección pancreática son especialmente relevantes la fístula pancreática, la hemorragia postoperatoria y los abscesos y colecciones intraabdominales. La incidencia de fístula pancreática varía bastante entre las series y también según el tipo de estudio, ya que suele ser más elevada cuando se trata de estudios prospectivos aleatorizados. Las cifras publicadas suelen oscilar entre el 5 y el 20% para la DPC. En nuestra serie la incidencia en DPC fue de 9,83%, valor similar a los publicados por autores con series amplias14,19,20. Para la pancreatectomía distal suelen publicarse cifras mayores, entre el 20 y el 40%20. En nuestra serie es de tan solo el 10% para la pancreatectomía corporocaudal, que es un valor similar a los publicados por otros autores11. En trabajos publicados previamente se ha visto que el sexo varón, el IMC mayor de 30, un páncreas de consistencia blanda y el ducto pancreático con diámetro inferior a 3mm son factores de riesgo para la aparición de fístula pancreática21. Sin embargo, en nuestra serie no hemos encontrado ninguna relación significativa con la aparición de esta complicación, seguramente por el escaso número de casos. Las fístulas pancreáticas tienen una especial transcendencia en la DPC, ya que sus consecuencias son más graves. En un intento de reducir su incidencia en estos pacientes se han diseñado varios tipos de anastomosis pancreática, pero de las múltiples variantes existentes ninguna ha demostrada suficientemente su superioridad frente a las otras22. De acuerdo con Sabater11 creemos que lo más importante es una técnica meticulosa y, en este sentido, tenemos la costumbre de utilizar gafas lupa de 3,5 aumentos para la confección de la anastomosis pancreática y biliar. En caso de que el diámetro del conducto pancreático sea excesivamente fino, hacemos una anastomosis pancreática por invaginación, en el estómago o en el yeyuno. En la pancreatectomía corporocaudal tampoco se han encontrado diferencias en la incidencia de fístula pancreática en función del tipo de cierre del páncreas proximal remanente23. Los abscesos intraabdominales son especialmente frecuentes en la DPC, llegando incluso a afectar al 29% de los pacientes24, aunque generalmente la incidencia es menor, entre el 5 y el 10%. La incidencia observada en nuestra serie, del 18% para la DPC y de l5% para la resección corporocaudal, es algo más elevada que la generalmente publicada. En nuestro estudio la única variable para la que hemos encontrado una asociación estadísticamente significativa con la aparición de absceso intraabdominal fue la resección multivisceral. La hemorragia postoperatoria es una de las complicaciones más temidas por el cirujano. En la resección corporocaudal es rara, pero en la DPC y en la pancreatectomía total tiene una incidencia que suele situarse entre el 5 y el 12%25. Puede ser intraluminal, generalmente producida a partir de una línea de sutura, o intraabdominal y puede ser precoz o tardía (a partir del quinto día de postoperatorio). Esta última suele asociarse con la existencia de una fístula pancreática25. La incidencia de hemorragia postoperatoria observada en nuestra serie es similar a la publicada por otros autores.
Otras complicaciones asociadas con la DPC y la pancreatectomía total son el retraso del vaciamiento gástrico y la fístula biliar. En nuestra serie la incidencia de retraso del vaciamiento gástrico es de aproximadamente el 10%, que es un valor medio al compararlo con el publicado por otros autores11,13,14, lo que podría explicarse, al menos en parte, porque en ningún paciente se hizo preservación pilórica. En la duodenopancreatectomía siempre hacemos antrectomía porque no hay evidencias de que la preservación pilórica reduzca la morbimortalidad o mejore la calidad de vida o el estado nutricional de los pacientes26. En nuestra serie la incidencia de fístula biliar es algo más elevada que la publicada por otros autores, pero la mitad de los casos se produjeron después de reintervenciones llevadas a cabo por otro motivo. Aunque es difícil disminuir la morbilidad, algunos autores han observado que la no utilización de drenaje la reduce de forma importante, ya que disminuye la incidencia de fístulas y abscesos13.
La elevada incidencia de complicaciones quirúrgicas graves condiciona una elevada tasa de reintervenciones, que en nuestra serie es de casi el 15% para el conjunto de las resecciones pancreáticas y de casi el 23% para la DPC. Esta incidencia de reintervenciones es mayor que la habitualmente publicada, en torno al 10%, para la DPC25. La tasa de reintervenciones está relacionada con la incidencia de complicaciones graves como la fístula pancreática, las hemorragias postoperatorias y los abscesos intraabdominales, pero también con la tasa de resolución de estas complicaciones mediante procedimientos no quirúrgicos. En nuestro centro se está intentando potenciar el drenaje endoscópico de las colecciones peripancreáticas y mejorar la tasa de éxito con el drenaje percutáneo, con el fin de disminuir la alta tasa de reintervenciones y, con ello, disminuir la mortalidad a valores inferiores al 5%.
La estancia postoperatoria de estos pacientes suele ser prolongada. En nuestra serie la mediana fue de 12 días para el conjunto de las resecciones pancreáticas y de 14 días para la DPC y está significativamente más elevada en caso de resección multivisceral, absceso intraabdominal, fístula pancreática, morbilidad global, gravedad de las complicaciones y necesidad de reintervención. Estos hallazgos están en consonancia con los publicados por otros autores14. En los últimos años se han puesto en marcha programas de fast track surgery que permiten reducir la estancia hospitalaria, e incluso las complicaciones postoperatorias, como han puesto de manifiesto en nuestro país el grupo de la clínica universitaria de Navarra13.
En conclusión, la resección pancreática, especialmente la duodenopancreatectomía, todavía está gravada con una importante morbimortalidad y estancias hospitalarias prolongadas, pero, junto con otro autores, creemos que ello no debe conducir al nihilismo terapéutico, ya que la resección es la única posibilidad de conseguir supervivencias prolongadas en caso de tumor maligno pancreático o de la encrucijada biliopancreática11. En pacientes mayores de 70 años, la mortalidad de la duodenopancreatectomía es más alta, pero aún así la consideramos indicada, excepto en pacientes con comorbilidad importante.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.