El rubor facial incontrolable (RFI) se ha convertido en uno de los síntomas cardinales de la fobia social. La hiperhidrosis facial (HF) es asimismo una rara condición en la cual los pacientes padecen una sudoración local excesiva en la cara. Este trastorno se ha asociado al estrés mental y constituye también un síntoma de la fobia social1.
Teniendo en cuenta que la fobia social tiene una prevalencia del 10%, el interés en el manejo y la mejora de ambos trastornos es importante.
Se asume que la simpaticotomía por videotoracoscopia (VATS) mejora el RFI2 y la HF3; sin embargo, únicamente una minoría de los cirujanos torácicos que realizan simpaticotomías por VATS tratan a pacientes con estas enfermedades. No hay estudios prospectivos y aleatorizados que evidencien su efectividad4 y los trabajos publicados son escasos en comparación con los de la hiperhidrosis (HH) palmar5. Algunos autores asumen ambas entidades como alteraciones independientes2, no obstante su tratamiento quirúrgico es el mismo6.
Analizamos nuestra experiencia en el tratamiento del RFI y la HF mediante la simpaticotomía por VATS.
Pacientes y métodoEntre marzo de 2000 y agosto de 2006 realizamos 82 simpaticotomías torácicas por VATS en 41 pacientes diagnosticados de RFI y/o HF. Dos de ellos habían sido intervenidos anteriormente en otros centros sin resultados satisfactorios. Se propuso la intervención quirúrgica a los pacientes en que se descartó un origen no idiopático de la HF y/o RFI, y que les causaba una limitación laboral y social importante. Su trastorno debía llevar más de un año de evolución habiendo sido ineficaces los tratamientos conservadores. En la primera visita médica descartamos un origen secundario del RFI o la HF mediante un interrogatorio exhaustivo y una exploración física minuciosa.
Asimismo, antes de la cirugía y como parte del preoperatorio, los pacientes se sometieron a una analítica completa, un electrocardiograma y una radiografía de tórax; previamente a la intervención se los evaluó para descartar cualquier enfermedad concomitante que pudiese ser la causa subyacente del RFI o la HF.
Se informó a los pacientes de que en caso de no ser factible el procedimiento por toracoscopia se llevaría a cabo una minitoracotomía axilar de asistencia.
La técnica empleada fue la simpaticotomía bilateral por VATS variando los niveles en función de la presencia de HH palmar y/o axilar asociada y de las limitaciones anatómicas. Los resultados y complicaciones fueron evaluados, como mínimo, mediante controles a la semana y a los 3-6 meses en los 41 pacientes; con un control al año de la intervención en 34 de ellos.
Todos los procedimientos se realizaron con anestesia general con intubación bronquial selectiva o con tubo de doble luz.
El paciente se colocó en posición de decúbito supino con los brazos en abducción; se monitorizaba la temperatura cutánea en ambas manos (termómetro adherido al pulpejo del dedo índice). La monitorización de la temperatura en cada mano durante el acto quirúrgico se realizó como guía orientativa de la efectividad inmediata del procedimiento. Se empleó una única puerta de entrada de 5 o 10 mm colocada a nivel del tercero-cuarto espacio intercostal (línea axilar media). Usamos un toracoscopio rígido de 5 o 10 mm con canal de trabajo, por el que se insertó un electrocauterio monopolar. La referencia anatómica utilizada en todos los pacientes fue la identificación visual y táctil (palpación con endoinstrumental) de la segunda costilla. En los primeros casos se seccionaba la cadena simpática sobre el borde inferior de la primera costilla y, posteriormente, con la evolución de la técnica, sobre el borde superior de la segunda costilla.
Dada la frecuente variación anatómica interindividual que existe no pudimos constatar si se trataba de la parte inferior del primer ganglio o la superior del segundo7. Si macroscópicamente visualizábamos nervios de Kuntz, los seccionamos independientemente de la coexistencia de HH palmar.
Una vez constatada visualmente la simpaticólisis y verificado el ascenso de la temperatura digital ipsolateral, insertamos una sonda torácica fina que se conectaba a un sello de agua. Se procedió entonces a reexpandir el pulmón. Se siguió el mismo procedimiento en el lado izquierdo. Finalmente, y tras verificar que no había fuga aérea, ambas sondas torácicas se retiraban. Se daba de alta al paciente a las 6 h de la intervención dentro del programa de cirugía sin ingreso, tras verificar la correcta reexpansión pulmonar con una radiografía de tórax, o antes de las 24 h si no estaba incluido en dicho programa.
Se solicitó a los pacientes que a los 6 meses (y en los últimos 34 casos, al año de la cirugía) evaluaran la intervención y sus resultados en una de estas tres categorías: “totalmente satisfecho”, “parcialmente satisfecho” o “insatisfecho”. En la actualidad, además de estas tres categorizaciones del grado de satisfacción llevamos a cabo cuestionarios de calidad preoperatorios y postoperatorios.
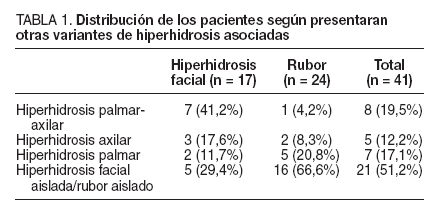
ResultadosLos 41 pacientes, 22 varones y 19 mujeres, tenían una media de edad de 33,7 (intervalo, 18-56) años. En 17 (41,5%) pacientes el síntoma principal era la HF y en 24 (58,5%), el RFI. En 20 pacientes se asoció HH palmar y/o axilar como se muestra en la tabla 1. El ascenso medio de la temperatura digital fue de 2,1 °C.
TABLA 1. Distribución de los pacientes según presentaran otras variantes de hiperhidrosis asociadas
Hubo complicaciones postoperatorias menores en 2 (4,9%) pacientes, un caso de ptosis palpebral transitoria y un caso de hemotórax diferido atribuido a sangrado postoperatorio acumulado, que precisó reingreso a las 48 h de la intervención quirúrgica y no necesitó transfusión sanguínea por presentar valores de hemoglobina y hematocrito dentro de la normalidad, y evolucionó favorablemente con el drenaje torácico. Todos los pacientes fueron dados de alta antes de las 24 h de la intervención, 14 de ellos antes de las 6 h en el programa de cirugía sin ingreso. Se obtuvo mejoría de la HF en todos los casos 17/17 (100%). En el grupo de rubor la técnica fue eficaz en 20/24 casos (83,3%); no se obtuvo la mejoría esperada en 4 (16,7%) casos. Los niveles en los que fracasó la técnica fueron: T1-T2, T1-T3, T1-T4 y T2-T5, sin poder asociar a la técnica el origen del fracaso.
En los 2 pacientes operados previamente (uno por rubor persistente y otro por HF), se obtuvo resultados satisfactorios con la segunda intervención. Se constató sudoración compensadora (SC) en 16/41 pacientes (39%), que fue severa en 6 (14,6%) casos: 4 con HF y 2 con rubor. En el grupo de HF, 8/17 (47%), y en el de rubor, 8/24 (33,3%). El índice de satisfacción general fue “totalmente satisfecho” en 31/41 casos (75,6%), “parcialmente satisfecho” por la SC en 6/41 (14,6%) e “insatisfecho” en 4/41 (9,7%). En el grupo de HF el índice de satisfacción fue “totalmente satisfecho” en 13/17 (76,5%) y “parcialmente satisfecho” por la SC en 4 (23,5%) casos. En el grupo de rubor “totalmente satisfecho” en 18/24 (75%), “parcialmente satisfecho” por la SC en 2 (8,3%) casos e “insatisfechos” en 4/24 (16,6%) por el fracaso de la técnica.
DiscusiónLas primeras descripciones de los efectos de la destrucción del primer ganglio torácico y el ganglio estrellado fueron realizadas por Henry Pancoast, que al describir su síndrome incluía entre los signos la anhidrosis y la palidez de la hemicara ipsolateral al tumor. Consecuentemente se empezó a seccionar la cadena simpática a este nivel para el manejo de la HF. Asimismo, los pioneros del tratamiento quirúrgico de la HH se dieron cuenta de que paradójicamente en la zona facial, la denervación simpática producía el efecto contrario que en la región palmar (palidez por vasoconstricción en vez de rubor y calor por vasodilatación); con ello mejoraban los ataques de rubor8. De hecho, la simpaticólisis toracoscópica para el tratamiento del rubor facial se describió por primera vez en 19851, pero no fue establecida como indicación hasta 19989.
Desde entonces, este procedimiento se ha empleado para el manejo de ambas afecciones y han aparecido algunos trabajos al respecto2,10-12.
Sin embargo, así como el tratamiento de la HH palmar y la axilar mediante simpaticotomía torácica por VATS ha sido el procedimiento que ha experimentado el mayor crecimiento cuantitativo dentro de la cirugía videotoracoscópica en la mayoría de los servicios de cirugía torácica13, en general, sólo una minoría de los cirujanos que realizan simpaticólisis toracoscópicas tratan a pacientes con RFI o HF.
A lo largo de la evolución de la simpaticólisis en el tratamiento de la HH han ido variando los niveles a los que se debía llevarla a cabo14.
En el momento actual no existe un consenso respecto a la extensión ni el nivel concreto de la simpaticólisis para el manejo del RFI y la HF. Algunos grupos llevan a cabo la lisis a nivel de T215, T1-T316, T2-T31,2, T2-T46 o T2-T511.
En nuestro estudio el nivel de la lisis varió entre T1 y T2 según la anatomía de cada paciente y la evolución de la técnica y en función de la presencia o no de hiperhidrosis palmar y/o axilar y de la anatomía de la cadena simpática. Los primeros 23 casos se llevaron a cabo sobre T1 y los últimos 18, sobre T2. Obtuvimos un 100% de mejoría en los casos de HF (17/17) y un 83,3% (20/24) en los de rubor.
Otros estudios han publicado resultados diversos; así en lo que a HF respecta, Kao et al15 publicaron en 1996 su serie de 30 pacientes diagnosticados de HF a los que realizaron simpatectomía a nivel de T2, con resultados satisfactorios en el 100% de los casos y un seguimiento medio de 15 meses. Como única complicación hubo un caso de ptosis transitoria. Refirieron SC en la mayor parte de sus pacientes (no publicaron el porcentaje), si bien, según comentan, todos la consideraron tolerable.
Lin et al10 en 2002, en su serie de 28 casos de HF a los que realizaron clipping del tercio inferior del ganglio estrellado, obtuvieron un 100% de mejorías sin complicaciones postoperatorias, con un seguimiento medio de 25,3 meses. Registraron SC en el 85,7% de los pacientes, que fue severa en un solo caso (3,6%).
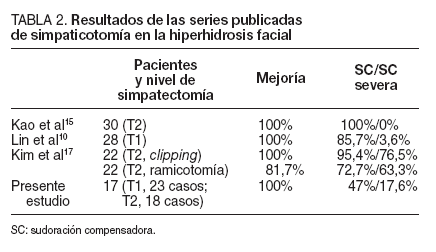
Kim et al17, en 2004, publicaron los resultados de una serie de 22 pacientes con HF a los que realizaron clipping de T2 y otra de 22 pacientes con HF a los que realizaron división de los ramos comunicantes a nivel de T2. Obtuvieron el 100% de mejoría con el clipping y el 81,7% con la ramicotomía, sin complicaciones operatorias en ninguno de los dos grupos en un seguimiento de más de 1 año. Hubo SC en el 95,4% de los pacientes del grupo de clipping (severa en el 76,5%) y en el 72,7% de las ramicotomías (severa en el 63,6%). Nuestros resultados son comparables con los de las series publicadas con niveles de SC menores (tabla 2).
TABLA 2. Resultados de las series publicadas de simpaticotomía en la hiperhidrosis facial
Respecto a las series de rubor incontrolable, Drott et al11, en 1998, publicaron los resultados de una serie de 219 pacientes con rubor facial incontrolable a los que realizaron simpatectomía a nivel de T1-T3 con un seguimiento medio de 8 meses. Obtuvieron mejoría en el 85% de los casos. Hubo 3 (1,4%) complicaciones menores y registraron SC en el 75% de los pacientes sin distinguir entre leve o severa.
En 2004, Callejas et al16 publicaron sus resultados en 100 pacientes diagnosticados de rubor facial incontrolable a los que realizaron simpatectomía (80 con bisturí ultrasónico) desde la parte baja de T1 hasta T3; obtuvieron mejoría en todos los casos, con complicaciones menores únicamente en 4 casos. No publicaron sus datos de SC.
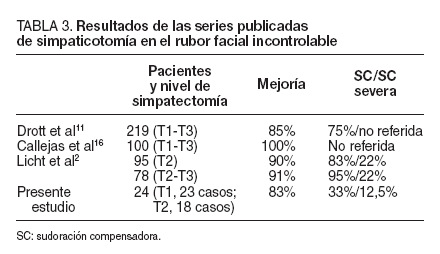
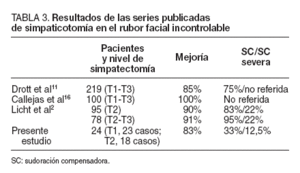
Licht et al2, en 2006, publicaron los resultados de 180 casos de rubor facial incontrolable con un seguimiento medio de 20 meses. Realizaron simpatectomía a nivel de T2 en 101 pacientes y T2-T3 en 79. Registraron mejoría en el 75% de los pacientes. En el seguimiento registraron 2 complicaciones, un síndrome de Horner transitorio y un hemotórax que requirió drenaje. Hubo SC en el 88% (el 83% en T2 y el 95% en T2-T3), que fue severa en el 22% de los pacientes (tabla 3).
TABLA 3. Resultados de las series publicadas de simpaticotomía en el rubor facial incontrolable
La SC es una entidad problemática y difícil de prever; su incidencia se estima desde el 3 al 98% y varía en función del tipo de interrogatorio postoperatorio. La mayor parte de las series grandes tienen índices por encima del 80%. Así en la serie de Drott et al18, de un total de 831 pacientes encuestados, el 83% refirió SC. Su origen estaría en la disfunción de la termorregulación corporal tras la simpaticólisis. Según las superficies corporales de Berkow se estima que la función de las glándulas sudoríparas disminuye un 40% tras la simpaticólisis y, aunque no está demostrado, varios estudios apuntan a que la SC podría ser más severa a mayor extensión de simpático resecado19.
Dada la benignidad de ambas entidades, creemos que es muy importante discutir con el paciente los posibles efectos secundarios antes de la cirugía. En particular, es importante enfatizar que la SC es un efecto secundario permanente tras la simpaticólisis, aunque en la actualidad se está experimentando en su reversebilidad mediante la reconstrucción del trayecto del simpático con un injerto de nervio intercostal20.
En conclusión, nuestros datos demuestran que el rubor facial aislado y la HF pueden ser tratados mediante la simpaticólisis por VATS con muy buenos resultados. La SC sigue siendo el principal inconveniente de la técnica.
Correspondencia: Dr. J.J. Fibla Alfara. Servicio de Cirugía Torácica. Hospital Universitari del Sagrat Cor. Viladomat, 288. 08029 Barcelona. España. Correo electrónico: juanjofibla@hotmail.com
Manuscrito recibido el 3-9-2007 y aceptado el 31-1-2008.